Нестероидные противовоспалительные средства / КонсультантПлюс
Нестероидные противовоспалительные средства.
Существующие в настоящее время нестероидные противовоспалительные средства (НПВС) относят к различным группам в зависимости от химической структуры, но они имеют единый механизм действия и сходный терапевтический эффект. В настоящее время наиболее широко используют ацетилсалициловую кислоту, диклофенак, ибупрофен, флурбипрофен, кетопрофен, напроксен, тиапрофеновую кислоту, индометацин, фенилбутазон, пироксикам, мелоксикам, целекоксиб.
В исследовании 2013 г. установлено, что экспрессия ЦОГ-2 значительно выше в миоме матки, чем в здоровых гладкомышечных клетках матки. НПВС снижают активность ЦОГ-2 и уровень простагландинов, содержание которых повышено у женщин с избыточной менструальной кровопотерей. Кроме того, они эффективны при дисменорее.
В систематическом обзоре Ассоциации Кохрана 2013 г. показано, что при миоме матки данные препараты могут уменьшить значительную менструальную кровопотерю, но менее эффективно, чем транексамовая кислота, даназол или ЛНГ-ВМС {уровень доказательности Iа).
НПВС эффективны при боли, связанной с асептическим некрозом лейомиомы (уровень доказательности IIа). У 2% беременных выявляют миому матки, из них 10% имеют осложнения, связанные с миомой во время беременности, такие как боль во II и начале III триместра и периодические кровянистые выделения. Короткие курсы ибупрофена успешно контролировали болевые ощущения в данных группах пациенток. Доказано, что индометацин может быть также эффективен в лечении боли, связанной с дегенерацией миомы матки во время беременности.
Таким образом, НПВС следует рекомендовать для лечения симптомов, связанных с миомой матки (уровень доказательности В).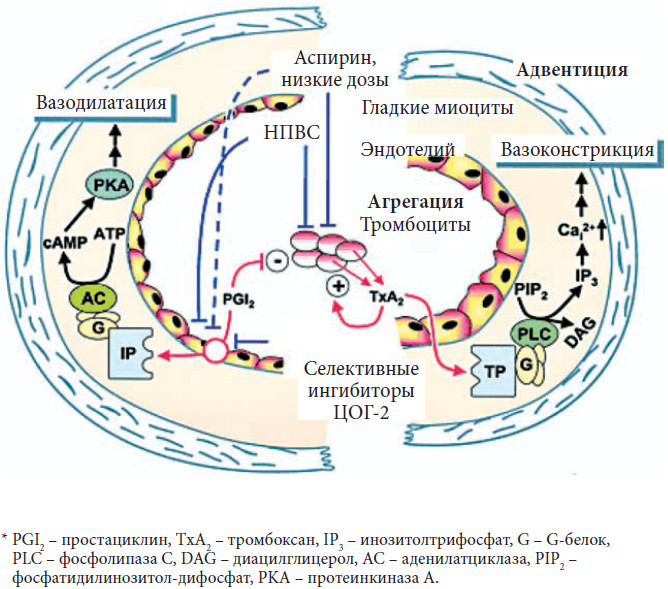
Открыть полный текст документа
Как работают НПВП — механизм действия
Нестероидные противовоспалительные препараты (НПВП) представляют собой группу негормональных противовоспалительных лекарств, которые обладают анальгезирующим и жаропонижающим действием. Они основаны на блокировании специфических ферментов, отвечающих за синтез простагландинов (липидных гормоноподобных веществ, способствующих активизации болезненных ощущений, воспалительного процесса и лихорадки).
Механизм действия НПВП
По сравнению с обезболивающими лекарствами, которые оказывают только анальгезирующее действие, нестероидные противовоспалительные препараты направлены на борьбу не только с болью, но и воспалительным процессом. Они одновременно блокируют две разновидности фермента циклогеназы – ЦОГ-1 и ЦОГ-2. К наиболее известным медикаментам этой группы относятся ибупрофен, аспирин, кетопрофен, мелоксикам и диклофенак.
Большинство медикаментов этой группы представляют собой неселективные ингибиторы ферментов ЦОГ, которые отвечает за синтез тромбоксаны и простагландинов. Этот механизм действия был открыт Дж.Вейном. Лекарственные средства выпускаются в форме таблеток, капсул, мазей, гелей, свечек, растворов для инъекционного введения.
Этот механизм действия был открыт Дж.Вейном. Лекарственные средства выпускаются в форме таблеток, капсул, мазей, гелей, свечек, растворов для инъекционного введения.
Применение НПВП
Обычно они используются для лечения хронического или остро протекающего воспалительного процесса, сопровождающегося болезненными ощущениями. Они находят применение для лечения суставов, а также для следующих заболеваний или патологий:
- Послеоперационный болевой синдром;
- Почечные колики;
- Подагра;
- Болезненные ощущения в костях при метастазах;
- Менструальные боли;
- Умеренный болевой синдром при воспалительном процессе или травмировании мягких тканей;
- Головные боли;
- Лихорадка;
- Кишечная непроходимость и т.д.
Препараты этой группы, как и лекарства для нервной системы, требуют грамотного приема. Они противопоказаны при нарушении функции печени и почек, во время беременности, при эрозии ЖКТ, дефиците клеток крови, а также при индивидуальной непереносимости.
При продолжительном приеме лекарственных средств наблюдаются осложнения, связанные с поражением слизистых тканей органов пищеварительной системы, появлением кровотечений и язвенных поражений.
Для предупреждения этих последствий были разработаны препараты новейшего поколения, которые блокируют только воспалительные ферменты (ЦОГ-1), и не оказывают влияния на защитные ферменты (ЦОГ-2).
Еще популярные статьи по теме
НПВС: препараты, механизм действия, как принимать
Статті10/10/2019
Нестероидные противовоспалительные средства (НПВС) повышают риск развития сердечной недостаточности. При этом, как показало исследование, опубликованное в журнале The BMJ*, степень риска для различных НПВС варьирует и зависит от дозы
«Это исследование служит напоминанием как для врачей – быть осторожными при назначении НПВС, так и для пациентов – принимать НПВС в наименьшей эффективной дозе в течение наименьшего возможного периода», – говорит Питер Вайсберг, медицинский директор Британского кардиологического общества.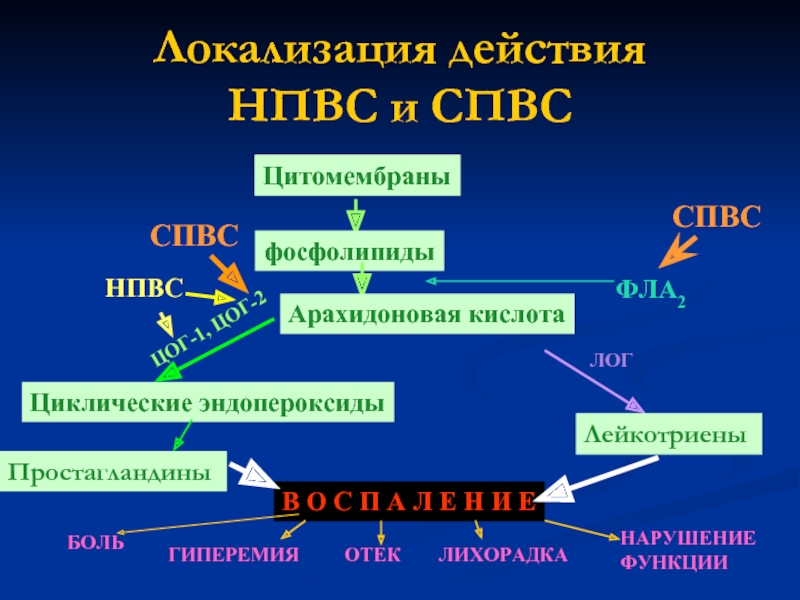
Связь между приемом НПВС и увеличением сердечно-сосудистого риска была установлена давно, однако данная работа позволяет количественно оценить риск приема НПВП и влияние на него дозировки препаратов. Авторы статьи проанализировали данные 8 млн человек в Европе (средний возраст 76-77 лет), выявили 92163 случая госпитализации в связи с сердечной недостаточностью и сравнили каждый случай с 100 пациентами из контрольной группы. В результате было установлено, что употребление НПВС увеличивает риск госпитализаций в связи с сердечной недостаточностью в среднем на 19%.
При изучении данных по 27 различным НПВС было выявлено, что прием 9 препаратов связан со значительным повышением риска госпитализации в связи с сердечной недостаточностью (в сравнении с риском у пациентов, принимавших данные НПВС в прошлом) и что этот риск возрастает с увеличением дозы. Речь идет о семи таких популярных традиционных НПВС (неселективных ингибиторах ЦОГ), как 
При приеме диклофенака, эторикоксиба, индометацина, пироксикама и рофекоксиба в очень высоких дозах (вдвое выше рекомендованной дневной дозы) риск развития сердечной недостаточности возрастает вдвое. Только у пациентов, принимающих целекоксиб в настоящее время, в сравнении с пациентами, принимавшими НПВС в прошлом, не отмечено увеличения риска сердечной недостаточности.
«Прием ибупрофена и напроксена связан в среднем с более низким риском госпитализаций по поводу сердечной недостаточности в сравнении с рядом более мощных средств, поэтому они могут лучше подходить для рутинного клинического применения, что обнадеживает, ведь они являются препаратами первой линии в большинстве организаций Национальной системы здравоохранения [Великобритании]», – отмечает Хелен Вильямс, фармацевт-консультант по кардиологии, спикер Королевского фармацевтического общества (Великобритания).
Традиционные НПВС, ингибирующие обе изоформы фермента циклооксигеназы – ЦОГ-1 и ЦОГ-2, используются уже не одно десятилетие как обезболивающие и противовоспалительные средства. При ряде заболеваний, в первую очередь, при хронических воспалительных заболеваниях суставов, их назначают длительными курсами. При этом серьезной проблемой являетс высокой риск развития побочных эффектов со стороны желудочно-кишечного тракта. Для минимизации этих нежелательных эффектов НПВС были разработаны препараты – селективные ингибиторы изофермента ЦОГ-2. Однако вскоре было обнаружено, что они вызывают побочные эффекты со стороны сердечно-сосудистой системы. Позднее обнаружилось, что традиционны НПВС также повышают риск сердечно-сосудистых событий.
При ряде заболеваний, в первую очередь, при хронических воспалительных заболеваниях суставов, их назначают длительными курсами. При этом серьезной проблемой являетс высокой риск развития побочных эффектов со стороны желудочно-кишечного тракта. Для минимизации этих нежелательных эффектов НПВС были разработаны препараты – селективные ингибиторы изофермента ЦОГ-2. Однако вскоре было обнаружено, что они вызывают побочные эффекты со стороны сердечно-сосудистой системы. Позднее обнаружилось, что традиционны НПВС также повышают риск сердечно-сосудистых событий.
Читайте также: ФОКУС НА БЕЗОПАСНОСТЬ: НПВП местного применения в ревматологии, неврологии и травматологии
Авторы указывают, что полученные ими результаты касаются в первую очередь рецептурных НПВС, применяемых пожилыми пациентами длительными курсами. В то же время, они дают основание пересмотреть безопасность применения безрецептурных НПВС.
Джон Смит, глава Ассоциации собственников Великобритании, представляющей интересы производителей безрецептурных лекарственных средств, указывает на то, что в исследовании нет данных об абсолютном риске, «поэтому вероятность развития у этих людей сердечной недостаточности без приема НПВС так и не известна».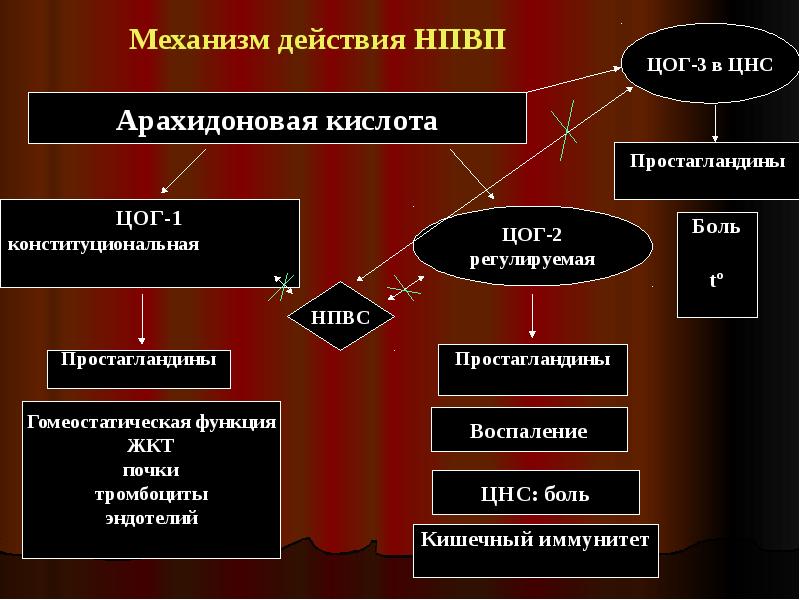
Читайте также: Если повысилась температура: выбираем жаропонижающий препарат
* Arfè A, Scotti L, Varas-Lorenzo C et al. (2016) Non-steroidal anti-inflammatory drugs and risk of heart failure in four European countries: nested case-control study // The BMJ, 354:i4857. doi: 10.1136/bmj.i4857
** Показатель относительного риска указывает на то, каким образом какой-либо фактор изменяет частоту какого-либо исхода. При значениях менее 1 говорят о снижении вероятности исхода при воздействии фактора, более 1 – о повышении вероятности исхода. Например, в описанном исследовании относительный риск 1,5 означает, что риск госпитализации в связи с сердечной недостаточностью возрастает в 1,5 раза, то есть на 50%.
Поділіться цим з друзями!
Вам також буде цікаво це:
Возможности применения Ибупрофена (Ибуфена® Ультра) в практике семейного врача
Возможности применения Ибупрофена (Ибуфена® Ультра) в практике семейного врача
УДК 616-009. 7-08-031.81:614.254.3
7-08-031.81:614.254.3
Е.Б. Ужегова
Казахский национальный медицинский университет им. С.Д.Асфендиярова, г. Алматы
Факультет последипломного образования, г.Алматы
Возможности применения Ибупрофена (Ибуфена® Ультра) в практике семейного врача
В статье описываются механизм действия, классификация, показания к назначению нестероидных противовоспалительных средств (НПВС). Особенности применения ибупрофена в практике семейного врача. Профиль его анальгетической эффективности и безопасности.
Ключевые слова: боль, лечение
Семейный врач в своей практической деятельности часто применяет нестероидные противовоспалительные средства (НПВС), которые за счет уникальной комбинации фармакологических свойств: противовоспалительных, жаропонижающих и антитромботических,— помимо ревматологии, применяются практически во всех областях медицины.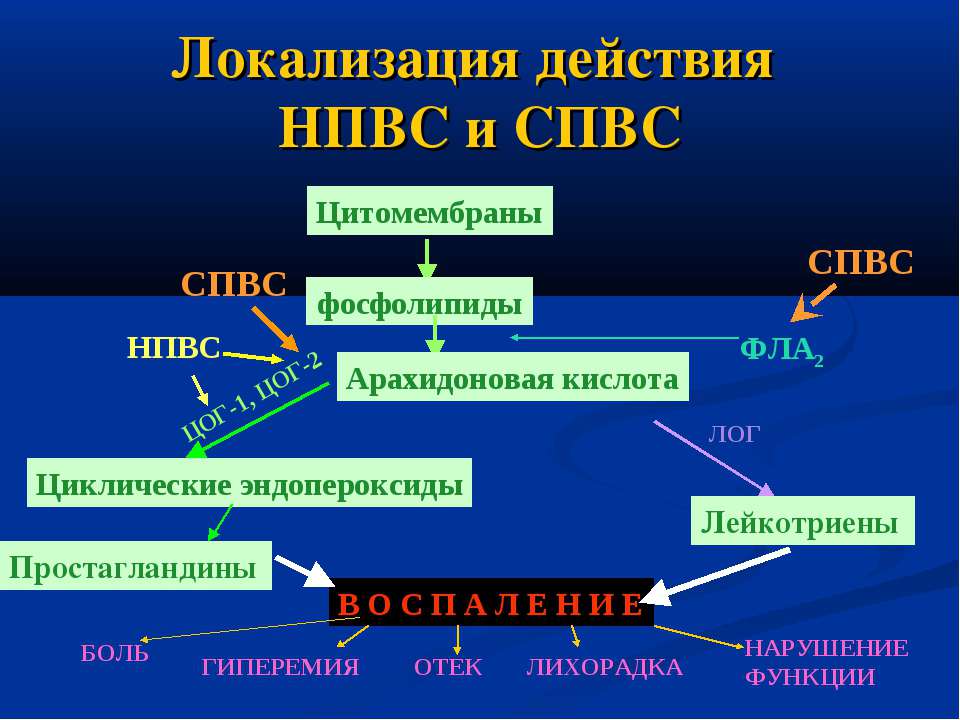 НПВС часто используются для купирования болевого синдрома различного происхождения. Эти препараты представляют собой патогенетическое средство лечения острой и хронической боли, связанной с тканевым повреждением и воспалением.
НПВС часто используются для купирования болевого синдрома различного происхождения. Эти препараты представляют собой патогенетическое средство лечения острой и хронической боли, связанной с тканевым повреждением и воспалением.
Глобальное исследование состояния здоровья, проведенное в 54 странах с участием 27 000 респондентов, показало, что головные боли, простуда, кашель являются самой частой причиной обращения за медицинской помощью к терапевтам.
Рисунок 1.
Ведущие жалобы пациентов при обращении за врачебной помощью (1).
По данным независимого исследовательского центра DSM Group анализ фармацевтического рынка в 2012 г. показал, что болеутоляющие средства оказались одними из самых популярных групп фармацевтических препаратов (1).
Около 30 млн человек в мире регулярно принимают НПВС. По прогнозам количество людей, принимающих НПВС, будет возрастать по мере старения населения и увеличения распространенности поражений опорно-двигательного аппарата и других патологических состояний, требующих лечения НПВС. В Европе НПВС назначают 82% врачей общей практики и 84% ревматологов поликлиники, в стационаре их применяют у 20% больных (2).
В Европе НПВС назначают 82% врачей общей практики и 84% ревматологов поликлиники, в стационаре их применяют у 20% больных (2).
Показания к назначению НПВС
Основными показаниями к назначению НПВС являются воспалительные процессы различного генеза: ревматические и неревматические заболевания опорно-двигательного аппарата (ревматическая лихорадка, ревматоидный и подагрический артриты, болезнь Бехтерева, остеоартроз, миозит, тендовагинит, травма). Кроме того, показаниями для назначения НПВС являются болевые синдромы при невралгии, радикулите, ишиасе, люмбаго, почечной и печеночной колике, а также головная, зубная, послеоперационная боль и дисменорея. НПВС могут применяться при лихорадке и профилактике артериальных тромбозов.
Механизм действия НПВС
Главным и общим элементом механизма действия НПВС является угнетение синтеза простагландинов (ПГ) из арахидоновой кислоты путем ингибирования фермента циклооксигеназы (ПГ-синтетазы). Установлено, что существуют, как минимум, два изофермента циклооксигеназы, которые ингибируются НПВС. Первый изофермент – ЦОГ-1 (СОХ-1 – англ.) – контролирует выработку простагландинов, регулирующий целостность слизистой оболочки желудочно-кишечного тракта, функцию тромбоцитов и почечный кровоток, а второй изофермент – ЦОГ-2 – участвует в синтезе простагландинов при воспалении. Противовоспалительное действие НПВС обусловлено ингибированием ЦОГ-2, а их нежелательные реакции – ингибированием ЦОГ-1.
Установлено, что существуют, как минимум, два изофермента циклооксигеназы, которые ингибируются НПВС. Первый изофермент – ЦОГ-1 (СОХ-1 – англ.) – контролирует выработку простагландинов, регулирующий целостность слизистой оболочки желудочно-кишечного тракта, функцию тромбоцитов и почечный кровоток, а второй изофермент – ЦОГ-2 – участвует в синтезе простагландинов при воспалении. Противовоспалительное действие НПВС обусловлено ингибированием ЦОГ-2, а их нежелательные реакции – ингибированием ЦОГ-1.
Классификация НПВС по селективности в отношении различных форм циклооксигеназы представлена в таблице 1.
Таблица 1.
Классификация НПВС по селективности в отношении различных форм циклооксигеназы (Drugs Therapy Perspectives, 2000, с дополнениями) (3)
Профиль эффективности ибупрофена
Одним из наиболее известных представителей класса НПВС является ибупрофен, который успешно применяется в клинической практике более 30 лет и более 10 лет в безрецептурной форме. Это связано с тем, что в повседневной практике врач часто сталкивается с болевыми синдромами у своих пациентов. Потребность в назначении эффективных обезболивающих препаратов постоянно растет. Согласно классификация НПВС по селективности в отношении различных форм циклооксигеназы ибупрофен обладает умеренной селективностью в отношении ЦОГ-1, а по фармакологической классификации относится к классу нестероидных противовоспалительных препаратов, является производным пропионовой кислоты. Его основные эффекты (жаропонижающий и противовоспалительный) опосредованы ингибированием активности циклооксигеназы и, соответственно, синтеза простагландинов — медиаторов боли, воспаления и температурной реакции.
Это связано с тем, что в повседневной практике врач часто сталкивается с болевыми синдромами у своих пациентов. Потребность в назначении эффективных обезболивающих препаратов постоянно растет. Согласно классификация НПВС по селективности в отношении различных форм циклооксигеназы ибупрофен обладает умеренной селективностью в отношении ЦОГ-1, а по фармакологической классификации относится к классу нестероидных противовоспалительных препаратов, является производным пропионовой кислоты. Его основные эффекты (жаропонижающий и противовоспалительный) опосредованы ингибированием активности циклооксигеназы и, соответственно, синтеза простагландинов — медиаторов боли, воспаления и температурной реакции.
Эффективность ибупрофена при различных состояниях была доказана во многих исследованиях. Анальгетическая эффективность ибупрофена доказана в исследованиях при зубной боли (4-5), при боли в горле (4), при мышечно-скелетной боли (4-5). Эффективность ибупрофена в терапии головной боли как у взрослых, так и у детей и подростков доказана во многих плацебо-контролируемых клинических исследованиях, а также нескольких метаанализах. Европейская федерация неврологических обществ (European Federation of Neurological Societies, EFNS) и ВОЗ рекомендуют ибупрофен как препарат первого ряда для терапии приступа мигрени легкой и средней тяжести (класс рекомендаций А) (6-12).
Европейская федерация неврологических обществ (European Federation of Neurological Societies, EFNS) и ВОЗ рекомендуют ибупрофен как препарат первого ряда для терапии приступа мигрени легкой и средней тяжести (класс рекомендаций А) (6-12).
Влияние ибупрофена и парацетамола на выраженность болевого и суставного синдромов при остеоартрозе изучалось в многоцентровом рандомизированном исследование IPSO (Ibuprofen, Paracetamol Study in Osteoarthritis), проведенном в 2004 г. с участием 222 пациентов, страдающим остеоартрозом (ОА) тазобедренного (30% пациентов) или коленного (70%) сустава. В исследовании оценивалось влияние ибупрофена (400–1200 мг/сут) и парацетамола (1000–3000 мг/сут) на выраженность болевого и суставного синдромов. Результаты исследования продемонстрировали более значительное уменьшение боли в группе ибупрофена по сравнению с парацетамолом. Авторы исследования сделали вывод, что ибупрофен при однократном (400 мг) или многократном (до 1200 мг) приеме обладает лучшим соотношением «эффективность/безопасность», чем парацетамол (13). Более выраженная эффективность НПВС, в том числе ибупрофена, по сравнению с парацетамолом у больных ОА была описана в Кокрановском обзоре (14). Учитывая способность НПВС купировать боли в опорно-двигательном аппарате, прием НПВС показан всем больным как симптоматическое лечение в период усиления болей при ревматоидном артрите и остеоартрозе (15-16).
Более выраженная эффективность НПВС, в том числе ибупрофена, по сравнению с парацетамолом у больных ОА была описана в Кокрановском обзоре (14). Учитывая способность НПВС купировать боли в опорно-двигательном аппарате, прием НПВС показан всем больным как симптоматическое лечение в период усиления болей при ревматоидном артрите и остеоартрозе (15-16).
Кроме описания эффективности ибупрофена при вышеописанных состояниях, в двойных слепых исследованиях получены данные об эффективности длительного применения ибупрофена в высоких дозах – 20-30 мг/кг (максимально 1600 мг) 2 раза в день в течение 4 лет – у больных муковисцидозом. Отмечено замедление прогрессирования легочной деструкции без серьезных нежелательных реакций (17).
Профиль безопасности терапии ибупрофеном
Наряду с эффективностью лекарственные препараты должны иметь хороший профиль безопасности. При применении НПВС могут возникнуть побочные эффекты такие как: поражения органов ЖКТ, бронхоконстрикция, поражения почек, поражения печени, поражения кожи и слизистых, нарушения функций ЦНС, поражения системы крови.
Одним из частых осложнений, которые развиваются на фоне приема НПВС, является желудочно-кишечное кровотечение. Установленными факторами риска развития НПВС-обусловленных гастродуоденальных перфораций, язв и кровотечений являются:
· возраст старше 60 лет;
· тяжесть основного заболевания;
· наличие язв, перфораций, кровотечений в анамнезе;
· противоязвенная терапия в анамнезе;
· НПВС-гастропатии в анамнезе;
· высокие дозировки НПВС;
· одновременный прием глюкокортикоидов;
· одновременный прием антикоагулянтов;
· одновременный прием двух НПВС (в том числе и аспирина).
Частота желудочно-кишечных кровотечений при применении НПВС зависит как от селективности препарата в отношении ЦОГ, так и от дозировки и длительности использования. При проведении метаанализа обсервационных эпидемиологических исследований за 2000-2008 гг. по выявлению влияния НПВС на риск кровотечений из верхних отделов ЖКТ установлено, что наименьшая частота ЖК-кровотечений была отмечена в группе коксибов (соотношение рисков (ОР) 1,88; 95% доверительный интервал (ДИ) 0,96–3,71). Среди неселективных НПВС лучшие результаты были получены у ибупрофена (ОР 2,69; 95% ДИ 2,17–3,33). Наибольший риск наблюдался у кеторолака (ОР 14,54; 95% ДИ 5,87–36,04) и пироксикама (ОР 9,94; 95% ДИ 5,99–16,50) (18). Результаты мета-анализа наблюдений за длительный период продолжительностью 21 год, свидетельствуют о меньшем относительном риске развития желудочно-кишечных кровотечений при использовании ибупрофена по сравнению с диклофенаком, мелоксикамом, нимесулидом, кетопрофеном, напроксеном, индометацином (19). В таблице 2 представлены результаты метаанализа и значения относительного риска развития ЖКТ-кровотечения при использовании различных НПВС.
При проведении метаанализа обсервационных эпидемиологических исследований за 2000-2008 гг. по выявлению влияния НПВС на риск кровотечений из верхних отделов ЖКТ установлено, что наименьшая частота ЖК-кровотечений была отмечена в группе коксибов (соотношение рисков (ОР) 1,88; 95% доверительный интервал (ДИ) 0,96–3,71). Среди неселективных НПВС лучшие результаты были получены у ибупрофена (ОР 2,69; 95% ДИ 2,17–3,33). Наибольший риск наблюдался у кеторолака (ОР 14,54; 95% ДИ 5,87–36,04) и пироксикама (ОР 9,94; 95% ДИ 5,99–16,50) (18). Результаты мета-анализа наблюдений за длительный период продолжительностью 21 год, свидетельствуют о меньшем относительном риске развития желудочно-кишечных кровотечений при использовании ибупрофена по сравнению с диклофенаком, мелоксикамом, нимесулидом, кетопрофеном, напроксеном, индометацином (19). В таблице 2 представлены результаты метаанализа и значения относительного риска развития ЖКТ-кровотечения при использовании различных НПВС.
Таблица 2
Относительный риск развития ЖКТ-кровотечения при использовании различных НПВС (мета-анализ 28 популяционных исследований за период 1980-2011г).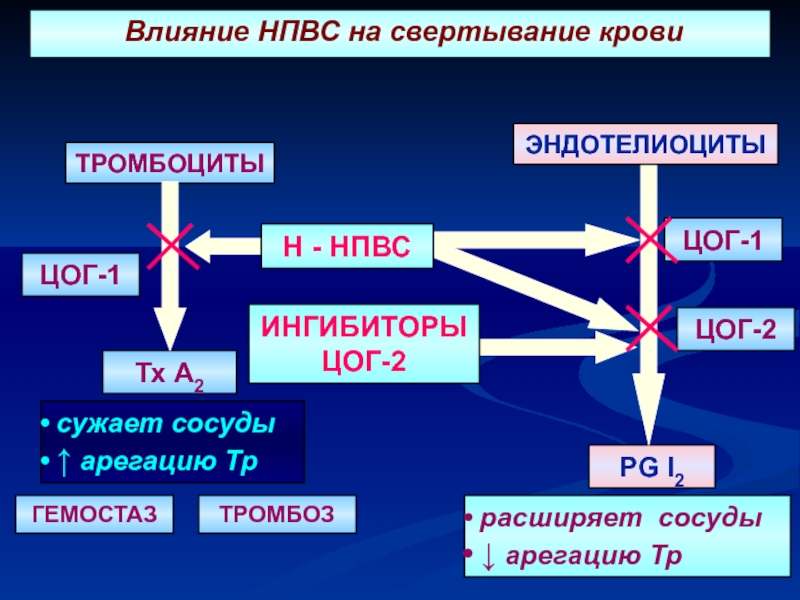
По данным других метаанализов (20-21) ибупрофен также характеризовался наиболее низким риском возникновения ЖК-кровотечения по сравнению с диклофенаком, напроксеном, индометацином, пироксикамом и кетопрофеном.
При использовании ибупрофена в обезболивающих дозах и соответствующей длительности лечения у больных риск развития осложнений со стороны пищеварительной системы был не выше, чем при назначении парацетамола, и это при том, что острая токсичность при намеренной или случайной передозировке ибупрофена намного ниже, чем у парацетамола (22-23). Низкая токсичность ибупрофена обусловлена быстрым метаболизмом и отсутствием образования активных метаболитов препарата, что выгодно отличает его от парацетамола.
В исследование (PAIN study — Paracetamol, Aspirin, Ibuprofen New tolerability study), проводившееся во Франции 1108 врачами общей практики, за период с сентября 1997 по март 1998 г. было включено 8677 взрослых пациентов (мужчины и женщины, в возрасте от 18 до 75 лет). Пациенты были рандомизированны на 3 группы: 2900 пациентов составили группу аспирина, 2886 — ибупрофена и 2888 — парацетамола (3 пациента получали лечение неизвестным препаратом, поэтому они были исключены из исследования). Пациенты получали препараты в анальгетических дозировках: аспирин и парацетамол — до 3 г в день, ибупрофен — до 1,2 г в день. Продолжительность терапии составила 7 дней.
Пациенты были рандомизированны на 3 группы: 2900 пациентов составили группу аспирина, 2886 — ибупрофена и 2888 — парацетамола (3 пациента получали лечение неизвестным препаратом, поэтому они были исключены из исследования). Пациенты получали препараты в анальгетических дозировках: аспирин и парацетамол — до 3 г в день, ибупрофен — до 1,2 г в день. Продолжительность терапии составила 7 дней.
Результаты исследования свидетельствуют об одинаковой переносимости ибупрофена и парацетамола, причем оба препарата переносились лучше, чем ацетилсалициловая кислота. Кроме того, прием ибупрофена был связан с меньшим количеством побочных эффектов со стороны пищеварительной системы по сравнению с парацетамолом.
Таблица 3
Частота побочных эффектов при приеме ибупрофена, парацетамола и аспирина (исследование Pain).
Таблица 4
Процент побочных эффектов при приеме ибупрофена, парацетамола и аспирина (исследование Pain).
При применении ибупрофена у детей и у взрослых в низких дозах (800–1200 мг в сутки) частота побочных эффектов сопоставима с таковой у парацетамола. Достоинством препарата ибупрофен является хорошая переносимость, редкое развитие нежелательных реакций. Из всех НПВС ибупрофен имеет один из лучших желудочно-кишечных профилей безопасности. Препарат ибупрофен в дозах до 1200 мг/сут. даже при длительном применении вызывает минимальные повреждения слизистой оболочки ЖКТ и считается «золотым стандартом» по безопасности использования. Поэтому в низких дозах (800 – 1200 мг в сутки) одобрен для безрецептурного применения.
В Казахстане ибупрофен (Ибуфен® Ультра — производитель «Медана Фарма» АО, Польша) в капсулах по 200 мг широко применяется в различных областях медицины для купирования боли и воспаления.
Фармакокинетика и фармакодинамика Ибуфена® Ультра
Период достижения максимальной концентрации в плазме крови при приеме натощак – 45 минут, при приеме после еды – 1,5-2,5 часа; в синовиальной жидкости – 2-3 часа, где создаются большие концентрации, чем в плазме крови. Быстро метаболизируется и выводится из организма. Период полувыведения 1,8-2,5 часа, поэтому анальгетический и жаропонижающий эффекты поддерживаются до 8 часов.
Ибуфен® Ультра выпускается в виде мягких желатиновых капсул, в которых препарат содержится в жидком виде. Такая форма выпуска имеет ряд преимуществ перед таблетками.
Во-первых: современное оборудование обеспечивает высокую точность заполнения капсул лекарственным веществом.
Во-вторых: такая форма выпуска обеспечивает высокую биодоступность ибупрофена, так как капсула распадается в ЖКТ быстрее, чем драже и таблетки, а ее жидкое содержимое быстрее и легче абсорбируется в организме человека.
В-третьих: оболочка защищает действующее вещество от света, воздуха и влаги, а так же исключает неприятный вкус и запах лекарства при приеме.
Ибуфен® Ультра оказывает обезболивающее, жаропонижающее и противовоспалительное действие. Препарат показан при повышении температура тела и болевом синдроме различного происхождения. Применяется внутрь по 1-2 капсулы каждые 4-6 часов. Максимальная суточная доза 6 капсул (1200 мг ибупрофена).
Заключение
Таким образом, применение ибупрофена при болевых синдромах показало его эффективность и хорошую переносимость не только как средства для купирования болевых эпизодов, но и для курсового лечения. Многолетний опыт успешного применения ибупрофена в широкой клинической практике более чем в 80 странах мира в качестве безрецептурного препарата служит наглядным примером высокого профиля его эффективности и безопасности (24).
Список литературы
1. Фармацевтический рынок России. Май 2012 г. DSMGroup. Доступно на:https://www.dsm.ru/content/file/cpravka_may_2012.pdf.
2. Топчий Н. В., Топорков А. С. Оптимизация применения нестероидных противовоспалительных препаратов в общемедицинской практике // РМЖ. 2011; 19 (2): 27–32.
3. Страчунский Л.С., Козлов С.Н. Нестероидные противовоспалительные средства //Методическое пособие. Смоленск. Смоленская государственная медицинская академия. 2000, — 54 с.
4. Derry C., Derry S., Moore R. A., McQuay H. J. Single dose oral ibuprofen for acute postoperative pain in adults // Cochrane Database Syst Rev. 2009, Jul 8; (3): CD001548. Review. PubMed PMID: 19588326.
5. Hersh E. V., Kane W. T., O’Neil M. G., Kenna G. A., Katz N. P., Golubic S., Moore P. A. Prescribing recommendations for the treatment of acute pain in dentistry // Compend Contin Educ Dent. 2011, Apr; 32 (3): 22, 24–30; quiz 31–2. PubMed PMID: 21560740.
6. Aids for management of common headache disorders in primary care 2007 www.who.int/entity/mental_health/neurology/who_ehf_aids_headache.pdf.
7. Evers S., Afra J., Frese A., Goadsby P. J., Linde M., May A., Sandor P. S. European Federation of Neurological Societies. EFNS guideline on the drug treatment of migraine — revised report of an EFNS task force // Eur J Neurol. 2009, Sep; 16 (9): 968–981. PubMed PMID: 19708964.
8. Rabbie R., Derry S., Moore R. A., McQuay H. J. Ibuprofen with or without an antiemetic for acute migraine headaches in adults // Cochrane Database Syst Rev. 2010, Oct 6; (10): CD008039. Review. PubMed PMID: 20927770.
9. Verhagen A. P. et al. Treatment of tension type headache: paracetamol and NSAIDs work: a systematic review // Ned Tijdschr Geneeskd. 2010; 154: A1924. Review. Dutch. PubMed PMID: 20699021.
10. Suthisisang C., Poolsup N., Kittikulsuth W., Pudchakan P., Wiwatpanich P. Efficacy of low-dose ibuprofen in acute migraine treatment: systematic review and meta-analysis // Ann Pharmacother. 2007, Nov; 41 (11): 1782–91. Epub 2007 Sep 18. Review. PubMed PMID: 17878396.
11. Silver S., Gano D., Gerretsen P. Acute treatment of paediatric migraine: a meta-analysis of efficacy // J Paediatr Child Health. 2008, Jan; 44 (1–2): 3–9. Epub 2007, Sep 14. Review. PubMed PMID: 17854415.
12. Damen L. et al. Symptomatic treatment of migraine in children: a systematic review of medication trials // Pediatrics. 2005, Aug; 116 (2): e295–302. Review. PubMed PMID: 16061583.
13. Boureau F., Schneid H., Zeghari N., Wall R., Bourgeois P. The IPSO study: ibuprofen, paracetamol study in osteoarthritis. A randomised comparative clinical study comparing the efficacy and safety of ibuprofen and paracetamol analgesic treatment of osteoarthritis of the knee or hip // Ann Rheum Dis. 2004 Sep; 63 (9): 1028–34. PubMed PMID: 15308513; PubMed Central PMCID: PMC1755112.
14. Towheed T. E., Maxwell L., Judd M. G., Catton M., Hochberg M. C., Wells G. Acetaminophen for osteoarthritis // Cochrane Database Syst Rev. 2006, Jan 25; (1): CD004257. Review. PubMed PMID: 16437479.
15. Ревматология. Клинические рекомендации / Под ред. Е. Л. Насонова. М.: ГЭОТАР-Медиа, 2008. 288 с.
16. Zhang W. et al. EULAR evidence based recommendations for the management of hand osteoarthritis: report of a Task Force of the EULAR Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT) // Ann Rheum Dis. 2007, Mar; 66 (3): 377–388. Epub 2006 Oct 17. PubMed PMID: 17046965; PubMed Central PMCID: PMC1856004
17. Konstan M.W., Byard PJ., Hoppel C.L., Davis P.B. Effect of high dose ibuprofen in patients with cystic fibrosis // N. Engl. J. Med., 1995, 332: 848-854
18. Masso Gonzalez E. L. et al. Variability among nonsteroidal antiinflammatory drugs in risk of upper gastrointestinal bleeding // Arthritis Rheum. 2010 Jun; 62 (6): 1592–1601. PubMed PMID: 20178131.
19. Castellsague J., Riera-Guardia N., Calingaert B. et al. Individual NSAIDs and upper gastrointestinal complications: a systematic review and meta-analysis of observational studies (the SOS project) // Drug Saf.- 2012.- V.35(12).- P. 1127 – 1146.
20. Lewis S. C. et al. Dose-response relationships between individual nonaspirin nonsteroidal anti-inflammatory drugs (NANSAIDs) and serious upper gastrointestinal bleeding: a meta-analysis based on individual patient data // Br J Clin Pharmacol. 2002, Sep; 54 (3): 320–326. PubMed PMID: 12236853; PubMed Central PMCID: PMC1874428.
21. Richy F. et al. Time dependent risk of gastrointestinal complications induced by non-steroidal anti-inflammatory drug use: a consensus statement using a meta-analytic approach // Ann Rheum Dis. 2004, Jul; 63 (7): 759–766. Review. PubMed PMID: 15194568; PubMed Central PMCID: PMC1755051.
22. Moore N., Noblet C., Breemeersch C. A review of the safety of Ibuprofen at the analgesic-antipyretic dose // Therapie. — 1996. — 51(4). — 458-63.
23. Bjarnason I. Ibuprofen and gastrointestinal safety: a dose-duration-dependent phenomenon // J R Soc Med. 2007; 100 Suppl 48: 11–14.
24. Rainsford K. D. Fifty years since the discovery of ibuprofen // Inflammopharmacology. 2011, Dec; 19 (6): 293–297. PubMed PMID: 22120888.
Түйіндеме
Е.Б.Ужегова
С.Ж. Асфендияров атындағы Қазақ Ұлттық Медицина Университеті, Алматы қаласы
Дипломнан кейінгі білім беру факультеті
Отбасылық дәрігер іс тәжірибесінде Ибупрофенді (Ибуфена® Ультра) қолдану мүмкіндігі.
Мақалада стероидтік емес қабынуға қарсы дәрілердің әсер ету механизмі, жіктелуі, және қолдануға көрсетімдер баяндалады. Отбасылық дәрігер іс тәжірибесінде Ибупрофенді қолдану ерекшеліктері. Оның ауырсынуды басатын тиімділігі мен қауіпсіздік мінездемелері.
Негізгі сөздер: ауырсыну, емдеу
Summary
E.B. Uzhegova
S.D.Asfendiyarov Kazakh National Medical University, Almaty city.
Faculty of Postgraduate Studies.
Possibilities of using Ibuprofen (Ibufen® Ultra) in the practice of family doctor.
The article describes mechanism of action, classification and indications to prescribing the non-steroidal anti-inflammatory agents. Peculiarities of using Ibuprofen in the practice of family doctor. Profile of its analgesic efficiency and safety.
Key words: pain, treatment.
НПВП-ИНДУЦИРОВАННЫЕ АСТРОЭНТЕРОПАТИИ | Опубликовать статью ВАК, elibrary (НЭБ)
Карамян А.С.1, Савочкина А.Ю.2, Ватников Ю.А.3
1Доцент, кандидат ветеринарных наук, 2Аспирант, 3Профессор, Доктор ветеринарных наук, Департамент Ветеринарной медицины, Российский университет дружбы народов, Москва
НПВП-ИНДУЦИРОВАННЫЕ АСТРОЭНТЕРОПАТИИ
Аннотация
Нестероидные противовоспалительные препараты широко используют в современной ветеринарной медицине в качестве анальгетических и противовоспалительных средств, купирующих развитие болевого синдрома и воспалительного процесса. НПВС подавляют фермент циклооксигеназу (ЦОГ), которая превращает арахидоновую кислоту в простагландины, тромбоксаны и простациклин. Блокировка данных эйкозаноидов обладает обезболивающим, жаропонижающим, антитромботическим, антиэндотоксическим и противовоспалительным действиями. Многие препараты из арсенала НПВП вызывают серьезные побочные эффекты (эрозивные нарушения в слизистой жкт и др.). Развитие современных фармакологических технологий позволяет создавать новые формы лекарственных средств, которые могут значительно снижать побочные (негативные) эффекты при их применении.
Ключевые слова: нестероидные противовоспалительные препараты, пленки, новые лекарственные средства, гастроэнтеропатии.
Karamyan A.S.1, Savochkina A.Y.2, Vatnikov Y.A.3
1Assistant Professor, PhD in Veterinary Medicine and Science, 2Postgraduate student, 3Professor, PhD in Veterinary Medicine and Science, Department of Veterinary Medicine, Russian Peoples’ Friendship University, Moscow
NSAID-INDUSED GASTROENTHEROPATHY
Abstract
Nonsteroidal anti-inflammatory drugs are widely used in modern veterinary medicine as an analgesic and anti-inflammatory drugs, relieves pain and the development of the inflammatory process. NSAIDs inhibit the enzyme cyclooxygenase (COX), which converts arachidonic acid to prostaglandins, thromboxanes and prostacyclin. Blocking these eicosanoids has analgesic, antipyretic, anti-thrombotic, anti-inflammatory actions and antiendotoksicheskim. Many drugs in the arsenal of NSAIDs cause serious side effects (erosive violations in the mucosa of the gastrointestinal tract, and others.). The development of modern pharmaceutical technology allows you to create new forms of drugs that can greatly reduce the adverse (negative) effects in their application
Keywords: nonsteroidal anti-inflammatory drugs, films, new drugs, gastroentheropathy.
Нестероидные противовоспалительные препараты (НПВП) эффективны при купировании острой и хронической боли различного генеза у животных. Понимание механизмов, за счет которых НПВП проявляют анальгетический эффект, необходимо для минимизации побочного действия препаратов и изменения их действия при комбинации с другими лекарственными средствами [3].
Интенсивное использование НПВП в ветеринарии объясняется, в первую очередь, тем фактом, что эти препараты практически незаменимы при терапии многих заболеваний с такими симптомами как воспаление, боль, лихорадка и др.
С точки зрения патогенеза и механизмов действия целесообразно использование именно НПВП, т.к. одни и те же медиаторы (простагландины, ПГ) вызывают развитие болевой и воспалительной реакции. НПВС проявляют свой противовоспалительный эффект за счет подавления выработки простагландинов [3,6]. Максимальная концентрация (Смах) фенилбутазона, кетопрофена и карпрофена накапливается в очаге воспаления и сохраняется в воспалительном экссудате в течение более длительного времени, чем в плазме. Это явление объясняет замедленное начало и продолжительное противовоспалительное действие препаратов, которое не связано с фармакокинетикой плазмы. Противовоспалительное действие НПВС связано не только с подавлением функций циклооксигеназы. Препараты данной фармакологической группы более липофильны при низком pH в воспаленных тканях. Противовоспалительное действие этих препаратов также связывают со способностью НПВС внедряться в двойной липидный слой клеток, тем самым прерывая обычные сигналы и взаимосвязи между белками в клеточных мембранах. В клеточных мембранах нейтрофилов НПВС подавляют их агрегацию, уменьшают выделение ферментов и образование пероксида, а также подавляют липоксигеназу. Несмотря на большое структурное разнообразие НПВП, механизм их действия одинаков [6]. Несмотря на существующее структурное различие НПВП, все эти препараты обладают сходным механизмом действия, а именно – ингибируют циклооксигеназу (ЦОГ) [3]. Две изоформы ЦОГ детерминируются различными генами. ЦОГ-1 постоянно экспрессируется в слизистой оболочке желудка, тромбоцитах и почках. Этот структурный изофермент регулирует продукцию простагландинов, участвующих в обеспечении нормальной (физиологической) функциональной активности клеток.
В то время как изофермент ЦОГ-2, экспрессия которого регулируется иммунными медиаторами (цитокинами), принимающими участие в развитии иммунного ответа и воспаления, участвует в синтезе противовоспалительных простагландинов [2,3,7].
НПВП увеличивают риск поражений верхних отделов жкт, которые проявляются такими симптомами как умеренная диспепсия или более серьезными осложнениями, например образование язв, геморрагий и перфораций [6].
Доподлинно известно, что желудочно-кишечный тракт (ЖКТ) – это система органов, которая отвечает за потребление и переваривание пищи, всасывание питательных веществ и выделение непереваренных остатков. Слизистая оболочка жкт взаимодействует с такими агрессивными факторами как:
– пищевой фактор: низкокачественный корм, использование кормов несоответствующей температуры (слишком горячие, слишком холодные, замороженные корма), попадание в корм ядовитых растений и веществ или их примесей;
– травматизация жкт инородными телами
– агрессивное воздействие лекарственных средств.
НПВП негативно влияют на слизистую оболочку жкт, существенно уменьшая ее защитную способность и устойчивость к воздействию агрессивных факторов эндо- и экзогенного происхождения [3,5,6].
Поражения жкт, индуцированные применением неселективных-НПВП, могут быть связаны с прямым, неспецифическим раздражением или различными биохимическими и фармакологическими механизмами, которые приводят к ингибированию ЦОГ. Слизистая оболочка желудка и двенадцатиперстной кишки богата ПГ, которые выполняют защитную роль в жкт посредством поддержания требуемого уровня кровоснабжения гастродуоденальной слизистой оболочки, секреции бикарбоната эпителиальными клетками, секреции слизи и поддержания нейтрального рН слизистой оболочки. Полагают, что ингибирование ЦОГ увеличивает восприимчивость слизистой оболочки желудка к травматизации в связи с ингибированием секреции цитопротективной слизи и бикарбоната и изменением физико-химического состава слизи.
Другие механизмы, потенциально вовлеченные в патогенез гастро-интестинальных поражений, вызванных применением неселективных НПВП, изученные на моделях животных включают:
– рост числа кишечных бактерий и увеличение эпителиальной проницаемости тонкой кишки, связанные с энтерогепатической рециркуляцией неселективных НПВП,
– инфильтрацию нейтрофилов в слизистую оболочку, как ответ на первоначальное повреждение тканей,
– разобщение окислительного фосфорилирования митохондрий, что приводит к повышенной кишечной проницаемости и выделению кальция в цитозоль,
– усиленную перистальтику желудка [7].
В последние годы существенный прогресс был достигнут в изучении и понимании процессов патогенеза при НПВП-энтеропатии, и, в частности, взаимосвязи кишечных бактерий, желчи и кишечно-печеночной рециркуляции НПВП. Кроме того, становится очевидным, что подавление секреции желудочной кислоты значительно увеличивает риск появления НПВП-энтеропатии [2].
Поражения жкт, индуцированные неселективными НПВП являются видоспецифичными. К примеру, предрасположенность кошек, собак и лошадей к возникновению побочных эффектов при применении НПВП выше, чем у человека. Собаки, например, более восприимчивы к негативному влиянию неселективных НПВП, чем крысы и человек. Но менее восприимчивы, чем кошки [4].
Сегодня практически не существует эффективных профилактических или лечебных мероприятий, которые доказали бы свою пригодность при устранении НПВП-индуцированных энтеропатий.
Одним из таких мероприятий может стать применение новых лекарственных форм препаратов, например таких как желатиновые пленки (рис.1).
Рис. 1 – Пленка желатиновая «Седатин», 10 мг
В настоящее время в ветеринарии используют множество различных форм лекарственных средств. Все большее внимание привлекают такие формы лекарственных средств, применение которых обеспечивает создание в поражённых тканях наибольшей концентрации лекарственного вещества и в тоже время приводит к ослаблению негативного воздействия на весь организм в целом.
Лекарственные желатиновые плёнки – это лекарственная форма, предназначенная для нанесения на слизистые оболочки, кожу. При контакте с влажной поверхностью проявляется адгезивное действие желатина, что обеспечивает прочную фиксацию пленки в заданной зоне. Реализуется направленная доставка лекарственных веществ в патологический очаг или близлежащую область, что позволяет достичь терапевтический эффект дозами, составляющими 1/10 или 1/20 средней терапевтической дозы [1].
Желатиновые пленки – это инновационный и удобный способ введения лекарственных средств в ветеринарии. Использование пленок в ветеринарии предполагает простоту применения, а их состав и форма обеспечивают быструю всасываемость препарата. Помимо этого пленки обладают рядом других преимуществ:
-значительное уменьшение разовой и курсовой дозы лекарственного вещества при сохранении его терапевтического эффекта,
-исключение либо значительное ослабление побочных эффектов,
-высокая степень безопасности лечения,
-быстрое достижение и длительное поддержание на постоянном уровне терапевтической концентрации лекарственных веществ в патологическом очаге,
-сокращение числа приёмов препарата в связи с длительностью действия,
-безболезненность применения,
-экономическая доступность [1].
Выводы:
Такие лекарственные системы, как желатиновые пленки, способны обеспечить быстрое, удобное и безопасное введение лекарственных веществ животным и существенно снизить уровень возникновения нежелательных побочных эффектов.
Список литературы / References
- Карамян А.С., Обидченко Ю.А. Современные неинвазивные терапевтические системы //Ветеринарная практика.- -№ 1.- С.44-47.
- Блакер Р., Гемици Б., Манко А., Уоласс Дж. НПВС- гастроэнтеропатии: новые аспекты патогенеза и терапии//Современный фармокологическое мнение.- -№19.- С. 11-16.
- Буч Куканич, Тара Бидгуд, Оливер Неслджи. Клиническая фармокология нестероидных противовоспалительных препаратов для собак // Ветеринарная анестезия и анальгезия.-2012.-№39.- С.69-90.
- Элиот Дж., Пурмалис А., Вандермеер Д., Денлингер Р. Пропионовая кислота. Разновидности токсинов в жкт //Токсикологическая патология.-1988.-№16.- С.245-260.
- Кэрол Метьюс, Питер Кронен, Дункан Ласцелс. Рекомендации по диагностике, оценке и лечению боли //Практика терапии мелких домашних животных. -2014.- №55.- С. 1-55.
- Мартин Тейчерт, Фабиен Гриенс, Эдгар Буджс, Мишель Венсинг и Питер Де Сме. Эффективность применения фармацевтических групп препаратов в снижении рисков развития побочных эффектов со стороны желудочно-кишечного тракта при применении неспецифических нестероидных противовоспалительных препаратов // Фармэпидемиология и безопасность лекарственных средств. -2014.-№23.- С.382-389.
- Ради З. Патогистологическая оценка блокады Циклооксигеназы (ЦОГ) на живых моделях // Токсикологическая патология.-2009.-№37.-С.34-46.
Список литературы на английском языке / References in English
- Karamyan A.S., Obidchenko Yu.A., Sovremennie neinvazivnie terapevticheskie sistemy [Modern noninvasive therapeutic systems] // Veterinarnaya praktika [Veterinary practice]. – 2013. #1. P. 44-47. [in Russian]
- Blakler R., Gemici B., Manko A., Uolass Dzh. NPVS- gastroenteropatii: novye aspekty patogeneza i terapii [NSAID-gatroenteropathy: new aspects of pathogenesis and prevention] //Sovremennoe farmokologicheskoe mnenie [Current opinion in pharmacology]. – 2014. #19. P. 11-16.
- Buch Kukanich, Tara Bidgud, Oliver Nesldzhi. Klinicheskaja farmokologija nesteroidnyh protivovospalitel’nyh preparatov dlja sobak [Clinical pharmacology of nonsteroidal anti-inflammatory drugs in dogs] // Veterinarnaja anestezija i anal’gezija [Veterinary Anaesthesia and Analgesia]. – 2012. #39. P.69-90.
- Jeliot Dzh., Purmalis A., Vandermeer D., Denlinger R. Propionovaja kislota. Raznovidnosti toksinov v zhkt [The propionis acid] // Toksikologicheskaja patologija [Gastrointestinal toxities and various species]. -1988. #16. P.245-260.
- Kjerol Met’jus, Piter Kronen, Dunkan Lascels. Rekomendacii po diagnostike, ocenke i lecheniju boli [Guidelines for recognition, assessment and treatment of pain] // Praktika terapii melkih domashnih zhivotnyh [Journal of Small Animal Practice]. – 2014. #55. P. 1-55.
- Martin Tejchert, Fabien Griens, Jedgar Budzhs, Mishel’ Vensing i Piter De Sme. effektivnost’ primenenija farmacevticheskih grupp preparatov v snizhenii riskov razvitija pobochnyh jeffektov so storony zheludochno-kishechnogo trakta pri primenenii nespecificheskih nesteroidnyh protivovospalitel’nyh preparatov [Effectiveness of interventions by community pharmacists to reduce risk of gastrointestinal side effects in nonselective nonsteroidal anti-inflammatory drug users] // Farmacoepidemiologija i bezopasnost’ lekarstvennyh sredstv [Pharmacoepidemiology and drug safety]. -2014. #23. P.382-389.
- Radi Z. Patogistologicheskaja ocenka blokady Ciklooksigenazy (COG) na zhivyh modeljah [Pathophysiology of cyclooxygenase inhibition in animal models] //Toksikologicheskaja patologija [Toxicologic pathology]. -2009. #37. P.34-46.
Механизмы действия НПВП при обезболивании
Ранг HP, Беван С., Дрей А. Химическая активация ноцицептивных периферических нейронов. Br Med Bull 1991; 47: 534–48
PubMed CAS Google ученый
Дрей А. Воспалительные медиаторы боли. Br J Anaesth 1995; 75: 125–31
PubMed CAS Google ученый
Вульф CJ.Последние достижения в патофизиологии острой боли. Br J Anaesth 1989; 63: 139–46
PubMed Статья CAS Google ученый
Вульф CJ. Генерация острой боли: центральные механизмы. Br Med Bull 1991; 47: 523–33
PubMed CAS Google ученый
Даль Дж., Кехлет Х. Нестероидные противовоспалительные препараты: обоснование использования при сильной послеоперационной боли.Br J Anaesth 1991; 66: 703–12
PubMed Статья CAS Google ученый
Даль Дж., Кехлет Х. Значение упреждающей анальгезии в лечении послеоперационной боли. Br J Anaesth 1993; 70: 434–9
PubMed Статья CAS Google ученый
Бьоркман Р. Центральные антиноцицептивные эффекты нестероидных противовоспалительных препаратов и парацетамола.Acta Anaesthesiol Scand 1995; 39 Дополнение. 103: 1–44
Google ученый
Ferreira SH. Воспалительная боль, гипералгезия простагландинов и развитие периферических анальгетиков. Trends Pharmacol Sci 1981; 2: 183–6
Статья CAS Google ученый
Раджа С., Мейер Р.А., Кэмпбелл Дж. Периферические механизмы соматической боли. Анестезиология 1988; 68: 571–90
PubMed Статья CAS Google ученый
Иордания CC. Анатомо-физиологические аспекты восприятия боли. В: Кауфман Л., редактор. Обзор анестезии 2. Эдинбург: Черчилль Ливингстон, 1984: 87–107
Google ученый
Бессон Дж. М., Чауш А. Периферические и спинномозговые механизмы ноцицепции. Physiol Rev 1987; 67: 67–186
PubMed CAS Google ученый
Дэвис С.Н., Лодж Д.Доказательства участия рецепторов N-метил-D-аспартата в «завороте» нейронов класса 2 в спинном роге крысы. Brain Res 1987; 424: 402–6
PubMed Статья CAS Google ученый
Кодерре Т.Дж., Мелзак Р. Вклад возбуждающих аминокислот в центральную сенсибилизацию и стойкую ноцицепцию после повреждения тканей, вызванного формалином. J Neurosci 1992; 12: 3665–70
PubMed CAS Google ученый
Vane JR, Botting RM. Механизм действия противовоспалительных препаратов. Postgrad Med J 1990; 66 Дополнение 4: С2–17
PubMed CAS Google ученый
Дрей А., Беван С. Воспаление и гипералгезия: акцент на коллективных усилиях. Trends Pharmacol Sci 1993; 14: 287–90
PubMed Статья CAS Google ученый
Ватанабе М., Ямаде М., Муэ С. и др.Усиление ингибиторами циклооксигеназы продукции фактора активации тромбоцитов в макрофагах, стимулированных тапсигаргином. Br J Pharmacol 1995; 116: 2141–7
PubMed Статья CAS Google ученый
Ferreira SH, Moncada S, Vane JR. Индометацин и аспирин отменяют высвобождение простагландина из селезенки. Nature 1971; 231: 237–9
Статья CAS Google ученый
Vane JR. Подавление синтеза простагландинов как механизм действия аспириноподобных препаратов. Природа (New Biol) 1971; 231: 232–5
CAS Google ученый
Ferreira SH. Периферическая анальгезия: механизм обезболивающего действия аспириноподобных препаратов и антагонистов опиатов. Br J Clin Pharmacol 1980; 10: 237S – 45S
PubMed Статья Google ученый
Ferreira SH. Простагландины, аспириноподобные препараты и обезболивающие. Природа (New Biol) 1972; 240: 200–3
Статья CAS Google ученый
Хиггс GA. Метаболизм арахидоновой кислоты, боль и гипералгезия: механизм действия нестероидных анальгетиков. Br J Clin Pharmacol 1980; 10: 233S – 5S
PubMed Статья Google ученый
Хиггс Г.А., Хиггс Е.А., Лосось Д.А.Простациклин при воспалении. В: Vane JR, Bergstrom S, редакторы. Простациклин. Нью-Йорк: Raven Press, 1979: 187–92
Google ученый
Хиггс Г.А., Лосось Д.А., Хендерсон Б. и др. Фармакокинетика аспирина и салицилата в отношении ингибирования арахидонатциклооксигеназы и противовоспалительной активности. Proc Natl Acad Sci USA 1987; 84: 1417–20
PubMed Статья CAS Google ученый
Земли WEM. Действия противовоспалительных препаратов. Trends Pharmacol Sci 1981; 2: 78–80
Статья CAS Google ученый
Rome LH, Lands WEM. Структурные требования для зависящего от времени ингибирования биосинтеза простагландинов противовоспалительными препаратами. Proc Natl Acad Sci USA 1975; 72: 4863–5
PubMed Статья CAS Google ученый
Цай А.Л., Кульмач Р.Дж., Палмер Г. Спектроскопические доказательства реакции тирозильного радикала простагландин-Н-синтазы-1 с арахидоновой кислотой. J Biol Chem 1995; 270: 10503–8
PubMed Статья CAS Google ученый
Hemler M, Lands WEM. Доказательства инициируемого перекисью свободнорадикального механизма биосинтеза простагландинов. J Biol Chem 1980; 255: 6253–61
PubMed CAS Google ученый
Lands WEM, Cook HW, Rome LH. Биосинтез простагландинов: последствия механизмов оксигеназы на in vitro анализах эффективности лекарств. Adv Prostaglandin Thromboxane Leukot Res 1976; 1: 7–17
CAS Google ученый
Vane JR, Flower RJ, Botting RM. Механизм действия аспирина. В: Vane JR, Botting RM, редакторы. Аспирин и другие салицилаты. Лондон: Chapman & Hall Medical, 1992: 35–59
Google ученый
Рот GJ, Majerus PW. Механизм действия аспирина на тромбоциты человека. 1. Ацетилирование белка фракции твердых частиц. J Clin Invest 1975; 56: 624–32
PubMed Статья CAS Google ученый
Roth GJ, Stanford N, Majerus PW. Ацетилирование простагландм-синтазы аспирином. Proc Natl Acad Sci USA 1975; 72: 3073–6
PubMed Статья CAS Google ученый
Kulmacz RJ, Lands WEM. Стоихометрия и кинетика взаимодействия простагландин H-синтазы с противовоспалительными средствами. J Biol Chem 1985; 260: 12572–8
PubMed CAS Google ученый
Picot D, Loll PJ, Garavito RM. Рентгеновская кристаллическая структура мембранного белка простагландина H 2 синтаза-1. Nature 1994; 367: 243–9
PubMed Статья CAS Google ученый
Loll PJ, Picot D, Garavito RM. Структурная основа активности аспирина определяется кристаллической структурой инактивированной простагландин H 2 синтазы. Nat Struct Biol 1995; 2: 637–43
PubMed Статья CAS Google ученый
Kulmacz RJ. Топография простагландин H-синтазы: противовоспалительные агенты и протеазочувствительная область аргинина 253. J Biol Chem 1989; 264: 14136–44
PubMed CAS Google ученый
Митчелл А., Акарасеринонт П., Тирманн С. и др. Селективность нестероидных противовоспалительных препаратов как ингибиторов конститутивной и индуцибельной циклооксигеназы. Proc Natl Acad Sci USA, 1993; 90: 11693–7
PubMed Статья CAS Google ученый
Vane JR, Mitchell JA, Appleton I, et al. Индуцируемые изоформы циклооксигеназы и синтазы оксида азота при воспалении. Proc Natl Acad Sci USA 1994; 91: 2046–50
PubMed Статья CAS Google ученый
Се В., Робертсон Д.Л., Симмонс Д.Л. Митоген-индуцируемая простагландин-G / H-синтаза: новая мишень для нестероидных противовоспалительных препаратов. Drug Dev Res 1992; 25: 249
Статья CAS Google ученый
Джонс Д.А., Карлтон Д.П., Макинтайр TM и др. Молекулярное клонирование эндопероксидсинтазы простагландина типа II человека и демонстрация экспрессии в ответ на цитокины. J Biol Chem 1993; 268: 9049–54
PubMed CAS Google ученый
Коулман Р.А., Смит В.Л., Наримия С. Классификация простаноидных рецепторов: свойства, распределение и структура рецепторов и их подтипов. Pharmacol Rev 1994; 46: 205–29
PubMed CAS Google ученый
Зайберт К., Жинаг Ю., Лихи К. и др. Фармакологическая и биохимическая демонстрация роли циклооксигеназы 2 в воспалении и боли. Proc Natl Acad Sci USA 1994; 91: 12013–7
PubMed Статья CAS Google ученый
Hla T, Нильсон К. кДНК циклооксигеназы-2 человека. Proc Natl Acad Sci USA 1992; 89: 7388–9
Статья Google ученый
Rang HP, Urban L. Новые молекулы в анальгезии. Br J Anaesth 1995; 75: 145–56
PubMed CAS Google ученый
Панара М.Р., Греко А, Сантини Дж. И др. Эффекты новых противовоспалительных соединений, N- [2- (циклогексилокси) -4-нитрофенил] метансульфонамида (NS-398) и 5-метансульфонамидо-6- (2,4-дифтортиофенил) -1-ин-данон (L -745,337), на циклооксигеназную активность простагландин-эндопероксидсинтаз крови человека.Br J Pharmacol 1995; 116: 2429–34
PubMed Статья CAS Google ученый
Маккормак К. Нестероидные противовоспалительные препараты и ноцицептивная обработка позвоночника. Pain 1994; 59: 9–43
PubMed Статья CAS Google ученый
Vane JR. К лучшему аспирину. Nature 1994; 367: 215–6
PubMed Статья CAS Google ученый
Anon. Сделают ли новые лекарства ненужными старые НПВП? Pharm J 1995; 255: 537
Hayllar J, Bjarnason I. НПВП, ингибиторы Цокс-2 и кишечник. Lancet 1995; 346: 521–2
PubMed Статья CAS Google ученый
Бойс С., Чан С., Гордон Р. и др. Селективный ингибитор циклооксигеназы-2 вызывает антиноцицепцию, но не желудочную секрецию у крыс. Neuropharm 1994; 33: 1609–11
Статья CAS Google ученый
Вейн Дж. НПВП, ингибиторы Цокс-2 и кишечник [буква]. Lancet 1995; 346: 1105–6
PubMed Статья CAS Google ученый
Ku EC, Lee W., Kothari HV, et al. Влияние диклофенака натрия на каскад арахидоновой кислоты. Am J Med 1986; 80 Дополнение 4B: 18–23
PubMed Статья CAS Google ученый
O’Neil LAJ, Lewis GP. Подавляющее действие диклофенака и индометацина на вызванные интерлейкином-1 изменения высвобождения PGE2.Biochem Pharmacol 1989; 38: 3707–11
Статья Google ученый
Абрамсон С., Корчак Х.М., Людвиг Р. и др. Способы действия аспириноподобных препаратов. Proc Natl Acad Sci USA 1985; 82: 7227–31
PubMed Статья CAS Google ученый
Минта Дж. О., Уильямс Мэриленд. Некоторые нестероидные противовоспалительные препараты подавляют образование супероксидных анионов активированными полиморфами, блокируя взаимодействия лиганд-рецептор.J Rheumatol 1985; 12: 751–7
PubMed CAS Google ученый
Брукс PM, Day RO. Нестероидные противовоспалительные препараты — различия и сходства. NEngl J Med 1991; 324: 1716–25
Статья CAS Google ученый
Лим Л.К., Хант Н.Х., Эйхнер Р.Д. и др. Циклический АМФ и регуляция выработки простагландинов макрофагами. Biochem Biophys Res Commun 1983; 114: 248–54
PubMed Статья CAS Google ученый
Абрамсон С.Б., Вайсманн Г. Механизмы действия нестероидных противовоспалительных препаратов. Arthritis Rheum 1989; 32: 1–9
PubMed Статья CAS Google ученый
Brune K, Beck WS, Geisslinger G, et al. Аспириноподобные препараты могут блокировать боль независимо от подавления синтеза простагландинов. Experientia 1991; 47: 257–61
PubMed Статья CAS Google ученый
Маккормак К., Брун К. Диссоциация между антиноцицептивными и противовоспалительными эффектами нестероидных противовоспалительных препаратов: обзор их анальгетической эффективности. Наркотики 1991; 41: 533–47
PubMed Статья CAS Google ученый
Маккормак К. Спинальное действие нестероидных противовоспалительных препаратов и диссоциация между их противовоспалительным и обезболивающим действием. Наркотики 1994; 47 Дополнение.5: 28–45
PubMed Статья CAS Google ученый
Hunskaar S. Аналогичные эффекты ацетилсалициловой кислоты и морфина на немедленную реакцию на острую токсическую стимуляцию. Pharmacol Toxicol 1987; 60: 167–70
PubMed Статья CAS Google ученый
Карлссон К. Х., Мангель В., Юрна И. Депрессия из-за морфина и неопиоидных анальгетиков, метамизола (дипирона), ацетилсалицилата лизина и парацетамола, активности в нейронах таламуса крысы путем электрической стимуляции ноцицепции.Pain 1988; 32: 313–26
PubMed Статья CAS Google ученый
Юрна И., Брюн К. Центральное действие нестероидных противовоспалительных агентов, индометацина, ибупрофена и диклофенака, определяемое по активности, вызванной С-волокном в отдельных нейронах таламуса крысы. Pain 1990; 41: 71–80
PubMed Статья CAS Google ученый
Ван BC, Ли Д., Хиллер Дж.Антиноцицептивный эффект S — (+) — ибупрофена у кроликов: эпидуральное или внутривенное введение. Anesth Analg 1995; 80: 92–6
PubMed CAS Google ученый
Мур Ю.Дж., Марш В.Р., Эштон С.Х. и др. Влияние анальгетиков периферического и центрального действия на соматосенсорные вызванные потенциалы. Br J Clin Pharmacol 1995; 40: 111–7
PubMed Статья CAS Google ученый
Девогель Дж.С. Небольшие интратекальные дозы лизин-ацетилсалицилата уменьшают трудноизлечимую боль у человека. J Int Med Res 1983; 11: 90–1
PubMed CAS Google ученый
Hougaard K, Nilsson B, Wieloch T. Ингибиторы циклооксигеназы жирных кислот и регуляция мозгового кровотока. Acta Physiol Scand 1983; 117: 585–7
PubMed Статья CAS Google ученый
Веннмальм Р., Карлссон А., Эдлунд А. и др. Центральные и периферические гемодинамические эффекты нестероидных противовоспалительных препаратов у человека. Arch Toxicol Suppl. 1984; 7: 350–9
PubMed Статья CAS Google ученый
Абдель-Халим М.С., Шоквист Б., Анггард Э. Ингибирование синтеза простагландинов в головном мозге крысы. Acta Pharmacol Toxicol 1978; 43: 266–72
Статья CAS Google ученый
Attal N, Kayser V, Eschalier A, et al. Поведенческие и электрофизиологические доказательства обезболивающего действия нестероидного противовоспалительного средства, диклофенака. Pain 1988; 35: 341–8
PubMed Статья CAS Google ученый
Martini A, Bondiolotti GP, Sacerdote P, et al. Диклофенак увеличивает концентрацию бета-эндорфина в плазме крови. J Int Med Res 1984; 12: 92–5
PubMed CAS Google ученый
Saccerdote P, Monza G, Mantegazza P и др. Диклофенак и пирпрофен изменяют концентрацию бета-эндорфина в гипофизе и гипоталамусе. Pharmacol Res Commun 1985; 17: 679–84
Статья Google ученый
Вескови П., Пассери М., Герра Г. и др. Налоксон подавляет раннюю фазу обезболивания диклофенаком у человека. Клиника боли 1987; 19: 151–5
Google ученый
Groppetti A, Braga PC, Biella G, et al. Влияние аспирина на серотонин и мет-энкафалин в головном мозге: корреляция с антиноцицептивной активностью препарата. Neuropharmacol 1988; 27: 499–505
Статья CAS Google ученый
Домер Ф. Характеристика анальгетической активности кеторолака у мышей. Eur J Pharmacol 1990; 177: 127–35
PubMed Статья CAS Google ученый
Герра Г., Вескови П.П., Пецзаросса А. и др. Успешное лечение синдрома отмены опиатов с помощью ацетилсалицилата лизина. Current Ther Res 1983; 33: 733–9
Google ученый
Герра Дж., Серезини Дж., Растелли Дж. И др. Влияние диклофенака на синдром отмены опиатов. Giornale Clin Med 1985; 66: 459–60
CAS Google ученый
Смуллин Д.Х., Скиллинг С.Р., Ларсон А.А.Взаимодействие между веществом P, пептидом, связанным с геном кальцитонина, таурином и возбуждающими аминокислотами в спинном мозге. Pain 1990; 42: 93–101
PubMed Статья CAS Google ученый
Malmberg AB, Yaksh TL. Гипералгезия, опосредованная глутаматом спинного мозга или рецептором вещества P, блокируется ингибированием спинномозговой циклооксигеназы. Science 1992; 257: 1276–9
PubMed Статья CAS Google ученый
Мальмберг AB, Якш TL. Антиноцицептивное действие спинномозговых нестероидных противовоспалительных агентов на формалиновый тест на крысах. J Pharmacol Ther 1992; 263: 136–46
CAS Google ученый
Malmberg AB, Yaksh TL. Антиноцицепция, вызванная спинальной доставкой S- и R-энантиомеров флурбипрофена в формалиновом тесте. Eur J Pharmacol 1994; 256: 205–9
PubMed Статья CAS Google ученый
Hunskaar S, Fasmer OB, Hole K. Ацетилсалициловая кислота, парацетамол и морфин подавляют поведенческую реакцию на вещество P или капсаицин, вводимое интратекально. Life Sci 1985; 37: 1835–41
PubMed Статья CAS Google ученый
Day RO, Williams KM, Graham GG, et al. Стереоселективное расположение энантиомеров ибупрофена в синовиальной жидкости. Clin Pharmacol Ther 1988; 43: 480–7
PubMed Статья CAS Google ученый
McCormack K, Urquhart E. Корреляция между эффективностью нестероидных противовоспалительных препаратов в модели клинической боли и диссоциацией их противовоспалительных и обезболивающих свойств в моделях на животных. Clin Drug Invest 1995; 9: 88–97
Статья CAS Google ученый
Напроксен: применение, взаимодействие, механизм действия
Напроксен — это НПВП, применяемый для лечения ревматоидного артрита, остеоартрита, анкилозирующего спондилита, полиартикулярного ювенильного идиопатического артрита, острого буриопатического идиопатического артрита. и от легкой до умеренной боли.
Aleve, Aleve PM, Aleve-D, Anaprox, EC-Naprosyn, Naprelan, Naprosyn, Sallus, Sudafed Sinus & Pain, Treximet, Vimovo
Напроксен классифицируется как нестероидное противовоспалительное средство (НПВП) и первоначально был одобрен для использования по рецепту в 1976 году, а затем для безрецептурного (OTC) использования в 1994 году. 3 Он может эффективно управлять острой болью, а также болью, связанной с ревматическими заболеваниями, и имеет хорошо изученный профиль побочных эффектов. 5 Учитывая его общую переносимость и эффективность, напроксен можно считать препаратом первой линии для различных клинических ситуаций, требующих обезболивания. 5 Напроксен доступен в формах как с немедленным, так и с отсроченным высвобождением, в комбинации с суматриптаном для лечения мигрени и в комбинации с эзомепразолом для снижения риска развития язвы желудка. 12 13 15 16
- Вес
- Среднее значение: 230,2592
Моноизотопное: 230,09 4294314 O Химическая формула 9019 9019 9019 9019 3
- (+) — (S) -6-Метокси-α-метил-2-нафталинуксусная кислота
- (+) — (S) -Напроксен
- (+) — 2- ( 6-Метокси-2-нафтил) пропионовая кислота
- (+) — 2- (Метокси-2-нафтил) пропионовая кислота
- (+) — 2- (Метокси-2-нафтил) пропионовая кислота
- (+) -Напроксен
- (S) — (+) — 2- (6-Метокси-2-нафтил) пропионовая кислота
- (S) — (+) — Напроксен
- (S) -2- (6-Метокси-2 -нафтил) пропановая кислота
- (S) -2- (6-Метокси-2-нафтил) пропионовая кислота
- (S) -6-Метокси-альфа-метил-2-нафталинуксусная кислота
- (S) -Напроксен
- Напроксен
- Напроксен 9 0002 Напроксен
- Напроксен
- Напроксен
Напроксен показан для лечения ревматоидного артрита, остеоартрита, остеоартрита, остеоартрита, артрита, артрита и полифенопатии. , а также для облегчения боли от легкой до умеренной. 12 13 3 Кроме того, это терапия первой линии для лечения остеоартрита, острого подагрического артрита, дисменореи, а также воспаления и боли опорно-двигательного аппарата. 3
Снижение количества неудач при разработке лекарств
Создание, обучение и проверка моделей машинного обучения с использованием структурированных наборов данных, основанных на фактических данных.
Создавайте, обучайте и проверяйте прогнозные модели машинного обучения с помощью структурированных наборов данных.
Избегайте опасных для жизни побочных эффектов лекарственных препаратов
Улучшите поддержку принятия клинических решений с помощью информации о противопоказаниях и предупреждениях «черного ящика», ограничениях населения, вредных рисках и многом другом.
Избегайте опасных для жизни побочных эффектов лекарств и улучшайте поддержку принятия клинических решений.
Напроксен — признанный неселективный НПВП, который полезен как болеутоляющее, противовоспалительное и жаропонижающее средство. 5 Подобно другим НПВП, фармакологическая активность напроксена может быть связана с ингибированием циклооксигеназы, которая, в свою очередь, снижает синтез простагландинов в различных тканях и жидкостях, включая синовиальную жидкость, слизистую оболочку желудка и кровь. 5
Хотя напроксен является эффективным анальгетиком, он может оказывать непреднамеренное вредное воздействие на пациента. Например, напроксен может отрицательно влиять на контроль артериального давления. 10 Исследование показало, что употребление напроксена вызывает повышение артериального давления, хотя это повышение не было таким значительным, как при использовании ибупрофена. 10
Кроме того, исследования показали, что риск кровотечения из верхних отделов желудочно-кишечного тракта в среднем в четыре раза выше у лиц, принимающих НПВП. 11 Другие факторы, повышающие риск кровотечения из верхних отделов желудочно-кишечного тракта, включают одновременный прием кортикостероидов или антикоагулянтов, а также язвы желудочно-кишечного тракта в анамнезе. 11
Как и другие неселективные НПВП, напроксен оказывает свое клиническое действие, блокируя ферменты ЦОГ-1 и ЦОГ-2, что приводит к снижению синтеза простагландинов. 3 Хотя оба фермента участвуют в производстве простагландинов, они имеют уникальные функциональные различия. 3 Ферменты ЦОГ-1 являются конститутивно активными и могут быть обнаружены в нормальных тканях, таких как слизистая оболочка желудка, в то время как фермент ЦОГ-2 является индуцибельным и производит простагландины, которые опосредуют боль, жар и воспаление. 4 Фермент ЦОГ-2 обеспечивает желаемые жаропонижающие, обезболивающие и противовоспалительные свойства, предлагаемые напроксеном, в то время как нежелательные побочные эффекты, такие как желудочно-кишечные расстройства и почечная токсичность, связаны с ферментом ЦОГ-1. 4
Напроксен доступен в виде свободной кислоты и натриевой соли. 5 При сопоставимых дозах (500 мг напроксена = 550 мг напроксена натрия) они немного различаются по скорости абсорбции, но в остальном они терапевтически и фармакологически эквивалентны. 5 Напроксен натрия достигает пиковой концентрации в плазме через 1 час, в то время как максимальная концентрация в плазме наблюдается через 2 часа с напроксеном (свободная кислота). 5 Нет различий между двумя формами в фармакокинетике постабсорбционной фазы. 5 При лечении острой боли следует учитывать разницу в начальной абсорбции, поскольку напроксен натрия может вызвать более быстрое начало действия. 5
Средняя Cmax для различных составов (немедленное высвобождение, энтеросолюбильное покрытие, контролируемое высвобождение и т. Д.) Напроксена сопоставимы и колеблются от 94 мкг / мл до 97,4 мкг / мл. 12 13 В одном фармакокинетическом исследовании средняя Tmax напроксена 500 мг (немедленное высвобождение), вводимого каждые 12 часов в течение 5 дней, составила 3 часа, по сравнению со средней Tmax 5 часов для Naprelan 1000 мг (контролируемое высвобождение), введенного каждые 24 часа в течение 5 дней. 12 В этом же исследовании AUC 0-24 часа составляла 1446 мкг · час / мл для напроксена с немедленным высвобождением и 1448 мкг · час / мл для состава с контролируемым высвобождением. 12 В отдельном исследовании, сравнивающем фармакокинетику таблеток напросина и EC-Naprosyn, наблюдались следующие значения: Tmax и AUC 0-12 часов EC-Naprosyn составляли 4 часа и 845 мкг · час / мл соответственно, а Tmax и AUC 0- 12 часов значения Напросина составили 1,9 часа и 767 мкг · час / мл соответственно. 13
При приеме в комбинации с суматриптаном C напроксена примерно на 36% ниже по сравнению с таблетками напроксена натрия 550 мг, а среднее значение T max составляет 5 часов. 15
На основании AUC и C напроксена биоэквивалентными можно считать Вимово (комбинированный продукт напроксен / эзомепразол) и напроксен с энтеросолюбильным покрытием. 16
В целом напроксен быстро и полностью абсорбируется при пероральном и ректальном применении. 6 5 Пища может способствовать задержке всасывания напроксена, вводимого перорально, но не влияет на степень абсорбции. 5
Напроксен имеет объем распределения 0.16 л / кг. 12 13
Напроксен обладает высокой степенью связывания с белками, при этом> 99% препарата связывается с альбумином на терапевтических уровнях. 12 13
Напроксен интенсивно метаболизируется в печени и претерпевает как Фазу I, так и Фазу II метаболизма. 12 13 7 Первый этап включает деметилирование напроксена через CYP 1A2, 2C8 и 2C9 8 9 .И напроксен, и десметилнапроксен переходят в метаболизм фазы II; однако десметилнапроксен может образовывать как ацил, так и фенольные глюкурониды, тогда как напроксен производит только ацилглюкуронид. 8 7 Процесс ацилглюкуронизации включает UGT 1A1, 1A3, 1A6, 1A7, 1A9, 1A10 и 2B7, тогда как фенольная глюкуронидация катализируется UGT 1A1, 1A7,1A9 и 1A10. 8 Десметилнапроксен также подвергается сульфатации, которая опосредуется SULT 1A1, 1B1 и 1E1. 7
Наведите указатель мыши на продукты ниже, чтобы просмотреть партнеров по реакции
После перорального приема около 95% напроксена и его метаболитов могут быть восстановлены с мочой, при этом 66-92% извлекаются в виде конъюгированного метаболита и менее 1% извлекается в виде напроксена или десметилнапроксена. 7 12 13 Менее 5% напроксена выводится с калом. 12 13
Период полувыведения напроксена составляет 12-17 часов. 3 13
Напроксен очищается со скоростью 0,13 мл / мин / кг. 12 13
Улучшение поддержки принятия решений и результатов исследований
Со структурированными данными о побочных эффектах, включая: предупреждений в виде черного ящика, побочные реакции, предупреждения и меры предосторожности, а также показатели заболеваемости.
Улучшите поддержку принятия решений и результаты исследований с помощью наших структурированных данных о побочных эффектах.
Хотя доступность напроксена без рецепта (OTC) удобна для пациентов, она также увеличивает вероятность передозировки. 3 К счастью, степень передозировки обычно умеренная с побочными эффектами, обычно ограниченными сонливостью, летаргией, болью в эпигастрии, тошнотой и рвотой. 3 12 13 Хотя противоядия от передозировки напроксена не существует, симптомы обычно проходят при соответствующей поддерживающей терапии. 12 13 3
Напроксен классифицируется как Категория B в течение первых 2 триместров беременности и как Категория D в течение третьего триместра. 14 Напроксен противопоказан в 3 триместре, так как он увеличивает риск преждевременного закрытия артериального протока плода, и его следует избегать у беременных женщин, начиная с 30 недель беременности. 12 13
Текущие перспективы гастропатии, индуцированной НПВП
Нестероидные противовоспалительные препараты (НПВП) являются наиболее часто назначаемыми лекарствами в мире.Их обезболивающее, противовоспалительное и жаропонижающее действие может быть полезным; однако они связаны с серьезными побочными эффектами, включая повреждение желудочно-кишечного тракта и язвенную болезнь желудка. Хотя было принято несколько подходов к ограничению этих побочных эффектов, таких как использование препаратов, специфичных для ЦОГ-2, применение кислотоподавляющих средств, таких как ингибиторы протонной помпы и аналоги простагландина, эти альтернативы имеют ограничения с точки зрения эффективности и побочных эффектов. В этой статье был рассмотрен механизм действия НПВП и их критические желудочно-кишечные осложнения.В этой статье также представлена информация о различных профилактических мерах, предписываемых для минимизации таких побочных эффектов, и анализируются новые предлагаемые стратегии разработки новых лекарств для поддержания противовоспалительных функций НПВП наряду с эффективной защитой желудочно-кишечного тракта.
1. Введение
Нестероидные противовоспалительные препараты (НПВП) являются наиболее признанными во всем мире лекарствами для лечения боли, воспаления и лихорадки [1–4]. НПВП обычно назначают для лечения воспалительных заболеваний, ревматоидного артрита, остеоартрита, дисменореи и ишемических цереброваскулярных нарушений [5].Недавно также сообщалось об использовании этих препаратов для лечения некоторых видов рака [6, 7]. Эти препараты подавляют биосинтез простагландинов и оказывают терапевтическое действие [8]. Однако длительный прием НПВП вызывает неблагоприятные симптомы со стороны желудочно-кишечного тракта (ЖКТ), включая поражения слизистой оболочки, кровотечение, язвенную болезнь и воспаление в кишечнике, ведущие к перфорации, стриктурам в тонком и толстом кишечнике, что приводит к хроническим проблемам [9–11]. Некоторые из побочных эффектов НПВП могут быть асимптотическими, но во многих случаях имеются сообщения об опасных для жизни инцидентах [10].
Такое безудержное использование НПВП требует целенаправленного подхода, чтобы избежать возможных побочных эффектов, возникающих при их применении. В связи с этим было использовано несколько методов профилактики. Они основаны на использовании нового класса НПВП, которые не ингибируют специфический гастропротекторный каскад или совместную рецепцию с ингибиторами протонной помпы (ИПП) и аналогами простагландина для подавления секреции кислоты [12-15]. Однако эти методы также имеют ограниченную эффективность из-за их дополнительных сердечно-сосудистых эффектов [16–19].
В нескольких руководствах по клинической практике предложены различные подходы к контролю желудочно-кишечных осложнений, связанных с приемом НПВП. Американский колледж гастроэнтерологии рекомендовал ряд стратегий для уменьшения повреждения желудочно-кишечного тракта, вызванного НПВП, включая использование селективных ингибиторов циклооксигеназы-2, совместное введение гастропротективных агентов, таких как мизопростол, ИПП или антагонисты рецепторов гистамина-2 [20]. Эти стратегии основаны на множественных факторах риска, связанных с осложнениями желудочно-кишечного тракта, вызванными приемом НПВП, включая возраст пациента, одновременный прием лекарств, анамнез заболевания и инфекцию Helicobacter pylori .Риск желудочно-кишечного кровотечения увеличивается, когда пациентам, уже получающим антитромбоцитарную терапию с использованием тиенопиридинов, таких как клопидогрел, назначают одновременно НПВП для уменьшения неблагоприятных сердечно-сосудистых событий [21]. В 2008 г. в документе о консенсусе клинических экспертов, подготовленном Американским колледжем кардиологов, Американским колледжем гастроэнтерологии и Американской кардиологической ассоциацией, были установлены руководящие принципы по снижению травм желудочно-кишечного тракта у пациентов, проходящих антиагрегантную терапию вместе с НПВП [22]. Согласно руководящим принципам, ИПП были рекомендованы для гастропротекторной терапии пациентам, принимающим тиенопиридины и НПВП.Однако на основании некоторых отчетов, предполагающих возможное взаимодействие между ИПП и тиенопиридинами [23, 24], рекомендации экспертов были дополнительно обновлены в 2010 г. [25]. Консенсусный отчет экспертов был подготовлен с учетом потенциальных рисков и преимуществ одновременного приема ИПП и тиенопиридинов. Назначение ИПП рекомендуется только пациентам, получающим антитромбоцитарную терапию, которые подвержены риску желудочно-кишечных осложнений [25].
До сих пор не было разработано эффективного лечения для устранения повреждения желудка, связанного с НПВП.Выявление защитных факторов при желудочно-кишечных осложнениях, связанных с приемом НПВП, по-прежнему представляет собой серьезную проблему. В этой статье описывается механизм действия НПВП с их преобладающими побочными эффектами и дается представление о новых достижениях в рациональном использовании НПВП для предотвращения возможных побочных эффектов без какого-либо ущерба для анальгетических свойств НПВП.
2. Свойства НПВП
НПВП обладают некоторыми общими фармакологическими свойствами.В основном это органические кислоты с pKa в диапазоне 3–5 [5]. Как правило, они содержат кислотную группу, в основном карбоновые кислоты или енолы. Кислотная составляющая важна для ингибирующей активности COX и связана с плоской ароматической группой. Последний также связан с липофильной частью через полярную группу. НПВП классифицируются на различные группы в зависимости от их химической структуры и механизма действия (Таблица 1). НПВС, как правило, представляют собой хиральные молекулы (за исключением диклофенака), но в основном один энантиомер фармакологически активен [26].
| ||||||||||||||||||||||||||||||||||||||||||||
3.Механизм противовоспалительного действия НПВП
Механизм действия НПВП был впервые определен в начале семидесятых годов и основан на ингибировании синтеза простагландинов (ПГ) [8]. PG является одним из основных медиаторов воспаления, боли и лихорадки и синтезируется из арахидоновой кислоты. Реакция катализируется ферментом циклооксигеназой (ЦОГ), ранее называвшимся PGH-синтазой [5]. НПВП блокируют образование PG путем связывания и ингибирования ЦОГ (рис. 1).
Было продемонстрировано, что анальгетическая активность НПВП обусловлена взаимодействием PGE1 и PGF2 в моделях боли у животных [27, 28].Также было замечено, что НПВП эффективны против боли из-за их способности ингибировать PG-опосредованную вазодилатацию сосудов головного мозга [29, 30]. Несколько исследований показали, что жаропонижающее действие НПВП проявляется через ингибирование синтеза PGE2 в преоптической области гипоталамуса и вблизи нее в окжелудочковых органах [31–33].
4. Механизм повреждения желудочно-кишечного тракта, вызванного НПВП
Существует три основных механизма развития желудочно-кишечных осложнений, вызванных НПВП: ингибирование фермента ЦОГ-1 и гастропротекторных PG, мембранная проницаемость и выработка дополнительных провоспалительных медиаторов (рис. 2).
4.1. Ингибирование ЦОГ-1 и гастропротекторный PG
Существует две изоформы ЦОГ, ЦОГ-1 и ЦОГ-2, которые выполняют разные функции [34]. ЦОГ-1 экспрессируется конститутивно и отвечает за нормальную физиологическую защиту слизистой оболочки желудка. Он отвечает за синтез простагландинов, которые защищают слизистую оболочку желудка от секретируемой кислоты, поддерживают кровоток в слизистой оболочке желудка и вырабатывают бикарбонат [35, 36]. Другая изоформа, ЦОГ-2, запускается повреждением клеток, различными провоспалительными цитокинами и опухолевыми факторами [37, 38].Гастропатия, вызванная НПВП, в основном вызывается ингибированием ЦОГ-1 НПВП [39–41].
4.2. Мембранная проницаемость
НПВП также оказывают прямое цитотоксическое действие на клетки слизистой оболочки желудка, вызывая повреждения и повреждения [42, 43]. Некоторые исследования показали, что прямая цитотоксичность не зависит от ингибирования активности ЦОГ [44]. Местное повреждение такого рода наблюдалось в случае кислых НПВП, таких как аспирин, в результате накопления ионизированных НПВП, явление, называемое «захватом ионов» [45].Предполагается, что НПВП вызывают проницаемость мембран, что приводит к нарушению эпителиального барьера [46]. НПВП также способны вызывать некроз и апоптоз в клетках слизистой оболочки желудка [47].
4.3. Производство дополнительных провоспалительных медиаторов
Ингибирование синтеза PG NSAID ведет к одновременной активации пути липоксигеназы и усилению синтеза лейкотриенов (Рисунок 1) [48–50]. Лейкотриены вызывают воспаление и ишемию тканей, что приводит к повреждению слизистой оболочки желудка [51, 52].Наряду с этим также усиливается продукция провоспалительных медиаторов, таких как факторы некроза опухоли [53]. Это также приводит к закупорке микрососудов желудка, что приводит к снижению кровотока в желудке и высвобождению свободных радикалов, полученных из кислорода [54]. Свободные кислородные радикалы реагируют с полиненасыщенными жирными кислотами слизистой оболочки, что приводит к перекисному окислению липидов и повреждению тканей [54].
5. Современные методы лечения для предотвращения повреждения желудка
Было принято несколько подходов к предотвращению и лечению возможных побочных эффектов, вызываемых НПВП в кишечнике.Некоторые из этих стратегий обычно прописываются пациентам, принимающим НПВП. В настоящее время наиболее распространенными защитными стратегиями являются (1) комбинированная терапия НПВП с гастропротекторными агентами и (2) использование селективных ингибиторов ЦОГ-2 (таблица 2).
| ||||||||||||||||||||||||||||||||||||
5.1. Комбинированная терапия НПВП с гастропротекторными средствами
5.1.1. Аналоги PG
Аналоги PG назначаются вместе с НПВП для восполнения ПГ, которая ингибируется НПВП. Было обнаружено, что мизопростол, широко используемый аналог PG, значительно снижает вызванное НПВП гастродуоденальные язвы [12]. Однако он не может предотвратить снижение диспепсии и других побочных эффектов со стороны ЖКТ и, следовательно, имеет ограниченную эффективность [55, 56]. Недавно появились сообщения о том, что однократные формы диклофенака и мизопростола, которые оказались эффективными при артрите и уменьшении гастропатии, вызванной НПВП [57].
5.1.2. Подавители кислоты
Кислота увеличивает вызванное НПВП повреждение слизистой оболочки и абсорбцию кислых НПВП в желудке. Чаще всего используются антагонисты h3-рецепторов и ингибиторы протонной помпы (ИПП), поскольку они не только снижают секрецию кислоты, но также повышают pH желудочного сока и играют роль в улавливании свободных радикалов [58, 59].
Антагонистыh3-рецепторов были первыми препаратами, которые использовались в качестве профилактического механизма против язвенной болезни, вызванной НПВП [60]. Было обнаружено, что они в значительной степени эффективны против язвы желудка [61].Однако никаких признаков улучшения не наблюдалось в случаях желудочного кровотечения [62], и, следовательно, эти препараты больше не рекомендуются в настоящее время.
ИПП эффективны с точки зрения подавления кислотности и предотвращения язвенной болезни при одновременном применении с НПВП. ИПП обычно назначают для длительного применения, поскольку они не показывают значительного риска каких-либо сопутствующих эффектов [63, 64]. Омепразол, ИПП, широко назначаемый вместе с НПВП, может специфически блокировать париетальные клетки / -АТФазу, тем самым значительно подавляя секрецию кислоты желудочного сока [65].За омепразолом последовали другие ИПП, такие как лансопразол, пантопразол, рабепразол и т. Д. [66]. В другом сообщении указано, что лансопразол имеет форму быстро распадающихся таблеток для уменьшения повреждения желудочно-кишечного тракта [67]. Эзомепразол, S-изомер омепразола, обеспечивает устойчивый контроль над кислотностью желудочного сока по сравнению с другими ИПП [68]. У пациентов, которым назначали эзомепразол вместе с НПВП или селективными ингибиторами ЦОГ-2, наблюдалось значительное уменьшение неблагоприятных симптомов со стороны ЖКТ [69, 70].Первым одобренным препаратом в виде одной таблетки НПВП / ИПП являются капсулы с модифицированным высвобождением кетопрофена / омепразола [71].
Двойная антитромбоцитарная терапия тиенопиридином, например клопидогрелом, и НПВП, например аспирином, назначается для уменьшения неблагоприятных сердечных событий у пациентов, страдающих острым коронарным синдромом или установки интракоронарного стента [72, 73], но они связаны с высоким риском желудочно-кишечного кровотечения [72, 73]. 21]. Установлено, что ИПП эффективны в снижении риска желудочно-кишечного кровотечения у таких пациентов [23].Клопидогрель — это пролекарство, которое in vivo превращается в активный метаболит с помощью ферментной системы цитохрома P450 [74]. Однако в некоторых сообщениях предполагается, что ИПП препятствуют действию клопидогрела, нарушая функцию тромбоцитов [23, 24, 75]. ИПП, возможно, ингибируют изофермент цитохрома P450 2C19 (CYP2C19) печени, предотвращая превращение клопидогреля в его активный метаболит. Сообщалось, что одновременное применение клопидогреля и ИПП было связано со значительным увеличением риска неблагоприятных сердечно-сосудистых событий у пациентов с острым хроническим синдромом [76, 77].В отличие от этого, в некоторых других исследованиях не было обнаружено повышенного риска побочных эффектов при применении ИПП в сочетании с клопидогрелом [78, 79]. Таким образом, хотя рутинное использование ИПП не рекомендуется пациентам в целом, но оно назначается пациентам с потенциальным риском желудочно-кишечного кровотечения [25, 80].
Главный недостаток ИПП состоит в том, что они менее эффективны против повреждений слизистой оболочки в более дистальных частях кишечника, таких как колонопатия, вызванная НПВП [81]. Более того, эти препараты не назначают пациентам, страдающим от H.pylori из-за возникновения гастрита тела [82].
5.2. Селективные ингибиторы ЦОГ-2
Селективные ингибиторы ЦОГ-2, как следует из названия, представляют собой группу препаратов, которые избирательно ингибируют ингибиторы ЦОГ-2, таким образом сохраняя противовоспалительные свойства НПВП, но сохраняя гастропротекторное действие, вызываемое ЦОГ. -1 путь [83–85]. Безусловно, целекоксиб и рофекоксиб выделяются как наиболее эффективные ингибиторы ЦОГ-2 и показывают эффективность по сравнению с неселективными НПВП в отношении осложнений со стороны ЖКТ, включая поражения слизистой оболочки и другие неблагоприятные симптомы со стороны ЖКТ [86, 87].
Было идентифицировано несколько классов селективных ингибиторов ЦОГ-2, включая диарилгетероциклические (или трициклические), кислые сульфонамиды и 2,6-дитрет-бутилфенолы, а также производные неселективных ингибиторов зомепирака, индометацина, пироксикама. , и аспирин [88–90]. Целекоксиб был впервые идентифицирован в 1997 г. и одобрен в 1998 г. [91, 92]. Было обнаружено, что он преимущественно ингибирует ЦОГ-2, но проявляет противовоспалительную, жаропонижающую и анальгезирующую активность НПВП [86, 93, 94].Рофекоксиб, запущенный в 1999 г., оказался эффективным при лечении остеоартрита и боли [87, 95–97]. Точно так же нимесулид был высокоселективным в отношении ЦОГ-2, так что в концентрациях, достигнутых in vivo, хотя он не оказывал существенного влияния на ЦОГ-1, он значительно подавлял ЦОГ-2 [98].
Хотя ингибиторы ЦОГ-2 значительно снижают токсичность для желудочно-кишечного тракта, существует связанный с ними риск сердечно-сосудистых осложнений из-за инфаркта миокарда и тромбоза, связанного с их применением [99–104].Было показано, что ингибиторы ЦОГ-2 подавляют выработку простациклина в сосудах, который обладает сосудорасширяющим действием и подавляет агрегацию тромбоцитов, в отличие от неселективных НПВП [105, 106]. Более долгосрочные данные о желудочно-кишечном тракте из исследования целекоксиба (CLASS) и данные о побочных эффектах сердечно-сосудистой системы из исследования рофекоксиба (VIGOR) поставили под сомнение использование этих новых препаратов [86, 87, 107]. Некоторые из этих сильнодействующих препаратов даже были отменены [108].
6. Последние достижения в лечении НПВП
6.1. Пролекарства НПВП
Пролекарства НПВП являются потенциальными агентами для усиления антиоксидантной активности, растворимости и растворения в воде, высвобождения оксида азота и сероводорода, сайт-специфического нацеливания и доставки, а также ингибирования антихолинергической и ацетилхолинэстеразной активности [109–113].
6.1.1. НПВС, высвобождающие оксид азота
Было замечено, что оксид азота (NO) обеспечивает защиту желудка за счет увеличения кровотока, выработки слизи и секреции бикарбоната в слизистой оболочке желудка [114–116].NO, образующийся под действием синтазы оксида азота, увеличивает секрецию слизи и бикарбоната, а также микроциркуляцию и снижает адгезию нейтрофилов к эндотелию [117]. Это привело к разработке новых терапевтических препаратов: НПВП, высвобождающих оксид азота (NO-НПВП) [118]. Эти препараты разработаны путем модификации НПВП, этерифицированных до фрагмента, высвобождающего NO. Исследования на животных показали, что NO-НПВП не влияют на слизистую оболочку гастродуоденальной зоны [119–121]. Также было обнаружено, что NO напроксен усиливает противовоспалительную и антиноцицептивную эффективность [122].Было обнаружено, что NO аспирин обладает повышенной антитромботической активностью по сравнению с обычным аспирином [123, 124].
6.1.2. NSAID, высвобождающий сероводород
Сероводород (h3S) также оказывает свое гастропротекторное действие и обращает вспять уже существующие язвы. Сообщалось о производных напроксена, диклофенака и индометацина, которые могут высвобождать h3S [125–128]. Фосфатидилхолин-ассоциированные НПВП, а также НПВС, высвобождающие NO и h3S, проходят обширные доклинические испытания на предмет их влияния на желудочно-кишечную токсичность, вызванную НПВП [129, 130].
Продолжаются дальнейшие исследования по разработке новых многообещающих НПВП, обеспечивающих общую защиту ЖКТ (верхних и нижних трактов ЖКТ) и не оказывающих токсического воздействия на сердечно-сосудистую систему. Недавно было продемонстрировано, что пролекарство диклофенака, 1- (2,6-дихлорфенил) индолин-2-он, обладает противовоспалительными свойствами, которые могут снижать уровни PGE2, экспрессию COX-2 и образование язв [131]. В еще одном эксперименте было обнаружено, что R (-) изомер ибупрофена является лучшим средством для предотвращения токсичности GI, чем изомер S (+), из-за короткого периода полувыведения из плазмы, его ограниченной способности ингибировать синтез PG.Затем изомер R (-) превращается в организме в изомер S (+) после абсорбции в желудочно-кишечном тракте [132].
6.2. Одновременное ингибирование ЦОГ и 5-LOX
Ингибирование ЦОГ, вызванное НПВП, также приводит к увеличению продукции лейкотриенов, одного из мощных медиаторов воспаления [49–51]. Недавний подход к лечению повреждения желудочно-кишечного тракта, вызванного НПВП, заключается в одновременной разработке ингибиторов COX / 5-LOX [133, 134]. Ликофелон ([2,2-диметил-6- (4-хлорфени-7-фенил-2,3-дигидро-1H-пирразолин-5-ил] уксусная кислота) был определен как одно из наиболее убедительных соединений в этой группе. [135].Ликофелон оказывает значительное обезболивающее и противовоспалительное действие без каких-либо побочных эффектов со стороны желудочно-кишечного тракта, как это наблюдалось в моделях на животных [136]. Он значительно уменьшил язвы желудка, вызванные индометацином, и предотвратил вызванное НПВП повышение уровня лейкотриенов в слизистой оболочке желудка [137]. Доклиническая оценка показала, что ликофелон обладает многообещающим фармакодинамическим эффектом [138]. Дальнейшие клинические испытания у пациентов с остеоартритом продолжаются [139]. Ликофелон также оказался эффективным из-за его антитромботических функций и ингибирования агрегации тромбоцитов [140].Ранее беноксапрофен, идентифицированный как двойной ингибитор ЦОГ / 5-LOX, был отменен, поскольку было обнаружено, что он вызывает тяжелую печеночную и другие токсические эффекты [141].
6.3. Роль лактоферрина в снижении повреждения кишечника, вызванного НПВП
Некоторые предварительные отчеты показали, что бычье молозиво обладает способностью предотвращать язвы желудка, вызванные НПВП [142, 143]. Дальнейшие исследования продемонстрировали роль рекомбинантного человеческого лактоферрина в уменьшении острого желудочно-кишечного кровотечения, вызванного НПВП, и уменьшении язв желудка [144, 145].Недавние сообщения также предполагают, что C-доля лактоферрина, которая устойчива к ферментативной деградации [146], обладает превосходной изоляционной способностью для такого класса лекарств [147]. Дальнейшие сообщения показали, что C-доля лактоферрина также может связываться с лекарствами, специфичными для ЦОГ-2, и вызывать наблюдаемые эффекты против воспаления желудка и кровотечений [148]. Эксперименты на модели грызунов предполагают, что C-доля лактоферрина значительно снижает вызванное НПВП кровотечение и воспаление желудочно-кишечного тракта в случае обычных НПВП, а также ЦОГ-2-специфичных НПВП [147].В связи с этим разработка таких новых молекул, которые могут изолировать несвязанные молекулы лекарственного средства, имеет важное значение для устранения повреждения ЖКТ, связанного с НПВП.
7. Выводы
Терапевтические эффекты НПВП сделали эти препараты чрезвычайно популярными при воспалительных заболеваниях в течение последних нескольких десятилетий. Однако эти препараты страдают серьезными недостатками при длительном применении, включая тяжелые осложнения со стороны желудочно-кишечного тракта. Несколько стратегий были адаптированы для контроля критических побочных эффектов.Хотя эти методы лечения в некоторой степени эффективны, но большинство из них также связано с другими рисками.
Таким образом, еще не создано лекарственного средства, которое могло бы полностью предотвратить возможные побочные эффекты. Существует острая необходимость в разработке новых терапевтических агентов, чтобы сделать использование НПВП более безопасным. Новые меры лечения, такие как двойные ингибиторы ЦОГ / 5-LOX, пролекарства НПВП или агенты, которые могут эффективно изолировать несвязанные НПВП, не влияя на их эффективность, могут оказаться лучшими стратегиями по сравнению с существующими.
Благодарности
Авторы выражают признательность за финансовую поддержку Департаменту биотехнологии (DBT), Нью-Дели. Т. П. Сингх благодарит Департамент биотехнологии (DBT) за присуждение ему звания «Выдающийся профессор биотехнологических исследований». М. Синха благодарит Департамент науки и технологий (DST), Министерство науки и технологий, Нью-Дели, Л. Гаутам благодарит Совет научных и промышленных исследований (CSIR), Нью-Дели, а П.К. Шукла благодарит Индийский совет медицинских исследований (ICMR). ), Нью-Дели, для присуждения стипендий.
(PDF) Механизм действия нестероидных противовоспалительных препаратов
[28] Хунскаар С. Сходные эффекты ацетилсалициловой кислоты и морфина на немедленную реакцию
на острую ядовитую стимуляцию. Фармакология и токсикология. 1987; 60: 167-170
[29] Тегедер I, Нидербергер Э, Исрар Э, Гюринг Х., Брюн К., Эухенхофер С., Грёш С.,
Гейсслингер Г. Ингибирование активации NF-каппа B и AP-1 с помощью R- и S-турбипрофен.
Журнал FASEB.2001; 15: 595-597
[30] Bryant CE, Farneld BA, Janicke HJ. Оценка способности карпрофена и u-
никсин меглумин ингибировать активацию ядерного фактора каппа B. Американский журнал
Ветеринарные исследования. 2003; 64: 211-215
[31] Монниссами В.М., Кавимани С., Балу В., Дрлин QS. Оценка противовоспалительных и мембраностабилизирующих свойств
этанольного экстракта Canjera rehedi. Иранский журнал
Фармакология и терапия.2008; 6: 235-237
[32] Mancini JA, Riendeau D, Falgueyret JP, Vickers PJ, O’Neill GP. Аргинин 120 проста-
гландин G / H-синтаза-1 необходим для ингибирования нестероидными анти-гамма-
торическими препаратами, содержащими фрагмент карбоновой кислоты. Журнал биологической химии.
1995; 270: 29372-29377
[33] Stanford N, Roth GJ, Shen TY, Majerus PW. Отсутствие ковалентной модификации проста-
гландин-синтетазы (циклооксигеназы) индометацином.Простагландины. 1977; 13: 669-675
[34] Курумбаил Р., Стивенс А., Гирсе Дж., Макдональд Дж., Стегеман Р.А., Пак Дж. Ю., Гильдехаус Д.,
Мияширо Дж. М., Пеннинг Т.Д., Зайберт К., Исаксон П.К., Столлингс WC. Структурная основа
для селективного ингибирования циклооксигеназы-2 противовоспалительными средствами. Природа.
1996; 384: 644-648
[35] Асако Х., Кубес П., Уоллес Дж., Гагинелла Т., Вольф RE, Грейнджер Д.Н. Индометацин-индуцированная адгезия
лейкоцитов в брыжеечных венулах: роль продуктов липоксигеназы.Американский
журнал физиологии. 1992; 262: G903-G908
[36] Асако Х., Кубес П., Уоллес Дж., Вольф Р. Э., Грейнджер Д. Н.. Модуляция адгезии лейкоцитов
к брыжеечным венулам крысы аспирином и салицилатом. Гастроэнтерология. 1992; 103 (1): 146-152
[37] Wallace JL, McKnight W., Miyasaka M, Tamatani T, Paulson J, Anderson DC, Granger
DN, Kubes P. Роль молекул эндотелиальной адгезии в индуцированных НПВС слизистая желудка —
травма. Американский журнал физиологии.1993; 265: G993-G998
[38] Wallace JL, McKnight W., Reuter BK, Vergnolle N. Повреждение желудка, вызванное НПВП, у
крыс: Требование ингибирования как циклооксигеназы 1, так и 2. Гастроэнтерология.
2000; 119: 706-714
[39] Wallace JL, Arfors KE, McKnight GW. Моноклональное антитело против молекулы адгезии цитов CD18 leuko-
предотвращает индуцированное индометацином повреждение желудка у кроликов.
Гастроэнтерология. 1991; 100: 878-883
[40] Wallace JL, Caliendo G, Santagada V, Cirino G, Fiorucci S.Безопасность желудочно-кишечного тракта и
противовоспалительных эффектов производного диклофенака, высвобождающего сероводород, у крыс
. Гастроэнтерология. 2007; 132: 261-271
Сердечно-сосудистые эффекты и безопасность (не аспириновых) НПВП
МакГеттиган, П. и Генри, Д. Сердечно-сосудистый риск при применении нестероидных противовоспалительных препаратов: систематический обзор популяции основанные на контролируемых наблюдательных исследованиях. PLoS Med. 8 , e1001098 (2011).
CAS PubMed PubMed Central Google ученый
Bhala, N. et al. Сосудистые и верхние желудочно-кишечные эффекты нестероидных противовоспалительных препаратов: метаанализ данных отдельных участников рандомизированных исследований. Ланцет 382 , 769–779 (2013).
CAS Google ученый
Антман, Э. М. и др. Использование нестероидных противовоспалительных препаратов: новости для врачей: научное заявление Американской кардиологической ассоциации. Тираж 115 , 1634–1642 (2007).
Google ученый
Датское кардиологическое общество. Лечение НПВП у пациентов с сердечно-сосудистыми заболеваниями. Датское кардиологическое общество https://www.cardio.dk/nsaid-behandling-hos-patienter-med-hjertekarsygdom (2016).
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. FDA усиливает предупреждение о том, что нестероидные противовоспалительные препараты, не содержащие аспирин (НПВП), могут вызывать сердечные приступы или инсульты. FDA https://www.fda.gov/drugs/drug-safety-and-availability/fda-drug-safety-communication-fda-strengthens-warning-non-aspirin-nonsteroidal-anti-inflamasted (2015).
Европейское агентство по лекарственным средствам. Отчет об оценке нестероидных противовоспалительных препаратов (НПВП) и сердечно-сосудистого риска. EMA https://www.ema.europa.eu/en/documents/referral/assessment-report-article-53-procedure-non-steroidal-anti-inflamasted-drugs-nsaids-cardiovascular_en.pdf (2012).
Gislason, G.H. et al. Повышенная смертность и сердечно-сосудистые заболевания, связанные с применением нестероидных противовоспалительных препаратов при хронической сердечной недостаточности. Arch. Междунар. Med. 169 , 141–149 (2009).
CAS Google ученый
Gislason, G.H. et al. Риск смерти или повторного инфаркта, связанный с применением селективных ингибиторов циклооксигеназы-2 и неселективных нестероидных противовоспалительных препаратов после острого инфаркта миокарда. Тираж 113 , 2906–2913 (2006).
Schjerning Olsen, A. M. et al. Продолжительность лечения нестероидными противовоспалительными препаратами и влияние на риск смерти и повторного инфаркта миокарда у пациентов, перенесших инфаркт миокарда в анамнезе: общенациональное когортное исследование. Тираж 123 , 2226–2235 (2011).
CAS Google ученый
Schjerning Olsen, A.M. et al. Связь применения НПВП с риском кровотечения и сердечно-сосудистых событий у пациентов, получающих антитромботическую терапию после инфаркта миокарда. JAMA 313 , 805–814 (2015).
CAS Google ученый
Lamberts, M. et al. Связь нестероидных противовоспалительных препаратов с риском серьезного кровотечения и тромбоэмболии у пациентов с фибрилляцией предсердий, получающих антитромботическую терапию: общенациональное когортное исследование. Ann. Междунар. Med. 161 , 690–698 (2014).
Google ученый
Dubois, R. N. et al. Циклооксигеназа в биологии и болезнях. FASEB J. 12 , 1063–1073 (1998).
CAS Google ученый
Антман, Э. М., ДеМетс, Д. и Лоскальцо, Дж. Ингибирование циклооксигеназы и сердечно-сосудистый риск. Тираж 112 , 759–770 (2005).
CAS Google ученый
Мукерджи, Д., Ниссен, С. Э. и Тополь, Э. Дж. Риск сердечно-сосудистых событий, связанных с селективными ингибиторами ЦОГ-2. JAMA 286 , 954–959 (2001).
CAS Google ученый
Гроссер Т., Фрис С. и Фитцджеральд Г. А. Биологические основы сердечно-сосудистых последствий ингибирования ЦОГ-2: терапевтические проблемы и возможности. J. Clin. Инвестировать. 116 , 4–15 (2006).
CAS PubMed PubMed Central Google ученый
Warner, T. D. et al. Циклооксигеназы 1, 2 и 3 и производство простагландина I2: исследование активности ацетаминофена и селективных ингибиторов циклооксигеназы-2 в тканях крыс. J. Pharmacol. Exp. Ther. 310 , 642–647 (2004).
CAS Google ученый
Timmers, L. et al. Ингибирование циклооксигеназы-2 увеличивает смертность, усиливает ремоделирование левого желудочка и ухудшает систолическую функцию после инфаркта миокарда у свиней. Тираж 115 , 326–332 (2007).
CAS Google ученый
Francois, H. et al. Простациклин защищает от повышенного артериального давления и сердечного фиброза. Cell Metab. 2 , 201–207 (2005).
CAS Google ученый
Фитцджеральд Г. А. и Патроно С. Коксибы, селективные ингибиторы циклооксигеназы-2. N. Engl. J. Med. 345 , 433–442 (2001).
CAS Google ученый
Уорнер Т. Д. и Митчелл Дж. А. Циклооксигеназы: новые формы, новые ингибиторы и уроки клиники. FASEB J. 18 , 790–804 (2004).
CAS Google ученый
Гроссер Т., Ю. Ю. и Фицджеральд Г. А. Эмоции, вспоминаемые в спокойствии: уроки, извлеченные из саги о СОХ-2. Ann. Rev. Med. 61 , 17–33 (2010).
CAS Google ученый
Минуз, П. Нестероидные противовоспалительные препараты и сердечно-сосудистый риск: является ли ингибирование простациклина ключевым событием? Дж.Являюсь. Coll. Кардиол. 52 , 1637–1639 (2008).
Google ученый
Ав, Т. Дж., Хаас, С. Дж., Лью, Д. и Крам, Х. Мета-анализ ингибиторов циклооксигеназы-2 и их влияния на кровяное давление. Arch. Междунар. Med. 165 , 490–496 (2005).
CAS Google ученый
White, W. B. et al. Влияние целекоксиба на амбулаторное артериальное давление у пациентов с гипертонией, принимающих ингибиторы АПФ. Гипертония 39 , 929–934 (2002).
CAS Google ученый
Кумар, Б. и Сви, М. Л. Использование нестероидных противовоспалительных препаратов у пациента с гипертонией: поучительный момент. JAMA Intern. Med. 175 , 892–893 (2015).
Google ученый
Джонсон, А.Г., Саймонс, Л.А., Саймонс, Дж., Фридлендер, Ю.И МакКаллум, Дж. Нестероидные противовоспалительные препараты и гипертония у пожилых людей: поперечное исследование на уровне сообщества. Br. J. Clin. Pharmacol. 35 , 455–459 (1993).
CAS PubMed PubMed Central Google ученый
Bally, M. et al. Риск острого инфаркта миокарда при применении НПВП в реальном мире: байесовский метаанализ индивидуальных данных пациента. BMJ 357 , j1909 (2017).
PubMed PubMed Central Google ученый
Masclee, G. M. C. et al. Риск острого инфаркта миокарда при использовании отдельных НПВП: вложенное исследование случай-контроль из проекта SOS. PLoS One 13 , e0204746 (2018).
PubMed PubMed Central Google ученый
Fosbol, E. L. et al. Схема использования нестероидных противовоспалительных препаратов (НПВП) с 1997 по 2005 год: общенациональное исследование 4.6 миллионов человек. Фармакоэпидемиол. Drug Saf. 17 , 822–833 (2008).
Google ученый
Olsen, A. M. et al. Связанный с конкретной причиной сердечно-сосудистый риск, связанный с приемом нестероидных противовоспалительных препаратов, среди пациентов с инфарктом миокарда — общенациональное исследование. PLoS One 8 , e54309 (2013).
CAS Google ученый
Trelle, S. et al. Сердечно-сосудистая безопасность нестероидных противовоспалительных препаратов: сетевой метаанализ. BMJ 342 , c7086 (2011).
PubMed PubMed Central Google ученый
Сотрудничество исследователей коксиба и традиционных НПВП (CNT). Сосудистые и верхние желудочно-кишечные эффекты нестероидных противовоспалительных препаратов: метаанализ данных отдельных участников рандомизированных исследований. Ланцет 382 , 769–779 (2013).
Google ученый
Соренсен Р. и др. Риск кровотечения у пациентов с острым инфарктом миокарда, получавших различные комбинации антагонистов аспирина, клопидогреля и витамина К в Дании: ретроспективный анализ данных общенационального регистра. Ланцет 374 , 1967–1974 (2009).
CAS Google ученый
Scally, B. et al. Эффекты гастропротекторов для профилактики и лечения язвенной болезни и ее осложнений: метаанализ рандомизированных исследований. Ланцет Гастроэнтерол. Гепатол. 3 , 231–241 (2018).
PubMed PubMed Central Google ученый
Olsen, A. M. et al. Долгосрочный сердечно-сосудистый риск использования нестероидных противовоспалительных препаратов в зависимости от времени, прошедшего после первого инфаркта миокарда: общенациональное когортное исследование. Тираж 126 , 1955–1963 (2012).
CAS Google ученый
Kearney, P. M. et al. Повышают ли селективные ингибиторы циклооксигеназы-2 и традиционные нестероидные противовоспалительные препараты риск атеротромбоза? Метаанализ рандомизированных исследований. BMJ 332 , 1302–1308 (2006).
CAS PubMed PubMed Central Google ученый
Рейли И. А. и Фитцджеральд Г. А. Ингибирование образования тромбоксана in vivo и ex vivo: значение для терапии препаратами, ингибирующими тромбоциты. Кровь 69 , 180–186 (1987).
CAS Google ученый
Антман, Э. М. Взаимодействие аспирина и НПВП: больше данных, но остается неясность. J. Am. Coll. Кардиол. 71 , 1752–1754 (2018).
PubMed PubMed Central Google ученый
Велтон, А. Почечные аспекты лечения обычными нестероидными противовоспалительными препаратами по сравнению с ингибиторами, специфичными для циклооксигеназы-2. Am. J. Med. 110 (Дополнение 3A), 33S – 42S (2001).
CAS Google ученый
Komhoff, M., Grone, H.J., Klein, T., Seyberth, H. W. & Nusing, R.M. Локализация циклооксигеназы-1 и -2 в почках взрослого и плода человека: влияние на функцию почек. Am. J. Physiol. 272 , F460 – F468 (1997).
CAS Google ученый
Аппель Г. Б. Ингибиторы ЦОГ-2 и почки. Clin. Exp. Ревматол. 19 (Приложение 25), S37 – S40 (2001).
CAS Google ученый
Брейер, М. Д., Хао, К. и Ци, З. Селективные ингибиторы циклооксигеназы-2 и почки. Curr.Opin. Крит. Уход 7 , 393–400 (2001).
CAS Google ученый
Zhang, J., Ding, E. L. & Song, Y. Неблагоприятные эффекты ингибиторов циклооксигеназы 2 на почечные и аритмические события: метаанализ рандомизированных исследований. JAMA 296 , 1619–1632 (2006).
CAS Google ученый
Бэк, М., Инь, Л. и Ингельссон, Э.Ингибиторы циклооксигеназы-2 и сердечно-сосудистый риск в общенациональном когортном исследовании после отмены рофекоксиба. Eur. Харт J. 33 , 1928–1933 (2012).
Google ученый
Krijthe, B.P., Heeringa, J., Hofman, A., Franco, O.H. & Stricker, B.H. Нестероидные противовоспалительные препараты и риск фибрилляции предсердий: последующее популяционное исследование. BMJ Open 4 , e004059 (2014).
PubMed PubMed Central Google ученый
Шмидт, М., Кристиансен, К. Ф., Менерт, Ф., Ротман, К. Дж. И Соренсен, Х. Т. Использование нестероидных противовоспалительных препаратов и риск фибрилляции или трепетания предсердий: популяционное исследование случай-контроль. BMJ 343 , d3450 (2011).
Google ученый
Chao, T. F. et al.Связь между использованием нестероидных противовоспалительных препаратов и фибрилляцией предсердий: общенациональное исследование методом случай-контроль. Внутр. J. Cardiol. 168 , 312–316 (2013).
Google ученый
Liu, G. et al. Мета-анализ использования нестероидных противовоспалительных препаратов и риска фибрилляции предсердий. Am. J. Cardiol. 114 , 1523–1529 (2014).
CAS Google ученый
Mamdani, M. et al. Ингибиторы циклооксигеназы-2 в сравнении с неселективными нестероидными противовоспалительными препаратами и исходы застойной сердечной недостаточности у пожилых пациентов: популяционное когортное исследование. Ланцет 363 , 1751–1756 (2004).
CAS Google ученый
Arfe, A. et al. Нестероидные противовоспалительные препараты и риск сердечной недостаточности в четырех европейских странах: вложенное исследование случай-контроль. BMJ 354 , i4857 (2016).
Google ученый
Хадсон, М., Ричард, Х. и Пилот, Л. Различия в исходах у пациентов с застойной сердечной недостаточностью, которым прописали целекоксиб, рофекоксиб или нестероидные противовоспалительные препараты: популяционное исследование. BMJ 330 , 1370 (2005).
CAS PubMed PubMed Central Google ученый
Хадсон, М., Рахме, Э., Ричард, Х. и Пилот, Л. Риск застойной сердечной недостаточности при применении нестероидных противовоспалительных препаратов и селективных ингибиторов циклооксигеназы 2: классовый эффект? Arthritis Rheum. 57 , 516–523 (2007).
CAS Google ученый
Silverstein, F. E. et al. Желудочно-кишечная токсичность целекоксиба по сравнению с нестероидными противовоспалительными препаратами при остеоартрите и ревматоидном артрите: исследование CLASS: рандомизированное контролируемое исследование.Долгосрочное исследование безопасности целекоксиба при артрите. JAMA 284 , 1247–1255 (2000).
CAS Google ученый
Bombardier, C. et al. Сравнение токсичности рофекоксиба и напроксена для верхних отделов желудочно-кишечного тракта у пациентов с ревматоидным артритом. Исследовательская группа VIGOR. N. Engl. J. Med. 343 , 1520–1528 (2000).
CAS Google ученый
Барон, Дж. А. и др. Сердечно-сосудистые события, связанные с рофекоксибом: окончательный анализ исследования APPROVe. Ланцет 372 , 1756–1764 (2008).
CAS Google ученый
Solomon, S. D. et al. Сердечно-сосудистый риск, связанный с целекоксибом в клинических испытаниях по профилактике колоректальной аденомы. N. Engl. J. Med. 352 , 1071–1080 (2005).
CAS Google ученый
Solomon, S.D. et al. Влияние целекоксиба на сердечно-сосудистые события и артериальное давление в двух испытаниях по профилактике колоректальных аденом. Тираж 114 , 1028–1035 (2006).
CAS Google ученый
Arber, N. et al. Целекоксиб для профилактики колоректальных аденоматозных полипов. N. Engl. J. Med. 355 , 885–895 (2006).
CAS Google ученый
Bresalier, R. S. et al. Сердечно-сосудистые события, связанные с рофекоксибом, в исследовании химиопрофилактики колоректальной аденомы. N. Engl. J. Med. 352 , 1092–1102 (2005).
CAS Google ученый
Bertagnolli, M. M. et al. Целекоксиб для профилактики спорадических колоректальных аденом. N. Engl. J. Med. 355 , 873–884 (2006).
CAS Google ученый
Nissen, S.E. et al. Сердечно-сосудистая безопасность целекоксиба, напроксена или ибупрофена при артрите. N. Engl. J. Med. 375 , 2519–2529 (2016).
CAS Google ученый
Solomon, S. D. et al. Сердечно-сосудистый риск целекоксиба в 6 рандомизированных плацебо-контролируемых исследованиях: перекрестный анализ безопасности. Тираж 117 , 2104–2113 (2008).
CAS PubMed PubMed Central Google ученый
Reed, G. W. et al. Влияние одновременного приема аспирина на безопасность целекоксиба, напроксена или ибупрофена. J. Am. Coll. Кардиол. 71 , 1741–1751 (2018).
CAS Google ученый
MacDonald, T. M. et al. Рандомизированное испытание перехода с прописанных неселективных нестероидных противовоспалительных препаратов на прописанный целекоксиб: стандартное лечение по сравнению с испытанием исходов целекоксиба (SCOT). Eur.Харт J. 38 , 1843–1850 (2017).
Google ученый
Гроссер Т., Риччиотти Э. и Фитцджеральд Г. А. Сердечно-сосудистая фармакология нестероидных противовоспалительных препаратов. Trends Pharmacol. Sci. 38 , 733–748 (2017).
CAS PubMed PubMed Central Google ученый
Руководящий комитет CAPRIE.Рандомизированное слепое исследование клопидогреля по сравнению с аспирином у пациентов с риском ишемических событий (CAPRIE) Руководящий комитет CAPRIE. Ланцет 348 , 1329–1339 (1996).
Google ученый
Connolly, S.J. et al. Дабигатран по сравнению с варфарином у пациентов с фибрилляцией предсердий. N. Engl. J. Med. 361 , 1139–1151 (2009).
CAS Google ученый
Dentali, F. et al. Эффективность и безопасность новых пероральных антикоагулянтов при фибрилляции предсердий: систематический обзор и метаанализ литературы. Тираж 126 , 2381–2391 (2012).
CAS Google ученый
Eikelboom, J. W. et al. Риск кровотечения при приеме 2 доз дабигатрана по сравнению с варфарином у пожилых и молодых пациентов с фибрилляцией предсердий: анализ рандомизированной оценки исследования долгосрочной антикоагулянтной терапии (RE-LY). Тираж 123 , 2363–2372 (2011).
CAS Google ученый
Kent, A. P. et al. Сопутствующая терапия пероральными антикоагулянтами и нестероидными противовоспалительными препаратами у пациентов с фибрилляцией предсердий. J. Am. Coll. Кардиол. 72 , 255–267 (2018).
CAS Google ученый
Davidson, B. L. et al.Риск кровотечения у пациентов с острой венозной тромбоэмболией, принимающих нестероидные противовоспалительные препараты или аспирин. JAMA Intern. Med. 174 , 947–953 (2014).
CAS Google ученый
Schjerning Olsen, A. M. et al. Риск желудочно-кишечного кровотечения, связанного с пероральными антикоагулянтами и нестероидными противовоспалительными препаратами, у пациентов с фибрилляцией предсердий: общенациональное исследование. Eur.Сердце J. Cardiovasc. Фармакотер. https://doi.org/10.1093/ehjcvp/pvz069 (2019).
Артикул Google ученый
Gadsboll, K. et al. Увеличение использования пероральных антикоагулянтов у пациентов с фибрилляцией предсердий: временные тенденции с 2005 по 2015 год в Дании. Eur. Харт J. 38 , 899–906 (2017).
Google ученый
Гроссер Т., Текен, К. Н. и Фитцджеральд, Г. А. Ингибирование циклооксигеназы: боль, воспаление и сердечно-сосудистая система. Clin. Pharmacol. Ther. 102 , 611–622 (2017).
Google ученый
Jacob, L. & Kostev, K. Распространенность рецептов обезболивающих во Франции, Германии и Великобритании — кросс-секционное исследование с участием 4 270 142 пациентов. Аспирантура. Med. 130 , 32–36 (2018).
Google ученый
Шмидт, М., Халлас, Дж. И Фриис, С. Возможности реестров рецептов для регистрации использования аспирина и других нестероидных противовоспалительных препаратов на индивидуальном уровне в Дании: тенденции использования в 1999-2012 гг. Clin. Эпидемиол. 6 , 155–168 (2014).
PubMed PubMed Central Google ученый
Шмагель, А., Нго, Л., Энсруд, К. и Фоули, Р. Использование рецептурных лекарств среди взрослых в США с хронической болью в пояснице: поперечное популяционное исследование. Дж. Пейн 19 , 1104–1112 (2018).
PubMed PubMed Central Google ученый
Ruscitto, A., Smith, B. H. и Guthrie, B. Изменения в использовании опиоидов и других анальгетиков 1995–2010: повторный поперечный анализ отпускаемых лекарств для большой географической популяции в Шотландии. Eur. Дж. Пейн 19 , 59–66 (2015).
CAS Google ученый
Bouck, Z. et al. Частота и взаимосвязь использования рецептурных нестероидных противовоспалительных препаратов среди пациентов с опорно-двигательным аппаратом и гипертонией, сердечной недостаточностью или хроническим заболеванием почек. JAMA Intern. Med. 178 , 1516–1525 (2018).
PubMed PubMed Central Google ученый
МакГеттиган, П. и Генри, Д. Использование нестероидных противовоспалительных препаратов, повышающих риск сердечно-сосудистых заболеваний: изучение списков продаж и основных лекарственных средств в странах с низким, средним и высоким уровнем доходов. PLoS Med. 10 , e1001388 (2013).
PubMed PubMed Central Google ученый
Хантер Д. Дж. И Бирма-Зейнстра С. Остеоартрит. Ланцет 393 , 1745–1759 (2019).
CAS Google ученый
Agca, R. et al. Рекомендации EULAR по управлению рисками сердечно-сосудистых заболеваний у пациентов с ревматоидным артритом и другими формами воспалительных заболеваний суставов: обновление 2015/2016. Ann. Реум. Дис. 76 , 17–28 (2017).
CAS Google ученый
Hochberg, M.C. et al. Рекомендации Американского колледжа ревматологов 2012 по использованию нефармакологических и фармакологических методов лечения остеоартрита кисти, бедра и колена. Arthritis Care Res. 64 , 465–474 (2012).
CAS Google ученый
Королевский австралийский колледж врачей общей практики. Руководство по лечению остеоартроза коленного и тазобедренного суставов: второе издание. RACGP https://www.racgp.org.au/download/Documents/Guidelines/Musculoskeletal/guideline-for-the-management-of-knee-and-hip-oa-2nd-edition.pdf (2018).
Робертс, Э.и другие. Парацетамол: не так ли безопасно, как мы думали? Систематический обзор литературы по обсервационным исследованиям. Ann. Реум. Дис. 75 , 552–559 (2016).
CAS Google ученый
Меара, А. С. и Саймон, Л. С. Рекомендации профессиональных обществ: правильное использование НПВП. Pain Med. 14 (Приложение 1), S3 – S10 (2013).
Google ученый
Schmidt, M. et al. Сердечно-сосудистая безопасность нестероидных противовоспалительных препаратов, не являющихся аспирином: обзор и позиционный документ рабочей группы по сердечно-сосудистой фармакотерапии Европейского общества кардиологов. Eur. Харт J. 37 , 1015–1023 (2016).
CAS Google ученый
Bhatt, D. L. et al. ACCF / ACG / AHA 2008 согласованный документ экспертов по снижению желудочно-кишечных рисков при антиагрегантной терапии и применении НПВП: отчет Целевой группы Фонда Американского колледжа кардиологии по согласованным клиническим документам экспертов. Тираж 118 , 1894–1909 (2008).
Google ученый
Bennett, J. S. et al. Использование нестероидных противовоспалительных препаратов (НПВП): научный совет Американской кардиологической ассоциации. Тираж 111 , 1713–1716 (2005).
Google ученый
Национальный фонд сердца Австралии. Лекарства, которых следует избегать при ОКС и сердечной недостаточности. Сердце онлайн https://www.heartonline.org.au/articles/medications/cautions-and-monitoring#medications-to-avoid-in-acs-and-heart-failure (2020).
Европейское агентство по лекарственным средствам. Лекарства, содержащие ибупрофен и дексибупрофен. EMA https://www.ema.europa.eu/en/medicines/human/referrals/ibuprofen-dexibuprofen-contain-medicines (2015).
Европейское агентство по лекарственным средствам. Европейское агентство по лекарственным средствам завершило обзор недавно опубликованных данных о безопасности НПВП для сердечно-сосудистой системы. EMA https://www.ema.europa.eu/en/news/european-medicines-agency-finalises-review-recent-published-data-cardiovascular-safety-nsaids (2012).
Европейское агентство по лекарственным средствам. В обзоре Европейского агентства по лекарственным средствам сделан вывод о положительном соотношении пользы и риска для неселективных НПВП. EMA https://www.ema.europa.eu/en/news/european-medicines-agency-review-concludes-positive-benefit-risk-balance-non-selective-nsaids (2006).
Европейское агентство по лекарственным средствам.Европейское агентство по лекарственным средствам завершает действие по ингибиторам ЦОГ-2. EMA https://www.ema.europa.eu/en/news/european-medicines-agency-concludes-action-cox-2-inhibitors (2005).
Управление терапевтическими товарами. Обзор сердечно-сосудистой безопасности нестероидных противовоспалительных препаратов. TGA https://www.tga.gov.au/sites/default/files/medicines-review-nsaid.pdf (2014).
Управление терапевтическими товарами. Материалы и ответ TGA: парацетамол и ибупрофен: предлагаемое дополнительное консультативное заявление. TGA https://www.tga.gov.au/submissions-and-tga-response-paracetamol-and-ibuprofen-proposed-additional-advisory-statement (2017).
Национальный институт здравоохранения и повышения квалификации. Нестероидные противовоспалительные препараты. NICE https://www.nice.org.uk/advice/ktt13/chapter/Evidence-context (2018).
Кейс, А. и Дитон, А. Рост заболеваемости и смертности в среднем возрасте среди белых неиспаноязычных американцев в 21 веке. Proc. Natl Acad. Sci. США 112 , 15078–15083 (2015).
CAS Google ученый
Сараджиотто Б. Т., Абдель Шахид К. и Махер К. Г. Парацетамол от боли у взрослых. BMJ 367 , l6693 (2019).
Google ученый
[Авторы не указаны] Сдерживающие от злоупотребления опиоиды. JAMA 319 , 2036–2037 (2018).
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Опоидные анальгетики, сдерживающие злоупотребление. FDA https://www.fda.gov/drugs/postmarket-drug-safety-information-patients-and-providers/abuse-deterrent-opioid-analgesics (2019).
Институт Катона. Опиоиды, сдерживающие злоупотребление, и закон непредвиденных последствий. Като https://www.cato.org/publications/policy-analysis/abuse-deterrent-opioids-law-unintended-consequences (2018).
Cicero, T. J., Ellis, M. S. & Surratt, H. L. Эффект сдерживающего злоупотребления препарата оксиконтина. N. Engl. J. Med. 367 , 187–189 (2012).
CAS Google ученый
Витингтон, Л., Чен, Х. и Йип, С. Развертка трубопровода: мнения экспертов по болезни Альцгеймера, опиоидам и каннабису. Фармацевтический руководитель https://www.pharmexec.com/pipeline-drill-down-expert-perspectives-alzheimers-opioids-and-cannabis-0?pageID=2 (2018).
BioSpace. Компания Galt Pharmaceuticals получила приоритетный обзор FDA для неконтролируемого обезболивающего препарата orphengesic forte, безопиоидной альтернативы для пациентов. BioSpace https://www.biospace.com/article/releases/galt-pharmaceuticals-receives-fda-priority-review-for-non-controlled-pain-management-drug-orphengesic-forte-an-opioid-free -альтернатив-для-пациентов / (2019).
Drugs.com. Статус одобрения НКТР-181. Drugs.com https: // www.Drugs.com/history/nktr-181.html (2020).
Национальная медицинская библиотека США. ClinicalTrials.gov https: // Clinicaltrials. gov / ct2 / show / NCT03304379 (2020).
Tive, L. et al. Объединенный анализ эффективности и безопасности танезумаба с анализами подгрупп клинических испытаний фазы III у пациентов с остеоартрозом и болью в колене или бедре. J. Pain Res. 12 , 975–995 (2019).
CAS PubMed PubMed Central Google ученый
Centrexion Therapeutics. Centrexion Therapeutics объявляет о завершении включения пациентов в основное клиническое испытание повторных доз CNTX-4975 у пациентов с умеренной и тяжелой болью в коленях при остеоартрите. Centrexion https://centrexion.com/wp-content/uploads/2019/06/FINAL_Centrexion_Victory-2-Patient-Enrollment_060519.pdf (2019).
BioSpace. Нектар спотыкается, поскольку FDA откладывает слушания консультативного комитета по NKTR-181. BioSpace https: // www.biospace.com/article/nektar-stumbles-as-the-fda-delays-advisory-committee-hearing-for-nktr-181/ (2019).
Фармафором. Неопиоидный обезболивающий препарат Pfizer / Lilly показывает более положительные результаты. Фармафором https://pharmaphorum.com/news/pfizer-lilly-non-opioid-pain-drug-shows-more-positive-results/ (2019).
Шолль, Л., Сет, П., Карииса, М., Уилсон, Н. и Болдуин, Г. Смертность от передозировки наркотиками и опиоидами — США, 2013–2017 годы. Morb. Смертный. Wkly. Реп. 67 , 1419–1427 (2018).
Google ученый
НПВП и сердечно-сосудистый риск
Опубликовано: 7 июня 2019 г.
НПВП и сердечно-сосудистый риск
Обновление Prescriber 40 (2): 26-28
Июнь 2019
Ключевые сообщения
- Все НПВП, включая как традиционные НПВП, так и НПВС, селективные по ЦОГ-2, увеличить риск сердечно-сосудистых побочных эффектов.
- Невозможно дифференцировать или ранжировать НПВП по их сердечно-сосудистый риск.
- Сердечно-сосудистые побочные эффекты возникают как при краткосрочном, так и при кратковременном воздействии. длительное использование.
- Используйте НПВП в минимальной эффективной дозе в течение кратчайшего времени возможный.
Фон
Комитет по побочным реакциям на лекарства (MARC) рассмотрел сердечно-сосудистые заболевания. безопасность нестероидных противовоспалительных препаратов (НПВП) на 177 th встреча 14 марта 2019 г.
Недавние исследования сердечно-сосудистой безопасности
Поскольку MARC ранее обсуждал сердечно-сосудистую безопасность диклофенака в 2013 г. 1 и ибупрофен в 2015 г. 2 , Было опубликовано несколько новых исследований безопасности НПВП для сердечно-сосудистой системы.
Medsafe представила MARC отчет о новейшей литературе на 177-е заседание, март 2019 г. 3 . Эти исследования включают два ключевых клинических испытания 4,5 , и два крупных обсервационных исследования с использованием медицинских баз данных 6,7 .Кроме того, было проведено два метаанализа более ранних исследований 8,9 , исследование датского реестра здравоохранения, изучающее риск выписки из больницы остановка сердца с НПВП 10 , а исследование случай-контроль, вложенное в когорту, полученную из европейского электронного здравоохранения базы данных, которые исследуют риск госпитализации по поводу сердечной недостаточности обострение у новых пользователей НПВП 11 .
MARC рассмотрел эти исследования и пришел к выводу, что в настоящее время можно дифференцировать НПВП по индивидуальному сердечно-сосудистому риску профили 12 .Все НПВП повышают риск сердечно-сосудистых заболеваний, а риск увеличивается как при краткосрочном, так и при долгосрочном использовании.
Клинические последствия
- Избегайте использования всех НПВП у пациентов с сердечно-сосудистыми заболеваниями. болезни, а также у лиц со значительными факторами риска.
- При необходимости используйте НПВП в минимальной эффективной дозе для кратчайшего пути. возможна продолжительность.
- Сообщите пациентам, что НПВП повышают риск сердечно-сосудистых заболеваний. побочные эффекты, даже у тех, у кого в анамнезе не было сердечно-сосудистых заболеваний, и о симптомах и признаках, на которые следует обратить внимание.
Механизм действия
НПВП уменьшают воспаление, подавляя выработку циклооксигеназы (ЦОГ), важный фермент в синтезе простагландинов. Есть два основных формы фермента ЦОГ: ЦОГ-1 и ЦОГ-2. Хотя ЦОГ-1 присутствует в большинстве тканях все время ЦОГ-2 экспрессируется в ответ на воспаление. Оба формы катализируют превращение арахидоновой кислоты через промежуточные соединения в тромбоксан А2 (протромботический) и простациклин (антитромботический).
Селективность по ЦОГ является относительной, а не абсолютной
НПВП обычно делятся на неселективные традиционные НПВП и селективные ингибиторы ЦОГ-2. Часто сравнивают выборочные Ингибиторы ЦОГ-2 и традиционные НПВП в клинических исследованиях. Однако там Эти два класса во многом совпадают по степени ингибирования ЦОГ-2. Например, среди традиционных НПВП индометацин и напроксен относительно селективны к ЦОГ-1, тогда как диклофенак и мелоксикам относительно ЦОГ-2 селективный.Кроме того, целекоксиб (селективный ингибитор ЦОГ-2) и диклофенак (традиционный НПВП) имеет аналогичную степень селективности ЦОГ-2 13 .
Баланс между ингибированием ЦОГ-1 и ЦОГ-2 может изменяться во время интервал дозирования в зависимости от активности и периода полувыведения НПВП из плазмы. Для диклофенака ингибирование ЦОГ-1 снижается по мере падения концентрации в плазме. в течение интервала дозирования, оставляя ингибирование ЦОГ-2 относительно безальтернативным. Напротив, как для ибупрофена, так и для напроксена ингибирование ЦОГ-1 превышает ингибирование ЦОГ-2. ингибирование во всем интервале доз 14,15 .
Когда ЦОГ-2 ингибируется по сравнению с ЦОГ-1, протромботический / антитромботический баланс на поверхности эндотелия смещается в пользу тромбоза, увеличивая риск сердечно-сосудистых тромботических нежелательных явлений. Относительная селективность ЦОГ также влияет на профиль нежелательных явлений со стороны желудочно-кишечного тракта у отдельных НПВП 16 .
Кардиотоксичность НПВП многофакторная
Помимо потенциальных протромботических эффектов, существуют другие факторы, способствующие к сердечно-сосудистой токсичности НПВП включают повышение артериального давления, снижение почечной перфузии, задержка жидкости и обострение сердечной недостаточности 13,17,18 .
Список литературы
- Medsafe. 2013. НПВП и риск сердечно-сосудистых событий. Предписатель Обновление 34 (3): 26. URL: https://medsafe.govt.nz/profs/PUArticles/Sept2013NSAIDS.htm (по состоянию на 8 мая 2019 г.).
- Medsafe. 2015. Ибупрофен и сердечно-сосудистый риск. Предписатель Обновление 36 (3): 42. URL: https://www.medsafe.govt.nz/profs/PUArticles/Sep2015/Ibuprofen&Cardiovascular.htm (по состоянию на 9 мая 2019 г.).
- Medsafe. 2019. НПВП и сердечно-сосудистый риск: обновленная информация . Представлено на 177 -м заседании Комитета по побочным реакциям лекарственных средств . Встреча 14 марта 2019 г. URL: https://medsafe.govt.nz/committees/MARC/reports/177-3.2.2%20NSAIDs%20-%20an%20update%20on%20CVD%20risk.pdf (по состоянию на 14 мая 2019 г.).
- Ниссен С.Е., Йоманс Н.Д., Соломон Д.Х. и др. 2016. Сердечно-сосудистая безопасность. целекоксиба, напроксена или ибупрофена при артрите. Новая Англия Медицинский журнал 375 (26): 2519–29. DOI: 10.1056 / NEJMoa1611593 (по состоянию на 14 января 2019 г.).
- MacDonald TM, Hawkey CJ, Ford I и др. 2017. Рандомизированное исследование переход с назначенных неселективных нестероидных противовоспалительных средств лекарства по назначению целекоксиба: стандартная помощь по сравнению с целекоксибом. Судебный процесс (SCOT). Европейский журнал сердца 38 (23): 1843–50. DOI: 10.1093 / eurheartj / ehw387 (по состоянию на 1 февраля 2019 г.).
- Schmidt M, Sørensen HT, Pedersen L. 2018. Использование диклофенака и сердечно-сосудистые заболевания. риски: серия общенациональных когортных исследований. BMJ 362: k3426. URL: https://www.bmj.com/content/362/bmj.k3426 (по состоянию на 1 февраля 2019 г.).
- Балли М., Дендукури Н., Рич Б. и др. 2017. Риск острого миокарда. инфаркт с НПВП в реальном мире: байесовский метаанализ индивидуальные данные пациента. BMJ 357: j1909.URL: https://www.bmj.com/content/357/bmj.j1909 (по состоянию на 8 февраля 2019 г.).
- Гюнтер Б.Р., Батлер К.А., Уоллес Р.Л. и др. 2017. Нестероидные противовоспалительные. побочные эффекты со стороны сердечно-сосудистой системы, вызванные лекарственными средствами: метаанализ. Журнал клинической фармации и терапии 42 (1): 27–8. DOI: 10.1111 / jcpt.12484 (по состоянию на 1 февраля 2019 г.).
- Ungprasert P, Srivali N, Kittanamongkolchai W. 2015. Нестероидные противовоспалительные препараты и риск обострения сердечной недостаточности: систематический обзор и метаанализ.Европейский журнал внутренней медицины 26 (9): 685–90. DOI: https://dx.doi.org/10.1016/j.ejim.2015.09.012 (по состоянию на 21 февраля 2019).
- Sondergaard KB, Weeke P, Wissenberg M, et al. 2017. Нестероидные. Использование противовоспалительных препаратов связано с повышенным риском выхода из стационара. остановка сердца: общенациональное исследование с контролем времени. Европейское сердце Журнал — Сердечно-сосудистая фармакотерапия 3 (2): 100–107.DOI: 10.1093 / ehjcvp / pvw041 (по состоянию на 1 февраля 2019 г.).
- Арфе А., Скотти Л., Варас-Лоренца С. и др. 2016. Нестероидные противовоспалительные. лекарства и риск сердечной недостаточности в четырех европейских странах: вложенный случай-контроль учиться. BMJ 354: i4857. URL: https://www.bmj.com/content/354/bmj.i4857 (по состоянию на 16 февраля 2019 г.).
- Medsafe. 2019. Протокол 177-й побочной реакции на лекарства Заседание комитета 14 марта 2019 г. .URL: https://www.medsafe.govt.nz/profs/adverse/Minutes177.htm (по состоянию на 29 апреля 2019 г.).
- Шмидт М., Ламбертс М., Шернинг Олсен А.М. и др. 2016. Сердечно-сосудистая система. Безопасность нестероидных противовоспалительных препаратов, не содержащих аспирин: обзор и позиционный документ рабочей группы по сердечно-сосудистой фармакотерапии Европейского общества кардиологов. Европейский журнал сердца — Сердечно-сосудистая фармакотерапия 2: 108–18. DOI: 10.1093 / ehjcvp / pvv054 (по состоянию на 8 февраля 2019 г.).
- Гроссер Т., Ю-Й, Фицджеральд Г.А. 2010. В спокойствии вспоминаются эмоции: уроки, извлеченные из саги о COX-2. Ежегодный обзор медицины 61: 17–33. DOI: 10.1146 / annurev-med-011209-153129 (по состоянию на 11 февраля 2019).
- Шварц Дж. И., Даллоб А. Л., Ларсон П. Дж. И др. 2008. Сравнительно ингибиторный.
активность эторикоксиба, целекоксиба и диклофенака на ЦОГ-2 по сравнению с ЦОГ-1
у здоровых людей. Журнал клинической фармакологии 48 (6):
745–54. DOI: 10.1177 / 00
008317590 (по состоянию на 16 февраля 2019 г.).
- Medsafe. 2010. Снижение риска желудочно-кишечных реакций с помощью НПВП и / или Ингибиторы ЦОГ-2. Prescriber Update 31 (4): 32. URL: https://medsafe.govt.nz/profs/PUArticles/ReducingGIReactionRiskwith%20NSAIDsAndCox2.htm (по состоянию на 14 мая 2019 г.).
- Новартис Новая Зеландия Лтд. Вольтарен 50 мг таблетка с энтеросолюбильным покрытием Лист данных Новой Зеландии 27 марта 2018 г.URL: www.medsafe.govt.nz/profs/Datasheet/v/voltarentab.pdf (по состоянию на 14 февраля 2019 г.).
- Pfizer New Zealand Ltd. 25 октября 2018 г. Целекоксиб Pfizer 100 мг, капсулы 200 мг, Новая Зеландия, лист данных , 25 октября 2018 г. URL: www.medsafe.govt.nz/profs/Datasheet/c/Celebrexcap.pdf (по состоянию на 14 февраля 2019 г.).
НПВП — Нестероидные противовоспалительные препараты
Нестероидные противовоспалительные препараты, обычно сокращенно NSAID s, представляют собой препараты с обезболивающим, жаропонижающим и противовоспалительным действием. эффекты — они уменьшают боль, жар и воспаление.Термин «нестероидный» используется, чтобы отличить эти препараты от стероидов, которые (среди широкого ряда других эффекты) обладают аналогичным эйкозаноидным, противовоспалительным действием. Как анальгетики, НПВП необычны тем, что не являются наркотиками. Иногда также назначают НПВП. to as нестероидные противовоспалительные средства / анальгетики ( NSAIAs ) или нестероидных противовоспалительных лекарственных средств ( NSAIMs ).
наиболее заметными представителями этой группы препаратов являются безрецептурные препараты, а именно ::
Начиная с 1829 г., с выделением салицина из народного средства коры ивы НПВП стали важной частью фармацевтическое лечение боли (в низких дозах) и воспаления (в высоких дозах).Частично популярность НПВП заключается в том, что, в отличие от опиоидов, они не производят седативный эффект или угнетение дыхания и очень низкий уровень зависимости. НПВП, однако не лишены своих проблем (см. ниже). Некоторые НПВП, в том числе ибупрофен и аспирин считаются относительно безопасными и доступны без рецепта.
Режим действия
Большинство НПВП действуют как неселективные ингибиторы фермент циклооксигеназа, ингибирующий как циклооксигеназу-1 (ЦОГ-1), так и циклооксигеназу-2 (ЦОГ-2) изоферменты.Циклооксигеназа катализирует образование простагландинов и тромбоксан из арахидоновой кислоты (сам является производным клеточного фосфолипида бислой фосфолипазой A 2 ). Простагландины действуют (среди прочего) как молекулы-посредники в процессе воспаления. Этот механизм действия был разъяснен Джоном Вейном, который позже получил Нобелевскую премию за свою работу. А недавно обнаруженный COX-3 также может иметь некоторую роль.
Примеры
НПВП могут быть широко классифицированы на основе их химической структуры.НПВП внутри группы будут иметь аналогичные характеристики и переносимость. Есть небольшая разница в клинической эффективности между НПВП при использовании в эквивалентных дозах. Скорее, различия между соединениями, как правило, касались режимов дозирования (связанных период полувыведения соединения), способ введения и переносимость профиль. Ниже приведены еще несколько распространенных примеров.
Парацетамол (ацетаминофен) иногда объединяют в группы с НПВП, однако, он не обладает значительными противовоспалительными свойствами. и не является настоящим НПВП.Хотя механизм действия неясен, есть подозрения что отсутствие противовоспалительного действия может быть связано с ингибированием циклооксигеназы преимущественно в центральной нервной системе. Есть также предположение, что парацетамол действует путем ингибирования недавно открытой изоформы ЦОГ-3 (см. ниже). Также считается, что НПВП действуют централизованно, возможно, в пределах спинной мозг. Однако механизм действия в этом случае недостаточно изучен.
Мост часто используемые НПВП:
Аспирин
Салсалат (амигезик)
Дифлунисал
(Долобид)
Ибупрофен (Мотрин)
Кетопрофен (Орудис)
Набуметон (Релафен)
Пироксикам (Фельден)
Напроксен (Алеве, Напросин)
Диклофенак (Вольтарен)
Индометацин (Индоцин)
Сулиндак (Клинорил)
Толметин (Толектин)
Этодолак
(Лодин)
Кеторолак (Торадол)
Оксапрозин (Дайпро)
Целекоксиб (Целебрекс)
Использует
НПВП обычно показаны для лечения острых или хронических состояний, при которых боль и воспаление присутствует.Продолжаются исследования их потенциала для предотвращения колоректального рака и лечения других состояний, таких как рак и сердечно-сосудистые заболевания. болезнь.
НПВП обычно показаны для облегчения симптомов следующие состояния: (Росси, 2006)
ревматоидный артрит, остеоартрит, Воспалительные артропатии (например, анкилозирующий спондилит, псориатический артрит, Синдром Рейтера), острая подагра, дисменорея, метастатическая боль в костях, головная боль. и мигрень, послеоперационная боль, слабая или умеренная боль из-за воспаления и повреждение тканей, гипертермия, почечная колика, Их также назначают только что родившимся младенцам. артериальный проток которого не закрылся в течение 24 часов после рождения
Аспирин, единственный НПВП, способный необратимо ингибировать ЦОГ-1, также показан для ингибирования агрегации тромбоцитов.; показания, полезные при лечении артериального тромбоза и предотвращение неблагоприятных сердечно-сосудистых событий. Показывает ингибирование тромбоцитов. агрегация, потому что он подавляет действие тромбоксана -А.
Фармакокинетика
Мост НПВП — это слабые кислоты с pKa 3-5. Они хорошо всасываются из желудка и слизистая кишечника. Они сильно связываются с белками плазмы (обычно> 95%), обычно до альбумина, так что их объем распределения обычно приблизительно равен к объему плазмы.Большинство НПВП метаболизируются в печени путем окисления и конъюгации. на неактивные метаболиты, которые обычно выводятся с мочой, хотя некоторые препараты частично выводятся с желчью. При некоторых заболеваниях метаболизм может быть ненормальным. состояний, и накопление может происходить даже при нормальной дозировке.
Ибупрофен и У диклофенака короткий период полувыведения (2-3 часа). Некоторые НПВП (обычно оксикамы) имеют очень длительный период полураспада (например, 20-60 часов).
Неблагоприятное эффекты
Широкое использование НПВП привело к тому, что нежелательные эффекты этих относительно безопасных лекарств становятся все более распространенными.В две основные побочные реакции (НЛР), связанные с НПВП, относятся к желудочно-кишечному тракту. (GI) эффекты и почечные эффекты агентов. Эти эффекты зависят от дозы, и во многих случаях достаточно серьезные, чтобы создать риск перфорации язвы в верхних отделах желудочно-кишечного тракта. кровотечение и смерть, ограничивающие применение терапии НПВП. Примерно 10-20% Пациенты, принимающие НПВП, страдают диспепсией и НПВП-ассоциированными верхними отделами желудочно-кишечного тракта. побочные эффекты оцениваются в 103 000 госпитализаций и 16 500 смертей в год в Соединенных Штатах, и составляют 43% чрезвычайных ситуаций, связанных с наркотиками посещения.Многие из этих событий можно избежать; обзор посещений врача и рецептов подсчитали, что ненужные рецепты на НПВП выписывались в 42% посещений. (Green, 2001)
Комбинированный риск
Если принимается ингибитор ЦОГ-2, не следует применять традиционные НПВП (рецепт или без рецепта) одновременно. [1] Кроме того, пациенты, ежедневно получающие аспирин (что касается снижения риск сердечно-сосудистых заболеваний или риск рака толстой кишки) необходимо соблюдать осторожность, если они также используют другие НПВП, так как последние могут блокировать кардиозащитные эффекты аспирина.
Сердечно-сосудистая система риск
Недавний метаанализ всех исследований, сравнивающих найденные НПВП повышение риска инфаркта миокарда на 80% при применении обоих новых антагонистов ЦОГ-2 и традиционные противовоспалительные средства в высоких дозах по сравнению с плацебо (Kearney et al. др., BMJ 2006; 332: 1302-1308).
НПВП удваивают риск развития симптоматических сердечная недостаточность у пациентов без сердечных заболеваний в анамнезе. У пациентов с такой анамнез, однако, использование НПВП может привести к более чем 10-кратному увеличению при сердечной недостаточности [2].В целом, НПВП, по оценкам, вызывают до 20 процентов госпитализаций по поводу застойной сердечной недостаточности [3].
Желудочно-кишечный тракт ADRs
Основные ADR (нежелательные лекарственные реакции), связанные с использованием НПВП относятся к прямому и косвенному раздражению желудочно-кишечного тракта (GIT). НПВП вызывают двойное поражение желудочно-кишечного тракта — молекулы кислоты непосредственно раздражают слизистая желудка; а ингибирование ЦОГ-1 снижает уровень защитных простагландинов.
Риск язв увеличивается с продолжительностью терапии и с более высокими дозами. В попытке чтобы свести к минимуму нежелательные реакции со стороны желудочно-кишечного тракта, разумно использовать самую низкую эффективную дозу для кратчайшего период времени, практика, которая, как показывают исследования, нечасто соблюдается.
Есть также есть некоторые различия в склонности отдельных агентов вызывать желудочно-кишечные ADR. Индометацин, кетопрофен и пироксикам, по-видимому, имеют самую высокую распространенность. нежелательных реакций желудка, в то время как ибупрофен (более низкие дозы) и диклофенак, по-видимому, имеют более низкие ставки.(Росси, 2006)
Некоторые НПВП, такие как аспирин, были проданы. в составах с энтеросолюбильным покрытием, которые, как утверждается, снижают частоту желудочно-кишечных ADR. Точно так же существует мнение, что ректальные составы могут уменьшить желудочно-кишечный тракт. ADR. Однако, учитывая механизм таких нежелательных реакций и клинические На практике не было показано, что эти составы снижают риск развития желудочно-кишечного тракта. изъязвление. (Росси, 2006)
Почечные ADR
НПВП также связаны с относительно высокой частотой нежелательных реакций со стороны почек.Механизм из этих почечных нежелательных реакций возникает из-за изменений почечной гемодинамики (кровотока), обычно опосредовано простагландинами, на которые действуют НПВП. Простагландины в норме вызывают расширение сосудов афферентных артериол клубочков. Это помогает поддерживать нормальная клубочковая перфузия и скорость клубочковой фильтрации (СКФ), индикатор почечной функции. Блокируя этот простагландин-опосредованный эффект, НПВП в конечном итоге может вызвать почечную недостаточность. Лошади особенно подвержены этим неблагоприятным воздействиям. по сравнению с другими видами домашних животных.
Светочувствительность
Светочувствительность — часто игнорируемый побочный эффект многих НПВП. (Мур, 2002) Это несколько иронично то, что эти противовоспалительные агенты могут сами производить воспаление в сочетании с воздействием солнечных лучей. 2-арилпропионовые кислоты с наибольшей вероятностью вызывают реакции светочувствительности, но другие Также были задействованы НПВП, включая пироксикам, диклофенак и бензидамин.Беноксапрофен, который был отменен из-за его гепатотоксичности, был наиболее светочувствительным. Наблюдали НПВП. Механизм светочувствительности, ответственный за высокую фотоактивность 2-арилпропионовых кислот, представляет собой готовое декарбоксилирование карбоновой кислоты часть. Удельные характеристики поглощения различных хромофорных 2-арильные заместители, влияют на механизм декарбоксилирования. Пока ибупрофен в некотором роде исключение, имея слабое всасывание, сообщалось, что это слабый фотосенсибилизирующий агент.
Во время беременности
НПВП не рекомендуются во время беременности, особенно в третьем триместре. Хотя НПВП как класс не являются прямыми тератогенами, они могут вызывать преждевременное закрытие. артериального протока плода и нежелательных реакций почек у плода. Кроме того, они связаны с преждевременными родами (Ostensen & Skomsvoll, 2004). Аспирин, однако, используется вместе с гепарином у беременных с антифосфолипидными антителами (Сервера и Балаш, 2004 г.).Напротив, парацетамол (ацетаминофен) считается как безопасный и хорошо переносимый во время беременности (Graham et al., 2005). Дозы следует принимать в соответствии с предписаниями из-за риска гепатотоксичности при передозировке (Уилкс и др., 2005).
Новые НПВП: селективные ингибиторы ЦОГ
ЦОГ-2 ингибиторы
Открытие COX-2 в 1991 году Дэниелом Л. Симмонсом в Университете Бригама Янга вселили надежду на разработку эффективного НПВП без желудочные проблемы, характерные для этих агентов.Считалось, что выборочный ингибирование ЦОГ-2 приведет к противовоспалительному действию без нарушения гастропротекторные простагландины.
ЦОГ-1 представляет собой конститутивно экспрессируемый фермент с «хозяйственной» ролью в регулировании многих нормальных физиологических процессов. Один из них находится в слизистой оболочке желудка, где простагландины служат защитным роль, предотвращая разрушение слизистой оболочки желудка собственной кислотой. Когда неизбирательный Ингибиторы ЦОГ-1 / ЦОГ-2 (например, аспирин, ибупрофен и напроксен) нижних отделов желудка уровни простагландина, эти защитные эффекты теряются и язвы желудка или двенадцатиперстной кишки, что может привести к внутреннему кровотечению.ЦОГ-2 — это фермент факультативно выражается в воспалении, и именно ингибирование ЦОГ-2 производит желаемый эффекты НПВП.
Относительно селективный ингибитор ЦОГ-2 оксикам, мелоксикам, был первым шагом к разработке настоящего селективного ингибитора ЦОГ-2. Коксибы, новейший класс НПВП, можно рассматривать как истинные селективные ингибиторы ЦОГ-2, и включают целекоксиб, рофекоксиб, вальдекоксиб, парекоксиб и эторикоксиб.
Споры с ингибиторами ЦОГ-2
Хотя можно было надеяться, что эта селективность ЦОГ-2 уменьшит нежелательные реакции со стороны желудочно-кишечного тракта (НЛР), окончательных выводов нет. доказательства того, что это правда.Оригинальное исследование, рекламируемое Searle (ныне являющееся частью Pfizer), показывающий снижение частоты нежелательных реакций для целекоксиба, позже выяснилось, что он основан на предварительные данные — окончательные данные не показали существенной разницы в ADR, когда по сравнению с диклофенаком.
Однако рофекоксиб, который с тех пор был отменен, было показано, что они вызывают значительно меньшее количество нежелательных реакций со стороны желудочно-кишечного тракта по сравнению с напроксен. (Bombardier et al, 2000). Это исследование, испытание VIGOR, подняло вопрос. сердечно-сосудистой безопасности коксибов — статистически незначимое увеличение по частоте возникновения инфарктов миокарда наблюдалось у пациентов, принимающих рофекоксиб.Дополнительные данные исследования APPROVe показали относительный риск сердечно-сосудистых заболеваний. события 1,97 по сравнению с плацебо — результат, который привел к отказу от употребления во всем мире рофекоксиба в октябре 2004 г.
Ингибиторы ЦОГ-3
Симмонс также совместно открыл ЦОГ-3 в 2002 году и проанализировал связь этого нового изофермента с парацетамолом (ацетаминофеном), возможно, наиболее широко используемым. обезболивающий препарат в мире. (Чандрасекхаран и др., 2002). Авторы постулировали что ингибирование ЦОГ-3 может представлять собой основной центральный механизм, с помощью которого эти препараты уменьшают боль и, возможно, жар.
Актуальность исследования был поставлен под сомнение, поскольку предполагаемый ген COX-3 кодирует белки с полностью отличные от ЦОГ-1 или ЦОГ-2 аминокислотные последовательности. Экспрессированные белки не проявляют активности ЦОГ и маловероятно, что они играют роль в простагландине опосредованные физиологические реакции. (Кис, 2005)
Ветеринария Использовать
НПВП Аналгезия
Исследования поддерживает использование НПВП для снятия боли, связанной с ветеринарными такие процедуры, как удаление рогов и кастрация телят.Наилучший эффект получается путем сочетания местного анестетика краткосрочного действия, такого как лидокаин, с НПВП, действующим как более длительный анальгетик. Однако большая часть имеющихся данных исследований относится к кетопрофену, в то время как это единственный НПВП, доступный в настоящее время для использования по назначению в США — флуниксин мегламин, показан для других состояний, кроме послеоперационных. боль.
Список литературы
- Предупреждение FDA для практикующих врачей целебрекса (целекоксиб)
- https: // www.fda.gov/cder/drug/infopage/vioxx/PHA_vioxx.htm
- Предупреждение для медицинских работников: валдекоксиб (продается как Bextra)
- Bombardier C, Laine L, Reicin A, Shapiro D, Burgos-Vargas R, Дэвис Б. и др. Сравнение токсичности рофекоксиба и верхних отделов желудочно-кишечного тракта. напроксен у пациентов с ревматоидным артритом. N Engl J Med 2000; 343 (21): 1520-8. PMID 11087881
- Сервера R, Balasch J. Ведение беременных с антифосфолипидным синдромом.Волчанка 2004; 13 (9): 683-7. PMID 15485103
- Чандрасекхаран Н.В., Дай Х., Роос К.Л., Эвансон Н.К., Томсик Дж., Элтон Т.С., Симмонс Д.Л. ЦОГ-3, циклооксигеназа-1 вариант, ингибируемый парацетамолом и другими обезболивающими / жаропонижающими препаратами: клонирование, структура и выражение. Proc Natl Acad Sci U S. A 2002; 99: 13926-31. PMID 12242329
- Грэм GG, Скотт KF, Day RO. Переносимость парацетамола. Drug Saf 2005; 28 (3): 227-40. PMID 15733027
- Зеленый GA.Понимание НПВП: от аспирина до ЦОГ-2. Clin Cornerstone 2001; 3 (5): 50-59. PMID 11464731
- Мур DE. Кожная светочувствительность, индуцированная лекарствами. Безопасность лекарств 2002; 25: 345-72. PMID 12020173
- Остенсен ME, Skomsvoll JF. Противовоспалительная фармакотерапия при беременности. Мнение эксперта Pharmacother 2004; 5 (3): 571-80. PMID 15013926
- Росси S, редактор. Австралийский Справочник по лекарствам 2006 г.
