Невропатия малоберцового нерва
Клиническая картина. Заболевание проявляется слабостью мышц разгибателей стопы и пальцев. Стопа висит, шлепает при ходьбе. Боль, онемение и парестезии распространяются от коленного сустава по боковой поверхности голени, по тылу стопы до 1 пальца. Боль в ноге может сопровождаться покалыванием, чувством жжения, ползания «мурашек» в стопе.
При объективном осмотре выявляют резкую болезненность в точке выхода малоберцового нерва. Снижена мышечная сила в разгибателе пальцев стопы, ограничено тыльное сгибание стопы, нарушено разгибание пальцев стопы. Шлепающая стопа производит «степпаж» при ходьбе.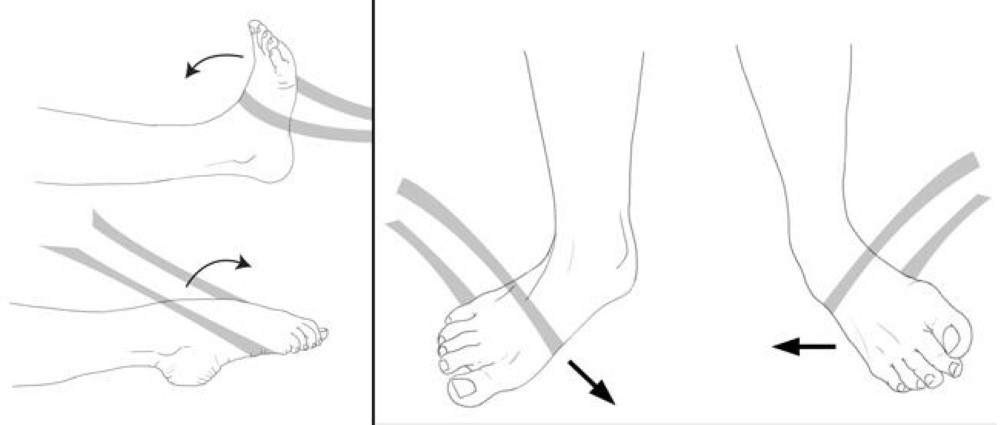
Нарушается чувствительность на тыле стопы и 1 пальце. Постукивание неврологическим молоточком над проекцией нерва в области головки малоберцовой кости (тест Тинеля) или прижатие нерва в этой точке (тест Фалена) провоцируют типичные боли, парестезии и онемение в ноге. При длительном течении заболевания происходит деформация стопы и пальцев по типу «конской».
Основные симптомы:
- слабость в ноге;
- свисающая стопа;
- шлепающая стопа;
- степпаж при ходьбе.
Диагностика невропатии малоберцового нерва:
- консультация невролога;
- УЗИ/МРТ коленного сустава позволяют уточнить причину компрессии нерва, исключить опухоль;
- МРТ головного мозга (очень редко опухоль вызывает развитие свисающей стопы).
- ЭНМГ малоберцового нерва подтверждает нарушение нервной проводимости по нерву, уточняет глубину поражения нерва;
- рентгенография коленного сустава исключает травматические причины заболевания.
Дифференциальный диагноз следует проводить с радикулопатией L4-L5, невропатией седалищного нерва, полинейропатией, переломом костей голени, опухолью.
Лечение невропатии малоберцового нерва.
Основные лекарственные препараты (имеются противопоказания, необходима консультация специалиста):
- мильгамма (комплекс витаминов группы Б) по 2 мл внутримышечно № 10 ежедневно, затем мильгамма композитум по 1 драже 3 раза в день внутрь 6-8 недель.
- тиоктацид (антиоксидант) по 600 мг внутривенно капельно на 200 мл физиологического раствора № 15, затем рекомендован прием препарата внутрь, утром за 30 минут до завтрака курсом от 1 до 3 месяцев.
- нейромидин (препарат для улучшения проведения нервных импульсов) по 20 мг 3 раза в день 1 месяц.
- трентал (сосудистый препарат для улучшения микроциркуляции). Режим дозирования: по 5 мл внутривенно капельно на 200 мл физиологического раствора № 10 1 раз в день.
Рекомендации. Для восстановления функции нерва показаны массаж, лечебная физкультура, грязелечение, иглорефлексотерапия. Хорошие результаты дает внутритканевая электростимуляция по методике лечения периферических нервов.
При позднем обращении в далеко запущенных случаях при неэффективности консервативного лечения производится оперативное освобождение нерва от сдавления.
Невропатия малоберцового нерва — причины, симптомы, диагностика и лечение
 Консервативное лечение осуществляется комбинацией медикаментозных, физиотерапевтических и ортопедических методов. При его несостоятельности показана операция (декомпрессия, шов нерва, транспозиция сухожилий и др.).
Консервативное лечение осуществляется комбинацией медикаментозных, физиотерапевтических и ортопедических методов. При его несостоятельности показана операция (декомпрессия, шов нерва, транспозиция сухожилий и др.).
Общие сведения

Следует также отметить, что зачастую специалистам в области неврологии приходится сталкиваться с пациентами, имеющими определенный стаж существования перонеальной невропатии, включающий послеоперационный период или время иммобилизации. Это затрудняет лечение, увеличивает его срок и ухудшает результат, поскольку, чем раньше начата терапия, тем она эффективнее.
Анатомии малоберцового нерва
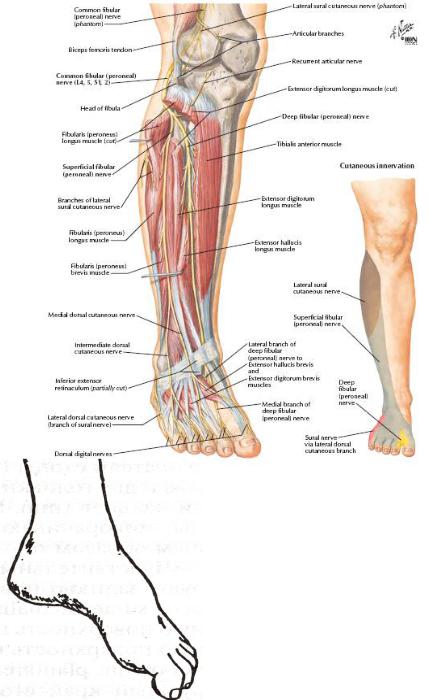
Малоберцовый нерв (n. peroneus) отходит от седалищного нерва на уровне нижней 1/3 бедра. Он состоит преимущественно из волокон LIV-LV и SI-SII спинальных нервов. После прохождения в подколенной ямке малоберцовый нерв выходит к головке одноименной кости, где его общий ствол делится на глубокую и поверхностную ветви. Глубокий малоберцовый нерв переходит в переднюю часть голени, спускается вниз, проходит на тыл стопы и разделяется на внутреннюю и наружную ветви. Он иннервирует мышцы, отвечающие за разгибание (тыльное сгибание) стопы и пальцев, пронацию (приподнимание наружного края) стопы.
Поверхностный малоберцовый нерв идет по переднелатеральной поверхности голени, где отдает двигательную ветвь малоберцовым мышцам, отвечающим за пронацию стопы с ее одновременным подошвенным сгибанием. В области медиальной 1/3 голени поверхностная ветвь n. peroneus переходит под кожу и разделяется на 2 тыльных кожных нерва — промежуточный и медиальный. Первый иннервирует кожу нижней 1/3 голени, тыльной поверхности стопы и III-IV, IV-V межпальцевых промежутков. Второй отвечает за чувствительность медиального края стопы, тыла I пальца и II-III межпальцевого промежутка.
Анатомически обусловленными участками наибольшей уязвимости малоберцового нерва являются: место его прохождения в районе головки малоберцовой кости и место выхода нерва на стопу.
Причины невропатии малоберцового нерва
Выделяют несколько групп триггеров, способных инициировать развитие перонеальной невропатии: травмы нерва; компрессии нерва окружающими его костно-мышечными структурами; сосудистые нарушения, ведущие к ишемии нерва; инфекционные и токсические поражения. Невропатия малоберцового нерва травматического генеза возможна при ушибах колена и других травмах коленного сустава, переломе голени, изолированном переломе малоберцовой кости, вывихе, повреждении сухожилий или растяжении связок голеностопного сустава, ятрогенном повреждении нерва в ходе репозиции костей голени, операций на коленном суставе или голеностопе.
Невропатия малоберцового нерва травматического генеза возможна при ушибах колена и других травмах коленного сустава, переломе голени, изолированном переломе малоберцовой кости, вывихе, повреждении сухожилий или растяжении связок голеностопного сустава, ятрогенном повреждении нерва в ходе репозиции костей голени, операций на коленном суставе или голеностопе.
Компрессионная невропатия (т. н. туннельный синдром) n. peroneus наиболее часто развивается на уровне его прохождения у головки малоберцовой кости —верхний туннельный синдром. Может быть связана с профессиональной деятельностью, например у сборщиков ягод, паркетчиков др. людей, работа которых предполагает длительное нахождение «на корточках». Такая невропатия возможна после длительного сидения, положив ногу на ногу. При компрессии малоберцового нерва в месте его выхода на стопу развивается нижний туннельный синдром. Он может быть обусловлен ношением чрезмерно тесной обуви. Зачастую причиной малоберцовой невропатии компрессионного характера выступает сдавление нерва при иммобилизации.
К более редким причинам перонеальной невропатии принадлежат системные заболевания, сопровождающиеся пролиферацией соединительной ткани (деформирующий остеоартроз, склеродермия, подагра, ревматоидный артрит, полимиозит), метаболические нарушения (диспротеинемии, сахарный диабет), тяжелые инфекции, интоксикации (в т. ч. алкоголизм, наркомания), местные опухолевые процессы.
Симптомы невропатии малоберцового нерва
Клинические проявления малоберцовой невропатии определяются типом и топикой поражения.
Поражение общего ствола малоберцового нерва проявляется расстройством разгибания стопы и ее пальцев. В результате стопа свисает вниз в позиции подошвенного сгибания и слегка ротирована кнутри. Из-за этого при ходьбе, перенося ногу вперед, пациент вынужден сильно сгибать ее в коленном суставе, чтобы не зацепить носком за пол. При опускании ноги на пол больной вначале становиться на пальцы, затем опирается на латеральный подошвенный край, а затем уже опускает пятку. Подобная походка напоминает петушиную или лошадиную и носит соответствующие названия.
Затруднены или невозможны: приподнимание латерального края подошвы, стояние на пятках и ходьба на них. Двигательные нарушения сочетаются с сенсорными расстройствами, распространяющимися на передне-латеральную поверхность голени и тыл стопы.
Невропатия малоберцового нерва с поражением глубокой ветви проявляется менее выраженным свисанием стопы, уменьшенной силой разгибания стопы и пальцев, сенсорными расстройствами на тыле стопы и в 1-ом межпальцевом промежутке. Длительное течение невропатии сопровождается атрофией мелкой мускулатуры на тыле стопы, что проявляется западением межкостных промежутков.
Невропатия малоберцового нерва с поражением поверхностной ветви характеризуется нарушением сенсорного восприятия и болями на латеральной поверхности нижней части голени и медиальной области тыльной поверхности стопы. При осмотре обнаруживается ослабление пронации стопы. Разгибание пальцев и стопы сохранено.
Диагностика невропатии малоберцового нерва
Алгоритм диагностики перонеальной невропатии основан на сборе анамнестических данных, которые могут указать на генез заболевания, и проведении тщательного исследования моторной функции и сенсорной сферы периферических нервов пораженной конечности. Проводятся специальные функциональные тесты для оценки мышечной силы различных мышц голени и стопы. Анализ поверхностной чувствительности осуществляется при помощи специальной иголки. Дополнительно используется электромиография и электронейрография, позволяющие по скорости проведения потенциалов действия установить уровень поражения нерва. Последнее время для исследования структуры нервного ствола и расположенных рядом с ним структур применяется УЗИ нерва.
Проводятся специальные функциональные тесты для оценки мышечной силы различных мышц голени и стопы. Анализ поверхностной чувствительности осуществляется при помощи специальной иголки. Дополнительно используется электромиография и электронейрография, позволяющие по скорости проведения потенциалов действия установить уровень поражения нерва. Последнее время для исследования структуры нервного ствола и расположенных рядом с ним структур применяется УЗИ нерва.
При травматической невропатии требуется консультация травматолога, по показаниям — УЗИ или рентгенография коленного сустава, рентгенография костей голени, УЗИ или рентгенография голеностопного сустава. В отдельных случаях могут применяться диагностические новокаиновые блокады нерва.
Невропатия малоберцового нерва требует дифференциальной диагностики с радикулопатией уровня LV-SI, наследственной рецидивирующей невропатией, болезнью Шарко-Мари-Тута, синдромом ПМА (перонеальной мышечной атрофии), БАС, полиневропатией, другими мононевропатиями нижних конечностей, церебральными опухолями и опухолями позвоночника.
Лечение невропатии малоберцового нерва
Больных с перонеальной невропатией курирует невролог. Вопрос хирургического лечения решается на консультации нейрохирурга. Составной частью лечения является устранение или уменьшение действия причинного фактора невропатии. В консервативной терапии используют противоотечный, противовоспалительный и противоболевой эффект НПВС (диклофенака, лорноксикама, нимесулида, ибупрофена и пр.). Препараты данной группы сочетают с витаминами группы В, антиоксидантами (тиоктовой кислотой), средствами для улучшения кровообращения нерва (пентоксифиллином, никотиновой кислотой). Назначение ипидакрина, неостигмина направлено на улучшение нервно-мышечной передачи.
Фармтерапия успешно сочетается с физиолечением: электрофорезом, амплипульстерапией, магнитотерапией, электростимуляцией, ультрафонофорезом и др. Для восстановления мышц, иннервируемых n. peroneus, обязательны регулярные занятия ЛФК. Для коррекции свисающей стопы пациентам показано ношение ортезов, фиксирующих ногу в правильном положении.
Показания к хирургическому лечению составляют случаи полного нарушения проводимости нерва, отсутствия эффекта консервативной терапии или возникновения рецидива после ее проведения. В зависимости от клинической ситуации возможно проведение невролиза, декомпрессия нерва, наложение шва или пластика. При застарелых невропатиях, когда мышцы, иннервируемые перонеальным нервом, утрачивают электровозбудимость, проводятся хирургические вмешательства по перемещению сухожилий.
Комплексное лечение тоннельных невропатий нижних конечностей Текст научной статьи по специальности «Клиническая медицина»
Ю.В. Мозолевский, А.Н. Баринов
Кафедра нервных болезней лечебного факультета ГБОУВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, Москва
Комплексное лечение тоннельных невропатий нижних конечностей
Обсуждены общие вопросы патогенеза тоннельных невропатий нижних конечностей с указанием эндогенных и экзогенных этиологических факторов. Подробно рассмотрены клинические проявления различных тоннельных невропатий нижних конечностей. Описаны методы диагностики и лечения тоннельных синдромов.
Подробно рассмотрены клинические проявления различных тоннельных невропатий нижних конечностей. Описаны методы диагностики и лечения тоннельных синдромов.
Ключевые слова: компрессионная невропатия; нарушения чувствительности; тесты Тинеля, Гольдберга.
Контакты: Алексей Николаевич Баринов [email protected] Для ссылки: Мозолевский ЮВ, Баринов АН. Комплексное лечение тоннельных невропатий нижних конечностей. Неврология,
нейропсихиатрия, психосоматика. 2013;(4):10—20.
Combination treatment for tunnel neuropathies of the lower extremities Yu.V. Mozolevsky, A.N. Barinov
Department of Nervous System Disorders, Faculty of Therapeutics, I.M. Sechenov First Moscow State Medical University, Ministry of
Health of Russia, Moscow
The paper discusses the general problems of the pathogenesis of tunnel neuropathies of the lower extremities with the endogenous and exogenous etiological factors being indicated. The clinical manifestations of tunnel neuropathies at this site are considered in detail. Various leg tunnel syndromes are characterized. Diagnostic and treatment methods for the above syndromes are considered.
The clinical manifestations of tunnel neuropathies at this site are considered in detail. Various leg tunnel syndromes are characterized. Diagnostic and treatment methods for the above syndromes are considered.
Key words: compression neuropathy; sensory disorders; Tinel’s test, Goldberg’s test.
Contact: Aleksey Nikolayevich Barinov [email protected] For reference: Mozolevsky YuV, Barinov AN. Combination treatment for tunnel neuropathies of the lower extremities. Neurology,
Neuropsychiatry, Psychosomatics. 2013;(4):10—20.
DOI: https://dx.doi.org/10.14412/2074-2711-2013-2449
Компрессия и нарушение микроциркуляции периферических нервов в анатомически узких фиброзных и фиброзно-костных каналах (тоннелях) нижних конечностей встречаются в практике невролога в два раза реже, чем тоннельные синдромы верхних конечностей [1], поэтому недостаточно хорошо известны широкому кругу практических врачей.
Патогенез
Тоннельные невропатии, относящиеся к мононевропатиям, часто наблюдаются на фоне эндокринных заболеваний (сахарный диабет, гипотиреоз, акромегалия), заболеваний суставов (деформирующий остеоартроз, ревматоидный артрит, подагра), объемных образований нервов (шван-нома, неврома) и вне нерва (саркома, липома), депозитарных невропатий (амилоидоз), при наследственной склонности к параличам от сдавления и некоторых физиологических изменениях гормонального статуса (беременность, климакс) [2—5]. Наиболее часто встречаются климактерические тоннельные невропатии, протекающие доброкачественно. Предполагается, что в их патогенез вовлечен процесс ослабления тормозящего влияния половых гормонов на секрецию соматотропного гормона гипофиза, который начинает выделяться в избытке, стимулируя набухание и гиперплазию соединительной ткани, в том числе внутри тоннелей (сходный механизм формирования тоннельных невро-
патий с более злокачественным течением наблюдается при акромегалии). Развитие тоннельных синдромов у беременных связывают с отеками и высоким содержанием в крови полипептида релаксина, приводящего к разрыхлению соединительной ткани. Тоннельные невропатии нижних конечностей могут возникать и у здоровых людей при профессиональных микротравмах, например во время строительных или сельскохозяйственных работ (в положении на коленях или на корточках), а также при воздействии вибрации и других травмирующих факторов [2, 6—8].
Развитие тоннельных синдромов у беременных связывают с отеками и высоким содержанием в крови полипептида релаксина, приводящего к разрыхлению соединительной ткани. Тоннельные невропатии нижних конечностей могут возникать и у здоровых людей при профессиональных микротравмах, например во время строительных или сельскохозяйственных работ (в положении на коленях или на корточках), а также при воздействии вибрации и других травмирующих факторов [2, 6—8].
К нарушению функции периферического нерва могут приводить механическая травма, ишемия (первичная или вследствие компрессии), венозный застой, отек тканей в «ловушечном пункте».
Существует ряд теорий возникновения тоннельных невропатий: дисметаболическая, воспалительная, гормональная, сосудистая, механическая, аномалийная, функциональная и другие, однако ни одна из них не может претендовать на роль универсальной [2, 4, 5, 7, 9—11]. Вероятно, следует говорить о мультифакторной природе тоннельных невропатий: для их развития необходима генетическая предрасположенность, а для проявления симптомов — воздействие различных средовых факторов (экзогенных и эндогенных).
К эндогенным факторам относят анатомические варианты строения костей и связок, а также периферических нервов;
особенности функционирования двигательного аппарата; сопутствующие эндокринные и метаболические расстройства, к экзогенным — механические и инфекционные факторы.
Во всех существующих теориях развития тоннельных невропатий фигурируют два фактора: декомпенсация в трофических системах нерва (нарушение аксоплазматического тока, кровоснабжения vasa nervorum) и локальные микротравмы периферических нервов. По наследству могут передаваться как недостаточность трофических систем периферических нервов, так и узость фиброзно-костных каналов (за счет особенностей строения и двигательного стереотипа). Поэтому в семьях больных тоннельными невропатиями часто наблюдается соответствующая патология [3, 4, 9].
Патогенез механического поражения периферических нервов хорошо изучен. Особенностью периферических нервов является то, что они приспосабливаются к существенным изменениям положения конечностей с помощью скользящих движений нерва в ложе. Подобная адаптация осуществляется вследствие высокоамплитудных, недифференцированных движений, во время которых нерв перемещается внутри ограниченного тоннеля, производя экстра-невральное движение. При интраневральных движениях отдельный пучок скользит относительно других в пределах нерва. Патологические процессы, такие как появление крови в эпиневральном пространстве, отек ложа нерва или ин-траневрального пространства, а также разволокнение или утолщение в тоннеле окружающей нерв фиброзной ткани (например, при коллагенозах, стенозирующем лигаменти-те), могут нарушать работу этого механизма. Движения конечностей при этом обусловливают значительный рост напряжения проксимальнее и дистальнее области патологических изменений. Диаметр нерва уменьшается, и интранев-ральное давление возрастает. Если оно превышает давление в эпиневральных артериолах, развивается преходящая ишемия нервных волокон.
Особенностью периферических нервов является то, что они приспосабливаются к существенным изменениям положения конечностей с помощью скользящих движений нерва в ложе. Подобная адаптация осуществляется вследствие высокоамплитудных, недифференцированных движений, во время которых нерв перемещается внутри ограниченного тоннеля, производя экстра-невральное движение. При интраневральных движениях отдельный пучок скользит относительно других в пределах нерва. Патологические процессы, такие как появление крови в эпиневральном пространстве, отек ложа нерва или ин-траневрального пространства, а также разволокнение или утолщение в тоннеле окружающей нерв фиброзной ткани (например, при коллагенозах, стенозирующем лигаменти-те), могут нарушать работу этого механизма. Движения конечностей при этом обусловливают значительный рост напряжения проксимальнее и дистальнее области патологических изменений. Диаметр нерва уменьшается, и интранев-ральное давление возрастает. Если оно превышает давление в эпиневральных артериолах, развивается преходящая ишемия нервных волокон. Это может приводить к формированию отека, усилению воспалительной реакции, нарастанию адгезии и дальнейшему уменьшению объема скользящего движения нерва или росту напряжения. В нервных стволах, особенно в участках нерва, прилегающих к зоне стенозиро-вания, образуются веретенообразные утолщения; в волокнах ствола происходят различные патоморфологические изменения (от демиелинизации до фрагментации осевых цилиндров и исчезновения аксонов [5, 7, 12].
Это может приводить к формированию отека, усилению воспалительной реакции, нарастанию адгезии и дальнейшему уменьшению объема скользящего движения нерва или росту напряжения. В нервных стволах, особенно в участках нерва, прилегающих к зоне стенозиро-вания, образуются веретенообразные утолщения; в волокнах ствола происходят различные патоморфологические изменения (от демиелинизации до фрагментации осевых цилиндров и исчезновения аксонов [5, 7, 12].
Помимо патологии соединительной ткани, диаметр тоннелей, в которых находится нерв, могут существенно менять форсированные движения, например, подошвенное сгибание и поворот внутрь стопы в голеностопном суставе вызывают перегиб и натяжение поверхностного малоберцового нерва в фиброзном отверстии глубокой фасции голени. Стереотипные длительные тонические и статические позиции и привычные характерные позы (положение нога на ногу, сидение на корточках и т. п.) также могут способствовать возникновению ишемии нерва, особенно если он при этом подвергается и внешнему сдавлению [3, 4, 7].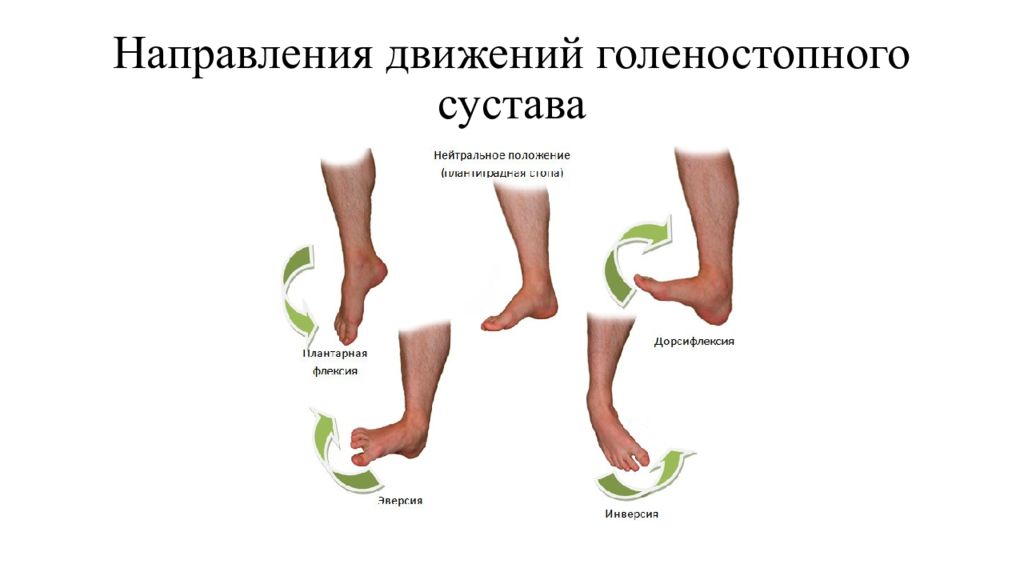
Таким образом, патогенез тоннельных компрессионно-ишемических невропатий включает увеличение объема периневральных тканей, повышение тканевого давления внутри тоннеля, нарушение кровообращения в комприми-рованном участке, гиперфиксацию нерва. Имеет значение изначальное состояние периферического нерва, подвергающегося компрессии: тоннельные невропатии развиваются
быстрее, если уже имеется поражение аксональных транспортных систем в проксимальном отделе (МАС-синдром — синдром множественного аксоплазматического сдавления при плексопатии или радикулопатии) или дистально (полиневропатии или множественные мононевропатии) на фоне дефицита аксоплазматического тока и нейротрофических факторов, требующихся для регенерации аксона [9, 11, 13]. Поэтому у каждого больного для уточнения патогенеза тоннельного синдрома и подбора оптимальной терапии необходимо учитывать наличие острых, подострых и хронических повреждений на всех уровнях периферической нервной системы, указывающих на наследственную или приобретенную узость фиброзно-костного канала.
Клинические проявления
Выделяют симптомы нарушения сенсорных, вегетативно-трофических (если нерв смешанный, то и моторных) функций с возможной невропатической болью в зоне, иннервируемой пораженным нервом, а также боль в области компрессии нерва, болезненность при поколачивании, растяжении, давлении (статическая гипералгезия). Эти симптомы могут усиливаться после физической нагрузки или в ночное время в связи с нарушением кровоснабжения нерва в области тоннеля [3, 7, 10, 14]. Клинические проявления невропатического болевого синдрома включают симптомо-комплекс спонтанной и стимул-зависимой боли в зоне иннервации периферического нерва, дистальнее зоны тоннельной компрессии (иногда — с иррадиацией боли проксимально) [15—17]. Интенсивная стреляющая, дергающая боль обычно не бывает постоянной, в то время как жгучая, ноющая боль может быть преходящей и временами высокоинтенсивной. Во многих случаях боль усиливается при физической или длительной статической нагрузке либо охлаждении. Спонтанная боль сопровождается, как правило, ал-лодинией, статической и динамической гипералгезией. Одними из наиболее ранних признаков тоннельной невропатии являются ночные парестезии, а также утреннее онемение конечностей (больные жалуются на «одеревенение» и «опухание» стопы, хотя при осмотре отек не обнаруживается), нарушение опорной функции ноги (стопа «подламывается», ощущение «ходьбы на костыле» и т. д.), особенно при вставании. Характерен феномен «расхаживания» — в ранних стадиях заболевания после нескольких минут ходьбы сенсорный и моторный дефицит регрессирует. В дебюте заболевания позитивная неврологическая симптоматика (боль, парестезии и онемение) преобладает над негативной невропатической симптоматикой (симптомы выпадения), которая проявляется снижением чувствительности различных модальностей, а при вовлечении двигательных волокон — гипорефлексией, слабостью и атрофией мышц. При вовлечении артерий и вен возможны сосудистые расстройства, при которых наблюдаются побледнение, снижение локальной температуры или появление цианоза и отечности в области поражения.
Спонтанная боль сопровождается, как правило, ал-лодинией, статической и динамической гипералгезией. Одними из наиболее ранних признаков тоннельной невропатии являются ночные парестезии, а также утреннее онемение конечностей (больные жалуются на «одеревенение» и «опухание» стопы, хотя при осмотре отек не обнаруживается), нарушение опорной функции ноги (стопа «подламывается», ощущение «ходьбы на костыле» и т. д.), особенно при вставании. Характерен феномен «расхаживания» — в ранних стадиях заболевания после нескольких минут ходьбы сенсорный и моторный дефицит регрессирует. В дебюте заболевания позитивная неврологическая симптоматика (боль, парестезии и онемение) преобладает над негативной невропатической симптоматикой (симптомы выпадения), которая проявляется снижением чувствительности различных модальностей, а при вовлечении двигательных волокон — гипорефлексией, слабостью и атрофией мышц. При вовлечении артерий и вен возможны сосудистые расстройства, при которых наблюдаются побледнение, снижение локальной температуры или появление цианоза и отечности в области поражения. Однако при изолированном поражении нерва могут также появиться сосудистые и трофические изменения за счет вовлечения автономных волокон, хотя чаще всего они выражены незначительно [5, 7, 15].
Однако при изолированном поражении нерва могут также появиться сосудистые и трофические изменения за счет вовлечения автономных волокон, хотя чаще всего они выражены незначительно [5, 7, 15].
Локализация нарушений чувствительности у разных пациентов широко варьирует вследствие преморбидных вариантов сенсорной иннервации кожи, существования зон перекрытия смежными нервами, а также асимметрии ком-
прессии нервного ствола [3, 4]. Это можно сказать и о слабости, которая нередко носит анталгический, а иногда и психогенный характер [2, 5, 17].
В связи с деликатностью или непостоянством объективных признаков повреждения нерва традиционное неврологическое исследование должно быть дополнено специальными клиническими тестами, провоцирующими парестезии и боль и направленными на поиск места компрессии [3, 14]:
1) тест Тинеля — при перкуссии в зоне повреждения над проекцией нерва, например в канале Рише (при заднем тарзальном синдроме) или тоннеле под нижним удерживателем разгибателей (при переднем тарзальном синдроме), появляются боль и/или парестезии в области иннервации нерва, дистальнее (иногда и про-ксимальнее) места перкуссии;
2) тест пальцевой компрессии Гольдберга — как и в тесте Тинеля, на протяжении 1 мин проводится давление большим пальцем на общий малоберцовый нерв в проекции фибулярного канала, давление между головками метатарзальных костей при метатарзалгии Мортона и т. д. В ответ возникают парестезии и боль по ходу компримированного нерва;
д. В ответ возникают парестезии и боль по ходу компримированного нерва;
3) турникетный (манжеточный) тест — чаще проводится при невропатиях рук, но может выполняться и на нижних конечностях: проксимальнее места предполагаемой компрессии нерва (на бедре или голени) накладывают манжету тонометра и нагнетают в ней давление до обычного систолического или немного выше, выжидают 1 мин. При наличии тоннельного синдрома появляются парестезии в зоне иннервации компримированного нерва. Этот тест может быть использован и для оценки степени тяжести заболевания, если измерять время от начала манжетной компрессии до появления парестезии. Он с успехом применяется и для контроля эффективности лечения;
4) тест поднятия конечностей (элевационный тест) — при невропатиях ног в положении лежа поочередно на 1 мин поднимают одну, а затем другую выпрямленную ногу. Вследствие уменьшения гидростатического давления в артериях конечностей нарушается кровоснабжение нервов и возникают парестезии;
5) тест форсированных, максимальных по объему пассивных движений — выбирают такое направление движения, при котором пораженный нерв испытывает еще большую степень компрессии и натяжения. При компрессионной невропатии седалищного нерва в подгрушевидном пространстве (синдром грушевидной мышцы) отведение вбок согнутой в колене ноги в положении на животе провоцирует боль и парестезии в проекции седалищного нерва (проба Бонне). При синдроме тарзального канала одновременная пронация и экстензия стопы вызывают боль и парестезии в подошвенной части стопы, иногда с распространением в заднемедиальный отдел голени. Механизм этой группы пассивных провоцирующих движений может быть отнесен к тракции нерва, нередко дополняемой его гиперангуляцией и компрессией.
При компрессионной невропатии седалищного нерва в подгрушевидном пространстве (синдром грушевидной мышцы) отведение вбок согнутой в колене ноги в положении на животе провоцирует боль и парестезии в проекции седалищного нерва (проба Бонне). При синдроме тарзального канала одновременная пронация и экстензия стопы вызывают боль и парестезии в подошвенной части стопы, иногда с распространением в заднемедиальный отдел голени. Механизм этой группы пассивных провоцирующих движений может быть отнесен к тракции нерва, нередко дополняемой его гиперангуляцией и компрессией.
Однако не все эти тесты бывают положительными даже в поздних стадиях тоннельных невропатий. Поэтому для точной диагностики поражения периферических нервов и МАС-синдрома и выбора терапии необходимо знание особенностей наиболее типичных тоннельных синдромов тазового пояса и ног и их связи с корешками спинномозговых нервов [4, 5, 7].
Поражение бедренного нерва (Ь-п) в забрюшинном пространстве (рис. 1) часто вызывается воспалением и мышечно-тоническими синдромами большой поясничной и/или подвздошной мышцы в результате травм или биомеханических перегрузок (профессионального или спортивного характера) [5, 18]. Бедренный нерв берет начало в поясничном сплетении и выходит из полости малого таза под паховой связкой между большой поясничной и подвздошной мышцами, будучи фиксирован к их фасциям. Соответственно, любые патологические процессы в области этих мышц могут вызывать повреждение бедренного нерва. Редкими, но гораздо более неблагоприятными в прогностическом плане причинами компрессии бедренного нерва могут быть опухоли (лимфо-ма, саркома), абсцессы и гематомы (вызванные гемофилией, антикоагулянтной терапией и т. п.) забрюшинного пространства. Описаны случаи повреждения нерва при аневризмах общей подвздошной и бедренной артерий, а также артериовенозных мальформациях, аппендэктомии, передней фузии поясничных позвонков, операциях на почках и мочеточниках и других вмешательствах в этой области.
1) часто вызывается воспалением и мышечно-тоническими синдромами большой поясничной и/или подвздошной мышцы в результате травм или биомеханических перегрузок (профессионального или спортивного характера) [5, 18]. Бедренный нерв берет начало в поясничном сплетении и выходит из полости малого таза под паховой связкой между большой поясничной и подвздошной мышцами, будучи фиксирован к их фасциям. Соответственно, любые патологические процессы в области этих мышц могут вызывать повреждение бедренного нерва. Редкими, но гораздо более неблагоприятными в прогностическом плане причинами компрессии бедренного нерва могут быть опухоли (лимфо-ма, саркома), абсцессы и гематомы (вызванные гемофилией, антикоагулянтной терапией и т. п.) забрюшинного пространства. Описаны случаи повреждения нерва при аневризмах общей подвздошной и бедренной артерий, а также артериовенозных мальформациях, аппендэктомии, передней фузии поясничных позвонков, операциях на почках и мочеточниках и других вмешательствах в этой области.
В типичных случаях поражение бедренного нерва в области подвздошно-поясничной мышцы приводит к развитию двигательных, чувствительных и вегетативно-трофических нарушений во всей зоне его иннервации. Однако анатомические вариации формирования и прохождения бедренного нерва (например, высокое разделение бедренного нерва на мышечные ветви и подкожный нерв, стволы которых могут проходить раздельно) в ряде случаев сопровождаются преимущественным или даже изолированным поражением чувствительной или двигательной порции этого нерва либо мозаичным распределением двигательных, чувствительных и вегетативно-трофических расстройств.
Двигательные нарушения обусловлены парезами подвздошно-поясничной и четырехглавой мышц. Слабость пояснично-подвздошной мышцы проявляется расстройством сгибания бедра в тазобедренном суставе и поднятия туловища из положения лежа и сидя. Однако полного расстройства этих функций не происходит, так как большая поясничная и подвздошная мышцы иннервируются, помимо бедренного нерва, еще и мышечными ветвями, отходящими непосредственно от поясничного сплетения.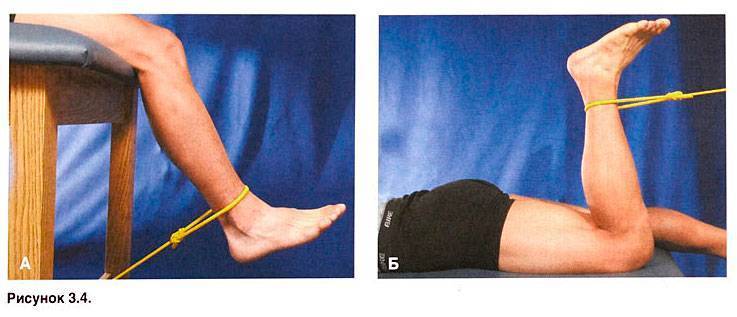 Кроме того, сгибание бедра возможно за счет гребешковой мышцы, иннервируемой, помимо бедренного, запирательным нервом. Как правило, хорошо заметно уменьшение окружности бедра вследствие выраженной гипотрофии четырехглавой и
Кроме того, сгибание бедра возможно за счет гребешковой мышцы, иннервируемой, помимо бедренного, запирательным нервом. Как правило, хорошо заметно уменьшение окружности бедра вследствие выраженной гипотрофии четырехглавой и
Латеральный кожный нерв бедра
Паховая
связка
Бедренный
нерв
Рис. 1. Топография бедренного нерва
портняжной мышц. Характерно выпадение коленного рефлекса. Из-за пареза четырехглавой мышцы нарушается разгибание в коленном суставе, затрудняются ходьба, бег и особенно подъем по лестнице. Частично разгибание голени компенсируется мышцей, напрягающей широкую фасцию бедра. Больные стараются не сгибать ногу, поскольку не могут ее разогнуть, и фиксируют конечность в положении чрезмерного разгибания в коленном суставе, что приводит к изменению походки. Нога слишком сильно разгибается в коленном суставе, поэтому при ходьбе выбрасывается вперед и ставится всей подошвой.
Нога слишком сильно разгибается в коленном суставе, поэтому при ходьбе выбрасывается вперед и ставится всей подошвой.
Чувствительные вазомоторные и трофические нарушения и невропатическая боль выявляются в передней и медиальной поверхностях бедра, голени и стопы до основания I пальца. Характерны симптомы натяжения Вассермана (появление боли по передней поверхности бедра и в паху при разгибании ноги в тазобедренном суставе в положении лежа на животе) и Мицкевича (боль в паховой области, иррадиирующая по передней поверхности бедра при максимальном сгибании голени в положении лежа на животе).
Поражение бедренного нерва под паховой связкой (между сухожилием подвздошно-поясничной и гребенчатой мышц; рис. 2) — область выхода нерва на бедро (рис. 3) особенно подвержена повреждениям из-за сравнительно плохого кровоснабжения. Здесь проходит «водораздел» между бассейнами двух артериальных стволов, снабжающих бедренный нерв (проксимальный отдел до паховой связки получает кровь из ветви подвздошно-поясничной артерии, а дистальный отдел, ниже паховой связки, — от ветвей артерий, огибающих бедренную кость). Частая причина бедренной невропатии на этом уровне — тракционное повреждение нерва и сдавление его паховой связкой при длительном вынужденном положении с гиперэкстензией либо чрезмерным отведением, сгибанием и наружной ротацией бедра (например, при гинекологических операциях и др.).
Частая причина бедренной невропатии на этом уровне — тракционное повреждение нерва и сдавление его паховой связкой при длительном вынужденном положении с гиперэкстензией либо чрезмерным отведением, сгибанием и наружной ротацией бедра (например, при гинекологических операциях и др.).
Кроме того, компрессию нерва могут вызывать бедренная грыжа, паховая
лимфаденопатия, аневризма бедренной артерии [4, 18]. Из ятрогенных факторов следует отметить хирургическую коррекцию паховых и бедренной грыж, артропластику и иные операции на тазобедренном суставе, осложнения при выполнении катетеризации бедренной артерии.
Клиническая картина в целом аналогична таковой при поражении бедренного нерва в забрюшинном пространстве, однако отсутствует парез подвздошно-поясничной мышцы, поэтому не нарушены сгибание бедра в тазобедренном суставе и поднимание туловища из положения лежа и сидя.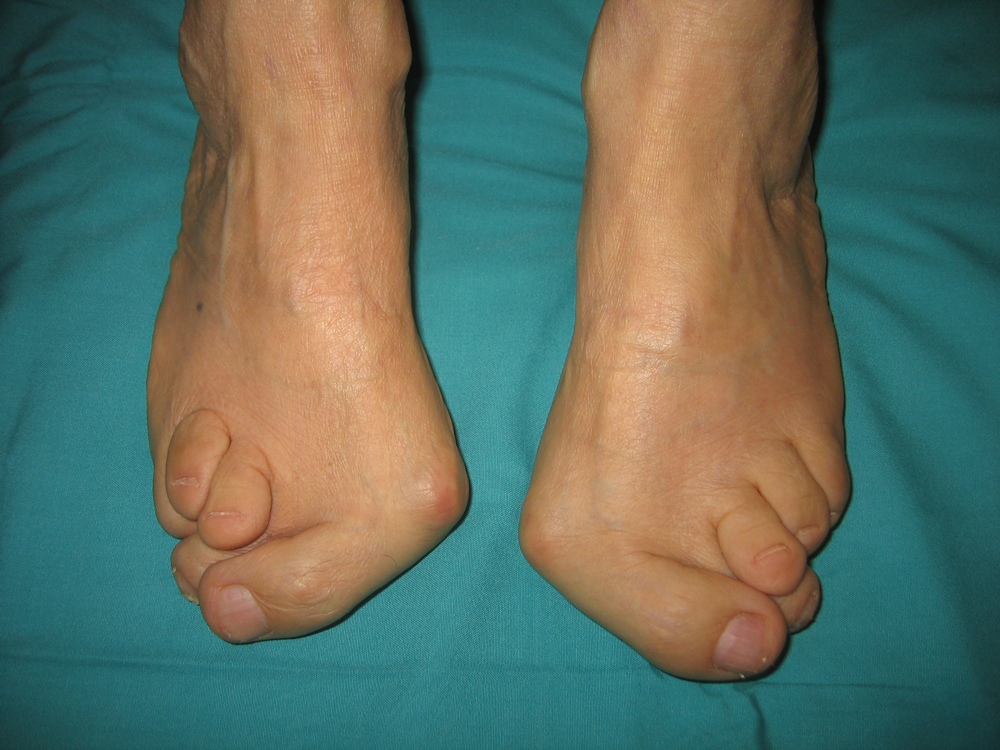 В тех случаях, когда бедренный нерв разделяется на двигательные ветви и подкожный нерв до уровня паховой связки, возмож-
В тех случаях, когда бедренный нерв разделяется на двигательные ветви и подкожный нерв до уровня паховой связки, возмож-
Рис. 2. Поражение бедренного нерва под паховой связкой
Рис. 3. Бедренный треугольник: выход бедренного нерва, артерии и вены из-под паховой связки
Рис. 4. Компрессионная невропатия подкожного нерва
но преобладание чувствительных расстройств над двигательными. Наряду с положительными симптомами натяжения обычно удается обнаружить болезненность в области середины паховой связки — место компрессии бедренного нерва.
Компрессионная невропатия подкожного нерва (терминальной ветви бедренного нерва; Ь-п) в приводящем «подпортняжном», или гунтеровском, канале бедра (рис. 4) — образованный медиальной широкой и большой приводящими мышцами канал спереди ограничен фиброзной пластинкой, натянутой между указанными мышцами, к этой же фасции спереди фиксирована портняжная мышца. Перенапряжение приводящих мышц, а также нестабильность коленного сустава, его врожденные или приобретенные деформации (особенно варусные) приводят к ущемлению нерва, в типичных случаях — в области прободения фасциальной пластинки (на ладонь выше медиального надмыщелка бедра под портняжной мышцей). Другими причинами поражения подкожного нерва могут быть бурсит в области гусиной лап-
Перенапряжение приводящих мышц, а также нестабильность коленного сустава, его врожденные или приобретенные деформации (особенно варусные) приводят к ущемлению нерва, в типичных случаях — в области прободения фасциальной пластинки (на ладонь выше медиального надмыщелка бедра под портняжной мышцей). Другими причинами поражения подкожного нерва могут быть бурсит в области гусиной лап-
Рис. 5. Компрессия седалищного нерва в подгрушевидном пространстве (стрелки)
ки (ре.? атеппш), компрессия аберрантными ветвями или аневризмой бедренной артерии, ятрогенные факторы (операция на коленном суставе).
Клинически синдром приводящего канала проявляется болью, парестезиями и расстройством чувствительности в области медиального края колена, передней и медиальной поверхности голени и внутреннего края стопы. Возможно снижение секреции потовых желез в этой области. Боль усиливается при разгибании и приведении бедра; в точке выхода подкожного нерва положительны симптомы Тинеля, Гольдберга. Характерно нарушение походки: пациент избегает усиливающей боль полной экстензии голени и предпочитает ходить, слегка согнув ногу в коленном суставе. Двигательные нарушения отсутствуют, коленный рефлекс сохранен [5, 7, 18].
Боль усиливается при разгибании и приведении бедра; в точке выхода подкожного нерва положительны симптомы Тинеля, Гольдберга. Характерно нарушение походки: пациент избегает усиливающей боль полной экстензии голени и предпочитает ходить, слегка согнув ногу в коленном суставе. Двигательные нарушения отсутствуют, коленный рефлекс сохранен [5, 7, 18].
Изолированное поражение поднадколенниковой ветви подкожного нерва в области медиального края надколенника (парестетическая гониалгия) проявляется болью, парестезиями и нарушением чувствительности. Иногда развитию заболевания предшествуют повторные мелкие травмы коленного сустава или длительное пребывание на коленях, но чаще оно появляется без видимых причин. В редких случаях подкожный нерв может быть поражен на уровне голени над медиальной лодыжкой. В качестве этиологических факторов обычно выступают повторные мелкие травмы, варикоз или тромбофлебит подкожной вены. Отмечаются жгучая боль и парестезии по медиальному краю стопы, усиливающиеся при ходьбе и подъеме по лестнице [5]. ш) между грушевидной мышцей и крестцово-остистой связкой (рис. 5), проявляется болью преимущественно по задней поверхности ноги, чувствительными и двигательными нарушениями в области иннервации большеберцового и малоберцового нервов.
ш) между грушевидной мышцей и крестцово-остистой связкой (рис. 5), проявляется болью преимущественно по задней поверхности ноги, чувствительными и двигательными нарушениями в области иннервации большеберцового и малоберцового нервов.
Грушевидная мышца расположена под большой ягодичной мышцей. Она начинается у переднего края верхнего отдела крестца и прикрепляется к внутреннему краю большого вертела бедра, которое при ее сокращении отводится кнаружи. Характерны болезненность при пальпации в области большого вертела бедра и нижнего отдела крестцово-
Рис. 6. Компрессия общего малоберцового нерва в фибулярном канале (стрелка)
(приведение с одновременной ротацией внутрь бедра сопровождается болью в области ягодицы и по ходу седалищного нерва вследствие натяжения грушевидной мышцы).
Фибулярный синдром (рис. 6) возникает вследствие компрессии общего малоберцового нерва (Ьу, Ьу, SI) в тоннеле, крыша которого образуется началом длинной малоберцовой мышцы и межмышечной перегородкой, верхняя порция арки прикрепляется к головке малоберцовой кости, а нижняя — к ее боковой поверхности.
6) возникает вследствие компрессии общего малоберцового нерва (Ьу, Ьу, SI) в тоннеле, крыша которого образуется началом длинной малоберцовой мышцы и межмышечной перегородкой, верхняя порция арки прикрепляется к головке малоберцовой кости, а нижняя — к ее боковой поверхности.
Повреждение нерва происходит на уровне головки малоберцовой кости от внешнего воздействия либо сосудисто-нервный пучок подвергается компрессии на этом уровне из-за длительного интенсивного сближения двуглавой мышцы бедра с головкой малоберцовой кости. Впервые эту патологию описали в 1934 г. французские клиницисты Гийен, Сез, де Блон-ден и Вальтер как профессиональный паралич копальщиков луковиц тюльпанов [19]. Преимущественно страдают лица, работающие на корточках и на коленях (сборщики мебели, корнеплодов, винограда, укладчики плитки и паркета, чистильщики обуви). В роли этиотропного и провоцирующего фактора могут также выступать продолжительная поза «нога на ногу» (у анорексичных фотомоделей), пребывание в высоком кресле со свободно свисающими ногами, сон в неудобной позе (согнутая в коленном суставе нога, свисающая через край кровати нога, сон сидя), гипсовая повязка и т. п. Фибулярный синдром характеризуется преимущественно острым (от 1 до 24 ч), реже — подострым (менее чем у 20% больных — от 2 до 10 сут) развитием периферического пареза разгибателей стопы с нарушением походки (степпаж), парестезиями и гипестезией по наружной поверхности левой голени и на тыльной поверхности левой стопы. Интенсивный болевой синдром при поражении малоберцового нерва (ввиду малого содержания тонких немиелинизированных «болевых» волокон) нехарактерен, поэтому в начальной стадии заболевания у пациентов отсутствуют настороженность и беспокойство по поводу сенсорных нарушений, и они нередко оказываются перед фактом уже развившегося пареза. Даже в тех случаях, когда невропатии сопутствует болевой синдром (<20%), парез способствует существенному уменьшению или исчезновению боли, и пациенты длительное время игнорируют двигательный дефект. В каждом 10-м случае нарушения выявляются с двух сторон. В патогенезе заболевания имеет значение то, что малоберцовые мышцы и нервы обеспечивают филогенетически новую функцию вертикальной ходьбы, а филогенетически молодые структурно-функциональные образования обладают повышенной чувствительностью к повреждающим агентам, это может служить предпосылкой для их частого и раннего повреждения при развитии патологических процессов на разных уровнях нервной системы [6, 8].
п. Фибулярный синдром характеризуется преимущественно острым (от 1 до 24 ч), реже — подострым (менее чем у 20% больных — от 2 до 10 сут) развитием периферического пареза разгибателей стопы с нарушением походки (степпаж), парестезиями и гипестезией по наружной поверхности левой голени и на тыльной поверхности левой стопы. Интенсивный болевой синдром при поражении малоберцового нерва (ввиду малого содержания тонких немиелинизированных «болевых» волокон) нехарактерен, поэтому в начальной стадии заболевания у пациентов отсутствуют настороженность и беспокойство по поводу сенсорных нарушений, и они нередко оказываются перед фактом уже развившегося пареза. Даже в тех случаях, когда невропатии сопутствует болевой синдром (<20%), парез способствует существенному уменьшению или исчезновению боли, и пациенты длительное время игнорируют двигательный дефект. В каждом 10-м случае нарушения выявляются с двух сторон. В патогенезе заболевания имеет значение то, что малоберцовые мышцы и нервы обеспечивают филогенетически новую функцию вертикальной ходьбы, а филогенетически молодые структурно-функциональные образования обладают повышенной чувствительностью к повреждающим агентам, это может служить предпосылкой для их частого и раннего повреждения при развитии патологических процессов на разных уровнях нервной системы [6, 8].
Следует дифференцировать фибулярный синдром от
подвздошного сочленения, положительная проба Бонне синдрома «мышечных лож» — переднего фасциального ло-
жа голени, также возникающего после непривычной длительной физической нагрузки на мышцы голени, а иногда у больных эпилепсией после длительной тетании с выраженным карпопедальным спазмом. Появляются боль, напряжение и отек мышц переднего фасциального ложа голени, иногда гиперемия кожи передней поверхности голени. Через 1—4 дня развивается парез разгибателей стопы. Хирургическая декомпрессия эффективна в первые 6 ч после появления слабости [5, 6].
Малоберцовая мононевралгия Генри — тракционная невропатия поверхностного малоберцового нерва (Ьу—у, SI) в фиброзном отверстии в глубокой фасции голени, перегиб и натяжение чувствительной ветви малоберцового нерва при форсированном подошвенном сгибании и повороте внутрь стопы в голеностопном суставе [4, 5]. Чувствительность нарушается на тыле стопы, кроме первого межпальцевого промежутка (иннервация осуществляется кожными ветвями глубокого малоберцового нерва) и наружного края стопы (иннервация осуществляется ветвями икроножного нерва).
Чувствительность нарушается на тыле стопы, кроме первого межпальцевого промежутка (иннервация осуществляется кожными ветвями глубокого малоберцового нерва) и наружного края стопы (иннервация осуществляется ветвями икроножного нерва).
Передний тарзальный тоннельный синдром — следствие компрессии терминальной части глубокого малоберцового нерва (Ьу—у, SI) в тоннеле под нижним удерживателем разгибателей. Изолированное поражение может появиться в медиальной ветви нерва, проходящей в костно-мышечном тоннеле под коротким разгибателем I пальца стопы. Этот синдром нередко возникает у бегунов при наличии сухожильных ганглиев, остеофитов в голеностопном, клиновидно-ладьевидном или предплюсне-плюсневых суставах. У бегунов или лыжников нерв нередко подвергается компрессии при ношении плотно пригнанной спортивной обуви [5]. При поражении общего ствола глубокого малоберцового нерва или обеих его ветвей отмечаются боль и парестезии в I и II пальцах стопы, боль на тыле стопы без четкой локализации, расстройство чувствительности кожи первого межплюсневого промежутка и смежных поверхностей I и II пальцев. Могут наблюдаться ослабление супинации стопы и разгибания пальцев, парез и атрофия мелких мышц стопы. Форсированное сгибание стопы и пальцев усиливает боль. При изолированной компрессии медиальной кожной ветви выявляют перечисленные симптомы за исключением боли на тыле стопы и двигательных нарушений. Диагностическое значение имеет новокаиновая проба. Сначала вводят 3—5 мл 0,5—1% раствора новокаина подфас-циально в проксимальной части первого межплюсневого промежутка. При поражении медиальной ветви нерва на этом уровне после анестезии боль прекращается. Исчезнове-
Могут наблюдаться ослабление супинации стопы и разгибания пальцев, парез и атрофия мелких мышц стопы. Форсированное сгибание стопы и пальцев усиливает боль. При изолированной компрессии медиальной кожной ветви выявляют перечисленные симптомы за исключением боли на тыле стопы и двигательных нарушений. Диагностическое значение имеет новокаиновая проба. Сначала вводят 3—5 мл 0,5—1% раствора новокаина подфас-циально в проксимальной части первого межплюсневого промежутка. При поражении медиальной ветви нерва на этом уровне после анестезии боль прекращается. Исчезнове-
ние боли после введения такого же количества новокаина в области удер-живателя разгибателей (см. ниже) подтверждает диагноз переднего тарзального тоннельного синдрома [4, 5].
Для локальной инъекционной терапии синдрома переднего тарзального канала при определении точек введения иглы (рис. 7) проводят ори-ентирные линии: вертикальную линию (1), расположенную на равном расстоянии от медиальной и латеральной лодыжек, верхнюю горизонтальную линию (2), соединяющую надлодыжечные области, и нижнюю горизонтальную линию (3), соединяющую верхушки лодыжек. Иглу вводят под углом 45° в сагиттальной плоскости сверху вниз в точке пересечения 4-й вертикальной и верхней горизонтальной линий, а в точке пересечения 5-й вертикальной и нижней горизонтальной линий иглу вводят снизу вверх под углом 45° в сагиттальной плоскости.
Синдром тарзального канала (синдром канала Рише) — следствие сдавления дистальной части большеберцового нерва (Ьу) во внутреннем лодыжечном костно-фиброзном канале (рис. 8), который соединяет область голеностопного сустава с плантарной областью.
Канал Рише имеет 2 отверстия (верхнее и нижнее), в нем проходят сухожилия задней большеберцовой мышцы, длинных сгибателей большого и других пальцев стопы и задний большеберцовый сосудисто-нервный пучок: нерв лежит снаружи артерии и проецируется на равном расстоянии между ахилловым сухожилием и задним краем внутренней лодыжки. Сдавление (тест Гольдберга) и перкуссия (тест Тинеля) нерва в этой области могут вызвать характерную боль и парестезии в подошвенной части стопы, иногда с распространением в заднемедиальный отдел голени. Эти же симптомы возникают при одновременной пронации и экстензии стопы. Чаще всего синдром тарзального канала вызывают механическое сдавление тесной обувью, травма или повторяющаяся мик-ротравматизация лодыжки с фиброзом и утолщением подошвенной фасции; он может наблюдаться при ревматоидном артрите, гипотиреозе и теносиновите. Необходимо исключить новообразования нерва (шванномы). При неэффективности консервативной терапии проводят хирургическое рассечение стенок канала Рише [5].
Тракционно-компрессионная невропатия подошвенных нервов (рис. 9) —возникает в фиброзных отверстиях в верхнемедиальной части мышцы, отводящей большой палец стопы. В канале лодыжки под удерживателем сгибателей большеберцовый нерв разделяется на две терминальные ветви — медиальный и латеральный подошвенные нервы, проходя-
Рис. 7. Определение точек введения иглы с помощью ориентирных линий (1—5, описание в тексте)
Рис. 8. Компрессия большеберцового нерва в тарзальном канале
щие на медиальном крае стопы под мышцей, отводящей большой палец.
Медиальный подошвенный нерв проходит в медиальной подошвенной борозде, частично прикрытый апоневрозом подошвы, между мышцей, отводящей большой палец, и коротким сгибателем пальцев, иннервируя пальцы от латеральной поверхности I пальца до медиальной поверхности IV пальца, включая ногтевые ложа. Латеральный подошвенный нерв проходит между коротким сгибателем пальцев и квадратной мышцей подошвы в латеральной борозде подошвы. Схема иннервации подошвенного нерва напоминает схему иннервации локтевого нерва на кисти.
Клиническая картина поражения подошвенных нервов — болезненные парестезии на подошве, которые усиливаются при ходьбе, нарушение чувствительности в подошве, дисгидроз и парез мелких мышц подошвы. При хронической невропатии подошвенных нервов (как и при любом дистальном поражении большеберцового нерва) парез коротких мышц стопы при сохранных длинных сгибателях пальцев и иннервируемых малоберцовым нервом разгибателях вызывает деформацию стопы по типу «кошачьей (когтистой) лапы» с ангидрозом подошвы [3, 5].
Невропатия нижнего пяточного нерва — поражение первой ветви латерального подошвенного нерва, иннервирующего мышцу, отводящую мизинец стопы, иногда квадратную мышцу стопы. Участки сенсорной иннервации этого нерва отсутствуют, однако он иннервирует надкостницу передней части пяточной кости. Поражение этой ветви может стать причиной интенсивной боли в области пятки без расстройства чувствительности [5]. Парез отводящей мизинец мышцы, подтвержденный электромиографически, служит основанием для диагностики этой патологии.
Рис. 10. Компрессия подошвенного пальцевого нерва (1) под глубокой поперечной метатарзальной связкой (2)
Метатарзалгия Мортона
(рис. 10) — первая описанная тоннельная невропатия (1876 г.), изолированное поражение подошвенных пальцевых нервов вследствие сдавления под глубокой поперечной метатарзальной связкой, натянутой между головками II—IV плюсневых костей при длительной гиперэкстензии в метатарзофа-ланговых суставах с одновременным разведением (для увеличения площади опоры) пальцев стопы. В дебюте заболевания появляется боль преимущественно жгучая, иногда стреляющая и ноющая, в П—ГУ пальцах стопы в сочетании с парестезиями, аллоди-нией и другими расстройствами чувствительности. От 70 до 80% больных составляют женщины, что связано с ношением тесной (суживающейся кпереди) обуви, хождением на высоких каблуках и развитием поперечного плоскостопия, приводящего к необычно высокому давлению на плюсневую область [3, 5, 7]. Часто метатарзалгия наблюдается в структуре синдрома диабетической стопы из-за гипертрофии и деформации метатарзофаланговых суставов вследствие остеоартроза. Поэтому лечение начинают с разгрузки стопы, периодического использования плюсневых прокладок и подъемников, ношения обуви с ретрокапитальной опорой. Затем переходят к введению глюкокортикоидов (ГК) с тыльной стороны стопы в межкостный промежуток, что в 50% случаев приводит к улучшению, а в 30% — к выздоровлению. При синдроме диабетической стопы во избежание декомпенсации сахарного диабета, а также инфекционных осложнений иммуносупрессивной терапии ГК целесообразно начать локальную инъекционную терапию нестероидными противовоспалительными препаратами (НПВП). В любом случае при наличии деформирующего артроза необходимо назначить длительную профилактическую терапию хондропроте-кторами (курс 3—6 мес). При безуспешности консервативной терапии показано хирургическое лечение с доступом на тыльной стороне стопы, поскольку это способствует ранней реабилитации с нагрузкой на подошву.
Невропатия икроножного нерва — поражение сенсорного ствола, формирующегося из волокон большеберцового и общего малоберцового нервов на задней поверхности голени, проходящих латеральнее ахиллова сухожилия, позади латеральной лодыжки. Икроножный нерв иннервирует нижнелатеральную поверхность голени, латеральную лодыжку, латеральный край стопы и У палец. Изолированное поражение икроножного нерва наблюдается редко, этиологические факторы: киста Бейкера в подколенной ямке, травма коленного сустава при артроскопии и хирургическом вмешательстве задним доступом, травма голени и перелом У метатарзальной кости, биопсия нерва с диагностической целью. Компрессионную невралгию икроножного нерва могут вызвать особый вид шнуровки армейских ботинок (с узлом сбоку, «синдром форменных ботинок»), а также давление края стопы на жесткий кант обуви и даже ношение цепочки на ноге [5].
Клинические признаки: невропатическая боль, парестезии и нарушение чувствительности в зоне иннервации икроножного нерва. Важным диагностическим нейрофизиоло-
Рис. 9. Компрессия подошвенных нервов мышцей, отводящей большой палец стопы (прямая линия)
гическим показателем является снижение амплитуды сенсорного вызванного потенциала до 50%. Хирургическое лечение эффективно при выявлении причин компрессии нерва.
Методы диагностики
Для оценки тяжести поражения и процессов восстановления функций нерва проводят нейрофизиологические исследования: электронейромиографию (ЭНМГ), количественное сенсорное тестирование. При ЭНМГ определяются снижение амплитуды и скорости проведения импульса по двигательным и чувствительным волокнам и увеличение резидуальной латенции в месте компрессии нерва и дис-тальнее [2, 3, 13, 20].
Перспективной методикой оценки морфологических изменений в периферических нервах является УЗИ: используют датчики с частотой 7—17 МГц. Изображение нерва имеет ряд характерных признаков: в поперечной проекции он выглядит как овальное или округлое образование с четким гиперэхогенным контуром и внутренней гетерогенной упорядоченной структурой («соль — перец», «медовые соты»), в продольной проекции — как линейная структура с четким эхогенным контуром, в составе которой правильно чередуются гипо- и гиперэхогенные полосы («электрический кабель»). В процессе сканирования оценивают анатомическую целостность нервного ствола, его структуру, четкость контуров и состояние окружающих тканей [5, 12, 20]. УЗИ позволяет не только выявлять объемные новообразования (шван-номы, невриномы и т.апНЬш используют футлярные блокады с местными анестетиками параневрально в точки наибольшей болезненности («ловушечный пункт») или предполагаемого сдавления, которые находят по анатомическим ориентирам [5, 7, 21]. Купирование парестезий и боли свидетельствует о том, что диагноз поставлен правильно. Проба отличается высокой чувствительностью при правильном выполнении блокады, но не самой высокой специфичностью. Плацебо-эффект блокад при синдроме психогенных акропарестезий исключается при использовании 0,9% раствора №С1 вместо анестетика.
Лечение
Для эффективного лечения тоннельного синдрома необходимо понять причину и механизмы возникновения компрессии и применить комплексный подход к терапии. Радикальным методом лечения большинства тоннельных синдромов является операция — рассечение тканей, сдавливающих нерв, и создание оптимальных условий для нервного ствола, предупреждающих его травматизацию. Наличие грубых выпадений двигательных и чувствительных функций, быстрое нарастание симптоматики с развитием контрактур — абсолютные показания к операции [21, 22]. Одна-
ко в подавляющем большинстве случаев прибегнуть к операции вынуждает безуспешность консервативного лечения, а не абсолютные показания.
Консервативная терапия заключается в фиксации конечности в функционально выгодном положении, чтобы исключить физическое воздействие в области компрессии [3—5]. Для этого существуют специальные ортопедическая обувь и приспособления: брейсы, ортезы, супинаторы и индивидуальные стельки, которые позволяют добиться разгрузки стопы и иммобилизации в зоне повреждения. Они очень удобны в использовании, их можно легко надевать и снимать. Для этиотропной терапии тоннельных невропатий, связанных с суставной патологией (передний тарзальный синдром, невралгия Мортона, невралгии подошвенных нервов и т. д.), наряду с ортопедической коррекцией стопы широко используются хондропротекторы или симптом-модифицирующие препараты медленного действия, содержащие глюкозамин и хондроитина сульфат. Они также оказывают обезболивающее и противовоспалительное действие, которое развивается медленно (в течение 2—3 мес), однако лишены характерных для нестероидных анальгетиков побочных эффектов, так как механизм их действия связан не с подавлением синтеза простагландинов, а с блокированием ядерного фактора кВ (NF-кB), являющегося ключевым звеном в инициации распада хряща, и усилением анаболизма хряща посредством активации пути, зависимого от трансформирующего фактора роста (TGF) |3ь Этиотропная терапия хондропротекторами позволяет постепенно значительно уменьшить дозы применяемых анальгетиков вплоть до полного отказа от них. Если учитывать, хроническое течение остеоартроза, требующее длительной противовоспалительной и обезболивающей терапии, и распространенную коморбидность (сахарный диабет, ишемическая болезнь сердца, амилоидоз и др.) у таких пациентов, это существенно снизит риск побочных эффектов, представляющих угрозу не только для здоровья, но иногда и для жизни.
Другим направлением этиотропной терапии тоннельных невропатий и профилактики их рецидивов является восстановление метаболизма и иммунного статуса, а также нормального двигательного стереотипа и биомеханики движений в ноге. К сожалению, этиотропная терапия не всегда позволяет быстро купировать болевой синдром, поскольку требует много времени [5, 15, 16].
Самым быстрым и эффективным методом купирования боли, воспаления и отека в «ловушечном пункте», если врач имеет необходимые навыки, являются инъекции ГК непосредственно в каналы или ткани, окружающие нерв [2, 3, 5, 21, 22]. ГК оказывают противовоспалительное и про-тивоотечное действие непосредственно в тканях, а также обладают ремиелинизирующим эффектом при локальных аутоиммунных поражениях периферических нервов. Однако необходимо учитывать и возможное системное действие ГК, поэтому в начале терапии целесообразно использовать растворы НПВП или короткодействующих ГК (дексаметазон) для оценки не только эффективности, но и безопасности лечения. При отсутствии выраженных побочных явлений (неконтролируемая гипергликемия и/или артериальная гипертония, сердечная недостаточность, дисменорея и т. п.) и в случае недостаточной эффективности препаратов короткого действия рекомендуется применение микрокристаллических суспензий ГК. Наибольшей эффективностью и дли-
тельностью действия характеризуется Дипроспан® — пролонгированный инъекционный двухкомпонентный ГК. Входящая в его состав быстрорастворимая соль бетаметазо-на натрия фосфат (2 мг) обеспечивает быстрое начало действия (через 20—40 мин после введения), а микрокристаллическая депо-фракция бетаметазона дипропионат (5 мг) — длительный (не менее 4 нед) противовоспалительный эффект.
Альтернативной методикой локальной терапии тоннельных невропатий является наложение на 20—30 мин компрессов с димексидом, анестетиками и ГК на область компрессии и воспаления нерва. Димексид обеспечивает транспорт анестетика и ГК через кожные покровы, кроме того, сам оказывает противовоспалительное действие [4, 7].
Для симптоматической терапии невропатического болевого синдрома при тоннельных невропатиях применяют антиконвульсанты, трициклические антидепрессанты и трансдермальные системы с анестетиком (лидокаин). Анти-конвульсанты и анестетики эффективно «успокаивают» расторможенные ноцицептивные структуры головного и спинного мозга, подавляя периферическую и центральную сенси-тизацию — основной патогенетический механизм возникновения невропатической боли при поражении периферических нервов [2, 16, 17]. Антидепрессанты повышают активность эндогенной антиноцицептивной системы мозга за счет подавления обратного захвата норадреналина, серотонина и дофамина. Применение трициклических антидепрессантов для терапии боли при тоннельных синдромах ограничено из-за наличия выраженных побочных явлений (сонливость, потеря координации движений, повышение артериального давления, задержка мочи и т. д.) и синдрома отмены (возобновление боли, развитие тревоги, психомоторного возбуждения и даже судорожных припадков при резком прекращении лечения). В связи с этим более безопасно назначение антидепрессантов из группы селективных ингибиторов обратного захвата серотонина (СИОЗС), таких как эсциталопрам, не вызывающих указанных побочных явлений и имеющих доказанную эффективность при невропатической боли.
При механической компрессии сосудисто-нервных стволов спазмированными мышцами (синдром грушевидной мышцы, невропатия бедренного нерва и т. п.) используют мио-релаксанты (баклосан 10—30 мг/сут, тизанидин 6—12 мг/сут, толперизон 150—450 мг/сут). Основной механизм их действия — торможение возбуждения двигательного нейрона в ответ на болевые стимулы и эмоциональный дискомфорт.
Миорелаксанты оказывают обезболивающее действие, помогая расторможенным отделам нервной системы вернуться в состояние покоя, т. е. стирают «болевую память». Это не только уменьшает выраженность спондило-генной боли при МАС-синдроме, но и предотвращает компрессию нервно-мышечных стволов, прилегающих к спаз-мированным мышцам.
Для патогенетической терапии тоннельных невропатий с целью активизации процесса восстановления структуры и функции нервных волокон могут применяться антиоксиданты (альфа-липоевая кислота), ингибиторы холинэсте-разы (прозерин, ипидакрин), вазоактивные препараты (пентоксифиллин, Гингко билоба и др.), репаранты (солко-серил, актовегин). Для активизации регенеративных процессов в периферических нервах успешно используются нейротропный комплекс мильгамма, содержащий большие дозы витаминов группы В (В1 Вй, В12) и лидокаин [3, 16, 23].
Нейротропные компоненты мильгаммы улучшают скорость проведения нервного импульса и репаративные процессы в периферическом нерве. Анестетик лидокаин в составе мильгаммы обеспечивает безболезненность инъекции. Схема терапии тоннельных невропатий включает курс из 10 внутримышечных инъекций мильгаммы с последующим переходом на драже мильгамма-композитум 3 раза в день в течение 2—8 нед (в зависимости от тяжести невропатии) [3, 16]. Курсы нейротропной терапии при МАС-синдромах, отличающихся от обычных тоннельных невропатий высокой склонностью к рецидивам, повторяют 2 раза в год.
Из физиотерапевтических методов наиболее эффективны массаж дистальнее и проксимальнее места компрессии, ультразвук с ГК на область компрессии в острой стадии воспаления, а при хронических рубцово-спаечных процессах — электрофорез с лидазой и ударно-волновая терапия высокой частоты и низкой интенсивности. Используются методы мануальной терапии (неоперативный невролиз), позволяющие воздействовать на механизм гиперфиксации нерва за счет уменьшения рубцово-спаечного процесса в тоннеле [10]. При МАС-синдроме необходимо воздействие на всех уровнях поражения аксональных транспортных систем, в том числе на вертебральном, что может потребовать применения мобилизационных техник мануальной терапии, однако чрезмерное увлечение жесткими манипуляционными методами может приводить к гипермобильности позвоночных двигательных сегментов и усугублению динамической компрессии пораженного корешка нерва, поэтому число таких манипуляций должно быть минимальным. Кроме того, процедуры мануальной терапии, несут большой психологический заряд (эффект плацебо — ноцебо), что, с одной стороны, может давать парадоксальный результат (эйфория, ложное чувство полного выздоровления, в том числе от болезней, не связанных с дисфункцией позвоночника и тоннельными синдромами, и наоборот, ощущение непоправимого вреда здоровью), а с другой — вызывать у пациента психологическую зависимость («привыкание к рукам»).
Принципы воздействия на спондилогенный компонент МАС-синдрома:
1) исключение неблагоприятных статико-динамиче-ских нагрузок на пораженный отдел позвоночника и область компрессии нерва в ноге (на первых этапах декомпенсации необходим покой) — воздействие на все очаги динамической компрессии нерва;
2) фазовость лечения: восстановление нормальной биомеханики движений в поясничном отделе и тазовой области при отсутствии необходимости в защитной фиксации пораженного позвоночного сегмента;
3) комплексность лечения: необходимость воздействия не только на поясничный отдел позвоночника, но и на экстравертебральные патологические очаги в малом тазу (например, лечение эндометриоза, простатита и т. п.), участвующие в развитии мышечно-тонических синдромов посредством активизации висцеромоторного рефлекса. Этот принцип, во-первых, соответствует общим теоретическим положениям о целостности организма; во-вторых, подчеркивает клиническую роль экстеро-, проприо- и интероцеп-тивных импульсов в развитии патологии позвоночника. Важно добиться не просто ремиссии, а устойчивой ремиссии, с такой фиксацией позвоночника и таким состоянием костных, сосудистых, мышечных и соединительнотканных
Рис. 11. Сравнение концентрации ПГЕ2 в спинномозговой жидкости на фоне приема эторикоксиба и плацебо у пациентов с постоперационным болевым синдромом [25]
элементов костно-мышечных тоннелей, которые обеспечили бы профилактику обострений невропатий;
4) щадящий характер лечения — оно не должно быть более вредным, чем сама болезнь;
5) уменьшение болевых ощущений — снижение возбудимости или функциональное выключение соответствующих центральных и периферических нервных структур. В условиях декомпенсации и нестабильности болевая импульсация в определенные моменты является источником сигналов для осуществления защитных и компенсаторных реакций.
Ключевым направлением аналь-гетической терапии МАС-синдрома является применение НПВП, блокирующих выработку медиаторов воспаления — простагландинов (ПГ) за счет ингибирования фермента циклооксигеназы (ЦОГ).
Существование центрального компонента антиноци-цептивного действия НПВП, обусловленного подавлением синтеза ПГ в ЦНС, подтверждается выраженной диссоциацией между противовоспалительным и антиноцицептивным эффектом [24]. Для проявления центрального антиноцицеп-тивного действия НПВП должны попасть в ЦНС из кровотока. Оптимальной доставке молекул препарата в ЦНС препятствует гематоэнцефалический барьер (ГЭБ), который строго контролирует обмен веществ между кровью и ЦНС. У разных НПВП проникновение в спинной мозг и супрас-пинальные структуры (процесс, осуществляемый в основном за счет пассивной диффузии) различается [24, 25]. Наивысшей способностью преодолевать ГЭБ обладает эторико-ксиб (Аркоксиа®), который благодаря этому может подавлять синтез ПГЕз в ЦНС (рис. 11).
НПВП должны назначаться на первом этапе ступенчатой терапии боли в спине, в структуре МАС-син-дрома, прежде всего врачами общей практики, а не только узкими специалистами (неврологами, ортопедами, ревматологами) [2]. Однако у этой группы препаратов имеются существенные побочные эффекты. Неселективные НПВП блокируют активность обеих изоформ ЦОГ, что приводит к побочным эффектам, которые связаны с ингибированием конституциональной ЦОГ1, в первую очередь к поражению желудочно-кишечного тракта, причем на всем его протяжении (стоматит, эзофагит, гастрит, язва желудка и двенадцатиперстной кишки, энтерит, язвенный колит, проктит). Являясь мощными анальгетиками, неселективные НПВП блокируют висцеральные болевые ощущения, и язвенное поражение желудочно-кишечного тракта у таких больных зачастую протекает
бессимптомно, заканчиваясь либо кровотечением, либо перфорацией язвы с последующим развитием перитонита. Применение парентеральных форм неселективных НПВП (инъекции и суппозитории) не позволяет избежать указанных побочных явлений. Селективные НПВП, специфические блокаторы индуцибельного изофермента ЦОГ2, имеют более высокую степень безопасности в отношении желудочно-кишечного тракта, но могут вызывать осложнения со стороны сердечно-сосудистой системы (повышение артериального давления, задержка жидкости, тромботические события — инфаркт миокарда, ишемический инсульт и др.) [2]. Таким образом, селективные НПВП можно считать препаратами выбора для купирования острых болевых синдромов во всех случаях, когда необходимо максимально быстро устранить боль, не вызывая серьезных побочных эффектов со стороны желудочно-кишечного тракта, например у молодых пациентов с отягощенным язвенным
В
Конский хвост Желтая связка
Поперечный отросток Задний первичный корешок
Передний первичный корешок
Соединительные ветви
Симпатическая цепочка
Спинальная сегментарная артерия
Твердая мозговая оболочка Межпозвоночный диск
Поясничная артерия
Рис. 12. Малоинвазивная терапия радикулопатии: локальная инъекционная терапия эпидуральным (А) и трансфораминальным (В) доступом
анамнезом. В то же время у пожилых пациентов, подверженных риску сердечно-сосудистых заболеваний, эти препараты желательно применять «под прикрытием» антиаг-регантной терапии (клопидогрель или низкие дозы аспирина). Эффективна ступенчатая дифференцированная терапия эторикоксибом (Аркоксиа®): 120 мг однократно в течение 7 дней в остром периоде при интенсивной боли, 90 мг в течение 7—14 дней в подостром периоде, если выраженный болевой синдром сохраняется, и 60 мг от 7 дней до нескольких месяцев при умеренной и хронической боли.
При миофасциальном синдроме можно использовать введение в триггерные зоны растворов анестетика (2% ли-докаина или 0,5% новокаина) и 1 мл дипроспана путем па-равертебральных блокад. Однократное введение дипроспа-на позволяет достичь устойчивой ремиссии не только болевого, но и мышечно-тонического синдрома, вызывающего компрессию сосудисто-нервного пучка, например при син-
дроме грушевидной мышцы. Продемонстрирована также эффективность фораминальных и сакральных эпидураль-ных блокад с использованием дипроспана и местных анестетиков в лечении хронических радикулопатий [2], играющих ключевую роль в патогенезе МАС-синдрома (рис. 12).
Понимание патогенетических механизмов развития тоннельной невропатии у конкретного пациента делает возможным индивидуальный подбор этиотропной, патогенетической и симптоматической терапии, способной не только облегчить состояние больного (уменьшить выраженность болевого синдрома, купировать воспаление и отек, улучшить вегетативно-трофические функции), но и предотвратить появление повторных компрессий периферических нервов. Прогноз при тоннельной невропатии зависит от своевременного начала терапии (до развития необратимых метаболических процессов в нерве, а также атрофии и контрактур в иннервируемых мышцах).
1. Papanicolaou GD, McCabe SJ, Firrell J. The prevalence and characteristics of nerve compression symptoms in the general population. Hand Surg Am. 2001;26(3):460—6. DOI: https://dx.doi.org/10.1053/jhsu.2001.24972.
2. Алексеев ВВ, Баринов АН, Кукушкин МЛ и др. Боль: руководство для врачей и студентов. Под ред. Н.Н. Яхно. Москва: МедПресс; 2009. 302 с. [Alekseev VV, Barinov AN, Kukushkin ML i dr. Bol’: rukovodstvo dlya vrachey i studentov. Yakhno NN, editor. Moscow: MedPress; 2009. 302 p.]
3. Баринов АН. Тоннельные невропатии: обоснование патогенетической терапии. Врач. 2012;(4):31—7. [Barinov AN. Entrapment neuropathies: rationale for pathogenetic therapy.
Vrach. 2012;(4):31—7.]
4. Лобзин ВС, Рахимджанов АР, Жулев НМ. Туннельные компрессионно-ишемические невропатии. Ташкент: Медицина; 1988. 232 с. [Lobzin VS, Rakhimdzhanov AR, Zhulev NM. Tunnel’nye kompressionno-ishemicheskie nevropatii. Tashkent: Meditsina; 1988. 232 p.]
5. Мументалер М, Штёр М, Мюллер-Фаль Г. Поражения периферических нервов и корешковые синдромы: руководство под общ. ред. А.Н. Баринова. Москва: МЕДпресс-информ; 2013. 616 с. [Mumentaler M, Shter M, Myuller-Fal’ G. Porazheniya perifericheskikh nervov i kore-shkovye sindromy: rukovodstvo pod obshch. red. A.N. Barinova. Moscow: MEDpress-inform; 2013. 616 p.]
6. Акимов ГА, Михайленко АА, Осетров БА, Недзведь ГК. Компрессионно-ишемические перонеальные невропатии. Журнал невропатологии и психиатрии им. С.С. Корсакова. 1986;6:898-901. [Akimov GA, Mikhaylenko AA, Osetrov BA, Nedzved’ GK. Kompressionno-ishemicheskie peroneal’nye nevropatii. Zhurnal nevropatologii i psikhiatrii im. S.S. Korsakova. 1986;6:898-901.]
7. Мельцер РИ, Ошукова СМ, Иванова ИУ. Нейрокомпрессионные синдромы: Монография. Петрозаводск: ПетрГУ; 2002. 134 с. [Mel’tser RI, Oshukova SM, Ivanova IU. Neyrokompressionnye sindromy: Monografiya. Petrozavodsk: PetrGU; 2002. 134 p.]
8. Хабиров ФА, Богданов ЭИ, Попелянский АЯ.
ЛИТЕРАТУРА
Синдромы малоберцового нерва. Журнал невропатологии и психиатрии им. С.С. Корсакова. 1984;(3):451-7. [Khabirov FA, Bogdanov EI, Popelyanskiy AYa. Sindromy malobertsovogo nerva. Zhurnal nevropatologii i psikhiatrii im. S.S. Korsakova. 1984;(3):451-7.]
9. Schmid AB. The double crush syndrome revisited- a Delphi study to reveal current expert views on mechanisms underlying dual nerve disorders. Man Ther. 2011;16(6):557—62. DOI: 10.1016/j.math.2011.05.005. Epub 2011 Jun 8.
10. Violante FS, Armstrong TJ, Fiorentini C et al. Carpal tunnel syndrome and manual work: a longitudinal study. J Occup Environ Med. 2007;49(11):1189-96. DOI: https://dx.doi.org/10.1097/JOM.0b013e3181594873.
11. Upton А, McComas А. The Double Crush in Nerve-Entrapment Syndromes. Lancet. 1973;2(7825):359-62.
12. Еськин НА, Матвеева НЮ, Приписнова СГ Ультразвуковое исследование периферической нервной системы. SonoAce-Ultrasound. 2008;(18):65—75. [Es’kin NA, Matveeva NYu, Pripisnova SG. Ul’trazvukovoe issledovanie per-ifericheskoy nervnoy sistemy. SonoAce-Ultrasound. 2008;(18):65-75.]
13. Lo SF, Chou LW, Meng NH. Clinical characteristics and electrodiagnostic features in patients with carpal tunnel syndrome, double crush syndrome, and cervical radiculopathy. Rheumatol Int. 2012;32(5):1257—63. DOI: 10.1007/s00296-010-1746-1. Epub 2011 Jan 23.
14. Gelberman RH, Szabo RM, Williamson RV et al. Sensibility testing in peripheral-nerve compression syndromes. An experimental study in humans. J Bone Joint Surg Am. 1983;65(5):632—8.
15. Баринов АН. Невропатическая боль: клинические рекомендации и алгоритмы. Врач. 2012;(9):17—23. [Barinow AN. Neuropathic pain: clinical guidelines and algorithms. Vrach. 2012;(9):17—23.]
16. Баринов АН, Мурашко НК, Терентьева НВ, Яворский ВВ. Невропатическая боль при поражении периферической нервной системы: стратификация лечения. Медицинский совет. 2013;(4):54—62. [Barinow AN, Murashko NK, Terentyeva NV, Yavorskiy VV. Neuropathic pain
and peripheral nervous system lesions: stratification of treatment. Meditsinskiy sovet. 2013;(4):54—62.]
17. Яхно НН, Баринов АН. Невропатическая боль: особенности клиники, диагностики и лечения. Врач. 2007;(3):16—22. [Yakhno NN, Barinov AN. Nevropaticheskaya bol’: osobennosti kliniki, diagnostiki i lecheniya. Vrach. 2007;(3):16—22.]
18. Зимакова ТВ, Хабиров ФА, Хайбуллин ТИ и др. Бедренные невропатии. Практическая медицина. 2012;(2):51—6. [Zimakova TV, Khabirov FA, Khaybullin TI et al. Femoral neuropathy. Prakticheskaya meditsina. 2012;(2):51—6.]
19. Guillain G, de Seze S, Blondin-Walter M. Bull Acad Med (Paris). 1934;111:633—43.
20. Kwon BC, Jung KI, Baek GH. Comparison of sonography and electrodiagnostic testing in the diagnosis of carpal tunnel syndrome. J Hand Surg Am. 2008;33(1):65—71. DOI: 10.1016/j.jhsa.2007.10.014.
21. Graham RG, Hudson DA, Solomons M,
Singer M. A prospective study to assess the outcome of steroid injections and wrist splinting for the treatment of carpal tunnel syndrome. Plast Reconstr Surg. 2004;113(2):550—6. DOI: https://dx.doi.org/10.1097/01.PRS.0000101055.765 43.C7.
22. Jarvik JG, Comstock BA, Kliot M et al.
Surgery versus non-surgical therapy for carpal tunnel syndrome: a randomised parallel-group trial. Lancet. 2009;374(9695):1074—81. DOI: https://dx.doi.org/10.1016/S0140-6736(09)61517-8.
23. Eckert M, Schejbal P. Therapy of neuropathies with a vitamin B combination. Fortschr Med. 1992;110(29):544—8.
24. Burian M, Geisslinger G. COX-dependent mechanisms involved in the antinociceptive action of NSAIDs at central and peripheral sites. Pharmacol Ther. 2005;107(2):139—54. DOI: https://dx.doi.org/10.1016Xj.pharmthera.2005.02.004.
25. Renner B, Zacher J, Buvanendran A et al. Absorption and distribution of etoricoxib in plasma, CSF, and wound tissue in patients following hip surgery — a pilot study. Naunyn Schmiedebergs Arch Pharmacol. 2010;381(2):127—36. DOI: 10.1007/s00210-009-0482-0. Epub 2010 Jan 6.
ФГБУ Центр реабилитации (для детей с нарушением слуха)
Плоскостопие — деформация стопы с уплощением ее сводов, в связи с чем стопа утрачивает свою амортизационную функцию, увеличивая нагрузку на суставы ног и нижние отделы позвоночника, что в последствие является одной из причин их заболеваний. Плоскостопие зависит от состояния мышечно- связочного аппарата подошвенной поверхности стопы и голеностопного сустава. До 3-5 лет у детей может наблюдаться, так называемое, физиологическое плоскостопие: наличие жировой прослойки в области внутреннего края стопы создает иллюзию «плоской стопы», хотя на самом деле нога ребенка развивается согласно возрастным нормам, поэтому всегда необходима консультация с врачом. Большое значение имеет своевременное выявление родителями изменений в стопе ребенка, так как применение профилактических мер может привести к благоприятному результату. Прислушайтесь к жалобам детей на «боли в ножках». Это, как и частые жалобы на утомляемость ног, может быть признаком плоскостопия.
В профилактике плоскостопия важную роль играет обувь. Она не должна быть тесной или слишком просторной, высота каблука не более 1, 5 — 2 см, подошва должна быть прочная и гибкая, с высоким задником и закругленным носком. Обувь нужно подбирать по размеру, который определяется следующим образом: длина подошвы обуви должна быть на 0,5–1 см больше длины стопы стоящего ребенка. Нельзя длительно в течение дня носить плоскую обувь и обувь без задников: резиновые сапоги, валенки, сланцы и пр. Категорически запрещается донашивать обувь за старшими детьми, какой бы хорошей она ни была. Запомните: плохо подобранная обувь приносит вред детским ногам.
Очень полезно как можно чаще ходить босиком по неровным поверхностям: по земле, по песку, по камням. Полы в квартире к таким поверхностям не относятся, поэтому дома тоже необходимо ходить в домашней обуви, отвечающей изложенным выше требованиям, или создавать «массажные поверхности». Для этого можно приобрести специальные массажные коврики, а можно разбросать на полу морские камушки или мелкие игрушки.
Меры по укреплению голеностопных мышц необходимо применять, начиная с грудного возраста ребенка, в этом помогут массаж и гимнастика. Для детей от 1 года до 3 лет рекомендуются следующие упражнения:
- «Мишка косолапый» — ходьба на наружном крае стопы.
- Ходьба по ребристой двускатной доске.
- Ходьба по рельефной поверхности полезна в качестве не только профилактики, но и лечебного упражнения при плоскостопии. Лучше всего это делать летом, когда ребенок может без опаски ходить по песку, мягкой земле и жестким камешкам. В холодное время года можно постелить малышу рифленый коврик или насыпать песок в коробку либо полотняный мешок.
- Захват пальцами ног мелких предметов развивает мышцы стоп, увеличивая ловкость и подвижность пальцев. Данное упражнение можно выполнять как стоя, так и сидя. Предложите ребенку «поймать» какой-либо небольшой предмет — палочку или карандаш — и некоторое время его удерживать.
- Собирание пальцами ног ткани. Попросите малыша захватить пальцами носовой платок или салфетку.
- Сидение «по-турецки» очень хорошо корректирует неправильное положение стопы. Постарайтесь, чтобы ребенок полюбил это положение.
- Подъем из положения «по-турецки». Поначалу помогайте ребенку встать, поддерживая его за руки. При этом его стопы должны оказаться в перекрещенном положении. Позу нужно менять, закладывая вперед то левую, то правую ногу, тогда подъем из описанного положения будет с опорой на разные ноги. Возможно, первое время стопы придется придерживать руками.
- Приседания на полной стопе. При выполнении этого упражнения нужно следить за тем, чтобы стопы ребенка стояли на полу всей поверхностью и располагались параллельно друг другу. На первых порах можно помогать малышу, поддерживая его за руки или под мышки.
- Подъем на носки. Это упражнение целесообразно объединить со знакомым упражнением «Стань маленьким — стань большим». В первом случае малыш должен потянуться вверх руками и подняться на носки, во втором — присесть на полную стопу.
Особое внимание нужно обратить на выработку правильного положения стоп при ходьбе и стоянии. Начиная ходить, ребенок широко расставляет стопы, тем самым увеличивая площадь опоры. До 2—3лет это нормально, но в этом возрасте у малыша должна выработаться правильная походка с параллельной установкой стоп на малом расстоянии друг от друга.
Основным упражнением, направленным на воспитание правильных навыков ходьбы, является ходьба по «дорожке» — доске или полосе на ковровой дорожке шириной 10–15 см. Ее можно даже нарисовать мелом прямо на полу. После того как она будет готова, предложите малышу пройти по ней, не наступая за ее пределы. При этом нужно следить за правильной установкой стоп. Кроме того, на прогулке можно водить ребенка по бревну, имеющемуся на каждой детской площадке, бортовому камню, ограждающему тротуар в сквере, и пр.
Все упражнения необходимо проводить в игровой форме.
Если врач ортопед диагностировал у ребенка плоскостопие, то перечень рекомендаций во многом будет определяться возрастом ребенка, формой и степенью плоскостопия. Чаще всего ставится диагноз «плоско-вальгусное плоскостопие», или «плоско-вальгусная установка стоп».
Впрочем, в любом случае, начинать лечение следует с выбора обуви и двигательной активности. Ребенок должен как можно чаще ходить босиком по неровной поверхности и делать лечебную гимнастику, а задача родителей — выбрать хорошую ортопедическую обувь и подокорректоры (стельки-супинаторы), а во время выполнения ребенком лечебной гимнастики родители должны помнить, что главная задача — максимально задействовать мышцы подошвенной и тыльной поверхности стопы, а также мышцы голени, отвечающие за пронацию/супинацию стопы и сгибание/разгибание пальцев. А также родители должны запастись терпением, ведь эффект от лечения появится не ранее, чем через полгода, но зато они избавят своего малыша от многих проблем со здоровьем в будущем.
Комплекс упражнений для выполнения в домашних условиях при плоско-вальгусном плоскостопии у детей старшего возраста.
В исходном положении лежа:
- Поочередно и вместе оттягивать носки стоп с одновременным приподниманием и опусканием их наружного края.
- Согнуть ноги в коленях, упереться стопами в пол, разводить пятки в стороны, возврат в исходное положение. После 5-6 движений — расслабление.
- Поочередное и одновременное приподнимание пяток от опоры.
- Лежа на спине, ноги согнуты в коленях, бедра разведены, стопы соприкасаются друг с другом по подошвенной поверхности. Отведение и приведение пяток с упором на пальцы стоп.
- Положить согнутую в колене ногу на колено другой полусогнутой ноги. Проводить круговые движения стопы в одну и другую стороны. Сменить ноги.
- Скользящие движения стопой одной ноги по голени другой с одновременным охватом голени. То же стопой другой ноги.
В исходном положении сидя:
- Ноги согнуты в коленях, стопы параллельны — приподнимание пяток вместе и поочередно.
- Тыльное сгибание стоп вместе и поочередно.
- Приподнимание пятки одной ноги с одновременным тыльным сгибанием стопы другой ноги.
- Ноги выпрямить в коленях. Сгибать и разгибать стопы.
- Положить ногу на колено другой ноги, круговые движения стопы в обе стороны. То же другой ногой.
- Захватывание пальцами стоп мелких предметов и перекладывание их на другую сторону.
- Сидя на коврике «по-турецки», подогнуть пальцы стоп, наклоняя туловище вперед, встать с опорой на внешнюю поверхность стоп.
- Сидя на полу с прямыми ногами, кисти рук в упоре сзади — разводить колени, подтягивать стопы до полного соприкосновения подошв.
В исходном положении стоя:
- Стопы параллельны, на расстоянии ширины ступни, руки на поясе.
А) Подниматься вместе и попеременно на носочки.
Б) Приподнимать пальцы стоп с опорой на пятки вместе и попеременно.
В) Перекат с пяток на носок и обратно. - Полуприседания и приседания на носках — руки в стороны. Вверх, вперед.
- Стопы параллельны, перейти в положение стоя на наружных краях стоп.
- Стоя, носки вместе, пятки врозь — полуприседание с одновременным движением рук вперед.
- Стоя, стопы параллельны, руки на поясе — поочередное поднимание пяток, не отрывая пальцев стоп от пола, ходьба на месте.
- Стоя на гимнастической палке, стопы параллельны — полуприседания. Руки вперед.
- Стоя на набивном мяче или массажной полусфере — приседание в сочетании с движением рук вперед.
Упражнения во время ходьбы:
- Ходьба на носках.
- Ходьба на наружных краях стоп.
- Ходьба на носках с высоким подниманием колен.
- Ходьба на носках с полусогнутыми коленями.
- Скользящие шаги с одновременной помощью за счет сгибания пальцев.
Врач-физиотерапевт
Байрамова Наталья Васильевна
Хроническая дизиммунная гипертрофическая плексопатия как вариант атипичной хронической воспалительной демиелинизирующей полинейропатии
Термин «хроническая воспалительная демиелинизирующая полинейропатия» (ХВДП) объединяет группу иммуноопосредованных [1] состояний с частотой встречаемости у детей до 0,48 на 100 000 [2]. Традиционно выделяют типичные и атипичные формы ХВДП. Классическая клиническая картина ХВДП характеризуется симметричными чувствительными и двигательными нарушениями в дистальных и проксимальных отделах рук и ног, прогрессирующим или рецидивирующим течением в период 8 нед и более, повышением концентрации белка в цереброспинальной жидкости (ЦСЖ) и ответом на иммуномодулирующую терапию. Предложенные в 2000 г. клинические, электрофизиологические и лабораторные критерии ХВДП детского возраста имеют низкую чувствительность — до 77% [3, 4], в связи с чем эксперты приняли решение использовать критерии EFNS [5] для взрослых, чувствительность которых достигает 94% [4]. Независимо от возраста пациента диагностическую сложность представляют атипичные формы дизиммунных нейропатий и особенно фокальная ХВДП, проявляющаяся поражением одной или двух конечностей [6]. Симптомы и электрофизиологические изменения, выявляемые при атипичных формах ХВДП, не соответствуют принятым критериям диагноза, затрудняя диагностический поиск. Представлено наблюдение хронического дизиммунного поражения пояснично-крестцового сплетения у ребенка 7 лет как варианта атипичной ХВДП.
Клиническое наблюдение. Мальчик В., 2010 года рождения, с неотягощенным семейным анамнезом и без особенностей раннего развития. В возрасте 6,5 года мать впервые отметила, что ребенок без видимых причин начал прихрамывать на левую ногу. Неврологом в поликлинике было предположено поражение левого седалищного нерва, для уточнения генеза которого ребенок был направлен на УЗИ, которое не выявило изменений на доступном визуализации отрезке нерва.
При осмотре обращали на себя внимание слабость (до плегии в мышцах тыльного сгибания стопы) и гипотрофия мышц, иннервируемых левым пояснично-крестцовым сплетением (четырехглавая мышца бедра, бицепс бедра, группа мышц, приводящих бедро, большая ягодичная мышца, передняя большеберцовая, икроножная, короткий разгибатель пальцев), а также слабость удерживающих лопатку слева мышц: широчайшей, зубчатой, надостной, подостной (рис. 1). Рис. 1. Пациент В., 7 лет. Клиническая оценка мышечной силы. а — отсутствие тыльного сгибания левой стопы; б — сохранность силы мышц подошвенного сгибания стопы; в — слабость мышц, удерживающих лопатку слева. Сухожильные рефлексы не вызывались только с левой ноги. Нарушения чувствительности ограничены зоной иннервации левого пояснично-крестцового сплетения. В остальном неврологический статус был без особенностей: менингеальных симптомов нет, движения глазных яблок в полном объеме, нистагма нет, сила мимической мускулатуры 5 баллов, лицо симметричное, сухожильные рефлексы, кроме ахиллова и коленного слева, в том числе, рефлекс с ости лопатки нормальной живости и симметричные, патологических стопных знаков нет. Координаторные пробы: пальценосовую пробу выполняет удовлетворительно.
Проведена электромиография (ЭМГ) в полном и достаточном объеме с исследованием всех четырех конечностей, по результатам которой получены изменения, свидетельствующие о поражении левого пояснично-крестцового сплетения: при тестировании моторных и сенсорных волокон нервов ног выявлена значимая асимметрия амплитуд моторных ответов с левой ноги при сравнении с противоположной стороной, потенциалы действия n. suralis и n. peroneus superficialis слева не регистрировались; F-волны при отведении с m. abductor hallucis и m.extensor digitorum brevis sinister отсутствовали, справа — представленность F-волн с m. abductor hallucis — 100%; игольчатым электродом выявлена перестройка потенциалов двигательных единиц и спонтанная активность (потенциалы фибрилляций и положительные острые волны) в мышцах, иннервируемых левым пояснично-крестцовым сплетением (mm. vastus lateralis, tibialis anterior, gluteus maximus).
Результаты осмотра, УЗИ периферических нервов и ЭМГ констатировали поражение на уровне пояснично-крестцового сплетения. Для уточнения причины изменений проведено МРТ с контрастным усилением гадолинием, обнаружено увеличение нервных стволов и накопление контрастного вещества в пояснично-крестцовом сплетении (рис. 2). Рис. 2. Тот же пациент. МРТ пояснично-крестцового сплетения в режиме Т1 с контрастным усилением гадолинием. МРТ плечевого сплетения не выявило изменений.
В соответствии с алгоритмом обследования пациентов с подозрением на ХВДП проведено исследование ЦСЖ, которое не выявило белково-клеточной диссоциации; также не обнаружено антител к ганглиозидам периферических нервов в сыворотке крови.
На основании течения болезни (более 8 нед), данных МРТ — накопление контрастного вещества нервными стволами, результатов ЭМГ, указывающих на вовлечение пояснично-крестцового сплетения, предположено наличие дизиммунного процесса периферической нервной системы. Назначена комбинированная патогенетическая терапия 4 курсами с интервалами 1 мес: метилпреднизолон 3000 мг (суммарная доза на 1 курс) внутривенно и внутривенные иммуноглобулины в дозе 2 г на 1 кг массы тела в первый курс и 1 г на 1 кг массы тела в следующие 3 инфузии без последующей поддерживающей терапии.
На фоне лечения отмечено значительное улучшение состояния ребенка в виде нарастания мышечной силы в левой ноге, мышцах, удерживающих левую лопатку, а также уменьшение выраженности мышечных гипотрофий (рис. 3). Рис. 3. Тот же пациент. Клиническая оценка мышечной силы на фоне иммуномодулирующей терапии через 4 мес. а — появилось тыльное сгибание стопы слева; б — сохранность силы мышц подошвенного сгибания стопы; в — регресс слабости мышц, удерживающих лопатку слева. Именно ответ на иммуномодулирующую терапию послужил фактом, подтверждающим диагноз фокальной формы ХВДП.
При очевидном улучшении состояния при повторном МРТ поясничного сплетения накопление контрастного вещества нервными стволами сохранялось (рис. 4). Рис. 4. Тот же пациент. МРТ пояснично-крестцового сплетения в режиме Т1 с контрастным усилением гадолинием на фоне иммуномодулирующей терапии через 4 мес.
Ответ на иммуномодулирующую терапию в представленном случае стал фактом, подтверждающим диагноз.
ХВДП вызывает в ряде случаев диагностические и дифференциально-диагностические сложности [7, 8].
Как и у взрослых, верификация ХВДП у детей основана на типичных находках при проведении ЭМГ: скорости распространения возбуждения по нервным волокнам, увеличение дистальной латентности, наличие блоков проведения и дисперсии ответов (при оценке поздних ответов), выявлении белково-клеточной диссоциации при исследовании ЦСЖ, изменений стволов плечевого и поясничного сплетений, а также конского хвоста при МРТ [9]. Однако менее чем в 50% случаев пациентам выставляется правильный диагноз ХВДП [10, 11]. Основной причиной этого является несоответствие данных обследования пациентов клиническим и электрофизиологическим критериям ХВДП, как правило, в результате неполного обследования больных и неправильной интерпретации полученных данных [12].
Пациенты часто проходят долгий диагностический путь с исключением наследственных форм моторно-сенсорной полинейропатии, вторичных нейропатий на фоне болезней соединительной ткани, нервно-мышечной передачи и даже синдрома Гиейна—Барре [7, 8, 13].
Ретроспективное исследование ранее проведенной экспертной оценки случаев ХВДП из разных клиник показало, что только 37% пациентов имели достаточно данных для постановки диагноза [12]. Такая же ситуация имеет место и в педиатрической практике, когда неправильное толкование полученных данных, технические ошибки при проведении ЭМГ, недостаточный опыт исследователя, а также неполное обследование ребенка приводит к неправильной постановке диагноза [14].
С другой стороны, есть ограничения существующих электрофизиологических критериев ХВДП, которые хорошо известны и признаны [15]. Повышение белка в ЦСЖ у детей с ХВДП присутствует у большинства пациентов, но не у всех [2, 16], и у части больных не проводят исследование ЦСЖ [12]. МРТ-изменения в виде гипертрофии корешков конского хвоста, спинномозговых нервов плечевого и поясничного сплетений, сопровождаемые контрастным усилением, описываются во всех возрастных группах пациентов с ХВДП, и они включены в дополнительные критерии EFNS/PNS [5, 8, 17—19], но о том, как часто обнаруживаются изменения и на каком этапе болезни, данных в литературе мало. Так, пациенты, уже получающие патогенетическое лечение, в 100% случаев имели изменения в поясничном сплетении и были оценены ретроспективно [20]. Выявление характерных изменений для ХВДП при биопсии нерва, несомненно, подтверждает диагноз, но их отсутствие не исключает его [21].
Атипичные формы ХВДП требуют более полной оценки клинических данных в соответствии с получаемыми результатами инструментального и лабораторного обследования пациента [12], как и в описанном нами случае, когда нет соответствия полученных данных ни клиническим, ни электрофизиологическим критериям ХВДП. Положительный ответ на иммуномодулирующую терапию может служить подтверждением дизиммунного характера процесса [5], что было учтено у нашего больного.
Если типичные случаи ХВДП у детей хорошо представлены в литературе [22], то атипичные и тем более фокальные формы ХВДП обсуждаются мало. Большинство представленных случаев является результатом длительного наблюдения за пациентами, имевшими изменения в одной или двух конечностях, которые впоследствии генерализовались до типичной картины ХВДП [23, 24], в связи с чем обсуждается именно фокальное начало ХВДП, а не проявление клинической картины атипичной формы рассматриваемой патологии. Аналогичное мнение высказано в дискуссии с профессором J. Léger на 2-м конгрессе Международной академии IG (Берн, Швейцария) в октябре 2018 г., на котором был представлен клинический случай 7-го наблюдения за пациентом с сенсорными изменениями только в левой руке с положительным ответом на введение иммуноглобулинов, расцененный как фокальная ХВДП. Экспертами рекомендовано наблюдение за такими больными даже в состоянии ремиссии.
Нами продолжается наблюдение за ребенком в виде клинического осмотра с частотой 1 раз в месяц с фото- и видеофиксацией результатов.
Представленный клинический случай является примером сложности трактовки неоднозначных результатов инструментальных методов обследования в сочетании с фокальным поражением конечности. Настороженность относительно атипичных форм ХВДП, в данном случае фокального варианта, позволяет уменьшить время постановки диагноза за счет сокращения дифференциально-диагностического ряда и начать патогенетическую терапию на ранних сроках, оправдывает использование ВВИГ ex juvantibus. Положительный ответ на иммуномодулирующую терапию следует рассматривать как дополнительный диагностический критерий в пользу дизиммунного процесса.
Информированное согласие. Матерью пациента подписано информированное согласие на публикацию данных сына.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Сведения об авторах
Дружинина Е.С. — https://orcid.org/0000-0002-1004-992X; e-mail: [email protected]
Никитин С.С. — https://orcid.org/0000-0003-3292-2758; e-mail: [email protected]
Бембеева Р.Ц. — https://orcid.org/0000-0002-4373-4747; e-mail: [email protected]
Дружинин Д.С. — https://orcid.org/0000-0002-6244-0867; e-mail: [email protected]
Как цитировать:
Дружинина Е.С., Никитин С.С., Бембеева Р.Ц., Дружинин Д.С. Хроническая дизиммунная гипертрофическая плексопатия как вариант атипичной хронической воспалительной демиелинизирующей полинейропатии. Журнал неврологии и психиатрии им. С.С. Корсакова. 2019;119(12):94-99. https://doi.org/10.17116/jnevro201911912194
Автор, ответственный за переписку: Дружинина Евгения Сергеевна — e-mail: [email protected]
Эквинусная деформация стоп у детей с церебральным параличом: вопросы диагностики, лечения | Шамик
Актуальность
Детский церебральный паралич (ДЦП) является одним из наиболее тяжёлых заболеваний нервной системы и опорно-двигательного аппарата, которое приводит к инвалидизации ребенка. ДЦП возникает вследствие повреждений головного мозга, которые проявляются во внутриутробном, интранатальном и постнатальном периодах развития ребенка. Характерной особенностью детских церебральных параличей является нарушение моторного развития ребенка, которое обусловлено аномальным распределением мышечного тонуса и нарушением координации движений и походки [1].
Несмотря на активный поиск новых методов диагностики и лечения, предпринятый в последнее время неонатологами, частота возникновения ДЦП остается довольно высокой и достигает 0,1-0,2 % у доношенных младенцев и 1 % у недоношенных [2]. В США более 100 тыс. детей и подростков моложе 18 лет страдают этим заболеванием [3].
Церебральный паралич является основной причиной детской неврологической инвалидности как в России, так и в мире. Врачи и ученые многих стран активно занимаются борьбой с этой патологией. За последние двадцать лет заболеваемость ДЦП не снижается, а имеет тенденцию к росту. Частота этого заболевания в России, в зависимости от региона, составляет 1,5-9 больных на 1000 новорожденных [4]. В соответствии со статистическими данными Минздрава и соцразвития РФ, в 2010 г. в РФ зарегистрированы 71 429 детей с ДЦП в возрасте 0-14 лет и 13 655 детей с таким диагнозом в возрасте 15-17 лет. Уровень заболеваемости ДЦП и темпы ее роста требуют более внимательного изучения этой проблемы с позиций современной медицины [5].
Патогенез
Существует мнение, что есть три отличительных черты, общие для всех больных с церебральным параличом: (1) некоторая степень двигательной недостаточности, которая отличает его от других состояний, таких как общая задержка развития или аутизм; (2) поражение, затрагивающее головной мозг, что делает его отличным от состояний, которые поражают зрелый мозг у детей старшего и младшего возрастов (3), а также неврологический дефицит непрогрессирующего характера, что отличает его от других моторных заболеваний детского возраста, таких как мышечные дистрофии [6].
У пациентов ДЦП есть особенности синдрома верхнего моторного нейрона, которые включают положительные и отрицательные знаки. Положительные знаки — ненормальные, которые приводят к непреднамеренно увеличенной мышечной активности и двигательным паттернам. Отрицательные знаки отражают недостаточную деятельность мышц или недостаточный контроль деятельности мышц, которые принимают участие в функции суставов [7].
Мышечный дисбаланс приводит к возникновению различных деформаций чаще всего в дистальных отделах верхних и нижних конечностей. Деформации стоп диагностируются в 60 % больных детским церебральным параличом, при этом не менее 40 % больных с деформациями стоп требуют хирургического вмешательства [8]. U. Cavlak, E. Kavlak при исследовании частоты встречаемости типов деформаций (n=436) установили, что эквиноварусная деформация встречается в 33,5 % (n = 146) [9]. Двигательные нарушения у детей с ДЦП носят первичный характер и связаны с мышечно-тоническими расстройствами. Формирование двигательных нарушений вторично происходит в процессе роста и развития ребёнка на фоне моторно-вегетативного рассогласования и характеризуется контрактурами, деформациями и патологическими установками [10].
Спастичность мышц является одним из основных синдромов, которые приводят к инвалидизации пациентов. На этом фоне у больных возникает ограничение объема активных и пассивных движений, что, в свою очередь, приводит к нарушению моторного развития ребенка и задерживанет формирование новых двигательных навыков. Развиваются патологический паттерн ходьбы, миогенные и фиксированные контрактуры [11].
L. Renee, M. Jurgen в своей работе отмечают, что эквинусное положение стопы в паттерне походки оценивается как дефект ходьбы и зачастую исключается важный аспект того, что именно такая деформация может оказаться эффективной в процессе передвижения с учетом всех мозговых дисфункций [12].
Эквинусная деформация стопы является самой частой среди деформаций нижних конечностей. Спастическое сокращение икроножных мышц в сочетании с относительной слабостью малоберцовых приводят к подошвенному сгибанию стопы и опоре на носок. При ходьбе пациент начинает нагружать передний отдел стопы, что приводит к фиксированному подошвенному сгибанию в голеностопном суставе [1]. Нижняя конечность является самым дистальным отделом в теле человека, а с точки зрения функциональности занимает центральное место в опорно-двигательном аппаратом [12][13]. Знание о происхождении спастического сокращения мышц голени дает общее представление о спастической модели походки, а также является важным при решении вопроса о тактике оперативного вмешательства. Соответственно, становится актуальным вопрос о расширенном использовании неинвазивных методов диагностики.
Диагностика
Лабораторные исследования могут быть использованы, чтобы исключить наследственные или нейродегенеративные расстройства. Обработка изображений исследования с использованием магнитно-резонансной томографии (предпочтительно), компьютерной томографии или УЗИ покажет структурные аномалии. Электромиография и исследования нервной проводимости могут быть использованы, чтобы исключить мышечные и нервные заболевания [14].
Достижения в области изучения мышц привели к увеличению количества исследований, связанных с неинвазивным измерением мышечной архитектуры, работы мышц во время функциональной деятельности у подготовленных и неподготовленных контингентов [15]. Важным моментом является определение взаимосвязи между структурой и функцией мышцы, которая оказывает специфическое действие на походку.
В диагностике степени ригидности деформации многими авторами широко используется непосредственно клиническая картина: симптом Штрумпеля, объем дорсифлексии при согнутом и разогнутом коленном суставе [16]. Анализируя опыт хирургического лечения эквинусной деформации стопы при ДЦП, В.Г. Босых с соавт. (2006 г.) настаивают на проведении трицепс-теста (теста Сильвершельда) в сочетании с листеноновой пробой с целью предотвращения ненужного хирургического вмешательства, а также для выбора метода оперативного лечения [17]. Annelies F. Van Bemmel с соавторами указывают на то, что если контрактура сохраняется при согнутом коленном суставе, то в процесс вовлечены и камбаловидная, и икроножная мышцы. Если тыльное сгибание ограничено при прямом колене, а в согнутом положении нет, то расценивают как патологию исключительно икроножной мышцы [18].
Стремительное развитие современных методов диагностики позволяет в полной мере визуализировать практически все мягкотканные образования конечностей [19].
При изучении литературы были найдены публикации, указывающие на прогностическую ценность спиральной компьютерной томографии, позволяющие выбрать оптимальный способ хирургической коррекции патологии стопы, но только у детей с эквино-плоско-вальгусной деформацией стоп [20].
Исследования Noble J.J. и др. показали, что МРТ- метод позволяет оценить объем мышц [21]. Авторы указывают, что объем мышц на патологической стороне существенно меньше по сравнению со здоровой, а также, что проксимальные мышечные группы больше в объеме относительно дистальных.
Методы визуализации при помощи ультразвука в основном ограничиваются оценкой поверхностных волокон в икроножной мышце [22]. Напротив, магнитнорезонансная томография обеспечивает более глубокую визуализацию, не подвергая субъект вредному излучению [23]. Объемы обеих групп мышц голени у детей с ДЦП были снижены примерно на 28 % по сравнению с непораженной конечностью.
Однако остается интересным и перспективным направлением изучение возможности использования ультразвуковой диагностики мышц голени при ДЦП. Ультрасонография мышц голени позволяет достоверно определить топику триггерной зоны и ее морфологическую характеристику с выявлением нескольких типов патологической перестройки [24].
Ультразвуковое исследование скелетных мышц имеет хорошую практическую значимость и прогностическую ценность (до 95 %) в диагностике нейромышечных заболеваний у детей. Чувствительность этого метода, по данным Brockmann K., в 81 % обладает специфичностью и в 96 % может быть использован для обнаружения любого аномального изменения мышечной ткани [25]. Для обнаружения нейрогенных изменений чувствительность составила 77 % с еще более высокой специфичностью (98 %). Наконец, данный метод визуализации мышц прост в выполнении, трактовке результатов, легко воспроизводим и экономичен [26].
Г.В. Дьячкова и соавторы при сканировании передней группы мышц голени отмечали характерную мышечную исчерченность, хорошо дифференцировались межмы- шечные перегородки, контрактильная функция сохранялась [19].
Alanen A.M., Falck B., Kalimo с соавт. обращают внимание на то, что совместное использование МРТ-метода, УЗИ, электромиографии увеличивает точность биопсии мышц, а также информативность изображений при гистологическом анализе [27].
При нейрогенных расстройствах мышечная ткань подвергается атрофии, некрозу, воспалению и фиброзу, потому сигнал от мышц более эхогенный. Среди преимуществ УЗИ мышц является то, что данный метод может быть использован для отслеживания изменений размера мышц в патологическом процессе [28].
Исследования Gao F., Zhao H., Gaebler-Spira D., Zhang L.Q. показали, что у детей с ДЦП более короткие пучки икроножной мышцы (Р < 0,003), больше укорочено ахиллово сухожилие (Р = 0,001) и имеет меньшую площадь поперечного сечения (P = 0.003) [29]. Изменения в ахилловом сухожилии могут быть результатом адаптации икроножной мышцы в результате длительного сокращения, что может повлиять на ее производительность.
В зарубежной и отечественной литературе данных о чувствительности и специфичности МРТ-исследования на этапе диагностики детей с подозрением на нервно-мышечные расстройства не найдено. Преимущества МРТ и КТ по сравнению с УЗИ — это способность визуализировать глубокие мышцы, что является положительным подспорьем и важным диагностическим критерием [30].
Важным моментом при исследовании мышц голени детей больных ДЦП является электронно-микроскопическая картина. Появляются данные, свидетельствующие о том, что структура спастических мышц отличается в сравнении с нормальной иннервируемой мышцей [31]. Спастическая мышца содержит короткие саркомеры и клетки большей жесткости, чем обычно иннервируемая мышечная ткань [32]. Несмотря на это, непосредственно мышечный межклеточный матрикс обладает наименьшей плотностью. В процессе роста и изменения мышечных сил, может привести к прогрессирующей потере движения, контрактурам, в результате чего развиваются дегенеративные изменения, которые могут потребовать ортопедического вмешательства [31].
Лечение
Лечение пациентов с церебральным параличом требует особого подхода: диагностики, раннего вмешательства, программы функциональных оценок, реабилитации, терапии консервативными методами (инъекции ботулотоксина, иммобилизации стоп) и хирургическими методами. Коррекция эквинусной деформации стопы — это только одна часть общего процесса лечения, целью которого является, как правило, выравнивание соотношения силы между антагонистическими группами мышц, что влияет на улучшение перемещения в пространстве, увеличение подвижности суставов, уменьшение боли и создание возможных ортопедических приспособлений [33].
Kedem P., Scher D.M. обращают внимание, что хирургическая коррекция эквинусной деформации стоп у детей с ДЦП носит роль многоуровневого лечения, цель которой — улучшить походку пациента. Коррекция положения стопы улучшает функцию коленного сустава, видимо за счет изменения плеча рычага в кинематике ходьбы [34].
Проблема исправления эквинусной деформации стоп у детей с ДЦП определяется высокой частотой и существенной ролью в нарушении опороспособности и поддержании патологической позы. Неэффективность консервативных методов лечения вызывает необходимость применения различных хирургических вмешательств у 12-70 % больных с ДЦП, по данным разных авторов [11][35].
Для оценки степени тяжести деформации стоп, а также общеклинического и ортопедо-неврологического статуса, необходима оценка постурального компонента.
Для детей с церебральным параличом характерны сложные и гетерогенные двигательные расстройства, которые формируют нарушения походки. Для определения, понимания и поддержки управления отклонениями походки при ДЦП необходим клинический анализ ходьбы, включающий большой объем количественных данных о характеристике походки пациента, таких как кинематика, кинетика, электромиография и данные о плантографии [33]. Общие отклонения походки при ДЦП для облегчения понимания могут быть сгруппированы в модели походки спастической гемиплегии (эквинусная деформация стопы с различными положениями колена) и спастической диплегии [33]. Чтобы интерпретировать клинический анализ походки, необходимо связать отклонения походки с клиническими нарушениями и отличить от компенсационных стратегий. Клинический анализ походки не указывает конкретно на то, как необходимо лечить пациента детским церебральным параличом, но может обеспечить объективную идентификацию отклонений и в дальнейшем понимание патологического типа походки. Тупиков В.А. (2012) считает оправданным определение коэффициента реципрокности на фоне предварительно выполненной огибающей электромиографии при определении плана хирургического лечения эквинусной деформации стопы [36]. Как правило, лечение стремится профилактировать вторичные деформации, восстановить функцию рычага голеностопного сустава и сохранить силу мышц [33].
Несмотря на значительные достижения в области хирургии детского церебрального паралича, проблема лечения эквинусной деформации стоп у данного контингента больных, особенно у детей дошкольного и раннего школьного возраста, остаётся актуальной.
На сегодняшний день существует множество оперативных вмешательств и их модификаций, направленных на коррекцию данной патологии [2][4][5][6][7]. Однако большое количество предложенных вариантов говорит о неоднозначности решения проблемы лечения эквинусной деформации стоп у детей с ДЦП. Также не определены четкие диагностические критерии, позволяющие выбрать способ и объем хирургической коррекции эквинусной деформации стоп.
Цель большинства операций — коррекция сухожилий мышц голени (ахиллово сухожилие в 80-90 % случаев) [24]. В то же время такие хирургические вмешательства патогенетически не обоснованы, носят механистический подход к данной проблеме. Полное пересечение мышцы или сухожилия формирует новую реакцию в коре головного мозга и, соответственно, другой стереотип движения, далеко не всегда безупречный. Анализ литературных источников свидетельствует о том, что существующие рутинные методы хирургической коррекции спастических деформаций стоп у детей с ДЦП осложняются потерей коррекции, рецидивами, обратными деформациями, развитием тибиального синдрома в 6,7-27,9% случаев независимо от применяемых способов, что связано с недооценкой неврологической составляющей этиопатогенеза этих деформаций [37].
Рецидивы встречаются у 41 % пациентов после удлинения ахиллова сухожилия, формирование пяточной стопы происходит у 36 % [38][39].
Соответственно, отсутствие системного подхода к лечению, определения тактики ведения пациентов, основанных на современных методах диагностики, приводят к возникновению большого количества рецидивов и неудовлетворительным результатам.
На сегодняшний день можно разделить оперативные вмешательства, направленные на коррекцию эквинусной деформации стоп, на следующие группы:
- — хирургические вмешательства на ахилловом сухожилии [8][33][35];
- — оперативные вмешательства на икроножной мышце [40];
- — коррекция с помощью аппарата Илизарова [41][42];
- — комбинированные операции [43].
Что касается аппаратной коррекции, то данный метод ограничен в силу возрастных критериев, но, несмотря на это, имеет относительное неплохие результаты [16].
Удлинение икроножной мышцы при её изолированном укорочении производится в мышечно-сухожильной части путём рассечения сухожильного апоневроза в различных модификациях (операции Strayer, Vulpius, Baker, Tachdjian) и обладают высоким клиническим эффектом [32]. К недостаткам этих операций можно отнести косметически неприглядный послеоперационный рубец, большое количество рецидивов (от 12 до 48 %) [4][26][44], связанных с повреждением так называемой «зоны роста», которая находится в месте перехода мышцы в сухожилие [45]. Удлинение ахиллова сухожилия в различных модификациях закрытым и открытым способом приводит не только к возникновению рецидивов в 6-25 % случаев, но и к формированию энергетически не выгодной «согнутой» ходьбы и плохо поддающейся лечению пяточной деформации стопы, причины которых заложены в самой сути «удлиняющих» операций [7]. Удлинение ахиллова сухожилия всего на 1 см приводит к снижению силы m. soleus на 30 %, на 1,2 см — на 50 %, а 2 см — на 85 % [46]. В этой связи актуальным является предложенный вариант вентрализации ахиллова сухожилия [47].
В своем исследовании (с 1994 по 2000 гг. 45 пациентов, 34 стопы) Lipczyk Z., Faflik J., Kraska T. указывают на применение хирургических методик, которые включали разделение порции сухожилия задней большеберцовой мышцы, транспозиции сухожилия короткой малоберцовой мышцы в комбинации с ахиллотомией и рецессией трехглавой мышцы по Вульпиусу. Отличные результаты — в 68,4 %, хорошие результаты — в 20,1 % и неудовлетворительные результаты — в 11,5 % [43].
Ряд авторов использует методику чрескожного удлинения икроножной мышцы в проксимальной части с последующим увеличением дорзальной флексии до угла не более 15° [17].
Исследования показали, что дети со спастической формой церебрального паралича (эквинусной деформацией стоп) имеют более длинное, чем обычно, ахиллово сухожилие и более короткие, чем обычно, мышечные волокна [9]. Эти признаки наблюдаются даже у детей с динамическим эквинусом до того, как формируется контрактура. Хирургическое удлинение сухожилия позволяет восстановить и увеличить объем тыльного сгибания стопы, однако это не влияет на восстановление нормальной архитектоники мышечных волокон [9]. Данная архитектоника, прежде всего, влияет на функцию, возможно, способствуя функциональному дефициту в виде слабости подошвенной флексии после ахиллопластики.
Умнов В.В., Кенис В.М., Степаненко А.Ю. (2006) придерживаются методик селективной ризотомии при лечении спастических форм ДЦП [48].
Grzegorzewski A., Borowski A., Pruszczyήski B. et al. (2007) указывают на то, что эквино-варусная деформация стопы является результатом нарушения баланса мышц голени, главным образом, задней и передней большеберцовой мышц, которые являются более сильными по сравнению с эверторами стопы [49]. У детей с церебральным параличом не вылеченная спастическая эквино-варусная деформация может вызвать серьезную фиксированную контрактуру стопы и болезненные мозоли под метатарзальными головками и на боковой стороне стопы. Походка становится менее эффективной и нуждается в большем количестве энергии. Правильное предоперационное планирование путем разделения большеберцовых мышц с последующей транспозицией сухожилия может принести хорошие клинические и функциональные результаты у детей с эквино-варусной деформацией. Они рекомендуют данный вид операции на ранней стадии деформации, что поможет исключить в последующем тройной артродез костей стопы [49].
Сычевский Л.З., Аносов В.С., Мармыш А.Г. (2009) предложили метод парциальной транспозиции малоберцовой и большеберцовой мышц при эквино-варусной деформации, основанный на принятии решения о методе оперативного лечения превалирования так называемой «заднетибиальной» или «переднетибиальной» этиологии [40].
Общепринятым и наиболее распространенным методом оперативного лечения эквинусных деформаций стоп является удлинение икроножной мышцы голени при ее изолированном поражении и удлинение ахиллова сухожилия при полном укорочении трехглавой мышцы голени [37].
Раннее выполнение оперативного вмешательства позволяет у большинства больных обойтись единственной операцией и прервать цепь развития вторичных деформаций [50].
По мнению Zuhrmann A., Weselov G. (1982), преимуществами открытой ахиллотомии являются наличие открытой раны и возможность рассекать сухожилие, не опасаясь повредить сосудистые пучки, а также дозированность удлинения. В то же время авторы признают ряд отрицательных сторон и стремятся снизить травматич- ность хирургического вмешательства путем сшивания концов сухожилия с минимальной травмой, а также расположением швов сухожилия, сухожильного влагалища и кожи на разных уровнях [51].
А.Ф. Краснов, А.П. Чернов, И.И. Лосев (2003, 2011) придерживаются способов оперативной коррекции по Байеру в сочетании с Z-образным рассечением сухожилия длинной малоберцовой мышцы, отсечением сухожилия передней большеберцовой мышцы и последующими сшиванием длинной малоберцовой мышцы и транспозицией передней большеберцовой мышцы [2][50]. Некоторые ученые считают целесообразным сочетание методов ахиллопластики по Байеру с фиксацией стоп аппаратом чрескостного остеосинтеза [4].
Существуют работы, посвященные сравнительному анализу таких оперативных вмешательств, как апоневротическое удлинение икроножной мышцы, операция Штоффеля-2, ахиллопластика с предварительным расчётом и без него [52].
Коррекция деформаций стоп при ДЦП с использованием компрессионно-дистракционных аппаратов может использоваться в трех вариантах [53]:
- При умеренно выраженных фиксированных или пограничных контрактурах проводят «закрытую» коррекцию за счет растяжения мягких тканей с помощью дистракции.
- При выраженных многоплоскостных деформациях стопы при ДЦП у детей до 12 лет аппаратная дистракция используется как способ докоррекции после теномиопластических вмешательств для профилактики трофических и неврологических осложнений и постепенного устранения деформации.
- При тяжелых деформациях стопы при ДЦП у детей старше 12 лет аппаратная коррекция используется в сочетании с теномиопластическими и артродезирующими вмешательствами.
Анализ публикаций [10][27][49][52][53] показывает, что все хирургические способы, несмотря на индивидуальный их подход, обычно, не учитывают многофакторности заболевания, которые определяют позу и ходьбу больных ДЦП, влияния патологических тонических рефлексов, патологической синергии, силового дисбаланса мышц, биомеханики приспособительных процессов.
Дальнейшие углубленные исследования мышц нижних конечностей у детей с ДЦП, создание математической модели нижних конечностей при ДЦП могут определить уровень, способ и объем хирургического вмешательства как неотъемлемой части системного лечения ДЦП.
1. Бадалян Л.О. Детская неврология. – М.: Медицина; 1984.
2. Краснов А.С. Хирургическое лечение эквинусной деформации стопы у детей с детским церебральным параличом (обзор) // Саратовский научно-медицинский журнал. – 2011. – Т. 7. – № 3. – С. 699-703. Доступно по: https:// www.ssmj.ru/system/fles/201103_699-703.pdf Ссылка активна на 12.12.2017.
3. Tyson J.E., Gilstrap L.C. Hope for perinatal prevention of cerebral palsy. // JAMA. – 2003. – V.290(20). – P.2730-2. doi: 10.1001/jama.290.20.2730
4. Буравцов П.П., Неретин А.С. Оперативное лечение эквинусной деформации стоп у пациентов со спастической формой детского церебрального паралича // Гений ортопедии. – 2006. – № 3. – С. 52–53.
5. Батышева Т.Т. Детский церебральный паралич – актуальный обзор // Доктор.ру. – 2012. – № 5. – С. 40-44.
6. Sawyer J.R. Cerebral Palsy. — Elsevier; 2013. Doi: 10.1016/b978-0-323-07243-4.00033-5
7. Gage J.R. Te treatment of gait problems in cerebral palsy. // J Pediatr Orthop. – 2001. – V.10(4). – P.267-274.
8. Рыжиков Д.В. Оперативное лечение эквино-плано-вальгусной деформации стоп у детей больных детским церебральным параличом. // Гений ортопедии. – 2010. — №3. – С.95-100.
9. Cavlak U., Kavlak E. Analysing of Ankle-Foot Deformities in Cerebral Palsied Children: Retrospective Study. // Journal of Medical Sciences. – 2005. – V.5(1). – P.55–60. doi: 10.3923/jms.2005.55.60
10. Щеколова Н.Б., Белокрылов Н.М., Ненахова Я.В. Ортопедическая коррекция двигательных нарушений у детей с церебральными параличами // Пермский медицинский журнал. – 2008. – Т.25, № 2. – С. 45-49.
11. МакКомак А.Д. Скелетные мышцы. — К.: Олимпийская литература. — 2001.
12. Renee L., Jurgen M. Research on the performance of the spastic calf muscle of young adults with cerebral palsy. // J Clin Med. – 2011. – V.3(1). – P.8-16. doi: 10.4021/jocmr483w
13. Bennet G.C., Rang M., Jones D. Varus and valgus deformities of the foot in cerebral palsy. // Dev Med Child Neurol. – 1982. – V.24. – P.499-503.
14. Craig J.J., Vuren J. Te importance of gastrocnemius recession in the correction of equinus deformity in cerebral palsy. // J Bone Joint Surg. – 1976. – V.58. – P.84-87. doi: 10.1302/0301-620x.58b1.1270500
15. Bland D.C., Prosser L.A., Bellini L.A., Alter K.E., Damiano D.L. Tibialis anterior architecture, strength, and gait in individuals with cerebral palsy. // Muscle Nerve. – 2011. – V.44(4). – P.509-17. doi: 10.1002/mus.22098.
16. Tachdjian М.O. Atlas of Pediatrics Orthopedics Surgery. — Philadelphia: W.B. Saunders, 1994.
17. Босых В.Г., Сологубов Е.Г. Хирургическое лечение детей с церебральными параличами и эквинусной деформацией стоп // Вопросы современной педиатрии. – 2006. – Т. 5. – № 1. – С. 74.
18. Van Bemmel AF, van den Bekerom MP, Verhart J, Vergroesen DA. Preliminary results of 97 percutaneous gastrocnemius muscular lengthening operations in neurologically healthy children with an equinus contracture. // Foot Ankle Surg. – 2012. – V.18(3). – P.160-3. doi: 10.1016/j.fas.2011.07.004.
19. Дьячкова Г.В., Меньшикова Т.И., Варки Д.Ш. Информативность различных методов визуализации при исследовании нижних конечностей у больных с ахондропалзией // Медицинская визуализация. – 2002. – № 2. – С. 133-137. Доступно по: https://vidar.ru/_getfle.asp?fd=MV_2002_2_133. Ссылка активна на 12.12.2017.
20. Умнов В.В., Умнов Д.В. Особенности патогенеза, клиники и диагностики эквино-плано-вальгусной деформации стоп у больных детским церебральным параличом // Травматология и ортопедия России. – 2013. — № 1. – С. 93-97. Доступно по: https://doi.org/10.21823/2311-2905-2013—1-93-98. Ссылка активна на 12.12.2017.
21. Noble J.J., Fry N.R., Lewis A.P., Keevil S.F., Gough M,. Shortland A.P. Lower limb muscle volumes in bilateral spastic cerebral palsy. // Brain Dev. – 2014. – V.36(4). – P.294300. doi: 10.1016/j.braindev.2013.05.008.
22. Bandholm T., Sonne Holm S., Tomsen C., Bencke J., Pedersen S.A., Jensen B.R. Calf muscle volume estimates: implications for botulinum toxin treatment? // Pediatr Neurol. – 2007. – V.37 (4). – P.263-269. doi: 10.1016/j.pediatrneurol.2007.05.019
23. Blemker S.S., Asakawa D.S., Gold G.E., Delp S.L. Image-based musculoskeletal modeling: applications, advances, and future opportunities. // J Magn Reson Imaging. – 2007. – V.25(2). – P.441-451. doi: 10.1002/jmri.20805
24. Дьякова В.Н. Оптимизация ортопедо-хирургического лечения эквинусной деформации стоп у детей с детским церебральным параличом: автореф. дис. … канд. мед. наук : 14.00.35 / РостГМУ. – Ростов н/Д, 2007. – 15 с.
25. Brockmann K., Becker P., Schreiber G., Neubert K., Brunner E., Bönnemann C. Sensitivity and specifcity of qualitative muscle ultrasound in assessment of suspected neuromuscular disease in childhood. // Neuromuscul Disord. – 2007. – V. 17(7). – P.517-523. doi: 10.1016/j.nmd.2007.03.015
26. Еськин Н.А, Куропаткин А.И., Горбатенко С.А. Ультразвуковые методы исследования в травматологии и ортопедии // Вестник травматологии и ортопедии им. Н.Н.Приорова. – 1996. – № 4. – С. 52-58.
27. Alanen A.M., Falck B., Kalimo H., Komu M.E., Sonninen V.H. Ultrasound, computed tomography and magnetic resonance imaging in myopathies: correlations with electromyography and histopathology. // Acta Neurol Scand. – 1994. – V.89(1). – P.336-346. doi: 10.1111/j.1600-0404.1994.tb02644.x
28. Hunt K.J., Ryu J.H. Neuromuscular Problems in Foot and Ankle. // Foot and Ankle Clinics. – 2014. – V.19(1). – P.1-16. doi: 10.1016/j.fcl.2013.10.002
29. Gao F., Zhao H., Gaebler Spira D., Zhang L.Q. In vivo evaluations of morphologic changes of gastrocnemius muscle fascicles and achillestendon in children with cerebral palsy. // Am J Phys Med Rehabil. – 2011. – V.90(5). – P.364-371. doi: 10.1097/PHM.0b013e318214f699.
30. Pillen S., Verrips A., van Alfen N., Arts I.M.P., Sie L.T.L., Zwarts M.J. Quantitative skeletal muscle ultrasound: Diagnostic value in childhood neuromuscular disease. // Neuromuscular Disorders. – 2007. – V.17(7). – P.509-516. doi: 10.1016/j.nmd.2007.03.008
31. Lieber R.L., Runesson E., Einarsson F. Inferior mechanical properties of spastic muscle bund lesdueto hypertrophic but compromised extracellular matrix material. // Muscle Nerve. – 2003. – V.28. – P.464-471. doi: 10.1002/mus.10446
32. Fridén J., Lieber R.L. Spastic muscle cells are shorter and stiffer than normal cells. // Muscle Nerve. – 2003. — V.27(2). – P.157-164. doi: 10.1002/mus.10247
33. Armand S., Decoulon G., Bonnefoy-Mazure A. Gait analysis in children with cerebral palsy. // EFORT Open Rev. – 2016. – V.1(12). – P.448-460. doi: 10.1302/2058-5241.1.000052.
34. Kedem P., Scher D.M. Foot deformities in children with cerebral palsy. // Curr Opin Pediatr. – 2015. – V.27(1). – P.67-74. doi: 10.1097/mop.0000000000000180
35. Устьянцев В.И., Коломиец Л.А. Способ пластики ахиллова сухожилия у больных дет.ским церебральным параличом // Ортопедия, травматология и протезирование. – 1991. – № 10. – С. 51-53.
36. Тупиков В.А., Шамик В.Б., Тупиков М.В. Применение комплекса биоуправления для прогнозирования исходов хирургического лечения детского церебрального паралича // Известия ЮФУ. Технические науки. – 2012. – № 9(134). – С. 160-164. Доступно по: https://izv-tn.tti.sfedu.ru/wp-content/uploads/2012/9/31.pdf. Ссылка активна на 12.12.2017.
37. Анализ результатов хирургического лечения деформаций стоп у детей с ДЦП // Эксперты в области медицины: сайт. — Ростов н/Д, 2013-2018. Доступно по: https:// vrach-prof.ru/?p=5543. Ссылка активна на 12.02.2018.
38. Borton D.C., Walker K., Pirpiris M. Isolated calf lengthening in cerebral palsy. Outcome analysis of risk factors. // Bone Joint Surg Br. – 2001. – V.83. – P.364-370. doi: 10.1302/0301-620x.83b3.0830364
39. Sala D.A., Grant A.D., Kummer F.J. Equinus deformity in cerebral palsy: recurrence afer tendo Achillis lengthening. // Dev Med Child Neurol. – 1997. – V.39. – P.45-48. doi: 10.1111/j.1469-8749.1997.tb08203.x
40. Сычевский Л.З., Аносов В.С., Мармыш А.Г. Результаты хирургического лечения эквиноварусных деформаций стоп у больных детским церебральным параличом // Журнал ГрГМУ. – 2009. – № 2. – С. 213-217.
41. Rezzouk J., Laville J.M. Devenir de la correction par appareil d’Ilizarov des déformations sévères du piedLong-term outcome afer Ilizarov corrective fxation for severe foot deformity. // Rev Chir Orthop Reparatrice Appar Mot. – 2001. – V.87(1). – P.61-66. doi: rco-02-2001-87-1-0035-1040-101019-art6 (in France)
42. Wren T.A., Cheatwood A.P., Rethlefsen S.A., Hara R., Perez F.J., Kay R.M. Achilles tendon length and medial gastrocnemius architecture in children with cerebral palsy and equinus gait. // J Pediatr Orthop. – 2010. – V.30(5). – P.479-84. doi: 10.1097/BPO.0b013e3181e00c80.
43. Lipczyk Z., Faflik J., Kraska T. Surgical treatment of spastic equino-varus deformity. // Ortop Traumatol Rehabil. – 2002. – V.4(1). – P.27-29.
44. Семенова К.А. Восстановительное лечение у детей с перинатальными поражениями нервной системы и ДЦП. – М.: Закон и порядок, 2007.
45. Damron T.A., Greenwald T.A., Breed A.L. Chronologic outcomes of surgical tendo Achilles lenghthening and natural history of gastrosoleus contracture in cerebral palsy: a two part study. // ClinOrthop. – 1994. – V.301. – P.249-255. doi: 10.1097/00003086-199404000-00039
46. Сычевский Л.З., Болтрукевич С.И. Биомеханическое обоснование метода хирургического лечения спастических эквинусных деформаций. Биомеханика стопы человека // Материалы I Междунар.науч.-практ. конф. – Гродно, 2008. – С. 150-152.
47. Сычевский Л.З., Аносов В.С., Михович М.С. Результаты оперативного лечения спастических фиксированных эквинусных деформаций методом вентрализации ахиллова сухожилия // Военная медицина. – 2009. – № 3. – С. 44–50.
48. Умнов В.В., Кенис В.М. Поражение нижних конечностей при ДЦП // Травматология и ортопедия: рук-во для врачей: в 4 т. Т. 3: Травмы и заболевания нижних конечностей / под ред. Н.В. Корнилова и Э.Г. Грязнухина. – СПб.: Гиппократ, 2006. – С. 1003–1024.
49. Grzegorzewski A., Borowski A., Pruszczyński B., Wranicz A., Domzalski M., Synder M. Split tibialis posterior tendon transfer on peroneus brevis for equinovarus foot in CP children. // Chir Narzadow Ruchu Ortop Pol. – 2007. – V.72(2). – P.117-120.
50. Чернов А.П., Лосев И.И. Комплексное лечение больных с паралитическими деформациями стоп. – Самара, 2003.
51. Zuhrmann A., Weselov G. Fünfahrergebnissebei der Klumpfut behandlung. // Ortop. Prax. – 1982. – V.18(1). – P.44-46.
52. Хамраев Ф.Ш., Мирзаев А.Г. Дифференцированный подход к ортопедохирургическому лечению эквинусных деформаций стоп при ДЦП // Врач-аспирант. — 2009. — № 9(36). — С. 789-797.
53. Чочиев Г.М., Алборов О.И., Филатова Н.Б., Елкина И.А. Хирургическое лечение в комплексе медико-социальной реабилитации больных ДЦП // Актуальные вопросы детской травматологии и ортопедии. – СПб., 2002. – С. 276.
Метод Понсети – Клиника Гемокод Симферополь
Метод Понсети — это нехирургический способ коррекции косолапости. Отклонение стоп от нормального положения приносит боли, трудности при передвижении, сказывается на состоянии коленных и тазобедренных суставов.
Эффективность лечения косолапости методом Понсети
Косолапость бывает врожденной и приобретенной. Применяя метод в раннем возрасте для коррекции положения, стоп можно исправить ошибку природы и оградить ребенка от проблем в будущем.
Лечение косолапости по методу ортопеда Понсети было разработано и введено в медицинскую практику в 50 г. прошлого столетия. Наблюдения за пациентами, перенесшими гипсование, доказали эффективность и надежность способа лечения.
И. Понсети разработал методику динамического гипсования, основанную на эластичности и мягкости связок ребенка, высокого содержания коллагена в тканях.
Гипсование Понсети имеет ряд преимуществ:
- неинвазивная методика;
- коррекция начинается в возрасте – 7–14 дней от роду;
- ребенок не испытывает боли;
- не нарушается порядок между сухожилиями стопы;
- не нарушается подвижность нижней конечности;
- длительность лечения составляет от 1 до 2 месяцев в зависимости от индивидуальных особенностей ребенка;
- эффективность – коррекция в 90% случаев;
- исправление нарушений, вызванных косолапостью – эквинус, супинацию и аддукцию;
- рецидивы косолапости наблюдаются всего у 6% пациентов.
Техника проведения методики
Методика гипсования по Понсети требует скрупулезности и внимательности, соблюдения сроков фиксации. В реабилитационном периоде – длительное использование брейсов для закрепления достигнутых результатов. Способ лечения является стандартом консервативного лечения в странах Европы, США.
Эффективность терапии зависит от качества взаимодействия врача и родителей. Ножка в гипсе хоть и вызывает жалость, но если поддаться этому чувству, можно усугубить состояние ребенка вплоть до инвалидизации. Ортопед должен четко соблюдать график растяжения связок стопы и информировать родителей об изменении режима гипсования и ношения брейсов.
Исправление деформации гипсовыми повязками
На этом этапе проводится исправление деформации стопы при помощи гипсовых повязок. Потребуется 6–7 эпизодов гипсования каждые 5–7 дней. Стопа выводится из состояния искривления в нормальное положение. Угол изменения конечности составляет 10–15 градусов за 1 сеанс гипсования. Повязка должна фиксировать коленный сустав и закрывать верхнюю треть бедра.
Процедуру проводит врач и его ассистент. Медсестра удерживает конечность, а ортопед производит гипсование.
Этапы коррекции:
- Первое наложение гипса – исправление кавуса – внутреннего поворота передней части ступни. Тыльное сгибание в голеностопе ограничено.
- Второе-четвертое гипсование – исправление поворота стопы и пальцев внутрь, варуса. У малышей первого года жизни кавус отличается эластичностью и подвижностью. Требуется супинация – вращение части конечности наружу – переднего отдела для коррекции продольного свода стопы.
- Проводится исправление деформации. Головка таранной кости остается зафиксированной, а стопа отводится. Затем стабилизируется положение таранной кости.
- Для исправления нарушения положения стопы достаточно 4–5 эпизодов гипсования. Если стопа трудно поддается коррекции, количество процедур придется увеличить.
- При эпизоде смены гипсовой повязки наблюдается улучшение. Но полной нормализации кавуса, поворота стопы в физиологическом положении, варуса, частичной коррекции эквинуса недостаточно. В редких случаях, при избыточной гибкости сухожилий, эквинус возможно исправить путем гипсования. На втором этапе проводится оперативная коррекция или ахиллотомия.
Ахиллотомия
Операция показана на втором этапе лечения. У малышей с врожденной косолапостью длина ахиллового сухожилия недостаточна для деятельности стопы. Требуется хирургическое удлинение структуры.
По методике Понсети операция проводится через небольшой – не более 0,5 см – разрез. Накладывается гипсовая повязка.
Длительность заживления составляет 3 недели. Этого периода достаточно для нормализации длины сухожилия и заживления. Процедура проводится под местным\общим обезболиванием.
Ношение брейсов
Ношение брейсов по Понсети – ботинков с жесткой подошвой и разделительной планкой – заключительная стадия лечения врожденной формы косолапости. Это позволяет закрепить результаты и минимизировать риск развития рецидива.
Ношение устройства длительное, требует скрупулезного отношения родителей ребенка. На начальных этапах использование ботинок практически круглосуточное. В 80% случаев развития рецидива происходит вследствии небрежного отношения родителей к требованиям методологии ношения брейсов.
Ширина планки и угол, под которым будут находиться ножки малыша, определяет врач. Ортопед должен провести инструктаж по срокам ношения специализированных конструкций.
Система применения брейсов для детей различного возраста:
Дети от новорожденности до 9 месяцев:
- 3 месяца – круглосуточно – снимать во время купания;
- 4-й месяц терапии – 20–22 часа;
- 5-й месяц – 18–20 часов;
- 6-й месяц – 16–18 часов в сутки;
- до начала самостоятельной ходьбы – 14–16 часов – во время дневного и ночного сна;
- до 5 лет – во время ночного сна.
При начале ношения лечебной обуви после 9 месяцев:
- 2 месяца – 18–20 часов в сутки;
- 4 месяца – 16 часов;
- До 5 лет – ночной сон в брейсах.
Терапия начата после года. В это время ребенок уже начал ходить:
- 4 месяца – 16–18 часов;
- до 5 лет – ночной сон в ботиночках.
Коррекция проводится по достижению 4 лет – ночной сон в брейсах в течение 1 года.
Прогноз лечения
Рецидивы заболевания возникают у 1–2 пациентов из 10. В подавляющем большинстве случаев это связано с несоблюдением правил ношения ортопедических конструкций или режима гипсования. В 90% случаев после лечения по методике Понсети ребенок начинает ходить в положенные природой сроки, а впоследствии – заниматься спортом наравне с другими детьми.
При односторонней косолапости после коррекции одна стопа может быть немного меньше другой. Это не мешает двигательной активности малыша, но он может уставать быстрее сверстников.
По всем возникшим вопросам Вы сможете получить полную консультацию у наших специалистов!
Падение стопы — Симптомы и причины
Обзор
Опускание стопы, иногда называемое опускающейся стопой, — это общий термин, обозначающий трудности с подъемом передней части стопы. Если у вас свисает стопа, передняя часть стопы может волочиться по земле при ходьбе.
Падение стопы — это не болезнь. Скорее всего, свисание стопы является признаком основной неврологической, мышечной или анатомической проблемы.
Иногда падение ступни временное, но может быть постоянным.Если у вас свисает стопа, возможно, вам придется носить бандаж на лодыжке и стопе, чтобы удерживать стопу в нормальном положении.
Продукты и услуги
Показать больше продуктов от Mayo ClinicСимптомы
Опускание стопы затрудняет подъем передней части стопы, поэтому при ходьбе она может волочиться по полу. Это может заставить вас приподнять бедро при ходьбе, как при подъеме по лестнице (ступенчатая походка), чтобы помочь ноге оторваться от пола.Эта необычная походка может привести к тому, что вы при каждом шаге будете шлепать ногой об пол. В некоторых случаях кажется, что кожа на верхней части стопы и на пальцах ног онемела.
В зависимости от причины падение ступни может повлиять на одну или обе ступни.
Когда обращаться к врачу
Если пальцы ног тянутся по полу при ходьбе, обратитесь к врачу.
Причины
Падение стопы вызвано слабостью или параличом мышц, участвующих в подъеме передней части стопы.Причины падения стопы могут включать:
-
Травма нерва. Наиболее частой причиной опускания стопы является сжатие нерва в ноге, который контролирует мышцы, участвующие в подъеме стопы (малоберцовый нерв). Этот нерв также может быть поврежден во время операции по замене тазобедренного или коленного сустава, что может привести к падению стопы.
Повреждение нервного корешка — «защемление нерва» — в позвоночнике также может вызвать провисание стопы. Люди, страдающие диабетом, более подвержены нервным расстройствам, связанным с отвисанием стопы.
- Мышечные или нервные расстройства. Различные формы мышечной дистрофии, наследственного заболевания, вызывающего прогрессирующую мышечную слабость, могут способствовать провисанию стопы. То же самое и с другими заболеваниями, такими как полиомиелит или болезнь Шарко-Мари-Тута.
- Заболевания головного и спинного мозга. Заболевания, поражающие спинной или головной мозг, такие как боковой амиотрофический склероз (БАС), рассеянный склероз или инсульт, могут вызывать опущение стопы.
Факторы риска
Малоберцовый нерв контролирует мышцы, поднимающие стопу.Этот нерв проходит у поверхности кожи на той стороне колена, которая ближе всего к руке. Действия, которые сдавливают этот нерв, могут увеличить риск падения стопы. Примеры включают:
- Скрестив ноги. Люди, которые обычно скрещивают ноги, могут сдавливать малоберцовый нерв на верхней части ноги.
- Длительное стояние на коленях. Работа, связанная с длительным сидением на корточках или на коленях, например сбор клубники или укладка плитки на пол, может привести к падению ступни.
- Ношение гипсовой повязки. Гипсовые слепки, закрывающие лодыжку и заканчивающиеся чуть ниже колена, могут оказывать давление на малоберцовый нерв.
4 декабря 2020 г.
Показать каталожные номера- Высота в футах. BMJ. 2015; 350: ч2736.
- Страница с информацией о падении стопы. Национальный институт неврологических расстройств и инсульта. https: //www.ninds.nih.gov/Disorders/All-Disorders/Foot-Drop-Information-Page. Доступ 13 сентября 2017 г.
- Рутково СБ. Обзор синдромов периферических нервов нижних конечностей. https // www.uptodate.com / contents / search. Доступ 13 сентября 2017 г.
- Падение стопы. GBS / CIDP Foundation International. https://www.gbs-cidp.org/ecomm/foot-drop/. Доступ 13 сентября 2017 г.
- Аппарат для лечения опущения стопы (перенос сухожилия). Американское общество ортопедов стопы и голеностопного сустава. https://www.aofas.org/footcaremd/treatments/Pages/Foot-Drop-Treatment-(Tendon-Transfer).aspx. Доступ 13 сентября 2017 г.
Связанные
Связанные процедуры
Показать другие связанные процедурыПродукты и услуги
Показать больше продуктов и услуг Mayo ClinicЛечение заболеваний ахиллова сухожилия | Клиника Сандерса Хьюстон
Тендонит ахиллова сухожилия (тендоноз)
Ахиллово сухожилие — это сухожилие икроножной и камбаловидной мышц задней ноги, которое соединяет эти мышцы с пяточной костью (пяточной костью).Он расположен вдоль нижней части спины икры и доходит до пятки. Эта группа сухожилий мышц отвечает за подошвенное сгибание голеностопного сустава и является основным двигателем для стояния и ходьбы на пальцах ног, а также отталкивания, когда человек бежит или прыгает.
Травма обычно возникает, когда сухожилие подвергается нагрузке из-за коротких быстрых движений или резких толчков и остановок, например, в ракетболе, теннисе, футболе или танцах. Это также может повлиять на женщин, которые часто носят обувь на высоком каблуке и переходят на кроссовки во время тренировок.Этот стресс может быть кумулятивным или возникать в результате одного спонтанного движения после недостаточной «разминки» или растяжения.
Воспаление этого сухожилия известно как тендинит ахиллова сухожилия. Это дегенеративное состояние сухожилия либо в его субстанции, либо в месте прикрепления к пятке. Хотя это обычно называется тендинитом, признаков истинного воспаления нет. Тендоноз ахиллова сухожилия, вероятно, более правильный термин с медицинской точки зрения. Это происходит, когда перегруженное сухожилие дегенерирует, вызывая увеличение сухожилия, ограничение гибкости и боль.
Обычно это состояние возникает у пациентов с IGC (идиопатической контрактурой икроножной мышцы). В этом чрезвычайно распространенном состоянии, которое предрасполагает по крайней мере к половине всех распространенных заболеваний стопы и голеностопного сустава, блок икроножных мышц / сухожилий чрезмерно напряжен. Диагноз ставится на клинической основе в клинике с помощью теста Сильфверскиольда.
Важным моментом анатомии является то, что икроножная мышца берет начало выше колена и более плотно при разгибании колена, чем при его сгибании.Если голеностопный сустав можно поместить в большее тыльное сгибание (пальцы ног направлены в сторону носа), когда колено согнуто, чем когда колено разгибается, то икроножная мышца сокращается. Для того, чтобы считаться нормальным, человеку необходимо не менее 10 градусов тыльного сгибания голеностопного сустава с разогнутым коленом. Многие авторитетные источники считают, что на самом деле нормальное измерение должно составлять 18 градусов. Несомненно, менее 10 градусов является ненормальным и предрасполагает пациентов к тендонозу ахиллова сухожилия и другим заболеваниям сухожилий, подошвенному фасцииту, растяжениям голеностопного сустава, бурситам и большинству других заболеваний передней части стопы!
Если не лечить тендоноз ахиллова сухожилия, он может прогрессировать и ухудшаться, а небольшой разрыв может привести к разрыву сухожилия, отделяющему икроножную мышцу от пяточной кости.Когда это происходит, нормальное движение голеностопного сустава невозможно.
Если тендоноз ахиллова сухожилия лечится до разрыва сухожилия, существует ряд неоперационных способов восстановить силы в этой области. Они включают растяжку, лед, модификацию обуви, пищевые добавки и изменения в индивидуальном расписании тренировок. Наиболее важными методами лечения являются растяжение и удлинение мышечного комплекса камбаловидной мышцы. Тем не менее, лучшее лечение — это профилактика. Тендинита можно избежать, если правильно укрепить все группы мышц ног, а также правильно растянуть и разогреться до и после тяжелых занятий или занятий спортом.
У некоторых пациентов эти меры безуспешны. Совсем недавно стали популярными инъекции плазмы, богатой тромбоцитами, но теперь доказано, что они не лучше плацебо. Другие хирургические меры имели лишь частичный успех. Освобождение сухожилия икроножной мышцы при сохранении нетронутой камбаловидной мышцы и сухожилия известно как процедура Strayer. Это очень простая и недорогая процедура, выполняемая в отделении дневной хирургии больницы с последующей иммобилизацией, а затем упражнениями.Это последовательно улучшает тыльное сгибание голеностопного сустава и снимает чрезмерное напряжение с ахиллова сухожилия, позволяя ему заживать самостоятельно.
Разрыв ахиллова сухожилия
Полный разрыв часто происходит спонтанно во время занятий спортом, без ранее существовавшего тендинита, обычно у спортсмена в возрасте от 30 до 40 лет. Большинство пациентов скажут, что они услышали громкий хлопок, и им показалось, что их голень вот-вот взорвется. Отек значительный, ходить трудно.Исторически сложилось так, что эти спортсмены выбирали хирургическое лечение для восстановления сухожилия с последующей иммобилизацией гипсовой повязкой. Рациональным для хирургического вмешательства было то, что будет лучшая максимальная прочность и меньшая частота повторных разрывов. Обратной стороной операции были осложнения, обычно связанные с плохим заживлением ран. Исторически сообщалось, что нехирургическое лечение приводит к более высокой частоте повторных разрывов, но, конечно, не вызывает проблем с заживлением ран.
За последние пару лет ускоренная реабилитация как оперированного, так и неоперированного пациента сократила разрыв между двумя группами.На данный момент частота повторного разрушения и предел прочности почти одинаковы для оперированных и не оперированных случаев. Хирургические осложнения все еще могут возникать в оперированных случаях, но в среднем эти пациенты возвращаются к работе примерно на три недели раньше, чем неоперированные пациенты. Оперированные пациенты вернулись в спорт через три месяца, неоперированные пациенты вернулись примерно через шесть месяцев. Доктор Сандерс имеет обширный опыт работы с обоими планами лечения, и, поскольку они приводят к аналогичным результатам, он оставляет решение за пациентом.
Паралич малоберцового нерва — обзор
Клиническая оценка асимметрии
Падение стопы, аномальное уменьшение тыльного сгибания во время фазы качания цикла походки, является серьезной проблемой для людей с рассеянным склерозом. 8 Другими словами, снижение способности к тыльному сгибанию большеберцовой мышцы приводит к перетягиванию пальца стопы, напрямую увеличивая риск споткнуться и упасть, что может привести к серьезным травмам. 38,55,56 Следует оценить механизмы падения стопы и факторы, которые могут преувеличить падение стопы, такие как асимметрия, чтобы минимизировать этот симптом из-за его влияния на риск падения.
Исследования показали, что передняя большеберцовая мышца (мышца, непосредственно связанная с опусканием стопы) поражается рассеянным склерозом как периферически, так и центрально. Биопсия мышц передней большеберцовой мышцы показала, что у людей с РС меньше волокон типа I, а мышечные волокна всех типов были в среднем на 26% меньше у людей с РС по сравнению с контрольной группой. 12 Кроме того, наблюдалось снижение активности окислительных ферментов на 40%, что заставляло мышцы полагаться на более неэффективные источники энергии (анаэробный метаболизм), что в дальнейшем влияло на ADL и QOL. 12 Сообщалось о замедлении или снижении нервного возбуждения передней большеберцовой мышцы у лиц с РС, что выражалось в снижении максимального мышечного сокращения на 27% после упражнений, что указывает на снижение общей производительности мышц и общего метаболического спроса. на мышцы. 23 Одна область, которую еще предстоит полностью оценить, — это то, как возможность двустороннего воздействия на скелетные мышцы влияет на опускание стопы. Возможно, что после того, как будут проведены клинические оценки, можно будет изучить прямые вмешательства для метаболической асимметрии.
Уменьшение массы скелетных мышц может иметь серьезные последствия для людей с рассеянным скелетом. Тем не менее, несколько исследований изучали влияние РС на размер скелетных мышц. Поскольку обычно диагноз рассеянного склероза диагностируется в раннем зрелом возрасте и пациенты, как правило, менее активны, чем их здоровые сверстники, важно понимать, как сочетание течения заболевания (и старения) влияет на скелетные мышцы. Большое беспокойство вызывает то, что мышечная слабость обычно поражает одну сторону тела больше, чем другую, 3,14,30 , и, учитывая двусторонний характер походки, односторонняя слабость становится более опасной.Люди с рассеянным склерозом действительно проявляют слабость в большей степени в одной конечности, чем в другой. Ларсон и его коллеги (2013) наблюдали разницу в изометрическом разгибателе колена примерно на 10 кг. 27 Чанг и его коллеги сообщили о значительной взаимосвязи между показателем асимметрии силы разгибателей колена и нормальным временем ходьбы (r = 0,63) и временем быстрой ходьбы (r = 0,61), так что те, у кого более высокий показатель асимметрии силы разгибателей колена, также имели более длительную ходьбу. раз. Эти данные подтверждают важность устранения такой асимметрии на ранних этапах развития болезни. 14
Из-за наблюдений за снижением силы скелетных мышц у человека с РС оценка площади поперечного сечения мышц имеет большое значение. Имеющиеся ограниченные данные указывают на то, что различия могут зависеть от мышц. Например, волокна скелетных мышц передней большеберцовой мышцы продемонстрировали значительную атрофию трех типов волокон (типы I, IIa и IIax) по сравнению со здоровыми аналогами. 12 Однако в связи с этиологией рассеянного склероза и представлением об асимметрии необходимо более детальное исследование мышц.
Распознавание и клинические последствия функциональной асимметрии при РС только начинают изучаться. Результаты исследований в таких областях, как сила, аэробная производительность, МПК, баланс и походка, неизменно указывают на важность асимметрии. Медицинские и клинические последствия подтверждают экономическое обоснование продолжения разработки исследовательских программ, специально нацеленных на полную оценку и лечение двусторонних различий.
Связь диапазона движения тыльного сгибания голеностопного сустава с кинематикой бедра и колена во время теста бокового смещения
Дизайн исследования Контролируемое лабораторное исследование.Актуальность проблемы Измененная кинематика бедра и колена была связана с рядом заболеваний коленного сустава, включая разрыв передней крестообразной связки, пателлофеморальную боль и синдром подвздошно-большеберцовой связки. Ограниченный диапазон движений (ROM) при тыльном сгибании голеностопного сустава, который был связан с некоторыми из этих нарушений, также был связан с измененной кинематикой коленного сустава. Цель: изучить связь DF ROM голеностопного сустава с кинематикой бедра и колена во время выполнения задания на спуск. Методы Тридцать здоровых участников прошли трехмерный анализ кинематики тазобедренного и коленного суставов во время теста бокового смещения вниз с последующим измерением DF ROM голеностопного сустава при нагрузке (WB) и без нагрузки (NWB).С использованием средних значений участники были разделены на подгруппы с низким и высоким DF как в WB, так и в NWB. Кинематика бедра и колена сравнивалась в подгруппах с низким и высоким DF. Результаты Участники в подгруппах с низким DF продемонстрировали большую пиковую аддукцию бедра (WB, P = 0,02; NWB, P <0,01) и большую пиковую внешнюю ротацию колена (WB, P = 0,02; NWB, P <0,01) по сравнению с с участниками из подгрупп с высоким DF. Кроме того, участники подгруппы WB с низким DF продемонстрировали снижение пикового сгибания колена по сравнению с участниками подгруппы WB с высоким DF (P <.01). Заключение У лиц с DF ROM нижней части голеностопного сустава кинематика тазобедренного и коленного суставов ранее ассоциировалась с несколькими заболеваниями коленного сустава, что позволяет предположить, что это нарушение может быть вовлечено в патогенез тех же заболеваний. Оценка DF ROM голеностопного сустава может быть полезна как часть предварительного обследования. Кроме того, может потребоваться устранение дефицита DF ROM в голеностопном суставе у людей с измененными паттернами движений. J Orthop Sports Phys Ther 2016; 46 (11): - 1. Epub 29 сентября 2016 г. doi: 10.2519 / jospt.2016.6621.
Ключевые слова: динамический вальгус; схема движения; голеностопный сустав.
Тыловое сгибание голеностопного сустава у здоровых мужчин с разным качеством движений нижних конечностей
J Athl Train. 2014 сентябрь-октябрь; 49 (5): 617–623.
, DPT, PhD, * , PhD, * , MD, † and, MD ‡Alon Rabin
* Университет Ариэля, Израиль
Цви Козол
* Университет Ариэля, Израиль
Элад Спитцер
† Медицинский центр Еврейского университета Хадасса, Эйн-Керем, Иерусалим, Израиль
Аарон Финстоун
‡ Медицинский центр Ассаф Арофе, Тель-Авивский университет, Медицинский корпус Сил обороны Израиля, Зеррифин, Израиль
* Университет Ариэля, Израиль
† Медицинский центр Еврейского университета Хадасса, Эйн-Керем, Иерусалим, Израиль
‡ Медицинский центр Ассаф Арофе, Тель-Авивский университет, Медицинский корпус Сил обороны Израиля, Зеррифин, Израиль
Адресная корреспонденция Алону Рабину, доктору наук, доктору философии, Университет Ариэля, Кирьят-Хамада, а / я 3, Ариэль, Израиль.Адрес электронной почты: [email protected] . Авторское право © Национальной ассоциации спортивных тренеров, Inc.Abstract
Контекст:
Модели движений нижних конечностей считаются фактором риска различных заболеваний коленного сустава. Диапазон движений (ROM) при тыльно-голеностопном суставе (DF) ранее был связан с неправильным двигательным паттерном среди здоровых женщин-участниц.
Цель:
Определить связь между DF ROM голеностопного сустава и качеством движения нижних конечностей во время теста латерального шага вниз среди здоровых участников мужского пола.
Дизайн:
Поперечное исследование.
Расположение:
Учебный комплекс Армии обороны Израиля.
Пациенты или другие участники:
Пятьдесят пять здоровых израильских солдат-новобранцев мужского пола (возраст = 19,7 ± 1,1 года, рост = 175,4 ± 6,4 см, масса = 72,0 ± 7,6 кг).
Вмешательство (-я):
ПЗУ тыльного сгибания измеряли в условиях нагрузки и отсутствия нагрузки с использованием инклинометра, заполненного жидкостью, и универсального гониометра, соответственно.Характер движений нижних конечностей оценивался визуально с помощью теста бокового смещения вниз и классифицировался как хороший или умеренный. Все измерения проводились с двух сторон.
Основной показатель результата:
Несущая и не несущая DF ROM была более ограничена среди участников со средним качеством движения, чем у участников с хорошим качеством движения на доминирующей стороне ( P =. 01 и P = 0,02 для несущего и ненесущего DF соответственно).DF без нагрузки продемонстрировал тенденцию к уменьшению диапазона среди участников с умеренным по сравнению с участниками с хорошим качеством движения на не доминирующей стороне ( P = 0,03 [скорректированный P = 0,025]). DF с нагрузкой не различалась между участниками с хорошими и умеренными моделями движений на не доминирующей стороне ( P = 0,10). DF ROM голеностопного сустава, несущего и не несущего нагрузку, значительно коррелировал с качеством движения с обеих сторон ( P <.01 и P <0,05 на доминирующей и недоминантной стороне соответственно).
Выводы:
Ankle DF ROM был связан с качеством движения среди здоровых участников мужского пола. Ассоциация казалась более слабой у мужчин, чем у женщин.
Ключевые слова: передняя крестообразная связка, бедро, колено, боковой тест с понижением, пателлофеморальный болевой синдром
Ключевые моменты
-
У здоровых мужчин с умеренным качеством движения в тесте с боковым понижением лодыжка была меньше -дорсифлексия диапазон движений, чем у людей с хорошим качеством движения.
-
Когда у мужчин наблюдается более низкое качество движений, врачи должны рассмотреть возможность вмешательства для увеличения тыльного сгибания голеностопного сустава.
Измененный паттерн движений нижних конечностей, состоящий из чрезмерного приведения бедренной кости и внутренней ротации, приводящих к чрезмерному выравниванию вальгусного сустава коленного сустава, считается фактором риска развития пателлофеморального болевого синдрома (PFPS) и неконтактных повреждений передней крестообразной связки. 1 — 3 Было высказано предположение, что различные факторы способствуют изменению модели движений, включая снижение силы ипсилатеральной мускулатуры бедра, 4 , 5 усиление пронации подтаранного сустава, 6 , 7 и измененное управление двигателем. 8 Оценка модели движений и факторов, связанных с ней, поэтому обычно выполняется при обследовании пациентов с PFPS, а также при скрининге риска травмы колена. 9 — 11
Еще одним возможным фактором, способствующим изменению модели движений, является доступный диапазон движений (ROM) ипсилатерального тыльного сгибания голеностопного сустава (DF). Снижение DF ROM голеностопного сустава может ограничивать продвижение большеберцовой кости вперед по таранной кости во время действий, требующих одновременного сгибания колена и DF голеностопного сустава (например, приседание, спуск по лестнице).Возможной компенсацией ограниченного движения большеберцовой кости может быть подтаранная пронация, которая может сместить большеберцовую кость и колено медиально в сторону большего вальгусного выравнивания. 6 , 12 — 14 Уже существуют некоторые доказательства связи между DF голеностопного сустава и паттерном движений нижних конечностей. Уменьшение DF ранее ассоциировалось с усилением вальгусной деформации колена во время маневра с падением на землю, 14 при приседании, 15 и маневре с опусканием 16 у здоровых участников.
Одним из ограничений современной литературы по этой теме является включение только женщин-участниц во многие исследования, оценивающие модели движений нижних конечностей и связанные с ними факторы. 8 , 19 , 20 Было показано, что женщины выполняют такие действия, как резка, прыжки и приземление, с большей вальгусностью колена и большим разгибанием колена, чем у мужчин. 19 , 20 Предполагается, что эти различия объясняют более высокую частоту бесконтактных разрывов передней крестообразной связки и PFPS среди женщин. 1 , 2 , 21 , 22 Соответственно, авторы 14 , 16 из 2 исследований, которые ранее связывали снижение DF голеностопного сустава с неправильным паттерном движений только участницы-женщины.Третье исследование смешанной популяции продемонстрировало только статистическую тенденцию ассоциации между DF голеностопного сустава и неправильным паттерном движений. 15 Таким образом, неясно, одинакова ли связь между DF голеностопного сустава и паттерном движений нижних конечностей для обоих полов.
Парадоксально, но еще одним ограничением современной литературы является использование сложных систем трехмерного анализа движений во многих исследованиях, оценивающих модели движений нижних конечностей. 2 , 4 , 14 , 17 , 18 Хотя этот тип анализа, безусловно, способствует высокому уровню точности и надежности, врачи и тренеры обычно не имеют доступ, время или навыки для работы с такими системами.Вместо этого визуальное наблюдение часто используется для оценки моделей движений в клинике или в полевых условиях. Однако неизвестно, в какой степени любые отклонения движения, выявленные во время трехмерного анализа движения, коррелируют с отклонениями движения, выявленными визуально. Следовательно, результаты исследований трехмерного анализа движения могут быть трудными для применения в клинических условиях или в полевых условиях. Поэтому мы решили оценить, связана ли DF ROM голеностопного сустава с качеством движений нижних конечностей при визуальной оценке здоровых мужчин-участников.
Тест бокового смещения (LSD) часто используется для оценки движений нижних конечностей. 9 , 11 , 23 — 25 Пива и др. 25 предложили визуально основанную систему оценок для классификации качества движения во время теста LSD. Надежность этой рейтинговой системы была установлена ранее. 16 , 25 Наша гипотеза заключалась в том, что участники мужского пола с более низким качеством движений на LSD будут демонстрировать меньше DF ROM на лодыжке.
МЕТОДЫ
Это исследование было одобрено Советом по институциональному надзору Сил обороны Израиля. Все участники прочитали и подписали форму информированного согласия перед началом процедуры исследования. Данные для этого исследования были собраны в рамках более крупного проспективного исследования потенциальных факторов риска различных травм во время базовой армейской подготовки.
Участники
Обследовано 55 мужчин. Их возраст, рост и масса тела — 19,7 ± 1,1 года, 175 человек.4 ± 6,4 см и 72,0 ± 7,6 кг соответственно. Участники были военнослужащими, которые были тщательно проверены на наличие травм или состояний опорно-двигательного аппарата перед началом базовой армейской подготовки. В исследование включались участники, если они были 18 лет и старше и не жаловались на боль в нижних конечностях или поясничном отделе позвоночника. Добровольцы исключались из участия, если они сообщали о боли или травмах в коленях или лодыжках в течение 2 лет до исследования. Эта информация была предоставлена самими участниками и впоследствии проверена научным сотрудником перед началом исследования.
Эксперты
Два эксперта проводили сбор данных для этого расследования. Один исследователь (A.R.) с 13-летним клиническим опытом физиотерапевтического лечения заболеваний опорно-двигательного аппарата выполнил все измерения DF ROM. Другой экзаменатор (З.К.) с более чем 25-летним преподавательским и клиническим опытом в области кинезиологии и неврологической реабилитации проводил все оценки ЛСД. Эти два экзаменатора ранее продемонстрировали средний уровень межэкспертной надежности при выполнении теста LSD (κ = 0.59), а также превосходный уровень надежности при выполнении измерений DF ROM голеностопного сустава с нагрузкой (WB) и без нагрузки (NWB) (коэффициент внутриклассовой корреляции = 0,95 и 0,86 для измерений WB и NWB, соответственно). 16 Перед сбором данных для этого исследования два экзаменатора встретились на 4-часовую сессию, чтобы рассмотреть каждую из процедур измерения.
Процедуры
Сначала была собрана демографическая информация, включая возраст, рост, массу тела и преобладание ног.Доминирующая нога была определена как нога, предпочтительная для удара по мячу. Затем передняя большеберцовая кость каждого участника была отмечена черным цветом на 15 см дистальнее большеберцовой кости. Позже эта отметка использовалась для измерения DF лодыжки WB. Каждый экзаменатор не был осведомлен об измерениях другого экзаменатора, чтобы избежать возможного введения систематической ошибки, основанной на гипотезе исследования. Участники переходили от одной станции сбора данных к другой в зависимости от доступности экзаменатора на каждой станции (например, LSD и DF для голеностопного сустава).Следовательно, порядок измерений не был ни установлен, ни рандомизирован.
Тест бокового смещения вниз
Бугристость большеберцовой кости каждого участника была отмечена синей наклейкой шириной 1 см для облегчения ее визуализации во время теста. Каждому участнику устно объяснили процедуру тестирования, после чего была проведена демонстрация. Сторона, испытанная первой, чередовалась между последовательными участниками. Участники выполнили тест с шагом 15 см (Reebok International, Кантон, Массачусетс).Они поместили тестируемую ногу у края ступеньки, а другая нога свисала сбоку от ступеньки. Участников проинструктировали держать туловище прямо и руки на талии и сгибать колено тестируемой ноги до тех пор, пока контралатеральная пятка не коснется пола рядом с ступенькой. Их попросили не класть вес на контралатеральную пятку, когда она достигала пола, и немедленно снова выпрямить колено и вернуться в исходное положение. Участников также попросили попытаться удерживать колено тестируемой ноги над вторым пальцем ипсилатеральной стопы во время теста (кусок черной ленты был помещен перпендикулярно вдоль передней части ступеньки, прямо под вторым пальцем ноги участника до пола. для облегчения оценки экзаменатором;).Участники выполнили 5 повторений упражнений, а затем 5 повторений тестов. Во время теста экзаменатор располагался на расстоянии 3 м от участника. Тест оценивался по 7-балльной шкале (0–6) в соответствии с критериями, изложенными Piva et al. 25 (). Если во время любого из 5 повторений теста было обнаружено одно из указанных выше отклонений в движении, считалось, что участник продемонстрировал это отклонение, и ему присваивалось соответствующее значение балла (1 или 2). Общий балл 0 или 1 был классифицирован как хорошее качество движения (), общий балл 2 или 3 был классифицирован как умеренное качество движения (), а общий балл 4 или более был классифицирован как плохое качество движения . 25 Только 3 участника были классифицированы как имеющие низкое качество движения (2 на доминирующей стороне LSD и 1 на недоминантной стороне), поэтому мы не включили их данные в первичный статистический анализ.
Хорошая картина движений в тесте поперечного понижения. Таблица 1. 1
Модель движений среднего качества боковой понижающий тест.
Ankle DF ROM
Ankle DF был измерен в условиях WB и NWB. Для обоих измерений пеленгования сторона, тестируемая первой, а также порядок измерения (WB или NWB) менялись между последовательными участниками. Для измерения WB на полу была нанесена линия длиной 50 см, а на стене, где должно было проводиться испытание, была нанесена непрерывная линия длиной 60 см. Участник поставил тестируемую ступню по линии пола так, чтобы линия делила пятку пополам, а второй палец ноги находился на линии.Затем его попросили сделать выпад вперед и подвести коленную чашечку как можно ближе к вертикальной линии, проведенной на стене, не отрывая пятки от пола. После достижения максимального пеленга исследователь поместил инклинометр (MIE Inclinometer; Nationwide Medical, Inc, Агура-Хиллз, Калифорния), который сначала был обнулен на фиксированном вертикальном ориентире, над ранее отмеченным местом на передней большеберцовой кости. Был записан угол пеленгования, и участник вернулся в исходное положение. Процедуру повторяли 3 раза и регистрировали средний диапазон.
Для измерения NWB участник принял положение лежа на животе с согнутым коленом под углом 90 °. Измерения проводились с помощью универсального гониометра (Baseline Plastic Goniometer; The Therapy Connection Inc, Windham, NH). Экзаменатор вручную проверил нейтральное положение подтаранного сустава и поместил голеностопный сустав на полную глубину. Дорсифлексию измеряли как угол между латеральной средней линией голени (линия от головки малоберцовой кости до кончика боковой лодыжки) и боковой границей стопы (линия вдоль задней части стопы и пяточной кости).Было записано среднее значение 3 измерений.
Статистический анализ
Мы провели раздельный анализ доминирующей и недоминантной сторон. В рамках каждой стороны участники были разделены на 2 группы в зависимости от их оценки LSD (хороший или средний). Различия в демографических переменных, а также в WB и NWB DF ROM голеностопного сустава между группами были проанализированы с помощью независимого теста t . Поскольку мы оценивали зависимую переменную (DF голеностопного сустава) двумя способами (WB и NWB), мы использовали скорректированное по Бонферрони значение P , равное.025 (.05 / 2) для анализа. Величины эффекта (ES) для различий в DF ROM между участниками с разным качеством движения с обеих сторон были рассчитаны путем деления разницы в средних баллах на их объединенное стандартное отклонение. ES 0,2 считается малым ; 0,5, средний ; и 0,8 или более, большой . 26 Из этого анализа были исключены 3 участника, которые продемонстрировали низкое качество движений.
Поскольку классификация качества движения на хороший и средний уровни несколько произвольна, мы также проанализировали корреляцию между исходным баллом теста LSD (0–6) и WB и NWB DF ROM для голеностопного сустава с ранговой корреляцией Спирмена. коэффициент ( r ).Корреляции оценивались отдельно для доминирующей и недоминантной сторон. Все участники были включены в этот анализ. Предопределенный уровень значимости (значение P ) для этого анализа был установлен на уровне <0,05. Все статистические анализы были выполнены с использованием SPSS (версия 19; IBM SPSS Inc, Чикаго, Иллинойс).
РЕЗУЛЬТАТЫ
Мы проверили 73 участника на соответствие критериям. Десять участников испытали растяжение связок голеностопного сустава, а еще 8 участников сообщили о боли в передней части колена за 2 года до исследования.Поэтому эти участники были исключены. В результате в анализ было включено 55 участников. Пятьдесят один (93%) сообщил, что правая нога является доминирующей, тогда как 4 сообщили, что левая нога является доминирующей. Основные демографические и клинические переменные всей выборки сведены в.
Таблица 2.
Описательная статистика участников (N = 55)
| Переменная | Среднее ± стандартное отклонение | Диапазон | ||
| Возраст, лет | 19.7 ± 1,1 | 18,1–24,6 | ||
| Высота, см | 175,4 ± 6,4 | 159,0–189,0 | ||
| Масса тела, кг | 72,0 ± 7,6 | 60,3–96,4 | тыльное сгибание, несущее нагрузку, °50,9 ± 6,3 | 35,3–66,0 |
| Недоминантное тыльное сгибание, несущее нагрузку, ° | 57,3 ± 7,0 | 40,0–72,0 | ||
| Недоминантное боковое сгибание тыльное сгибание подшипника, ° | 27.8 ± 6,2 | 12,3–40,3 | ||
| Недоминантное боковое тыльное сгибание без нагрузки, ° | 27,9 ± 6,2 | 10,0–40,7 |
Несущая и NWB DF ROM участников с разным качеством движения с обеих сторон (доминирующей и недоминантной) отображаются в. На доминирующей стороне 33 участника продемонстрировали хорошее качество движения, а 20 — умеренное качество движения. Что касается недоминирующей стороны, 26 участников показали хорошие модели движений, а 28 — умеренные ( P =.14).
Таблица 3.
Диапазон движений тыльного сгибания и сгибания голеностопного сустава для разницы между участниками с хорошими и умеренными результатами теста бокового смещения вниз
| Статус несущей способности при тыльном сгибании | Доминантная сторона a | Недоминантная сторона b | ||||
| Оценка, средняя (доверительный интервал 95%) | Оценка, средняя (95% доверительный интервал) | |||||
| Размер эффекта | Хороший | Средний | Размер эффекта | |||
| Подшипник | 52.7 (50,6, 54,8) | 48,3 (45,6, 51,0) | 0,72 | 58,8 (56,1, 61,5) | 55,7 (53,1, 58,3) | 0,45 |
| Без груза | 29,6 (27,6 (27,6) , 31,6) | 25,7 (23,1, 28,3) | 0,68 | 29,9 (27,5, 32,2) | 26,1 (23,8, 28,4) | 0,63 |
На доминирующей стороне нет разницы в возрасте или массе тела был отмечен между участниками с хорошим или умеренным качеством движения ( P >.05). Участники с хорошим качеством движения были выше, чем участники со средним качеством движения (177,0 против 173,2 см, P = 0,04). ПЗУ DF голеностопного сустава, измеренное в WB и NWB, было больше среди участников с хорошим качеством движения по сравнению со средним качеством ( P = 0,01 и P = 0,02 для WB и NWB, соответственно). ES для разницы WB и NWB на доминирующей стороне были умеренными (0,72 и 0,68 соответственно).
Что касается недоминантной стороны, не было отмечено разницы в возрасте, росте или массе тела между участниками с хорошим или умеренным качеством движения ( P >.05). DF голеностопного сустава без WB продемонстрировал тенденцию к уменьшению диапазона среди участников с умеренным качеством движения по сравнению с хорошим качеством движения ( P = 0,03). ES для этой разницы был умеренным (0,63). DF с нагрузкой не различалась среди участников с разным качеством движения на недоминантной стороне ( P = 0,10, ES = 0,45).
Значения WB и NWB DF ROM для 2 участников с плохим качеством движения на LSD доминирующей стороны составили 46.5 ° ± 2,1 ° и 18,0 ° ± 1,4 ° соответственно. Значения WB и NWB DF ROM для участника с плохим качеством движения на недоминантной стороне LSD составляли 60,7 ° и 28,3 °, соответственно.
Взаимосвязь между DF ROM (WB и NWB) и качеством движения с обеих сторон представлена в. Как WB, так и NWB DF ROM лодыжки значительно коррелировали с качеством движения с обеих сторон ( P <0,05). Характер корреляции указывает на то, что более высокий балл по LSD-тесту (т. Е. Более низкое качество движения) был связан с меньшим количеством DF ROM для голеностопного сустава ().
Таблица 4.
Корреляция (Spearman ρ) между диапазоном движения тыльного сгибания и качеством бокового шага вниз при тестировании качества движения на доминантной и недоминантной сторонах
| Переменная | Коэффициент корреляции | 9020 Значение |
| Оценка дорсифлексии с опорой на доминантную сторону и латерального шага вниз с доминирующей стороны | −0,44 | <0,01 |
| Дорсифлексия с доминантной стороны без нагрузки и боковой шаг с доминирующей стороны -низкая оценка | −0.43 | <0,01 |
| Недоминантная боковая несущая тыльная флексия и недоминантная боковая поперечная ступенчатая смещение | -0,31 | <0,05 |
| Недоминантная боковая ненесущая дорсифлексия и недоминантная дорсифлексия — оценка бокового бокового смещения | -0,37 | <0,01 |
ОБСУЖДЕНИЕ
Связь между DF ROM голеностопного сустава и качеством движений у мужчин выгодно отличается от предыдущих результатов среди здоровых женщин. 16 Однако есть несколько интересных отличий. Во-первых, в то время как 60% участников мужского пола в нашем исследовании продемонстрировали хороший паттерн движений на доминантной стороне ЛСД, только 28% участниц женского пола сделали это в предыдущем исследовании. 16 Это согласуется с более ранними исследованиями 19 , 20 , указывающими на половые различия в кинематике нижних конечностей и, возможно, на более рискованные модели движений женщин во время различных функциональных нагрузок.Еще одно интересное отличие — большее значение NWB DF ROM у мужчин по сравнению с женщинами (27,8 ° против 23,5 °). 16 Поскольку эти измерения были выполнены одним и тем же исследователем в обоих исследованиях, разумно полагать, что они отражают истинное различие. Это различие также может помочь объяснить большую разницу в DF ROM у женщин с разным качеством движений по сравнению с мужчинами (ES = 1,1 у женщин против 0,68 у мужчин). 16 DF ROM голеностопного сустава у мужчин в этом исследовании, возможно, не было достаточно ограниченным, чтобы объяснить различия в качестве движений по сравнению с женщинами в предыдущем исследовании. 16 Точно так же корреляция между исходной оценкой для LSD доминантной стороны и WB и NWB DF ROM голеностопного сустава кажется большей среди женщин ( r = -0,66 и -0,68, соответственно, 16 по сравнению с r = −0,44 и −0,43 соответственно среди мужчин). Возможно, что DF ROM сильнее связан с паттерном движений нижних конечностей у женщин по сравнению с мужчинами. Эта ассоциация может быть объяснена более ограниченным DF ROM голеностопного сустава у женщин. Однако, поскольку нам неизвестны какие-либо предыдущие исследования половых различий в DF ROM голеностопного сустава, эта гипотеза требует дальнейшего тестирования.
Наши результаты также согласуются с выводами Sigward et al. 14 и Bell et al, 15 , которые связывают снижение DF голеностопного сустава с неправильным движением во время приземления и приседания соответственно. 14 , 15 Наши методы, однако, несколько отличались тем, что мы просили наших участников попробовать выполнить LSD с «идеальным» паттерном движений. Одна инструкция, которую мы дали нашим участникам перед выполнением ЛСД, заключалась в том, чтобы во время теста держать колено выше второго пальца ноги.Поскольку паттерн движения может просто отражать ваш выбор, 18 мы полагали, что инструктаж наших участников выполнять ЛСД с идеальным паттерном движений с большей вероятностью выявит нарушения, которые могут помешать такому паттерну движений. В частности, мы предположили, что участники с менее доступным DF голеностопного сустава не смогут выполнять LSD, сохраняя этот идеальный паттерн движения, несмотря на попытки это сделать. Это могло бы объяснить более четкую связь между DF ROM и паттерном движения в нашем исследовании по сравнению с этими двумя другими исследованиями. 14 , 15
Данные 3 участников с плохим качеством движения (2 на доминирующей стороне LSD и 1 на недоминирующей стороне) не были включены в первичный анализ. Среднее значение NWB DF на доминирующей стороне двух участников с плохим качеством движения на LSD доминирующей стороны, по-видимому, отличалось от такового у участников с хорошим качеством движения (18,0 ° против 29,6 °) или умеренным качеством движения на этой стороне. сбоку (18,0 ° против 25,7 °).Эти данные также предполагают связь между DF и движением мужчин.
Хотя наши результаты в целом подтверждают связь между DF ROM голеностопного сустава и паттерном движений нижних конечностей у здоровых мужчин, некоторые из наших результатов требуют дальнейшего рассмотрения. Во-первых, величину корреляции между DF (WB или NWB) и паттерном движения, а также ES для разницы в DF ROM между участниками с разным качеством движения можно в лучшем случае считать умеренными.Это неудивительно, учитывая множество факторов, которые ранее были связаны с паттернами движений нижних конечностей. 4 — 8 Более чем вероятно, что модель движения является многофакторной конструкцией. 27 Кроме того, ПЗУ WB DF нашего образца было на 4–11 ° больше, чем было обнаружено в предыдущих исследованиях, 28 – 30 , а ПЗУ NWB было на 6–7 ° больше, чем сообщалось. ранее. 15 , 31 , 32 В результате предполагаемое неблагоприятное влияние ограниченного DF голеностопного сустава на паттерн движений нижних конечностей могло быть ограничено в нашей выборке.
Еще одним интересным открытием было то, что ни измерение DF (ни WB, ни NWB) не показало статистически значимой разницы между участниками с хорошим и умеренным качеством движения на недоминантной стороне. Это можно объяснить меньшей мощностью анализа недоминантной стороны по сравнению с доминирующей (апостериорный анализ мощности: 0,37 против 0,71 для WB DF и 0,62 против 0,66 для NWB DF).
Наконец, участники с хорошим качеством движения на доминирующей стороне также были выше, чем участники с умеренным качеством движения.Рост мог повлиять на качество движения в нашем исследовании, поскольку все участники выполняли LSD со стандартным 15-сантиметровым шагом. LSD, возможно, был менее сложным для более высоких участников, поскольку для его выполнения, возможно, требовалось меньше сгибания колена или DF лодыжки (или того и другого). Однако участники с хорошим качеством движений на доминирующей стороне все же продемонстрировали большую доступную DF ROM на голеностопном суставе. Будущие исследователи, использующие LSD-тест, могут пожелать рассмотреть возможность регулировки высоты ступеньки в соответствии с ростом своих участников.
Основная сила этого исследования заключается в его простоте и клинической полезности. Мы использовали недорогое оборудование, доступное в большинстве случаев. Кроме того, в повседневной практике врачи и тренеры обычно полагаются на визуальное наблюдение за качеством движений. Еще одной сильной стороной нашего исследования является независимая оценка качества движения и DF ROM, которая минимизировала предвзятость наблюдателя. Наконец, двусторонние измерения, сделанные в этом исследовании, являются еще одним уникальным фактором по сравнению со многими другими исследованиями, изучающими паттерны движений нижних конечностей.Обычно измерения проводились на доминирующей нижней конечности участников. 9 , 10 , 14 , 16 Неизвестно, влияет ли доминирование ног на связь между качеством движения и ROM или другими физическими показателями. Наши результаты показывают, что DF ROM голеностопного сустава ассоциируется с качеством движения любой нижней конечности. Тем не менее, наши данные также последовательно демонстрируют более слабую связь между DF голеностопного сустава и качеством движений на недоминантной стороне.В будущих исследованиях моделей движений нижних конечностей и связанных с ними факторов исследователи могут пожелать включить в анализ обе стороны.
Хотя мы не можем сделать вывод, что снижение DF голеностопного сустава является причиной изменения модели движений на основе этого исследования, наши результаты имеют несколько возможных последствий. Во-первых, может потребоваться оценка DF голеностопного сустава при визуальном выявлении измененной модели движений. Во-вторых, вмешательства для увеличения DF ROM голеностопного сустава могут быть показаны, когда целью является улучшение качества движения.В-третьих, учитывая связь между измененным паттерном движений и расстройствами коленного сустава, такими как PFPS и разрывы передней крестообразной связки, 1 — 3 увеличение доступного DF голеностопного сустава может уменьшить возникновение таких расстройств.
Потенциально полезным направлением будущих исследований могло бы стать определение того, присутствует ли связь между двигательным паттерном и DF голеностопного сустава у пациентов с такими расстройствами, как PFPS. Предыдущее исследование 30 , 31 дало противоречивые результаты относительно связи между DF голеностопного сустава и PFPS.Интересно, что Пива и др., 31 , которые продемонстрировали эту связь, использовали измерение NWB DF, тогда как Barton et al. 30 использовали измерение WB и не нашли связи. Эти различия могут быть обусловлены различными используемыми методами измерения. В качестве альтернативы, поскольку PFPS считается многофакторным заболеванием, возможно, что только подгруппа пациентов с PFPS демонстрирует ограниченный DF голеностопного сустава. Эта подгруппа может также демонстрировать более измененный паттерн движений.
Наше исследование имеет несколько ограничений. Во-первых, наши результаты применимы только к здоровым участникам мужского пола, выполняющим ЛСД после получения инструкций по правильному образцу движений. Неизвестно, будут ли пациенты с такими расстройствами, как PFPS, или те, кто не получает инструкций о том, как проводить LSD, аналогичные результаты. Во-вторых, это исследование не позволяет установить причинно-следственную связь из-за его перекрестных методов.
ВЫВОДЫ
Здоровые мужчины с более низким качеством движений на доминирующей стороне продемонстрировали меньшую доступность DF ROM голеностопного сустава.Кроме того, DF ROM голеностопного сустава умеренно коррелировал с качеством движения в обеих нижних конечностях. Хотя связь между DF голеностопного сустава и качеством движений кажется более слабой среди здоровых мужчин по сравнению с женщинами, оценка и возможное вмешательство для увеличения DF голеностопного сустава должны рассматриваться, когда наблюдается более низкое качество движения среди мужчин.
Рекомендуется провести дальнейшее исследование связи DF голеностопного сустава и качества движений среди клинических популяций, таких как пациенты с PFPS.
ССЫЛКИ
1.Boling MC, Padua DA, Marshall SW, Guskiewicz K, Pyne S, Beutler A. Проспективное исследование биомеханических факторов риска пателлофеморального болевого синдрома: когорта совместных усилий по мониторингу и предотвращению травм ACL (JUMP-ACL). Am J Sports Med . 2009. 37 (11): 2108–2116. [Бесплатная статья PMC] [PubMed] [Google Scholar] 2. Hewett TE, Myer GD, Ford KR и др. Биомеханические показатели нервно-мышечной и вальгусной нагрузки на колено позволяют прогнозировать риск повреждения передней крестообразной связки у спортсменок. Am J Sports Med . 2005. 33 (4): 492–501. [PubMed] [Google Scholar] 3. Накагава TH, Мория ET, Maciel CD, Serrao FV. Кинематика туловища, таза, бедра и колена, сила бедра и активация ягодичных мышц во время приседаний на одной ноге у мужчин и женщин с синдромом пателлофеморальной боли и без него. J Orthop Sports Phys Ther . 2012. 42 (6): 491–501. [PubMed] [Google Scholar] 4. Соуза РБ, Пауэрс СМ. Различия в кинематике тазобедренного сустава, мышечной силе и мышечной активации между субъектами с пателлофеморальной болью и без нее. J Orthop Sports Phys Ther . 2009. 39 (1): 12–19. [PubMed] [Google Scholar] 5. Диркс Т.А., Манал К.Т., Хэмилл Дж., Дэвис И.С. Проксимальное и дистальное влияние на кинематику бедра и колена у бегунов с пателлофеморальной болью во время длительного бега. J Orthop Sport Phys Ther . 2008. 38 (8): 448–456. [PubMed] [Google Scholar] 6. Джозеф М., Тиберио Д., Бэрд Дж. Л. и др. Вальгусное колено во время прыжков с падением у спортсменок первого дивизиона Национальной ассоциации легкой атлетики: влияние медиальной стойки. Am J Sports Med . 2008. 36 (2): 285–289. [PubMed] [Google Scholar] 7. Уильямс Д.С., 3-е место, МакКлей Дэвис I, Бэйч С.П. Влияние перевернутых ортезов на механику нижних конечностей у бегунов. Медико-спортивные упражнения . 2003. 35 (12): 2060–2068. [PubMed] [Google Scholar] 8. Сигвард С.М., Пауэрс СМ. Влияние пола на кинематику колена, кинетику и паттерны активации мышц во время срезания бокового шага. Clin Biomech (Бристоль, Эйвон) 2006; 21 (1): 41–48. [PubMed] [Google Scholar] 9.Chmielewski TL, Hodges MJ, Horodyski M, Bishop MD, Conrad BP, Tillman SM. Исследование согласия клинициста в оценке качества движений при выполнении односторонних функциональных задач нижних конечностей: сравнение 2-х методов оценки. J Orthop Sports Phys Ther . 2007. 37 (3): 122–129. [PubMed] [Google Scholar] 10. Экегрен CL, Миллер WC, Celebrini RG, Eng JJ, Macintyre DL. Надежность и валидность наблюдательного скрининга риска при оценке динамической вальгусной локализации коленного сустава. J Orthop Sports Phys Ther .2009. 39 (9): 665–674. [Бесплатная статья PMC] [PubMed] [Google Scholar] 11. Лоури К.Д., Клеланд Дж. А., Дайк К. Ведение пациентов с пателлофеморальным болевым синдромом с использованием мультимодального подхода: серия случаев. J Orthop Sports Phys Ther . 2008. 38 (11): 691–702. [PubMed] [Google Scholar] 12. Валовая MT. Скрининг нижней четверти на искривление скелета — рекомендации по ортопедии и обуви. J Orthop Sports Phys Ther . 1995. 21 (6): 389–405. [PubMed] [Google Scholar] 13. Полномочия CM. Влияние измененной кинематики нижних конечностей на дисфункцию пателлофеморального сустава: теоретическая перспектива. J Orthop Sports Phys Ther . 2003. 33 (11): 639–646. [PubMed] [Google Scholar] 14. Сигвард С.М., Сусуму О., Пауэрс С.М. Предикторы экскурсии колена во фронтальной плоскости при падении у юных футболисток. J Orthop Sports Phys Ther . 2008. 38 (11): 661–667. [PubMed] [Google Scholar] 15. Белл Д.Р., Падуя, Д.А., Кларк, Массачусетс. Характеристики силы и гибкости мышц у людей с чрезмерным медиальным смещением колена. Arch Phys Med Rehabil . 2008. 89 (7): 1323–1328.[PubMed] [Google Scholar] 16. Рабин А., Козол З. Измерения диапазона движений и силы среди здоровых женщин с разным качеством движений нижних конечностей во время теста на латеральное смещение вниз. J Orthop Sports Phys Ther . 2010. 40 (12): 792–800. [PubMed] [Google Scholar] 17. Bolgla LA, Malone TR, Umberger BR, Uhl TL. Сила бедра и кинематика бедра и колена при спуске по лестнице у женщин с пателлофеморальным болевым синдромом и без него. J Orthop Sports Phys Ther . 2008. 38 (1): 12–18.[PubMed] [Google Scholar] 18. Мизнер Р.Л., Кавагути Дж.К., Хмелевский Т.Л. Сила мышц нижних конечностей не позволяет прогнозировать улучшение посадки спортсменок после инструктажа. J Orthop Sports Phys Ther . 2008. 38 (6): 353–361. [PubMed] [Google Scholar] 19. Декер MJ, Torry MR, Wyland DJ, Sterett WI, Steadman RJ. Гендерные различия в кинематике, кинетике и поглощении энергии нижних конечностей при приземлении. Clin Biomech (Бристоль, Эйвон) 2003; 18 (7): 662–669.[PubMed] [Google Scholar] 20. Маклин С.Г., Уокер КБ, ван ден Богерт А.Дж.. Влияние пола на кинематику нижних конечностей при быстрой смене направления: комплексный анализ трех спортивных движений. J Sci Med Sport . 2005. 8 (4): 411–422. [PubMed] [Google Scholar] 21. Агель Дж., Арендт Е.А., Бершадский Б. Травма передней крестообразной связки в баскетболе и футболе Национальной студенческой спортивной ассоциации: обзор за 13 лет. Am J Sports Med . 2005. 33 (4): 524–531. [PubMed] [Google Scholar] 22.Witvrouw E, Lysens R, Bellemans J, Cambier D, Vanderstraeten G. Внутренние факторы риска развития боли в передней части колена у спортсменов. Am J Sports Med . 2000. 28 (4): 480–489. [PubMed] [Google Scholar] 23. Остин А.Б., Соуза Р.Б., Мейер Дж.Л., Пауэрс К.М. Выявление аномального движения бедра, связанного с патологией вертлужной впадины. J Orthop Sports Phys Ther . 2008. 38 (9): 558–565. [PubMed] [Google Scholar] 24. Mascal CL, Landel R, Powers C. Управление пателлофеморальной болью, направленной на функцию мышц бедра, таза и туловища: отчеты о 2 случаях. J Orthop Sport Phys Ther . 2003. 33 (11): 642–660. [PubMed] [Google Scholar] 25. Пива С.Р., Фицджеральд К., Иррганг Дж. Дж. И др. Надежность оценки нарушений, связанных с пателлофеморальным болевым синдромом. BMC Разрушение опорно-двигательного аппарата . 2006; 7: 33. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26. Коэн Дж. Статистический анализ мощности для поведенческих наук . 2-е изд. Хиллсдейл, Нью-Джерси: Lawrence Erlbaum Associates, Inc ;; 1988. [Google Scholar] 28. Беннелл К.Л., Талбот Р.К., Вайсвельнер Х., Техованич В., Келли Д.Х., Холл А.Дж..Надежность измерения тыльного сгибания голеностопного сустава в выпаде с опорой на весовую нагрузку и между экспертами и между экспертами. Ауст Дж. Физиотер . 1998. 44 (3): 175–180. [PubMed] [Google Scholar] 29. Маллиарас П., Кук Дж. Л., Кент П. Уменьшение диапазона тыльного сгибания голеностопного сустава может увеличить риск травмы сухожилия надколенника у волейболистов. J Sci Med Sports . 2006. 9 (4): 304–309. [PubMed] [Google Scholar] 30. Бартон С.Дж., Бонанно Д., Левингер П., Менз Х.Б. Характеристики стопы и голеностопного сустава при пателлофеморальном болевом синдроме: случай-контроль и исследование надежности. J Orthop Sports Phys Ther . 2010. 40 (5): 286–296. [PubMed] [Google Scholar] 31. Пива С.Р., Гуднайт Е.А., Чайлдс Дж. Д.. Сила бедра и гибкость мягких тканей у людей с пателлофеморальным болевым синдромом и без него. J Orthop Sports Phys Ther . 2005. 35 (12): 793–801. [PubMed] [Google Scholar] 32. Кауфман К.Р., Бродайн С.К., Шаффер Р.А., Джонсон С.В., Каллисон Т.Р. Влияние структуры стопы и диапазона движений на травмы опорно-двигательного аппарата. Am J Sports Med .1999. 27 (5): 585–593. [PubMed] [Google Scholar]Расстройство периодических движений конечностей | Центр медицины сна
Расстройство периодических движений конечностей включает ритмичные подергивания ног, а иногда и рук, что может привести к ухудшению качества сна и дневной усталости. В отличие от синдрома беспокойных ног, эти движения являются непроизвольными и обычно происходят, когда человек спит.
Это состояние чаще всего возникает в первой половине ночи во время сна, известного как не-REM (быстрое движение глаз).Эти периодические движения лишь частично возбуждают спящего, но последствия этих частичных пробуждений способствуют плохому сну и ухудшению здоровья.
Расстройство периодических движений конечностей классифицируется как парасомния или расстройство возбуждения. Его можно разделить на подрывные и неразрушающие. В большинстве случаев задействованы движения ног, однако нельзя исключать движения рук. Эти движения также могут быть связаны с чрезмерной дневной сонливостью или бессонницей.
Симптомы
Это заболевание периодически характеризуется тыльным сгибанием (сгибанием вверх) большого пальца ноги, стопы или сгибанием всей ноги, обычно с интервалами в 20–30 секунд.Часто люди не замечают этих движений во время сна. Часто о происшествиях сообщает кто-то из близких, или человек с этим расстройством может заметить, что покрывала и простыни полностью оторваны от кровати.
Люди могут испытывать чрезмерную дневную сонливость, трудности с засыпанием или раннее просыпание. Расстройство периодических движений конечностей, хотя само по себе во многих случаях незначительное, часто сопровождает другие, более серьезные нарушения сна, и его нельзя игнорировать.
Диагностика
Расстройство периодических движений конечностей — это диагноз, устанавливаемый полисомнографическим исследованием или исследованием сна.Если врач центра сна считает, что движения конечностей вызывают нарушения во время сна, тогда клинически показано исследование сна. Люди с расстройством периодических движений конечностей часто не страдают синдромом беспокойных ног.
Другие состояния также могут быть ошибочно диагностированы как синдром беспокойных ног или периодические движения конечностей. Эти состояния могут включать миоклонус, эпилепсию, синдром болезненных ног и движущихся пальцев ног, а также ночные судороги в ногах. Пациенты с почечной недостаточностью, низким уровнем железа или ферритина и периферической невропатией в анамнезе часто ощущают движения ног и дискомфорт во время сна.
Лечение
После постановки диагноза обычно используются лекарства для лечения расстройства периодических движений конечностей, если оно играет роль в фрагментированном сне. Доступно множество лекарств, и рекомендации можно дать во время консультации и / или после исследования сна.
Чтобы проконсультироваться со специалистом по медицине сна, позвоните в Центр медицины сна по телефону 314-362-4342 .
Падение стопы — Physiopedia
Падение стопы вызвано повреждением общего малоберцового нерва, который контролирует активное тыльное сгибание голеностопного сустава, что приводит к отсутствию удара пяткой во время походки, отсюда и термин «провисание стопы».Изображение к R показывает обычную скобу (AFO) для опускания стопы.
Клинически значимая анатомия [править | править источник]
Общий малоберцовый нерв — это меньшая и терминальная ветвь седалищного нерва, которая состоит из задних отделов L4, 5, S1, 2. Нерв можно пальпировать за головкой малоберцовой кости, когда он обвивает шейку малоберцовой кости. малоберцовая кость. [1]
Обычно при повреждении общего малоберцового нерва возникает слабость передней большеберцовой мышцы и других ключевых тыльных сгибателей стопы.
Механизм повреждения / патологического процесса [править | править источник]
Общий малоберцовый нерв находится в особенно уязвимом положении, поскольку он обвивает шейку малоберцовой кости. На этом участке он может быть поврежден:
Типичное проявление провисания стопы можно отметить при изолированном тестировании стопы и голеностопного сустава, однако в клинических условиях оно может быть выявлено первоначально посредством оценки походки.
Стопа и лодыжка [править | править источник]
- При тестировании стопы и голеностопного сустава положительным результатом теста на падение стопы является NO активного тыльного сгибания в ненагруженном положении.
- Важно протестировать пассивное ПЗУ, чтобы убедиться, что лодыжка не жесткая.
- См. Страницу обследования стопы и голеностопного сустава для полной оценки стопы и голеностопного сустава.
Оценка походки [править | править источник]
- Походку следует оценивать в любых клинических условиях.
- Опущенная походка стопы может проявляться по-разному у разных пациентов.
- Некоторые пациенты могут увеличивать сгибание бедра, которое они производят на пораженной стороне, таким образом, очищая пол более эффективно:
-
- [7]
- Другие пациенты могут обходить бедро и тянуть переднюю часть стопы по полу:
[8]
Боль [править | править источник]
- Нейрогенная боль может возникнуть при повреждении общего малоберцового нерва.
- Эта боль может присутствовать в боковой части колена, а также в тыльной части стопы.
- Сенсорные изменения могут также указывать терапевту на повреждение нерва. [9]
- Субъективный анамнез: акцент на любой травме колена, недавней операции на позвоночнике / периферических конечностях или семейном анамнезе неврологического заболевания
- Оценка тыльного сгибания голеностопного сустава
- Неврологический осмотр [9]
- Оценка походки
- Электромиография (ЭМГ) / исследования нервной проводимости [10] [6]
Менеджмент / Вмешательства [править | править источник]
Основным остаточным симптомом после паралича общего малоберцового нерва может быть опущение стопы из-за разрушения групп мышц L4 / 5, выполняющих тыльное сгибание.
Было показано, что это разрешается у двух третей пациентов через год после травмы. [2]
Боль также следует устранять, если пациент испытывает невропатическую боль, с помощью соответствующего обезболивания. [9]
Шинирование [править | править источник]
Один из способов улучшить функцию при устранении падения стопы — это наложение шины.
Для поддержания стопы в подошвенном состоянии можно использовать цельные ортезы голеностопного сустава (AFO) или шину, поднимающую стопу.
Эти работы увеличивают степень тыльного сгибания стопы во время походки и могут предотвратить падение, поскольку пальцы ног не зацепляются за пол.
Упражнение[править | править источник]
Физиотерапевтические вмешательства обычно сосредоточены на поэтапных упражнениях, которые стимулируют активное тыльное сгибание и задействование мышц. Было показано, что эти упражнения предотвращают атрофию и ускоряют выздоровление, но необходимы дополнительные исследования. [2]
У пациентов с неврологическими нарушениями, таких как болезнь Шарко-Мари-Тута, улучшение состояния при укрепляющих упражнениях на переднюю большеберцовую мышцу улучшалось, однако при других неврологических заболеваниях, таких как мышечная дистрофия, силовые тренировки не были эффективными для уменьшения провисания стопы. [12]
Предотвращение контрактур и скованности также является важной поддерживающей целью физиотерапии, поскольку это более вероятно у пациентов с неврологическими заболеваниями, чем после травм колена.
Электростимуляция пораженных групп мышц также улучшает время восстановления. [2]
Хирургия [править | править источник]
Прямая репарация общего малоберцового нерва возможна при хирургическом вмешательстве, однако было показано, что это приводит к плохим результатам, так как остаточное падение стопы приводит к дальнейшему хирургическому вмешательству. [13]
В крайних случаях задняя большеберцовая мышца может быть переставлена для восстановления активного тыльного сгибания с использованием сухожилия, не иннервируемого общим малоберцовым нервом. Было показано, что эта операция более успешна, чем восстановление нерва. [4] [13] [11]
Хирургия показала свою успешность в улучшении силы активного тыльного сгибания и уменьшении использования AFO. [14]
Оценка Stanmore
- ↑ Palastanga N & Soames R Анатомия и движения человека, структура и функции. 6-е изд. Китай: Elsevier (Churchill Livingstone) Limited; 2012 г.
- ↑ 2,0 2,1 2,2 2,3 2,4 Park JH, Restrepo C, Norton R, Mandel S, Sharkey PF, Parvizi J. Распространенный паралич малоберцового нерва после тотальной артропластики коленного сустава: факторы прогноза и ход выздоровления . Журнал артропластики. 1 октября 2013 г .; 28 (9): 1538-42
- ↑ Everaert DG, Stein RB, Abrams GM, Dromerick AW, Francisco GE, Hafner BJ, Huskey TN, Munin MC, Nolan KJ, Kufta CV.Влияние стимулятора опускания стопы и ортезов голеностопного сустава на ходьбу после инсульта: многоцентровое рандомизированное контролируемое исследование. Нейрореабилитация и нейроремонт. 2013 сентябрь; 27 (7): 579-91.
- ↑ 4,0 4,1 Байма Дж., Кривицкас Л. Оценка и лечение малоберцовой невропатии. Актуальные отзывы в опорно-двигательной медицине. 1 июня 2008 г .; 1 (2): 147-53.
- ↑ Хенрихс А. Обзор вывихов колена. Журнал спортивной подготовки. 2004 Октябрь; 39 (4): 365.
- ↑ 6,0 6,1 Краткое описание JM, et al. Травма малоберцового нерва с опущением стопы, осложняющим растяжение связок голеностопного сустава. Серия из четырех случаев с обзором литературы. Бюллетень больницы NYU для заболеваний суставов. 2009; 67 (4): 374-7.
- ↑ Steppage Gait. Джуди Мишрики Доступно по адресу: https://www.youtube.com/watch?v=TijuPg8_JhY [последний доступ 09.02.2013]
- ↑ Ален Вамбе, доктор медицины. Правосторонняя хлопковая походка / шаговая походка / опускание стопы у послеоперационного пациента. Доступно по адресу: https: // www.youtube.com/watch?v=EjPUpKUbZSg [последний доступ 03.11.2019]
- ↑ 9,0 9,1 9,2 9,3 Байма Дж., Кривицкас Л. Оценка и лечение малоберцовой невропатии. Актуальные отзывы в опорно-двигательной медицине. 1 июня 2008 г .; 1 (2): 147-53.
- ↑ 10,0 10,1 Масакадо Ю., Каваками М., Сузуки К., Абэ Л., Ота Т., Кимура А. Клиническая нейрофизиология в диагностике паралича малоберцового нерва. Медицинский журнал Keio. 25 июня 2008 г .; 57 (2): 84-9.
- ↑ 11,0 11,1 Lingaiah P, Jaykumar K, Sural S, Dhal A. Функциональная оценка раннего переноса сухожилия при отвисании стопы. Журнал ортопедической хирургии. 2018 сентября 19; 26 (3): 230949
99766.
- ↑ Sackley C, Disler PB, Turner-Stokes L, Wade DT, Brittle N, Hoppitt T. Реабилитационные вмешательства при опускании стопы при нервно-мышечном заболевании. Кокрановская база данных систематических обзоров. 2009 (3).
- ↑ 13,0 13,1 Озкан Т., Тунцер С., Озтюрк К., Айдын А., Озкан С.Перенос сухожилия задней большеберцовой мышцы для стойкого отвисания стопы после восстановления малоберцового нерва. Журнал реконструктивной микрохирургии. 2009 Апрель; 25 (03): 157-64.
- ↑ Hove LM, Nilsen PT. Перенос сухожилия задней большеберцовой кости при отвисшей стопе: 20 случаев наблюдались в течение 1–5 лет. Acta Orthopaedica Scandinavica. 1998, 1 января; 69 (6): 608-10.
- ↑ Брюэр РБ, Грегори А.Дж. Хроническая боль в голени у спортсменов: руководство по дифференциальной диагностике, оценке и лечению. Спортивное здоровье. 2012 Март; 4 (2): 121-7.
