(PDF) SURGICAL TREATMENT OF A PATIENT WITH PARKES-WEBER-RUBASHOV SYNDROME (CASE REPORT)
ДИАГНОСТИЧЕСКАЯ И ИНТЕРВЕНЦИОННАЯ РАДИОЛОГИЯ Том 11 №4 2017 стр. 70–74
72
артерии (АВМ). Уровень контрастирования поверх-
ностных вен правой голени и частично бедра практиче-
ски равен контрастированию артерий. В подколенных,
большеберцовых и малоберцовых артериях изменений
не выявлено (рис. 1).
Для исключения сосудистых аномалий в центральной
нервной системе, проведена компьютерная томогра-
фия спинного мозга: в переднем и заднем дуральных
пространствах определяется протяженная сосудистая
мальформация, состоящая из сети мелких, извитых
сосудов. Явного питающего сосуда и сброса не опре-
деляется (рис. 2). Далее проведена компьютерная
томография головного мозга: патологических измене-
ний со стороны вещества головного мозга не выявле-
но. Данных за АВМ головного мозга нет.
Консилиумом в составе нейрохирурга, сердечно-сосу-
дистого хирурга и специалиста по рентгеноэндоваску-
лярным методам лечения было принято решение о
проведении эндоваскулярной эмболизации АВМ.
Пациенту в плановом порядке выполнена эмболизация
АВМ правой нижней конечности. Под местной анесте-
зией произведена антеградная пункция общей бедрен-
ной артерии справа, установлен интродьюсер 6 F. Под
флюроскопическим контролем последовательно в
артериовенозные соустья имплантированы три
спирали Flipper (3×4 мм). Ангиографический контроль:
по поверхностной бедренной и подколенной артериям
кровоток магистральный, патологического сброса в
венозную систему нет. Выполнен гемостаз. Наложена
асептическая давящая повязка.
После эндоваскулярного вмешательства болевой син-
дром в нижней правой конечности купировался, пуль-
сация на венах отсутствует, на 7 сутки пациент был
выписан в удовлетворительном состоянии. Пациенту
присвоена 3 группа инвалидности, однако это не
мешает ему работать инженером-технологом.
Через два месяца после эндоваскулярной эмболиза-
ции пациент был госпитализирован для динамического
обследования. Болевой синдром регрессировал; раз-
Болевой синдром регрессировал; раз-
меры конечности, цвет кожи не изменились; пульсация
вен отсутствует, варикозные узлы визуально уменьши-
лись в размерах. Также наблюдается уменьшение АД
со 150/90 мм рт. ст. предоперационно до 140/80 мм рт.
ст. на момент настоящей госпитализации. Проведена
аортоартериография нижних конечностей: состояние
после эмболизации множественных артериовенозных
соустий. Кровоток по артериям магистральный. На
уровне дистальной трети поверхностной бедренной
артерии визуализируются 3 спирали. Определяется
незначительный резидуальный сброс (рис. 3). По
результатам обследований принято решение о консер-
вативном ведении пациента.
Через два года в плановом порядке больной госпита-
лизирован для динамического обследования. Жалоб
не предъявляет, динамики развития симптомов забо-
левания не отмечается. Размеры конечностей уве-
личились по мере роста, но правая нижняя конечность
по размерам на 1,5 см в диаметре и 2 см в длину боль-
ше левой.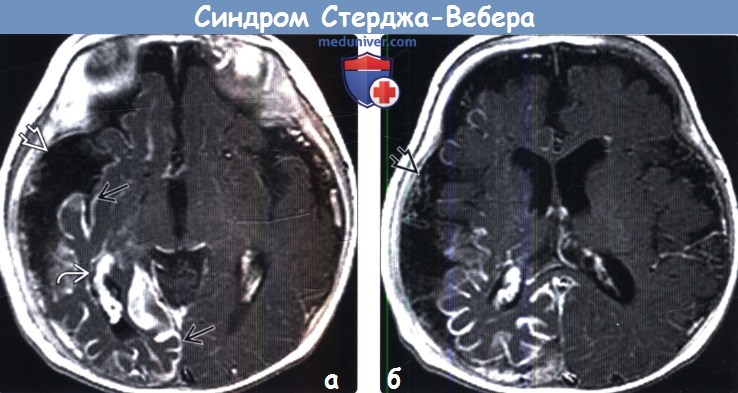 Пациенту выполнена аортография нижних
Пациенту выполнена аортография нижних
конечностей, по результатам которой выраженных
изменений не отмечается. Проведено дуплексное ска-
нирование артерий нижних конечностей: асимметрия
артерий D>S. Слева кровоток магистральный, справа
смешанный из-за сосудистых артерио-венозных
соустий с высокой диастолической составляющей.
Справа от средней трети голени по медиальной
поверхности лоцируются множественные извитые
сосуды со смешанным кровотоком. По ЗББА кровоток
низкоамплитудный. Пациент выписан с прежними
рекомендациями лечения.
Через год пациент повторно госпитализирован для
планового осмотра. Отмечается регресс в динамике
клинических симптомов: меньше отечность конечнос-
ти. По данным аортоартериографии динамических
изменений по сравнению с более ранними обследова-
ниями не отмечается. Клинически определяется раз-
ница в диаметре правой конечности на 2,5 см и в дли-
не на 1,8 см перед левой. Развития других признаков
Развития других признаков
заболевания не отмечено.
Рис. 2. Мультиспиральная компьютерная томограмма
спинного мозга; в переднем и заднем дуральных
пространствах определяется протяженная от 3-го до
12-го грудного позвонка сосудистая мальформация,
состоящая из сети мелких извитых сосудов.
а
б
Пороки развития вен | ILYSSA MEDICAL GROUP
Достаточно редкая и весьма неоднородная группа сосудистых заболеваний – пороки развития вен. Такие патологии нередко сочетаются с мальформациями сосудов. Остановимся подробнее на самых распространенных патологиях.
Врожденный флебэктаз
Данное состояние характеризуется расширенными и извитыми венами, которые очень напоминают вены при варикозе. Заболевание регистрируется, как правило, уже в первые месяцы после появления младенца на свет. Чаще всего поражаются вены конечностей. Флебэктазы способны изменять геометрию конечности, кроме того, при данном заболевании истончаются кожные покровы больной части тела, кожа имеет синюшный оттенок. Пораженная конечность выглядит более толстой, чем здоровая парная конечность, пациент жалуется на болезненность.
Пораженная конечность выглядит более толстой, чем здоровая парная конечность, пациент жалуется на болезненность.
Если пропальпировать такие вены, то они будут легко спадаться и вновь наполняться кровью. Кроме венозной патологии, обычно выявляются проблемы с трофикой других тканей, регистрируется гипоплазия и замедленный рост мышц и костей. При переполнении вены могут рваться.
Диагностика флебэктаза производится посредством флебографии и дуплексного сканирования. Лечение подразумевает хирургическое вмешательство, которое проводится обычно в первые годы жизни. Иногда эффективна склеротерапия.
Синдром Клиппеля-Треноне
Этот порок развития глубоких вен относят к врожденным, он поражает обычно нижние конечности у мальчиков. Причиной становится сдавление глубоких вен эмбриональными тяжами и мышцами. Также проблема может быть спровоцирована недоразвитыми и суженными венами. Уже при рождении видны сосудистые пятна, а когда малыш начинает ходить, будут проявляться и остальные симптомы.
Диагностика синдрома Клиппеля-Треноне подразумевает дуплексное сканирование, флебографию и т.д. Лечение болезни хирургическое, оно обычно проводится, когда ребенок достигает 3-5 лет. В ходе операции устраняется причина сдавления или же поврежденная вена заменяется аутотрансплантатом.
Синдром Паркса-Вебера-Рубашова
Вены могут расширяться и в результате патологических артериовенозных соединений и свищей. Последние могут быть как врожденными (это и есть синдром Паркса-Вебера-Рубашова), так и приобретенными.
Свищи в артериях и в венах могут располагаться в любом органе или ткани, однако чаще всего они выявляются в области конечностей. Итог заболевания – увеличение полостей сердца и развитие хронической сердечной недостаточности.
К симптомам патологии относятся расширенные у поверхности вены, ощущение дрожания при пальпации. Лечение синдрома Паркса-Вебера-Рубашова проходит в несколько этапов, все зависит от конкретного случая. Ангиохирурги иссекают сосуды, иногда патологические сосуды прошивают прямо через кожу. Необходима и компрессионная терапия. В тяжелых случаях показана ампутация конечности.
Лечение синдрома Паркса-Вебера-Рубашова проходит в несколько этапов, все зависит от конкретного случая. Ангиохирурги иссекают сосуды, иногда патологические сосуды прошивают прямо через кожу. Необходима и компрессионная терапия. В тяжелых случаях показана ампутация конечности.
Эктазия яремных вен
Данное заболевание, связанное с патологией яремных вен, обычно выявляется уже у двух-трехлетних детей. Когда ребенок начинает кричать, тужиться, плакать, в районе кивательной мышцы прощупывается небольшая опухоль, которая исчезает после того, как снимается напряжение.
Диагностика заболевания производится дуплексным сканированием вен и флебографией. Лечение эктазии яремных вен хирургическое.
Синдром Маффучи
Это врожденное заболевание, связанное с хондродисплазией, варикозом и гемангиомами. Расширение вен при этой патологии равномерное; гемангиомы находятся на пальцах рук, если их сдавить, то они не спадают, кроме этого, пациент во время подобных манипуляций будет жаловаться на боль.
Патология характеризуется длительным течением. Лечение синдрома Маффучи только оперативное, оно связано с удалением ангиоматозных образований.
Тяжесть в ногах — причины, диагностика и лечение
Тяжесть в ногах в основном возникает при заболеваниях вен: варикозной болезни, посттромбофлебитическом синдроме, хронической венозной недостаточности. Симптом также развивается при лимфедеме, продольном и поперечном плоскостопии, отеках на фоне сердечной или почечной дисфункции. Диагностический поиск предполагает инструментальные методы: УЗДГ вен, реовазографию, лимфангиографию, лимфосцинтиграфию, рентгенологические исследования (рентгенографию стопы, КТ позвоночника). Для купирования тяжести в ногах назначают препараты группы флеботоников и антиагрегантов, инъекционную склеротерапию вен, эластическую компрессию.
Причины тяжести в ногах
Физиологические факторы
Небольшая тяжесть в ногах — нормальное явление при физической нагрузке. После длительных пеших прогулок ощущаются распирающие боли в стопах, голенях, иногда возникает покалывание и чувство ползания мурашек. Чтобы облегчить дискомфорт, человек ложится и придает ногам возвышенное положение. На следующий день тяжесть исчезает, но возможна небольшая скованность движений, болезненность в мышцах при ходьбе.
После длительных пеших прогулок ощущаются распирающие боли в стопах, голенях, иногда возникает покалывание и чувство ползания мурашек. Чтобы облегчить дискомфорт, человек ложится и придает ногам возвышенное положение. На следующий день тяжесть исчезает, но возможна небольшая скованность движений, болезненность в мышцах при ходьбе.
Варикозная болезнь
Является самой частой причиной тяжести в конечностях. Жалобы появляются ближе к вечеру, особенно, если в течение всего дня пациент находился на ногах. В икроножных мышцах ощущаются распирание и жжение, болезненность. Неприятные симптомы уменьшаются или полностью исчезают при возвышенном положении конечностей. На декомпенсированной стадии варикоза больные постоянно испытывают тяжесть в ногах, которая не зависит от положения тела или времени суток.
Симптоматика сопровождается мучительными болями в голенях, которые усугубляются во время ходьбы. Ноги сильно отекают, кожа приобретает бледный или синюшный оттенок.
Посттромбофлебитический синдром
Симптомы проявляются спустя несколько месяцев после перенесенного тромбоза глубоких вен. Больного беспокоят тяжесть и боли распирающего характера в пораженной ноге, которые усиливаются при стоянии и ходьбе. Если конечность находится в возвышенном положении, мучительные ощущения исчезают. По ночам бывают болезненные судороги. При длительном течении посттромбофлебитического синдрома пациенты испытывают постоянную тяжесть и болезненность, из-за нарушения кровообращения формируются мокнущие язвы.
Сердечная недостаточность
Дисфункция правого желудочка и застой в большом круге кровообращения проявляется постоянными отеками ног, что и приводит к чувству тяжести. Симптомы возникают во второй половине дня: ноги наливаются, обувь начинает давить, появляется распирающая боль в ступнях и голенях.
Тяжесть в ногах
Лимфедема
При нарушении лимфообращения тяжесть сочетается с выраженным отеком всей нижней конечности. При врожденной лимфедеме неприятные ощущения сначала затрагивают стопу и голень, затем перемещаются выше. Для приобретенных форм патологии характерны тяжесть и отек в области бедра с последующим нисходящим распространением. Кожа становится натянутой, при надавливании на мягкие ткани образуется ямка, которая долго не расправляется.
Плоскостопие
Дискомфорт и тяжесть в ступнях возникают после длительной ходьбы, при ношении неудобной и неправильно подобранной обуви. Пациенты жалуются на ноющую или резкую боль в своде стопы, тяжесть и напряжение мышц голени. При тяжелом плоскостопии сильная болезненность беспокоит даже при статической нагрузке.
Редкие причины
- Врожденные патологии венозной системы: синдром Клиппеля-Треноне, синдром Паркса-Вебера-Рубашова.
- Заболевания позвоночника: пояснично-крестцовый остеохондроз, спондилолистез.
Диагностика
Учитывая, что большинство случаев тяжести в ногах связаны с нарушениями венозного кровообращения, необходимо обследование у врача-флеболога. Зачастую предварительный диагноз ставится уже при объективном исследовании, когда обнаруживаются расширение вен, отеки, гиперпигментация, другие типичные проявления. Для уточнения диагноза и выявления других этиологических факторов, вызывающих тяжесть в конечностях, проводятся:
- УЗДГ вен. Дуплексное сканирование сосудов используется, чтобы изучить анатомическое строение венозного русла, оценить тонус и работу клапанов.

- Реовазография нижних конечностей. Современный диагностический метод, который показывает даже незначительные изменения гемодинамики и микроциркуляции. По результатам исследования врач дает заключение о состоянии периферических вен при нагрузочных пробах и в покое. Иногда для дополнительного обследования сосудов назначают флебографию.
- Лимфангиография. Визуализация лимфатических сосудов с применением контрастного вещества требуется для определения их проходимости и работы клапанного аппарата. Разница в диаметре на разных участках сосудов и неравномерное контрастирование указывают на патологию. Для динамической оценки лимфообращения показана лимфосцинтиграфия.
- Рентгенография стопы. При подозрении на плоскостопие к диагностическому поиску присоединяется ортопед-травматолог. На основании рентгеновских снимков врач измеряет высоту сводов и патологические углы между костными структурами, устанавливает тип и степень тяжести заболевания.
 Диагноз уточняют с помощью плантографии.
Диагноз уточняют с помощью плантографии. - Дополнительные исследования. Для диагностики остеохондроза, провоцирующего тяжесть в ногах, проводится рентгенография или компьютерная томография позвоночника. Чтобы подтвердить кардиологические болезни, рекомендованы ЭКГ, эхокардиография, рентгенография ОГК. Обзорная и экскреторная урография информативны для исключения почечных причин отеков.
Консультация флеболога
Лечение
Помощь до постановки диагноза
Чтобы избавиться от тяжести в ногах, пациентам рекомендуют подбирать удобную обувь, использовать ортопедические стельки. При необходимости весь день проводить в положении стоя (парикмахеры, продавцы, повара) нужно носить компрессионные чулки, способствующие уменьшению венозного застоя. Необходимо поддерживать массу тела в пределах нормы, чтобы не создавать дополнительную нагрузку на стопы.
Чтобы улучшить периферическое кровообращение и повысить тонус венозных сосудов, полезны занятия спортом (плавание, езда на велосипеде). Следует сократить количество силовых и статичных тренировок, которые усиливают депонирование крови в венах. Важную роль играет изменение образа жизни: повышение повседневной активности, частые пешие прогулки.
Следует сократить количество силовых и статичных тренировок, которые усиливают депонирование крови в венах. Важную роль играет изменение образа жизни: повышение повседневной активности, частые пешие прогулки.
Консервативная терапия
Лечение заболеваний вен в клинической флебологии начинается с медикаментозных средств: приема антиагрегантов, флеботоников, нанесения мазей и кремов на участки кожи с трофическими поражениями. В качестве общеукрепляющих средств показаны витамины группы В, десенсибилизирующие препараты. В редких случаях лечебную схему усиливают кортикостероидными гормонами.
Терапию дополняют эластической компрессией (бинты, чулки), чтобы поддерживать венозные сосуды в тонусе и уменьшить тяжесть в ногах. Для лечения варикоза широко практикуется компрессионная склеротерапия — введение в вены препаратов, которые вызывают склеивание сосудистых стенок и уменьшают венозный застой. После манипуляции устраняется болезненность и отечность голеней.
Для уменьшения отеков при кардиологической и почечной патологии используют диуретики. При постоянном приеме лекарства выводят лишнюю жидкость, устраняют одышку, тяжесть в ногах. При сердечной недостаточности дополнительно назначают бета-блокаторы, гликозиды и другие препараты для улучшения силы сокращений миокарда.
Хирургическое лечение
При варикозной болезни проводится несколько видов хирургических вмешательств:
Больным с лимфедемой рекомендованы лимфовенозное шунтирование, туннелирование, аутотрансплантация тканевого лимфоидного комплекса.
Плоскостопие лечат опытные ортопеды-травматологи. В стадии плосковальгусной стопы выполняют резекцию выступающих участков костей, пересадку сухожилий, удаление пяточной шпоры. Пациентам с поперечным плоскостопием тяжелой степени показана резекция Hallux valgus с последующей пластикой суставной капсулы.
Врожденная ангиодисплазия (синдром Паркса-Вебера-Рубашова): симптомы, лечение, прогноз
Синдром Паркса Вебера (врожденная ангиодисплазия) — это заболевание, проявляющееся увеличением подкожных кровеносных сосудов.
Основой развития данного синдрома является наличие врожденных дефективных анастамозов между венами и артериями. Стадия тяжести болезни зависит от численности анастамозов и их величины. В зависимости от диаметра соустья разделяются на два вида: микрофистулы и макрофистулы.
Место локализации фистул — зона подколенных, бедренных и большеберцовых артерий. Прохождение артериальной крови через артерио-венозные свищи может привести к увеличению давления крови в венах. Высокая функциональная нагрузка приводит к изменению гистологического строения венозной стенки.
В результате увеличивается ее миотическая фасция и формируется эндогенная эластичная мембрана. Наличие фистул приводит к попаданию артериальной крови в венозный канал, вызывая кислородное голодание и нарушение обменных процессов.
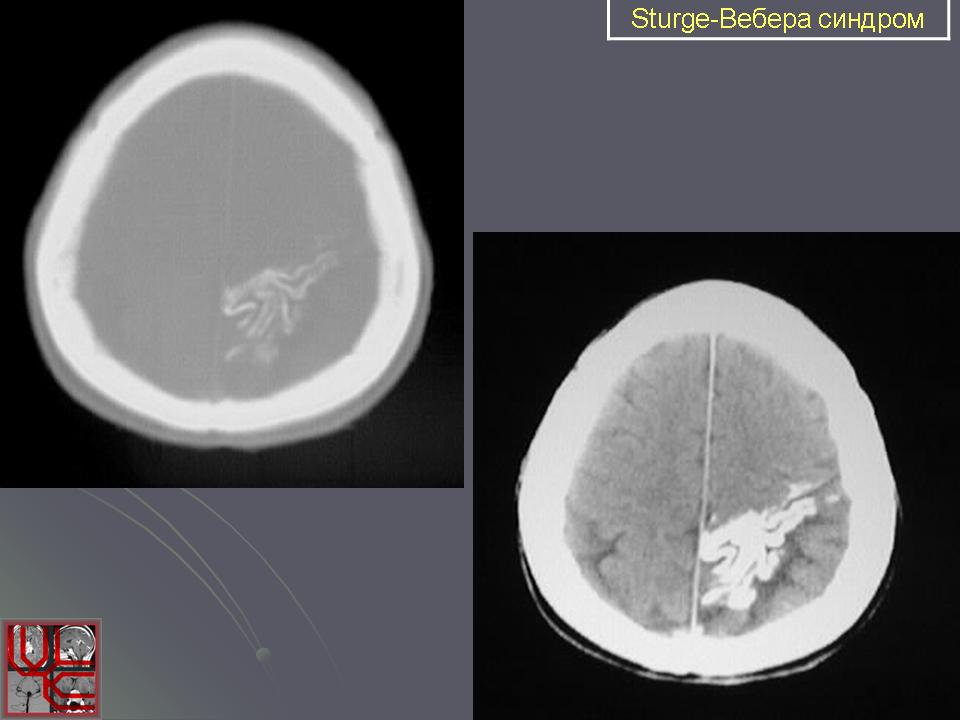
Причины и механизмы заболевания
Чаще всего болезнь возникает на фоне патологических изменений, которые происходят в области расположения ножек мозга. Данные изменения могут быть вызваны расстройством мозгового кровообращения, формированием опухолей и нарушением целостности мозговых сосудов.
Возникновение патологий также может быть связано с давлением опухолевых образований на ножки мозга. При этом опухоль может быть расположена на определенном расстоянии от области нахождения ножек.
Механизм зарождения синдрома Паркса Вебера заключается в следующих факторах:
- субарахноидальное кровоизлияние в среднюю черепную ямку;
- разлаженность кровообращения внутри главного артериального сосуда;
- развитие воспалительных процессов в мозговых оболочках в зоне основания мозга;
- прохождение паталогических процессов в области височной доли головного мозга.
Существует несколько факторов риска, при которых может возникнуть ангиодисплазия:
- наличие черепно-мозговых травм;
- геморрагический или ишемический инсульт;
- новообразования в головном мозге доброкачественного и злокачественного характера.
Клиническая картина
Первые признаки синдрома проявляются в виде капилярной эктазии и систоло-диастолического шума. При этом происходит гипертрофия или вытягивание конечностей, повышается кожная температура и изменяется окрас кожи (появление так называемых винных пятен). Общие перемены в организме проявляются в виде разрушения магистрального кровообращения.
При этом происходит гипертрофия или вытягивание конечностей, повышается кожная температура и изменяется окрас кожи (появление так называемых винных пятен). Общие перемены в организме проявляются в виде разрушения магистрального кровообращения.
Проявление всех вышеуказанных симптомов зависит от величины и числа артериовенозных соустий и области их расположения. От этих же факторов зависит и время течения болезни (быстрое или медленное развитие). На начальной стадии заболевания увеличение вен незначительно.
При пальпации извитые вены с легкостью сжимаются, но после прекращения давления они появляются обратно. В некоторых случаях наблюдается пульсирование вен.
В дальнейшем пораженные конечности увеличиваются в длине и объеме. Отмечается удлинение конечностей на восемь-десять сантиметров.
Причина гипертрофии заключается в обостренной васкуляризации зон роста кости и в нарастании давления крови около эпифизарного хряща. Самым ранним и неизменным признаком синдрома Паркса Вебера является увеличение температуры кожи над местом размещения фистул.
Данный симптом возникает из-за поступления артериальной крови в венозную систему и торможения венозного оттока. Разница кожной температуры между больной и здоровой конечностью составляет пять-восемь градусов.
Диагностические критерии
На фото «винные пятна» — характерный симптом капиллярной ангиодисплазии
На сегодняшний день, не разработано специфических методов диагностики, которые стопроцентно могли бы определить наличие ангиодисплазии Вебера.
Поэтому диагностика данной болезни имеет определенные трудности.
Для постановки диагноза используется полный исследовательский комплекс с использованием лабораторных и инструментальных методов диагностики.
Лабораторная диагностика заключается в применении методов обследования функций мозга. При наличии болезни не отмечается никаких изменений в составе крови и мочи, поэтому сдача подобных анализов не поможет выявить заболевание.
В некоторых случаях назначается взятие спинномозговой пункции. Параллельно с пункцией определяется давление ликвора. Что касается используемых инструментальных методов, то они включают в себя следующие методы исследования:
Что касается используемых инструментальных методов, то они включают в себя следующие методы исследования:
- Исследование сосудистой сети глазного дна — выявление отечности, сосудистого спазма, кровоизлияния и наполненности сосудов.
- Проведение компьютерной томографии. Заключается в резонансном излучении или поглощении электромагнитным средством.
- Нейросонография. Проведение УЗИ структурных элементов головного мозга (желудочки и др.).
В сложных ситуациях диагноз устанавливается путем определения насыщенности венозной крови кислородом. Также проводится наблюдение за изменением венозного давления в пораженных конечностях.
Что предлагает современная медицина?
Очень часто при синдроме Паркса-Вебера назначается консервативный метод лечения, который заключается в использовании компрессионного трикотажа третьего класса. Рекомендации на использование белья даются исходя из проявляемых симптомов заболевания.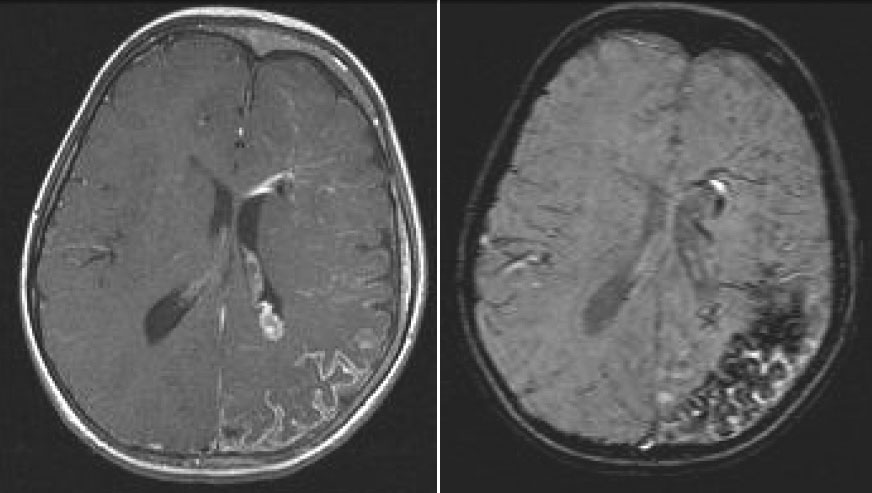
Применяется лазерное удаление так называемых «винных пятен». При тяжелых случаях проводится хирургическое вмешательство, заключающееся в иссечении или перевязке анастомозирующих ветвей и расширенных сосудов.
Больным, у которых изменения в конечностях достаточно велики, и их функции полностью утрачены, проводится их ампутация.
Прогноз на данное заболевание неблагоприятен. Это связано с поэтапным развитием сердечной дефицитности. Из осложнений существует вероятность развития трофических нарушений в тканях конечностей. При данном синдроме имеется предрасположенность к формированию тромбов в сосудистой стенке. При полученных травмах возможно внутреннее кровотечение.
Смотрите видео: Елена Малышева. Тромбоз вен нижних конечностей
Microsoft Word Тесты 4 курс лф doc
Министерство здравоохранения Республики Беларусь
УЧРЕЖДЕНИЕ ОБРАЗОВАНИЯ
«ГРОДНЕНСКИЙ ГОСУДАРСТВЕННЫЙ
МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
Кафедра хирургических болезней №1
Н.И.Батвинков
М.А.Можейко
Н.Д.Маслакова
В.П. Василевский
ХИРУРГИЯ
Тесты для студентов 4 курса
лечебного факультета
Издание 3-е, переработанное
Гродно
ГрГМУ
2012
2
УДК 617(076.3)=111
ББК 54.5я73
В19
Рекомендовано Центральным научно-методическим советом УО «ГрГМУ»
(протокол №___ от ________ 2012 г.).
Авторы: зав.каф., профессор каф. хирургических болезней №1 Н.И. Батвинков, доц. каф.
хирургических болезней №1 М.А. Можейко, доц. каф. хирургических болезней
№1 Н.Д.Маслакова; ассистент каф. хирургических болезней №1 В.П.
Василевский
Рецензент: декан лечебного факультета, проф. кафедры общей хирургии Г.Г. Мармыш.
Батвинков Н.И.
В19
Хирургия: тесты для студентов 4 курса лечебного факультета /
Н.И.Батвинков, М.А.Можейко, Н.Д.Маслакова, В.П. Василевский. Изд. 3-е,
переработанное. — Гродно: ГрГМУ, 2012. — 232.
ISBN 978-985-496-717-2
Tесты по хирургии для студентов 4 курса лечебногофакультета составлены с уче-
том положений и требований вновь утвержденных и введенных в действие типовой и
рабочей программ по дисциплине и в соответствии с последними достижениями научно-
практической деятельности. Позволяют осуществить самоконтроль при подготовке тео-
ретического материала и способствуют овладению врачебными навыками обучаемыми,
делают возможным достижение максимальной эффективности при оценке знаний сту-
дентов преподавателем, а также предназначены для аттестации на переводных курсовых
экзаменах по хирургическим болезням.
© Батвинков Н.И., Можейко М.А., Василевский В.П., Н.Д.Маслакова, 2012
© УО «ГрГМУ», 2012
Хроническая венозная недостаточность (ХВН). Информация для пациентов.
Хроническая венозная недостаточность патологическое состояние, обусловленное нарушением венозного оттока, проявляющееся характерными симптомами (отек, кожные изменения и трофические язвы).
Распространенность хронической венозной недостаточности
По данным различных эпидемиологических исследований та или иная форма ХВН выявляется у женщин от 1% до 40% и у мужчин от 1% до 17% общей популяции. Частота встречаемости кожных изменений при ХВН в развитых странах варьирует от 3% до 13%, а активных и заживших венозных трофических язв от 1% до 2,7%. Пик заболеваемости у женщин приходится в возрасте 40-49 лет и мужчин в возрасте 70-79 лет.
Причины и патофизиология ХВН
В организме человека вены являются частью системы кровообращения — они обеспечивают возврат крови к сердцу. Особое строение венозной стенки, наличие клапанного аппарата, работа мышц ног, диафрагмы, сердца определяет сложный и умный механизм венозного возврата. Всему организму приходится совершать работу по подъему крови против силы гравитации до уровня сердца.
Ключевое звено хронической венозной недостаточности – нарушение венозного оттока и повышение внутривенозного давления в системах поверхностных и глубоких вен. Среди основных причин ХВН выделяют:
Варикозная болезнь
– врожденная слабость венозной стенки и нарушение работы венозных клапанов приводят к расширению поверхностных вен и хроническому повышению внутривенозного давления. Травмы или поверхностный тромбофлебит могут также привести к недостаточности клапанов вен.
Посттромботическая болезнь (посттромбофлебетическая болезнь, ПТФС, ПТФБ) – нарушение основного оттока венозной крови вследствие тромбоза глубоких вен. При этом происходит уменьшение просвета сосуда (в крайнем случае полное закрытие венозной магистрали) и/или разрушение клапанов глубоких вен.
Врожденные нарушения венозной системы такие, как синдром Клиппеля-Треноне и синдром Паркса-Вебера-Рубашова.
Проявления ХВН
Эдема (отек) – это скопление жидкости в мягких тканях из-за нарушения венозного оттока. Выраженность отека может значительно варьировать. Характерным симптомом эдемы является оставшаяся вмятина на коже после надавливания пальцем.
Фото 1. Отек левой голени на фоне посттромботической болезни левой нижней конечности.
Гиперпигментация – потемнение кожи ног, как правило, коричневого оттенка вследствие хронического повышенного давления внутри вен. Характерная локализация — нижняя треть голени, но возможно распространение на другие сегменты голени и на стопу.
Фото 2. Гиперпигментация по внутренней поверхности нижней трети левой голени.
Венозная экзема (застойный дерматит) — покраснение и шелушение кожи нижних конечностей. В тяжелой форме кожа голени иссушается, ощущается интенсивный зуд, а расчесы способствуют присоединению вторичной инфекции.
Фото 3. Хроническая венозная недостаточность вследствие длительно существующей варикозной болезни. В нижней трети левой голени участки покраснения и шелушения кожи с размытыми границами.
Липодерматосклероз – фиброзное перерождение кожи и подкожной жировой клетчатки. Ткани теряют свою эластичность и подвижность. Крайняя форма липодерматосклероза – белая атрофия кожи, которая расценивается как предъязвенное состояние.
Фото 4. Белая атрофия кожи. На фоне гиперпигментации участки кожи белого цвета округлой формы.
Венозная трофическая язва — дефект кожи и подлежащих тканей, возникающий вследствие нарушения венозного оттока. Чаще всего проявляется по внутренней поверхности нижней трети голени. Фото 5.
Фото 5. Венозная трофическая язва у внутренней лодыжки правой голени.
Инфекционные осложнения: на фоне хронической венозной недостаточности кожа теряет барьерную функцию, что влечет за собой повышенный риск наслоения инфекционных заболеваний кожи вплоть до тяжелых микст дерматитов.
Фото 6. Хроническая язвенная пиодермия на фоне хронической венозной недостаточности.
Прогноз при ХВН
ХВН может стать причиной инвалидности. Без коррекции основных причин, венозная недостаточность неумолимо прогрессирует. При этом субъективные симптомы обычно ухудшаются с течением времени. Незаживающая и постоянно рецидивирующая трофическая венозная язва – одно из самых негативных состояний, с которым сталкиваются многие больные. Риск такого состояния увеличивается при наличии тяжелых форм липодерматосклероза и после 2 лет с момента первого эпизода образования язвы. Гиперпигментация и липодерматосклероз – необратимые состояния. Однако обоснованные комплексные лечебные мероприятия способны значительно замедлить изменения мягких тканей.
Диагностика хронической венозной недостаточности
Успешность будущего лечения зависит от правильного и точного диагноза. Множество проявлений ХВН, наличие нескольких возможных причин развития заболевания диктует необходимость дополнять врачебный осмотр, что называется, вооруженным глазом. Основной метод диагностики заболеваний вен — ультразвуковое дуплексное сканирование (УЗДС), которое позволяет определить локализацию поражённых вен и характер нарушения венозного кровотока. Однако это субъективный метод, и в современной флебологии стало правилом — умение лечащего врача самому выполнять УЗДС. Дополнительные методы исследования применяются редко, но в некоторых случаях могут существенно повлиять на тактику лечения. К ним относятся рентгенконтрастная флебография, компьютерная томография (КТ), магнитно-резонансная томография (МРТ).
Хирургическое лечение ХВН
Оперативное лечение направлено на устранение основного звена заболевания – нарушение венозного оттока соответственно причине приведшей к ХВН.
Хирургическое лечение варикозного расширения поверхностных вен:
- Классические открытые оперативные вмешательства на поверхностных венах выполняются из нескольких разрезов и подразумевают удаление пораженных вен.
- Методы внутрисосудистой термооблитерации: эндовенозная лазерная облитерация (ЭВЛО) и радиочастотная облитерация (РЧО) выполняются пункционно (без разрезов), позволяют закрыть просвет больной вены вместо ее удаления под интраоперационным ультразвуковым контролем.
- Устаревшая операция при варикозном расширении поверхностных вен — перевязка подкожной вены без ее удаления.
Хирургия перфорантных вен:
- Метод выбора — ЭВЛО перфорантных вен в зоне трофических расстройств кожи.
- Альтернатива – минифлебэктомия с разобщением перфорантной вены.
- Устаревшие операции на перфорантных венах: операция Линтона, Фельдера — выполняющиеся из больших травматичных доступов, сопровождаются плохим заживлением послеоперационной раны, частыми гнойными осложнениями и краевым некрозом кожи. Операция по Коккету — выполняется из доступа 1-2 см. Данное вмешательство имеет ограничения в зоне трофических расстройств кожи. Эндоскопическая субфасциальная диссекция перфорантных вен (SEPS) – получившая широкое распространение во флебологии до появления ЭВЛО, обладает меньшей травматичностью в сравнении с открытыми операциями.
Реконструктивные операции при посттромботической болезни:
- Стентирование глубоких вен. В структуре трофических язв от 1% до 6% больных имеют сужение подвздошных вен. Данная операция доказала свою эффективность, выполняется в специализированных сосудистых стационарах, требует соответствующего медицинского оснащения и квалифицированного мед персонала.
- Реконструктивные операции клапанов глубоких вен находятся в стадии накоплении материала, имеют узкие показания и в широкой практике не применяются.
Пластические операции при трофических язвах подразумевают различные способы пересадки кожного лоскута для закрытия кожных дефектов.
Флебосклерозирующее лечение
Закрытие просвета пораженных вен с помощью химических агентов, является эффективным способом лечения варикозно расширенных поверхностных вен небольшого диаметра. Для этих целей используются жидкие и пенные формы препарата. Абсолютные противопоказания: известная аллергия на препарат, тромбоз глубоких вен, беременность, грудное вскармливание.
Компрессионная терапия
Компрессионная терапия — одно из неотъемлемых условий лечения ХВН. Методы постоянной компрессии включают в себя ношение подобранных по размеру компрессионных гольф, чулок, колготок. В России общепринят наиболее распространенный в странах Европы германский стандарт компрессионных медицинских изделий — RAL-387. При выраженных дерматитах и наличии венозных трофических язв используется так называемый двойной гольф, который уменьшает трение трикотажа и кожи. В случае нестандартных размеров, рекомендован индивидуальный пошив трикотажа, так как форма конечности при ХВН может значительно изменяться. Так же применяется однослойное или многослойное бинтованные эластичными бинтами различной растяжимости. Метод перемежающейся компрессии подразумевает аппаратную пневмокомпрессию манжетами, наложенными на различные уровни конечности, что ускоряет регресс отека мягких тканей. Лечебная физкультура является важным дополнением комплексного лечения ХВН – это комплекс упражнений, направленных на улучшение работы мышечно-венозной помпы ног.
Медикаментозная терапия
При ХВН обосновано применение венотоников, способных уменьшать хронический венозный и лимфатический отек, чувство тяжести в ногах, боль, повышенную усталость, и т.д.. Для препарата Детралекс, содержащего микронизированную флавоноидную фракцию, доказано ускорение заживления венозных трофических язв. Рекомендованная длительность приема препаратов — не менее 3 месяцев. Не рекомендовано одновременное употребление нескольких венотоников, а так же продолжение терапии при отсутствии эффекта от проводимого лечения в течение 2 месяцев. Дополнительная фармакотерапия назначается ситуационно при осложненном течении ХВН, наиболее часто применяются: антибактериальные, нестероидные противовоспалительные средства, препараты местного действия. В некоторых случаях, учитывая многообразие кожных изменений при ХВН, необходимо привлечение дерматолога.
Рекомендации пациенту не зависимо от причины и формы ХВН
- Вести активный образ жизни
- Избегать длительного стояния или сидения
- Регулярно выполнять физические упражнения, предписанные врачом.
- Постоянное дневное ношение компрессионного трикотажа, если нет противопоказаний.
Ответы на часто задаваемые вопросы по ХВН более подробно будут изложены в соответствующих разделах. Если Вам нужна дополнительная информация, Вы можете обратиться с вопросом на форум.
Синдром Паркса-Вебера | Бостонская детская больница
Что такое синдром Паркса Вебера (СПВ)?
PWS — это исключительно редкая врожденная (присутствующая при рождении) сосудистая аномалия, которая приводит к появлению у ребенка большого количества аномальных кровеносных сосудов. Он похож на более распространенный синдром Клиппеля-Треноне (KTS) и лечится примерно так же.
В отличие от детей с КТС, дети с СПВ имеют артериовенозные мальформации (АВМ) — аномальные связи между артериями и венами в пораженной конечности, которые могут вызвать сердечную недостаточность.
Синдром Паркеса Вебера неизлечим; Самый эффективный способ справиться с этим заболеванием — лечить симптомы, которые оно вызывает.
Ни один специалист не может справиться с СПВ и связанными с ней проблемами, потому что часто требуются различные интервенционные техники и хирургические процедуры. Вот почему первый шаг в управлении СПВ — это обследование вашего ребенка членами опытной междисциплинарной бригады по сосудистым аномалиям.
Каковы симптомы синдрома Паркса Вебера?
Синдром Паркеса Вебера поражает разных детей по-разному.У одного ребенка может быть легкая форма с небольшой капиллярной аномалией и одна рука или ступня немного больше другой. У другого ребенка может быть капиллярная аномалия, которая идет от груди к ноге, сильные отеки, проблемы с сердцем и одна конечность намного больше другой.
Некоторые возможные симптомы СПВ включают:
- плоское, розовое, теплое родимое пятно, называемое винным пятном, вызванное капиллярной аномалией на коже вашего ребенка
- частое или повторяющееся кровотечение из аномальных капилляров у поверхности кожи
- целлюлит (кожные инфекции)
- гипертрофия — опухоль и разрастание — конечности (обычно ноги)
- Боль, часто сильная, в пораженной конечности
- Проблемы с сердцем из-за повышенного кровотока из-за артериовенозной мальформации
Что вызывает синдром Паркса Вебера?
У многих пациентов СПВ вызывается мутацией в гене RASA1 .Эта мутация может передаваться по наследству. Пациент с СПВ может передать эту мутацию своим детям. Однако не каждый пациент с СПВ имеет мутацию RASA1 .
Никакие известные продукты питания, лекарства или действия во время беременности не могут вызвать СПВ.
Как мы лечим синдром Паркеса Вебера
Поскольку СПВ встречается очень редко, очень немногие врачи имеют опыт диагностики и лечения. Центр сосудистых аномалий Бостонской детской больницы обследовал больше детей с СПВ, чем любая другая больница в мире.Более 25 врачей VAC, представляющих более 16 медицинских и хирургических специальностей, используют этот опыт для постоянного совершенствования методов лечения и достижения лучших долгосрочных результатов для детей с СПВ.
Синдром Паркеса Вебера — Диагностика и парадигмы управления: систематический обзор
Цели Синдром Паркса-Вебера — врожденная сосудистая аномалия, которая состоит из капиллярной мальформации, венозной мальформации, лимфатической мальформации и артериовенозной мальформации.Хотя синдром Паркса Вебера является клинически отличительной формой с серьезными осложнениями, его все еще часто ошибочно диагностируют как синдром Клиппеля-Тренауне, который состоит из триады капиллярной мальформации, венозной мальформации и лимфатической мальформации. Методы. Мы провели систематический обзор клинических, диагностических и лечебных методов лечения синдрома Паркса Вебера (базы данных PubMed / MEDLINE, Embase и Cochrane). Критериям отбора соответствовали 36 публикаций (48 пациентов).Результаты. Средний возраст пациентов составлял 23 года (IQR, 8–32), и 24 года (50,0%) были мужчинами. Нижняя конечность была поражена у 42 (87,5%), верхняя конечность — у 6 (12,5%) пациентов; У 15 (31,3%) пациентов развилась сердечная недостаточность с высоким выбросом; У 12 (25,0%) пациентов были хронические венозные язвы, у 4 (8,3%) наблюдалась ишемия дистальной артерии. Артериовенозные мальформации позвоночника были зарегистрированы у шести (12,5%) пациентов, а сосуществование аневризматической болезни — у пяти (10,4%) пациентов. Наиболее часто используемыми инвазивными методами лечения были эмботерапия с последующей ампутацией и хирургической резекцией артериовенозной мальформации, а иногда и имплантацией стент-графта.Все методы показали клиническое улучшение. Однако длительное наблюдение и исход оставались неясными. Заключение. Диагноз синдрома Паркса-Вебера следует ставить на основании наличия капиллярной мальформации, венозной мальформации, лимфатической мальформации и артериовенозной мальформации (как основного дефекта) в разрастающейся конечности. Артериовенозная мальформация представляет собой критерий отличия синдрома Паркса Вебера от синдрома Клиппеля-Тренаунае, что имеет важное значение для стратегии лечения. Первичной целью лечения должно быть улучшение качества жизни пациента и уменьшение осложнений.Сама по себе эмболизация / в сочетании с хирургической резекцией, направленной на окклюзию, или удалением «очага» артериовенозной мальформации надежно приводит к клиническому улучшению.
Ключевые слова: Синдром Клиппеля – Тренауне; Синдром Паркса Вебера; артериовенозная мальформация; врожденная аномалия сосудов.
Синдром Кобба — обзор
Сосудистые мальформации спинного мозга
Сосудистые мальформации спинного мозга можно разделить на три основные категории: (1) генетические наследственные поражения (напр.g., наследственная геморрагическая телеангиэктазия), (2) генетические ненаследственные поражения, связанные с сосуществующими кожными сосудистыми поражениями на одном и том же дерматомном уровне (например, синдром Кобба, синдром Паркеса-Вебера), и (3) единичные сосудистые поражения, которые включают спинной мозг, нерв корень или конечная нить нити (например, артериовенозная мальформация (АВМ), артериовенозная фистула (АВФ)) (Rodesch et al., 2002). На рис. 104.2A и B показаны особенности МРТ метамерной сосудистой мальформации у 10-летнего мальчика, соответствующие синдрому Кобба.Большинство сосудистых поражений спинного мозга возникают как одиночные поражения, которые в дальнейшем подразделяются на дуральные и пиальные артериовенозные (АВ) шунты, в зависимости от сосудов, питающих поражение (Rodesch et al., 2002). Согласно недавно предложенной эмбриологической классификации, сосудистые мальформации также можно разделить на АВФ и АВМ. Экстрадуральные и интрадуральные АВФ, расположенные на вентральной части спинного мозга, различаются как связанные с: (1) незначительным шунтированием крови, (2) умеренным шунтированием и (3) значительным шунтированием.Расположенные дорсально АВФ подразделяются на АВФ с одним сосудистым притоком и АВФ с несколькими притоками (Spetzler et al., 2002).
Рис. 104.2. МРТ сосудистых миелопатий у детей. ( A и B ) Сагиттальная Т2-взвешенная МРТ позвоночника с быстрым спин-эхом (FSE) у 10-летнего мальчика с острой болью в спине и парапарезом. Крупные корешковые артерии и дренирующие вены видны от Т6 до Т9. В позвонках от T9 до T11, в позвоночном канале от T7 до T12, а также в мышцах, выпрямляющих позвоночник, и мягких тканях дорсальнее спинного мозга в точках T7 – L2 имеется аномальная сигнальная пустота.Также очевидна интрамедуллярная гиперинтенсивность от Т5 до Т9. ( C и D ) Сагиттальная Т2-взвешенная МРТ позвоночника 10-летнего мальчика. Вокруг шейного канатика от большого затылочного отверстия, каудально до уровня C6, визуализируются множественные образования с небольшими проточными пустотами. Поражение АВМ очевидно на дорсальной стороне спинного мозга на уровне C3 – C4. Нет аномального интрамедуллярного сигнала.
Изображения любезно предоставлены доктором М. Шрофф, Отделение нейрорадиологии, Больница для больных детей, Торонто, Онтарио, Канада.У детей АВМ в отличие от АВФ наблюдаются чаще и, вероятно, обнаруживаются на дорсальной стороне спинного мозга (Tacconi and Findlay, 2000; Du et al., 2009). Это подтверждает мнение о том, что АВФ твердой мозговой оболочки могут быть приобретенными, а не врожденными (Du et al., 2009). В сообщении о 1168 случаях поражения сосудов позвоночника 6,1% составляли дети. Около 44% детей имели АВМ спинного мозга и 24% имели перимедуллярные АВФ, в то время как у остальных 28% были синдром Кобба, кавернозная ангиома спинного мозга, позвоночная ангиома, эпидуральная АВМ и аневризма спинного мозга (Du et al., 2009). Как и взрослые, мужчины могут быть поражены чаще, чем женщины в соотношении 2: 1 (Du et al., 2009; Krings and Geibprasert, 2009). Одно исследование показало, что грудопоясничная область имеет повышенную склонность к сосудистым мальформациям (Du et al., 2009), особенно сегменты между T6 и L2, хотя АВМ могут присутствовать на любом уровне спинного мозга (Krings and Geibprasert, 2009), поскольку наш случай демонстрирует (рис. 104.2C и D).
За исключением АВФ твердой мозговой оболочки спинного мозга, большинство сосудистых мальформаций имеют врожденное происхождение и образуются на третьей эмбриональной неделе (Du et al., 2009). Возраст клинических проявлений дефицита спинного мозга имеет бимодальный характер. Пиковый возраст приходится на раннее детство до 2 лет (Du et al., 2009) или после 10 лет (Kitagawa et al., 2009). Повышенные потребности в кровоснабжении во время фаз быстрого роста в младенческом и подростковом возрасте вместе с повышенным уровнем физической активности, наблюдаемым в подростковом возрасте, могут объяснить бимодальный возраст начала заболевания.
Клинические проявления пороков развития спинного мозга возникают либо в контексте эпизодов субарахноидальной геморрагии, либо, реже, из-за окклюзии сосудов (с проявлениями, аналогичными описанному выше инфаркту спинного мозга).Кровоизлияние как механизм появления симптомов наблюдается примерно у 20% пациентов с сосудистыми мальформациями позвоночника (Berenstein and Lasjaunias, 1992; Swaiman et al., 2006) и может указывать на более перимедуллярный (пиальный) атриовентрикулярный шунт в отличие от атриовентрикулярного шунта. дуральная АВФ (Krings, Geibprasert, 2009). У пациентов с кровоизлиянием, связанным с сосудистой мальформацией, внезапное появление неврологических симптомов связано с сильной болью в спине, вторичной по отношению к гематомиелии, двусторонней слабостью нижних конечностей и сенсорным дефицитом (парестезии, диффузная или неоднородная сенсорная потеря и корешковая боль, которая может влиять на одно или оба. конечности).У пациентов с медленно расширяющимися сосудистыми мальформациями неврологический дефицит постепенно прогрессирует. Недержание мочевого пузыря и кишечника, задержка мочи и эректильная дисфункция чаще наблюдаются у пациентов с длительными сосудистыми мальформациями позвоночника (Krings and Geibprasert, 2009). У пациентов с более коварным клиническим течением прогрессирующее поражение сосудов спинного мозга может привести к сколиозу из-за массового воздействия на растущий позвоночник и застойной сердечной недостаточности, вторичной по отношению к повышению спинномозгового венозного давления и феномену обкрадывания сосудов.Кожная ангиома, усугубленная маневром Вальсальвы, встречается у 20% детей с сосудистыми мальформациями позвоночника. Аускультация спинномозгового шума может усилить диагностическую подозрительность, и совершенно необходимо, чтобы люмбальная пункция не проводилась в области уродства. Спинальные сосудистые мальформации следует рассматривать как излечимую причину прогрессирования симптомов спинного мозга (Aghakhani, 2008; Krings and Geibprasert, 2009).
Диагноз часто основывается на МР-ангиографии с подтверждением цифровой субтракционной ангиографией (DSA) (Krings and Geibprasert, 2009).Отличительные признаки МРТ включают центромедуллярный отек (Т2-взвешенная гиперинтенсивность в нескольких позвоночных сегментах позвоночника) и перимедуллярно расширенные сосуды (край Т2-взвешенной гипоинтенсивности) (Krings and Geibprasert, 2009). В отсутствие этих данных спиральные сосуды, указывающие на сосудистую мальформацию, могут быть очевидны на постконтрастной Т1-взвешенной визуализации, но будут лучше оценены при трехмерной турбо-спин-эхо-визуализации (Krings et al., 2007). На рис. 104.2C и D показаны особенности МРТ АВМ спинного мозга у 10-летнего мальчика.Т2-взвешенные признаки наличия пустот для потока часто более выражены на дорсальной поверхности, чем на вентральной. Однако, если поражение представляет собой медленно протекающий шунт, пустоты потока можно оценить только на постконтрастной Т1-взвешенной визуализации (Krings and Geibprasert, 2009). Диффузное усиление наблюдается на постконтрастных T1-взвешенных последовательностях, что указывает на хронический венозный застой и проницаемость гематоэнцефалического барьера (Chen et al., 1998). МР-ангиография с контрастным усилением в значительной степени помогла локализовать атриовентрикулярные поражения и направить интервенционное радиологическое лечение (Krings and Geibprasert, 2009).
Терапевтическое лечение направлено на оказание неотложной помощи и профилактическое лечение во избежание дальнейшего повреждения спинного мозга, вызванного рецидивирующим кровотечением или сдавлением спинного мозга. Неотложная помощь сосредоточена вокруг достижения полной окклюзии места шунтирования (Jellema et al., 2005). Оптимальной терапией является полная окклюзия самой дистальной части артерии и проксимальной части дренирующей вены в месте шунтирования (Jellema et al., 2005; Fernández et al., 2008). При только проксимальной окклюзии дистальной артерии у порока есть высокая вероятность рецидива в течение нескольких месяцев, что приводит к заполнению коллатерального сосудистого поражения (Krings and Geibprasert, 2009).
Двумя основными методами лечения являются хирургическая окклюзия вены, в которую кровь поступала из надира зоны шунтирования (Huffmann et al., 1995), или эндоваскулярная окклюзия жидким эмболическим агентом после суперселективной катетеризации артерии, питающей кровь. зона шунтирования (Krings et al., 2005). Одно недавнее исследование детей, получавших лечение по поводу АВ-шунтирования спинного мозга, показало улучшение на 40%, у 52% не было клинических изменений, а у 8% наблюдался дальнейший неврологический дефицит после лечения эмболизацией (Du et al., 2009). Риск кровотечения или повторного кровотечения низок из-за улучшения постэмболизации венозного оттока (Rodesch et al., 2005). Однако пациенты, которым потребовалось вторичное хирургическое вмешательство из-за неполной эндоваскулярной эмболизации, имели плохой клинический результат (Andres et al., 2008). Успешная эмболизация может снизить риск дальнейшего кровотечения, но не может обратить вспять ишемическое повреждение, уже нанесенное во время острого события. Степень клинического дефицита зависит от уровня преэмболизационной инвалидности и продолжительности симптомов (Krings and Geibprasert, 2009).
