Что такое дисплазия шейки матки?
Дисплазия шейки матки(cin) — это предраковое изменение эпителия шейки. 😰 Это еще доброкачественное состояние, но в отсутствии лечения это состояние может озлокачествиться и перейти в рак🧨.
В зависимости от выраженности процесса разделяют три стадии дисплазии:
1️⃣легкая дисплазия(cin I/ lsil), 2️⃣умеренно выраженная дисплазия(сin II/hsil) и
3️⃣тяжелая (cin III/hsil) — фактически рак.
В первую очередь такие изменения вызывает ВПЧ, 🦠 а точнее его высокоонкогенные типы.
Самое опасное в дисплазиях шейки матки, это то, что состояние протекает практически бессимптомно🤭, а значит установить диагноз без врача акушера-гинеколога и врача цитолога 🔬невозможно.
Как устанавливается диагноз?🤔
Для этого необходимы регулярные осмотры у врача, на которых берётся мазок на онкоцитологию и мазок на ВПЧ. А для наиболее полноценного обследования необходимо провести кольпоскопию🔎, где врач визуально может оценить шейку матки и наличие изменений на ней.
Диагноз «дисплазия шейки матки» можно установить, только при комплексном обследовании☝️☝️
Что же в него входит?
1️⃣Первое, что вы должны сделать — это посетить🏃♀️ гинеколога, для рутинного осмотра шейки матки в зеркалах.
2️⃣Следующий этап — это мазок на онкоцитологию, который возьмет вам врач. ❗️По последним рекомендациям мазок берется один раз в три года с 21 до 29 лет(или после 3 лет от начала половой жизни), с 30 до 65 — один раз в 5 лет.
3️⃣ВПЧ-скрининг🦠 1 раз в 5 лет, для женщин старше 30 лет, при условии, что вирус папилломы человека не был выявлен ранее, а если в предыдущих анализах уже был обнаружен ВПЧ онкогенного типа — контроль один раз в год.
Важно знать, что если вам когда-то уже ставили диагноз дисплазия шейки матки, и он был подтвержден гистологически‼️, то вам необходимо ежегодно сдавать мазки как на онкоцитологию❗️, так и на впч❗️, а также контроль кольпоскопии в течении 20 лет‼️ от постановки диагноза вне зависимости от возраста.
4️⃣Следующий немаловажный этап — расширенная кольпоскопия🔎, где шейка матки будет обработана специальными растворами (читай наш пост про кольпоскопию⬇️⬇️), для выявления патологических участков на ней.
Если изменения выявлены кольпоскопически, то проводится биопсия шейки матки для гистологического анализа патологического участка📍.
5️⃣Также если ВПЧ онкогенного типа уже выявлен, а на шейки фиксируются незначительные изменения, то вы можете сдать иммуноцитохимическое/иммуногистохимическое исследование p16 и Ki67, для определения риска развития рака шейки матки(данные анализы не входят в полис ОМС😞).
Дисплазия шейки матки: лечение и диагностика
Дисплазия шейки матки: лечение и диагностика
13.03.2020Обычно дисплазия эпителия шейки матки протекает бессимптомно и не влияет на качество половой жизни, не мешает забеременеть. Заболевание это чаще всего обнаруживается при регулярном осмотре у гинеколога, который каждая здоровая женщина должна проходить ежегодно.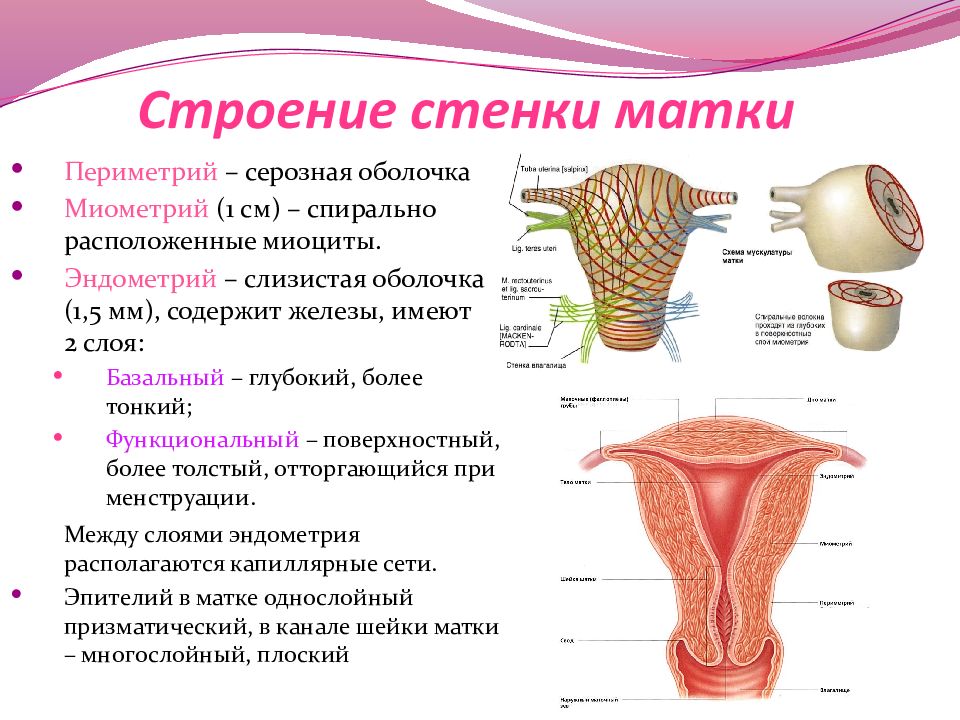
Однако “бессимптомность” здесь не значит “безопасность”, поскольку запущенная дисплазия может перейти в предраковое состояние, а после — и переродиться в рак.
Что такое дисплазия шейки матки?
Дисплазия матки — это нарушения в структуре и строении базальных клеток плоскоклеточного эпителия, выстилающего шейку. Она возникает у рожавших и нерожавших вне зависимости от возраста. Факторами риска могут стать курение, частая смена партнеров, аборты, вагинальный дисбиоз, авитаминоз и гормональные сбои, но чаще всего причина заключается в заражении вирусом папилломы человека или ВПЧ.
В зависимости от тяжести заболевания различают три типа дисплазии:
- Первая или легкая степень, которая обозначается как CIN I (L-SIL). В этом случае во время кольпоскопии диагностируется дисплазия, но изменения в строении плоскоклеточного эпителия не выявляются, перерожденных клеток нет.
- Вторая или умеренная степень, то есть CIN II (H-SIL). В этом случае обнаруживается поражение половины эпителиального слоя.

- Третья или тяжелая степень (она же CIN III (H-SIL), при которой ⅔ эпителия поражены, а в структуре клеток появляются крупные ядра.
Чем больше клеток плоского эпителия видоизменяются, тем выше риск перерождения дисплазии в злокачественное образование.
Как диагностируют дисплазию?
Симптомы дисплазии шейки матки обычно проявляются на последних, “предраковых” стадиях. Это кровотечения или появление кровяных сгустков в выделениях, задержка месячных без объективных причин или тянущие боли внизу живота. На ранних стадиях ничего этого может и не быть. Визуально дисплазия похожа на эрозию, шейка матки при этом становится рыхлой, на ней могут появляться кровоточащие “царапины”. Заметить это самостоятельно не представляется возможным. Поэтому регулярный осмотр у гинеколога игнорировать не стоит.
Поскольку дисплазия шейки матки — это заболевание, которое проходит практически без симптомов, существуют способы, помогающие ее диагностировать визуально, непосредственно при осмотре. Чаще всего используют кольпоскопию. Ее проводят специальным инструментом, кольпоскопом с бинокулярной оптической системой, позволяющей увеличивать участки тканей в 10-30 раз.
Чаще всего используют кольпоскопию. Ее проводят специальным инструментом, кольпоскопом с бинокулярной оптической системой, позволяющей увеличивать участки тканей в 10-30 раз.
Как лечат дисплазию?
Все признаки дисплазии шейки матки видны гинекологу при осмотре. При подозрении на это заболевание он назначит необходимые лабораторные и инструментальные исследования. В частности, назначают анализы на ВПЧ 16 и 18 типа, а также мазок на цитологию или ПАП-тест, позволяющий определить степень перерождения клеток. После этого назначают лечение. Традиционно предлагают такие варианты удаления пораженных участков:
- лазерная вапоризация, когда пораженный очаг как бы “испаряется”;
- криодеструкция, когда пораженные участки разрушаются под действием экстремально низких температур;
- эксцизия, удаление электропетлей;
- иссечение или ампутация шейки матки, конизация.
Параллельно обязательно проводится терапия сопутствующих заболеваний, в том числе влагалищных инфекций и нарушений гормонального статуса.
Консультация врача гинеколога в волгограде
Большинство женщин мало знают о раке шейки матки (РШМ) и предраковых заболеваниях.
РШМ — единственная форма генитального рака с достоверно доказанной вирусной этиологией. Вирус папилломы человека (ВПЧ) выявляется в 99.7% случаев РШМ. Основной путь заражения — половой. РШМ занимает 1 место среди раков у женщин в возрасте 30-40 лет.
Что же относится к предраковым заболеваниям шейки матки?
К предраковым заболеваниям шейки матки относится дисплазия. Её нельзя путать с эрозией шейки матки, которая возникает при механической травматизации эпителия шейки матки, лечится консервативно и не представляет никакой опасности.
По классификации выделяют три степени дисплазий:
Чаще всего развитие дисплазии шейки матки вызывают высокоонкогенные типы вируса папилломы человека (ВПЧ-16 и ВПЧ-18).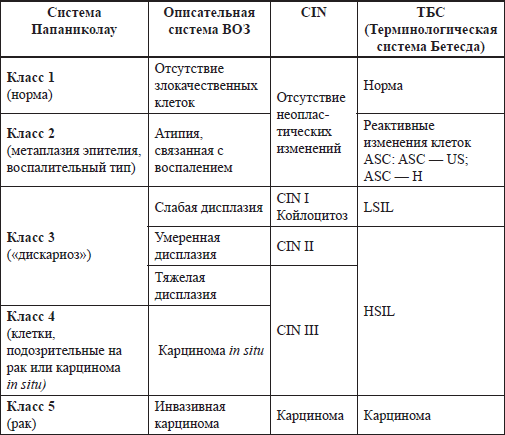 Этому способствует ряд отягощающих факторов:
Этому способствует ряд отягощающих факторов:
-
Иммунодефицит, вызванный хроническими заболеваниями, стрессами, неправильным питанием и т.д.;
-
Курение — повышает риск развития дисплазии в 4 раза;
-
Хронические воспалительные заболевания самой шейки матки — цервицит;
-
Ранее начало половой жизни и частая смена половых партнеров.
С момента инфицирования до развития РШМ проходит от нескольких лет до десятилетий.
-
1 фаза — латентное инфицирование. ВПЧ обнаруживается при молекулярных методах исследования, но морфологические изменения отсутствуют. У большинства женщин (<90%) вирус элиминируется самостоятельно (наступает самоизлечение).
-
2 фаза — субклиническая форма, развивается приблизительно у 10% инфицированииых, характеризуется появлением койлоцитов.
-
3 фаза — дисплазия 1 степени (CIN I). Появление атипических клеток, занимают 1/3 эпителиального пласта.
-
Дисплазия 2 степени (CIN II) — атипические клетки занимают 2/3 эпителиального пласта.

-
Дисплазия 3 степени и рак in situ (CIN III) — весь эпителиальный пласт занят атипическими клетками.
CIN I, II, III — это предрак и обнаружение его на этих стадиях дает возможность провести своевременное лечение и не допустить развитие РШМ.
Автор статьи: И.А. Цветкова ,
врач акушер-гинеколог,
специалист по патологии
шейки матки
полностью избавляет от ВПЧ у одной трети предраков шейки матки
Исследователи наблюдали за участниками еще в течение двух с половиной лет после операции, что является самым длительным из всех исследований с участием женщин в этих испытаниях. Они показали, что долгосрочное наблюдение было лучше для тех, кто получил вакцину, чем плацебо, при этом большее количество женщин в группе вакцинированных оставались полностью свободными от ВПЧ. Исследование опубликовано в
Харпер отмечает, что терапевтическая вакцина под названием Tipapkinogen Sovacivec, или TS, полностью отличается от Gardasil9, вакцины, вводимой для предотвращения инфекции HPV. В то время как Гардасил9 предотвращает заражение ВПЧ, TS очищает ткани, уже инфицированные ВПЧ. CIN2 и CIN3 всегда вызваны инфекциями ВПЧ высокого риска.
В то время как Гардасил9 предотвращает заражение ВПЧ, TS очищает ткани, уже инфицированные ВПЧ. CIN2 и CIN3 всегда вызваны инфекциями ВПЧ высокого риска.
БОЛЬШЕ ОТ MICHIGAN: Подпишитесь на нашу еженедельную рассылку
Типичная процедура лечения CIN2 или CIN3 включает удаление конусообразной части шейки матки, называемой LEEP или конусом. Это приводит к образованию рубцов и укорочению шейки матки, что может вызвать проблемы во время родов и повысить риск кесарева сечения.Кроме того, женщины, перенесшие эту процедуру, имеют очень высокий риск развития рака шейки матки в течение следующих 20 лет, если они не будут продолжать проходить обследование.
«Хирургическая процедура удаляет всю ткань, которая ведет к раку, но не удаляет весь ВПЧ. Ты не дома бесплатно. У вас все еще есть ВПЧ », — говорит Харпер, международно признанный исследователь ВПЧ, член онкологического центра Рогеля Мичиганского университета и старший заместитель директора Мичиганского института клинических исследований и медицинских исследований (MICHR).
С помощью вакцины исследователи обнаружили, что она не только устранила поражения, но и устранила инфекцию ВПЧ.
«На самом деле он лечит причину заболевания, которым является ВПЧ», — говорит Харпер.
Женщины, которым делали инъекции вакцины, сообщали о иногда тяжелых реакциях в месте инъекции. Харпер говорит, что это было ожидаемо, потому что вакцина предназначена для запуска иммунной системы. Иммунная реакция может вызвать воспаление кожи.
В исследовании рассматривались только поражения шейки матки, но ВПЧ связан с несколькими другими типами рака, включая рак головы и шеи и рак анального канала.Исследователи предполагают провести тестирование TS на эти виды рака в будущем. Прежде чем получить одобрение TS от Управления по контролю за продуктами и лекарствами США, необходимы дополнительные клинические испытания. Пробных версий пока нет.
Кольпоскопия — Результаты — HSE.ie
Ваш врач или медсестра часто могут сказать вам, что они обнаружили, сразу после того, как вам сделают кольпоскопию.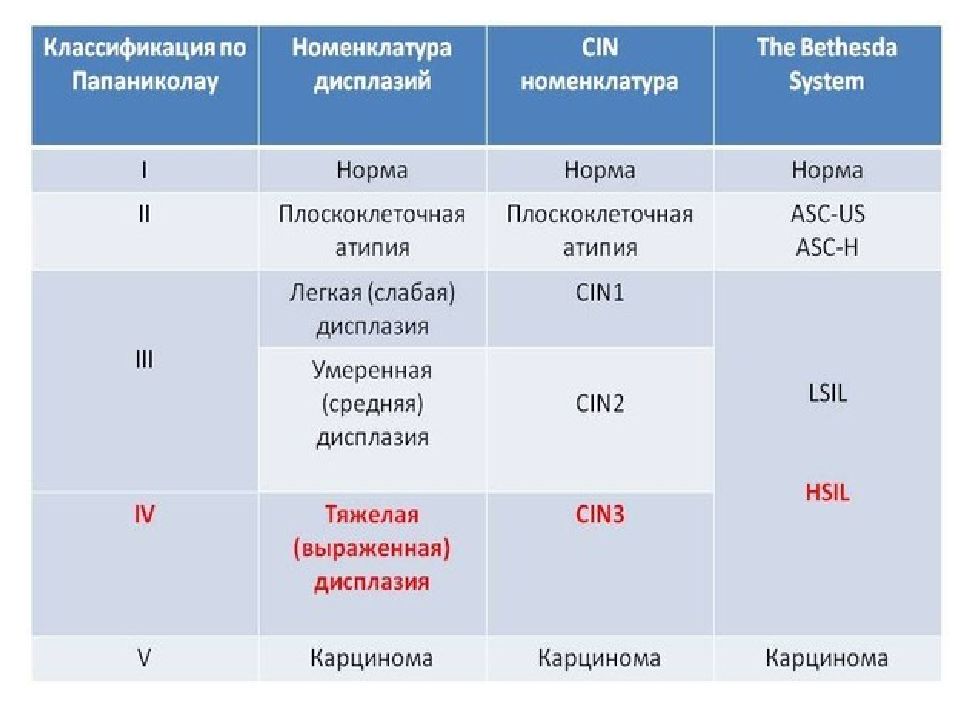
Обычно ваши результаты будут нормальными или ненормальными.
Если очевидно, что у вас аномальные клетки, вам может быть назначено лечение по немедленному удалению клеток.
Если это не очевидно, ваш врач или медсестра возьмут биопсию. Эта биопсия представляет собой небольшой образец ткани шейки матки. Он будет исследован в лаборатории.
Нормальный результат
Это означает, что аномальных клеток не обнаружено. Вам не нужно немедленное лечение.
Вам будет предложено либо:
- прийти на контрольную кольпоскопию — это на случай, если аномальные клетки разовьются позже
- продолжите скрининг шейки матки как обычно — у вас будет следующий тест через 3 года , независимо от вашего возраста
Аномальный результат
Нередко обнаружение аномальных клеток в шейке матки во время кольпоскопии.Это не рак. Но если не лечить, это может перерасти в рак.
Если кольпоскопия подтвердит наличие аномальных клеток, также будет сделана биопсия.
Здесь можно увидеть:
- , каков риск того, что эти клетки станут злокачественными.
- , если вам нужно лечение
Типы аномальных результатов биопсии
Различные типы аномальных результатов биопсии:
CIN означает шейный внутриэпителиальная неоплазия.
CGIN обозначает внутриэпителиальную неоплазию шейных желез.
CIN 1
Маловероятно, что клетки станут злокачественными. Они могут уйти сами.
Обычно лечение не требуется. Обычно вам нужно пройти еще один скрининговый тест через 12 месяцев, чтобы проверить, исчезли ли аномальные клетки.
CIN 2
Существует умеренная вероятность того, что клетки станут злокачественными. Обычно рекомендуется лечение для их удаления, но не всегда.
CIN 3
Существует высокая вероятность того, что клетки станут злокачественными. Рекомендуется лечение для их удаления.
CGIN
Существует высокая вероятность того, что клетки станут злокачественными. Рекомендуется лечение для их удаления.
Рекомендуется лечение для их удаления.
Подробнее о лечении аномальных клеток шейки матки
В редких случаях кольпоскопия и биопсия обнаруживают рак шейки матки.
Если это произойдет, вас направят к группе специалистов для обсуждения лечения.
Пятилетний риск CIN 3+ и рака шейки матки у женщин с отрицательным Пап-тестом, но с положительным результатом на ВПЧ
Задача:
Текущие американские руководящие принципы по котестированию рекомендуют, чтобы большое количество женщин с отрицательным результатом теста на Пап-тест, но с положительным результатом на вирус папилломы человека (ВПЧ) вернулись через 1 год, а также тем, у кого остается ВПЧ-положительный результат или имеется плоское интраэпителиальное поражение низкой степени злокачественности (LSIL). или того хуже результаты Папаниколау должны быть направлены на кольпоскопию.Однако эффективность этих рекомендаций в повседневной клинической практике не оценивалась.
Методы: Мы оценили кумулятивные 5-летние риски цервикальной интраэпителиальной неоплазии 3 степени и выше (CIN 3+) среди 32 374 женщин в возрасте от 30 до 64 лет с положительными / Пап-отрицательными результатами котест в Kaiser Permanente, Северная Калифорния, в период с 2003 по 2010 год.
Полученные результаты:
Пятилетний риск CIN 3+ после ВПЧ-положительного / Пап-отрицательного результата котеста, который был обнаружен у 3.6% женщин, было 4,5% (95% доверительный интервал [ДИ] = 4,2% -4,8%). Пятилетний риск рака составлял 0,34% (95% ДИ = 0,26–0,45%), и половина случаев приходилась на аденокарциному. В целом, 48% женщин по возвращении остались положительными на ВПЧ (медиана = 418 дней после исходного уровня), процент, который мало варьировал в возрасте от 30 до 64 лет. При возврате после исходного ВПЧ-положительного / Пап-отрицательного результата почти каждый повторный результат котировки предсказывал больший последующий 5-летний риск CIN 3+, чем тот же результат котеста на исходном уровне (HPV-положительный / LSIL, 9.2% против 6,1%, p = 0,01; ВПЧ-положительные / атипичные плоскоклеточные клетки неустановленной значимости [ASC-US], 7,9% против 6,8%, p = 0,2; ВПЧ-положительный / Пап-отрицательный, 7,4% против 4,5%, p <0,0001; ВПЧ-отрицательный / LSIL, 1,7% против 2,0%, p = 0,8; ВПЧ-отрицательный / ASC-US, 2,9% против 0,43%, p = 0,0005; ВПЧ-отрицательный / Пап-отрицательный, 0,93% против 0,08%, p <0,0001).
При возврате после исходного ВПЧ-положительного / Пап-отрицательного результата почти каждый повторный результат котировки предсказывал больший последующий 5-летний риск CIN 3+, чем тот же результат котеста на исходном уровне (HPV-положительный / LSIL, 9.2% против 6,1%, p = 0,01; ВПЧ-положительные / атипичные плоскоклеточные клетки неустановленной значимости [ASC-US], 7,9% против 6,8%, p = 0,2; ВПЧ-положительный / Пап-отрицательный, 7,4% против 4,5%, p <0,0001; ВПЧ-отрицательный / LSIL, 1,7% против 2,0%, p = 0,8; ВПЧ-отрицательный / ASC-US, 2,9% против 0,43%, p = 0,0005; ВПЧ-отрицательный / Пап-отрицательный, 0,93% против 0,08%, p <0,0001).
Выводы:
Используя принцип «равного управления равными рисками», женщины, у которых был обнаружен ВПЧ-положительный / Пап-отрицательный, последующий риск CIN 3+ соответствовал пороговым значениям риска для доходности в течение 1 года. Однако по возвращении примерно через 1 год около половины женщин будут направлены на кольпоскопию из-за сохраняющегося положительного результата на ВПЧ или патологии Папаниколау. Клиницисты должны иметь в виду, что результаты котировок при возврате после исходных положительных / Пап-отрицательных результатов более рискованны, чем такие же исходные результаты котировок в общей популяции, что способствует усиленному клиническому ведению пациентов при повторном обследовании.
Однако по возвращении примерно через 1 год около половины женщин будут направлены на кольпоскопию из-за сохраняющегося положительного результата на ВПЧ или патологии Папаниколау. Клиницисты должны иметь в виду, что результаты котировок при возврате после исходных положительных / Пап-отрицательных результатов более рискованны, чем такие же исходные результаты котировок в общей популяции, что способствует усиленному клиническому ведению пациентов при повторном обследовании.
Если у вас рак шейки матки
ЛЕГКО ЧТЕНИЕ
Что такое рак шейки матки?
Рак может начаться в любом месте тела.Рак шейки матки начинается с шейки матки. Это начинается, когда клетки шейки матки выходят из-под контроля и вытесняют нормальные клетки. Это мешает организму работать должным образом.
Раковые клетки могут распространяться на другие части тела. Раковые клетки шейки матки иногда могут перемещаться в легкие и там расти. Когда раковые клетки делают это, это называется метастаз . Для врачей раковые клетки на новом месте выглядят точно так же, как клетки шейки матки.
Когда раковые клетки делают это, это называется метастаз . Для врачей раковые клетки на новом месте выглядят точно так же, как клетки шейки матки.
Рак всегда назван в честь того места, где он начинается.Поэтому, когда рак шейки матки распространяется на легкие (или любое другое место), его по-прежнему называют раком шейки матки. Это не рак легких, если он не начинается с клеток легких.
Попросите вашего врача использовать эту картинку, чтобы показать вам, где находится рак .
Шейка матки
Шейка матки — это нижняя часть матки. Он соединяет матку с влагалищем (родовыми путями), который выходит за пределы тела.
Существуют ли разные виды рака шейки матки?
Существует несколько видов рака шейки матки.Ваш врач может рассказать вам больше о том, какой у вас тип.
Самая распространенная форма называется плоскоклеточной карциномой. Этот вид начинается в клетках, покрывающих поверхность шейки матки.
Вопросы к врачу
- Как вы думаете, почему у меня рак?
- Есть шанс, что у меня нет рака?
- Не могли бы вы записать, какой вид рака, по вашему мнению, у меня может быть?
- Что будет дальше?
Как врач узнает, что у меня рак шейки матки?
Рак шейки матки часто не вызывает признаков или симптомов, пока не распространился за пределы шейки матки.
Некоторые признаки рака шейки матки:
- Кровотечение из влагалища, не связанное с месячными,
- Кровянистые выделения или выделения из влагалища,
- Боль во время секса.
Врач задаст вам вопросы о вашем здоровье и проведет физический осмотр и осмотр органов малого таза.
Если признаки указывают на рак шейки матки, будут проведены дополнительные анализы. Вот некоторые из тестов, которые могут вам понадобиться:
Кольпоскопия : Внимательный осмотр внутренней части влагалища и шейки матки с помощью камеры с подсветкой на конце тонкой трубки, называемой кольпоскопом.
Мазок Папаниколау: (или Мазок Папаниколау) Исследование, используемое для соскабливания клеток с шейки матки, чтобы их можно было проверить на рак и предраковые заболевания.
Биопсия шейки матки: При биопсии врач берет небольшой кусочек ткани, чтобы проверить его на наличие раковых клеток. Есть много способов сделать биопсию шейки матки. Спросите врача, какая биопсия вам нужна. Биопсия — единственный способ точно определить, есть ли у вас рак.
КТ (компьютерная томография): Это также называется «компьютерной томографией».«Это особый вид рентгеновского снимка, который позволяет детально сфотографировать, чтобы увидеть, распространился ли рак. КТ также можно использовать для проведения биопсии (см. Ниже).
Сканирование МРТ (магнитно-резонансная томография): Этот тест исследует мягкие ткани тела иногда лучше, чем другие методы визуализации, например компьютерная томография. Ваш врач решит, какой тест на визуализацию лучше всего подходит.
Ваш врач решит, какой тест на визуализацию лучше всего подходит.
Рентген грудной клетки: Можно сделать рентген размером x , чтобы увидеть, распространился ли рак на ваши легкие.
ПЭТ (позитронно-эмиссионная томография) сканирование: В этом тесте вам дают особый вид сахара, который можно увидеть внутри вашего тела с помощью специальной камеры. Если есть рак, этот сахар проявляется как «горячие точки», где обнаруживается рак. Этот тест может помочь определить, распространился ли рак.
Анализы крови: Анализы крови не используются для выявления рака шейки матки, но их проводят, чтобы больше рассказать врачу о вашем здоровье .
Вопросы к врачу
- Какие тесты мне нужно будет пройти?
- Кто будет проводить эти тесты?
- Где они будут делать?
- Кто мне их объяснит?
- Как и когда я получу результаты?
- Кто мне объяснит результаты?
- Что мне делать дальше?
Насколько серьезен мой рак?
Если у вас рак шейки матки, врач захочет выяснить, насколько далеко он распространился. Это называется staging . Возможно, вы слышали, как другие люди говорили, что их рак был «стадией 1» или «стадией 2». Ваш врач захочет выяснить стадию вашего рака, чтобы решить, какой вид лечения лучше всего подходит для вас.
Это называется staging . Возможно, вы слышали, как другие люди говорили, что их рак был «стадией 1» или «стадией 2». Ваш врач захочет выяснить стадию вашего рака, чтобы решить, какой вид лечения лучше всего подходит для вас.
Этап описывает рост или распространение рака через шейку матки. Это также говорит о том, распространился ли рак на близлежащие органы или в более отдаленные места.
Ваш рак может быть 1, 2, 3 или 4. Чем меньше число, тем меньше рак распространился.Более высокое число, например стадия 4, означает более серьезный рак, распространившийся за пределы шейки матки. Обязательно спросите врача о стадии рака и о том, что это значит для вас.
Вопросы к врачу
- Вы знаете стадию рака?
- Если нет, как и когда вы узнаете стадию рака?
- Не могли бы вы объяснить мне, что в моем случае означает сцена?
- Как вы думаете, сколько я проживу, исходя из стадии рака?
- Что будет дальше?
Какое лечение мне понадобится?
Есть много способов лечения рака шейки матки. План лечения, который лучше всего подходит для вас, будет зависеть от:
План лечения, который лучше всего подходит для вас, будет зависеть от:
- Стадия рака
- Вероятность того, что типичное лечение вылечит рак или каким-то образом поможет.
- Ваш возраст
- Другие проблемы со здоровьем
- Ваши чувства по поводу лечения и связанных с ним побочных эффектов.
Операция по поводу рака шейки матки
Большинству женщин с раком шейки матки требуется хирургическое вмешательство.
Криохирургия
Это лечение убивает раковые клетки, замораживая их.Его можно использовать для лечения предраковых заболеваний — аномальных клеток, которые могут превратиться в рак, если их не лечить. .
Лазерная хирургия
Во время этой процедуры используется лазер для выжигания раковых клеток. Его можно использовать для лечения предраковых заболеваний.
Конизация
Конизация также называется конической биопсией . Для этого вынимается небольшой конусообразный кусочек той части шейки матки, которая поражена раком или предраком.
Для этого вынимается небольшой конусообразный кусочек той части шейки матки, которая поражена раком или предраком.
Гистерэктомия
При гистерэктомии удаляются матка и шейка матки.Это наиболее распространенный способ лечения рака шейки матки. Есть много способов сделать эту операцию.
Иногда одновременно удаляют яичники. Также можно удалить близлежащие лимфатические узлы, чтобы проверить, есть ли в них раковые клетки.
Спросите своего врача, какая операция вам понадобится. У каждого типа есть риски и преимущества.
Побочные эффекты операции
Любая операция может иметь риски и побочные эффекты. Обязательно спросите у врача, чего вам следует ожидать. Если у вас возникнут проблемы, сообщите об этом своим врачам.Врачи, которые лечат женщин с раком шейки матки, должны быть в состоянии помочь вам с любыми возникающими проблемами.
Лучевая терапия
Радиация использует лучи высокой энергии (например, рентгеновские лучи) для уничтожения раковых клеток.
Радиация может быть направлена на шейку матки от аппарата, находящегося вне тела. Это называется излучением внешнего луча . Или источник радиоактивного излучения можно ввести во влагалище рядом с шейкой матки. Это называется брахитерапией .
Побочные эффекты лучевой терапии
Если ваш врач предлагает лучевую терапию, спросите, какие побочные эффекты могут возникнуть.Побочные эффекты зависят от типа используемого излучения. Наиболее частые побочные эффекты радиации:
- Изменения кожи в местах облучения
- Чувство сильной усталости
Большинство побочных эффектов проходят после окончания лечения. Некоторые могут длиться дольше. Поговорите со своей бригадой по лечению рака о том, чего вы можете ожидать.
Chemo
Химиотерапия — это короткое слово для обозначения химиотерапии — использования лекарств для борьбы с раком. Лекарства часто вводятся в вену.Эти препараты попадают в кровь и распространяются по организму. Химиотерапия проводится циклами или раундами. После каждого цикла лечения следует перерыв. В большинстве случаев назначают 2 или более химиопрепаратов. Лечение часто длится много месяцев.
Химиотерапия проводится циклами или раундами. После каждого цикла лечения следует перерыв. В большинстве случаев назначают 2 или более химиопрепаратов. Лечение часто длится много месяцев.
Когда химиотерапия и лучевая терапия проводятся одновременно, это называется химиолучевой терапией .
Побочные эффекты химиотерапии
Химиотерапия может вызвать у вас усталость, тошноту и выпадение волос. Но эти проблемы проходят после окончания лечения.
Есть способы лечения большинства побочных эффектов химиотерапии. Если у вас наблюдаются побочные эффекты, обязательно сообщите об этом своей онкологической бригаде, чтобы они могли помочь.
Таргетная терапия
Таргетная терапия — это не то же самое, что химиотерапия, потому что эти препараты в основном воздействуют на раковые, а не на нормальные клетки. У них разные побочные эффекты от химиотерапии.
Иммунотерапия
Иммунотерапия — это лечение, которое либо укрепляет вашу собственную иммунную систему, либо использует искусственные версии частей иммунной системы, которые атакуют клетки рака шейки матки. Эти препараты вводятся в вену.
Эти препараты вводятся в вену.
Побочные эффекты иммунотерапии
Иммунотерапия может вызывать множество различных побочных эффектов в зависимости от того, какой препарат используется. Эти препараты могут вызывать у вас усталость, тошноту или сыпь. Большинство этих проблем проходят после окончания лечения.
Есть способы лечения большинства побочных эффектов, вызванных иммунотерапией. Если у вас есть побочные эффекты, сообщите об этом своей команде по лечению рака, чтобы они могли помочь.
Клинические испытания
Клинические испытания — это научные исследования, в ходе которых проверяются новые лекарства или другие методы лечения на людях.Они сравнивают стандартные методы лечения с другими, которые могут быть лучше.
Если вы хотите узнать больше о клинических испытаниях, которые могут вам подойти, сначала спросите своего врача, проводятся ли клинические испытания в вашей клинике или больнице. См. «Клинические испытания», чтобы узнать больше.
Клинические испытания — один из способов получить новейшее лечение рака. Это лучший способ для врачей найти более эффективные способы лечения рака. Если ваш врач сможет найти того, кто изучает ваш тип рака, вам решать, принимать ли в нем участие.А если вы все же запишетесь на клиническое испытание, вы всегда можете прекратить его в любой момент.
А как насчет других методов лечения, о которых я слышал?
Если у вас рак, вы можете услышать о других способах лечения рака или лечения ваших симптомов. Это не всегда может быть стандартное лечение. Эти методы лечения могут включать витамины, травы, специальные диеты и многое другое. Вы можете задаться вопросом об этих методах лечения.
Известно, что некоторые из них помогают, но многие не тестировались.Было показано, что некоторые не помогают. Некоторые даже оказались вредными. Поговорите со своим врачом обо всем, что вы думаете об употреблении, будь то витамины, диета или что-то еще.
Вопросы к врачу
- Какое лечение, по вашему мнению, лучше всего для меня?
- Какова цель этого лечения? Как вы думаете, он может вылечить рак?
- Будет ли лечение включать хирургическое вмешательство? Если да, то кто будет делать операцию?
- Какая будет операция?
- Смогу ли я иметь детей после операции?
- Потребуются ли мне и другие виды лечения?
- Какова цель этих процедур?
- Какие побочные эффекты могут быть у меня от этих методов лечения?
- Может ли лечение привести меня к ранней менопаузе?
- Изменится ли моя сексуальная жизнь после лечения?
- Что я могу сделать с возможными побочными эффектами?
- Подходит ли мне какое-либо клиническое испытание?
- А как насчет специальных витаминов или диет, о которых мне рассказывают друзья? Как я узнаю, что они в безопасности?
- Как скоро мне нужно начать лечение?
- Что мне делать, чтобы быть готовым к лечению?
- Могу ли я что-нибудь сделать, чтобы лечение улучшилось?
- Что делать дальше?
Что будет после лечения?
Будете рады, когда лечение закончится. Но трудно не беспокоиться о возвращении рака. Даже когда рак больше не возвращается, люди все равно беспокоятся об этом. В течение многих лет после окончания лечения вы будете посещать своего онколога. Обязательно посетите все эти контрольные визиты. Ваши врачи спросят о симптомах, проведут медицинский осмотр и могут сделать анализы крови и, возможно, другие анализы, чтобы увидеть, вернулся ли рак. Вам также необходимо будет продолжать сдавать мазки Папаниколау независимо от того, какое лечение вы проходили.
Но трудно не беспокоиться о возвращении рака. Даже когда рак больше не возвращается, люди все равно беспокоятся об этом. В течение многих лет после окончания лечения вы будете посещать своего онколога. Обязательно посетите все эти контрольные визиты. Ваши врачи спросят о симптомах, проведут медицинский осмотр и могут сделать анализы крови и, возможно, другие анализы, чтобы увидеть, вернулся ли рак. Вам также необходимо будет продолжать сдавать мазки Папаниколау независимо от того, какое лечение вы проходили.
Сначала вы можете приходить каждые несколько месяцев.Затем, чем дольше вы не страдаете от рака, тем реже вам нужны посещения.
Заболеть раком и лечиться может быть непросто, но это также может быть временем, чтобы взглянуть на свою жизнь по-новому. Возможно, вы думаете о том, как улучшить свое здоровье. Позвоните нам по телефону 1-800-227-2345 или поговорите со своим врачом, чтобы узнать, что вы можете сделать, чтобы почувствовать себя лучше.
Вы не можете изменить тот факт, что у вас рак. Что вы можете изменить, так это то, как вы проживете остаток своей жизни — делая выбор в пользу здорового образа жизни и чувствуя себя настолько хорошо, насколько это возможно.
Что вы можете изменить, так это то, как вы проживете остаток своей жизни — делая выбор в пользу здорового образа жизни и чувствуя себя настолько хорошо, насколько это возможно.
Отчетных условий | Университет здоровья Юты —
Рак обозначен как заболевание, подлежащее регистрации в штате Юта (Правило сообщения о раке, R384-100).
Реестр рака штата Юта собирает диагностическую информацию, лечение и последующие наблюдения в соответствии со стандартами данных Программы SEER Национального института рака, Североамериканской ассоциации центральных реестров рака и Национальной программы реестров рака.
случаев рака выявлено посредством систематического обзора:
- отчеты о патологии
- медицинские карты
- Списки выписки из больницы
- и записи актов гражданского состояния
Как сообщать о случаях рака
Для получения подробной информации о регистрации случаев рака в онкологический реестр штата Юта, пожалуйста, обратитесь к следующему:
О каких условиях необходимо сообщать?
В соответствии с руководящими принципами программы SEER Национального института рака и Национальной программы реестров рака, случаи, подлежащие регистрации в реестр, соответствуют Руководству по кодированию и стадированию программы SEER 2021.
Сводку условий, подлежащих регистрации, см. Ниже. Подробные требования к отчетности см. В Руководстве по программированию и постановке программ SEER на 2021 год, начало на странице 6. Чтобы получить доступ к историческим версиям руководств по постановке и кодированию за годы диагностики до 2021 года, посетите веб-сайт SEER.
In situ и злокачественные / инвазивные гистологии (код поведения / 2, / 3, см. ICD-O-3) подлежат регистрации, включая:
- Ранняя или развивающаяся меланома, in situ и инвазивная: По состоянию на 01.01.2021, ранняя или развивающаяся меланома in situ или любая другая ранняя или развивающаяся меланома подлежит регистрации.
- Все опухоли GIST подлежат отчетности по состоянию на 01.01.2021.
- По состоянию на 01.01.2021 г. почти все тимомы подлежат отчетности. Исключения составляют:
- Микроскопическая тимома или тимома доброкачественная (8580/0)
- Микронодулярная тимома с лимфоидной стромой (8580/1)
- Эктопическая гамартоматозная тимома (8587/0)
- Карциноид, БДУ аппендикса подлежит регистрации.
 По состоянию на 01.01.2015 код поведения МКБ-О-3 изменен с / 1 на / 3.
По состоянию на 01.01.2015 код поведения МКБ-О-3 изменен с / 1 на / 3. - Интраэпителиальная неоплазия III степени (примеры: AIN III C210 и C211; VAIN III и VIN III)
- Дольковая карцинома in situ (LCIS) груди
- Цитологический анализ мочи с положительным результатом на злокачественные новообразования подлежит регистрации для диагнозов в 2013 г. и позже (исключение: если последующая биопсия участка мочи отрицательна, не сообщать)
- Неинвазивное муцинозно-кистозное новообразование (МКН) поджелудочной железы с дисплазией высокой степени
- Зрелая тератома яичек у взрослых является злокачественной и регистрируется как 9080/3
Доброкачественные / незлокачественные гистологические исследования:
- Доброкачественные и пограничные первичные опухоли внутричерепной и центральной нервной системы (ЦНС) с кодом поведения / 0 или / 1) в МКБ-О-3 (эффективны в случаях, диагностированных с 01.01.2004 по 31.12.
 2020) или МКБ -О-3.2 (действительно для случаев, диагностированных 01.01.2021 и позже). Для получения информации о конкретных сайтах см. Таблицу в Руководстве по программированию и разработке программ SEER 2021, стр. 8.
2020) или МКБ -О-3.2 (действительно для случаев, диагностированных 01.01.2021 и позже). Для получения информации о конкретных сайтах см. Таблицу в Руководстве по программированию и разработке программ SEER 2021, стр. 8.
Примечание: доброкачественные и пограничные первичные внутричерепные опухоли и аденомы гипофиза подлежат отчетности в соответствии с требованиями штата к отчетности с момента создания Реестра рака штата Юта в 1966 году.
- Пилоцитарная ювенильная астроцитома подлежит регистрации и должна иметь код 9421 с поведением / 3 (9421/3)
- Новообразования и опухоли относятся к внутричерепным и ЦНС, потому что они перечислены в МКБ-О-3.2 с кодами поведения / 0 и / 1
- «Масса» и «поражение» — это , а не , подлежащие регистрации термины для внутричерепных и ЦНС, поскольку они не перечислены в МКБ-O-3.2 с кодами поведения / 0 или / 1
Исключения в отчетах
Злокачественные и инвазивные гистологические исследования, которые не требуются :
- Не сообщать первичные кожные покровы (C440-C449) с любой из следующих гистологий:
- Злокачественное новообразование (8000-8005)
- Эпителиальная карцинома (8010-8046)
- Папиллярный и плоскоклеточный рак (8050-8084)
- Базальноклеточный рак (8090-8110)
- AIN III (8077), возникающий в коже перианальной области (C445)
- Не сообщать о карциноме шейки матки in situ (/ 2) или цервикальной интраэпителиальной неоплазии (CIN III или SIN III) шейки матки (по состоянию на 1 января 1996 г.
 )
) - Не сообщать об интраэпителиальной неоплазии предстательной железы (PIN III) простаты (C619) (по состоянию на 1 января 2001 г.)
См. Раздел «Отчетность» Руководства по кодированию и постановке программ SEER 2021, начинающийся на странице 6, где представлен более подробный список отчетов о диагностике и исключениях.
Антиоксиданты при раке шейки матки: химиопрофилактические и химиотерапевтические эффекты полифенолов
https://doi.org/10.1016/j.bbadis.2011.10.005Получить права и содержаниеРезюме
Поражения от рака шейки матки представляют серьезную угрозу для здоровья женщин. представляет собой второй по распространенности вид рака в мире. Общепризнанным этиологическим фактором, вызывающим рак шейки матки, является инфекция вирусом папилломы человека (ВПЧ).Инфекция ВПЧ, хотя и необходима, не является достаточной per se , чтобы вызвать рак. Другие факторы должны быть вовлечены в прогрессирование инфицированных клеток до полного неопластического фенотипа. Окислительный стресс представляет собой интересный и малоизученный кандидат в качестве фактора, способствующего канцерогенезу, инициированному ВПЧ. Известно, что окислительный стресс нарушает окислительно-восстановительный статус клеток, что приводит к изменению ответов на экспрессию генов за счет активации нескольких окислительно-восстановительных факторов транскрипции.Этот сигнальный каскад влияет как на рост клеток, так и на их гибель. Способность встречающихся в природе антиоксидантов модулировать пути передачи клеточного сигнала посредством активации / репрессии множественных окислительно-восстановительных факторов транскрипции была заявлена для их потенциального терапевтического использования в качестве химиопрофилактических агентов. Было обнаружено, что среди этих соединений полифенолы являются многообещающими агентами против рака шейки матки. Помимо действия как антиоксиданты, полифенолы проявляют широкий спектр биологических функций, включая индукцию апоптоза, остановку роста, ингибирование синтеза ДНК и модуляцию путей передачи сигнала.
Окислительный стресс представляет собой интересный и малоизученный кандидат в качестве фактора, способствующего канцерогенезу, инициированному ВПЧ. Известно, что окислительный стресс нарушает окислительно-восстановительный статус клеток, что приводит к изменению ответов на экспрессию генов за счет активации нескольких окислительно-восстановительных факторов транскрипции.Этот сигнальный каскад влияет как на рост клеток, так и на их гибель. Способность встречающихся в природе антиоксидантов модулировать пути передачи клеточного сигнала посредством активации / репрессии множественных окислительно-восстановительных факторов транскрипции была заявлена для их потенциального терапевтического использования в качестве химиопрофилактических агентов. Было обнаружено, что среди этих соединений полифенолы являются многообещающими агентами против рака шейки матки. Помимо действия как антиоксиданты, полифенолы проявляют широкий спектр биологических функций, включая индукцию апоптоза, остановку роста, ингибирование синтеза ДНК и модуляцию путей передачи сигнала. Они могут вмешиваться в каждую стадию инициации, развития и прогрессирования канцерогенеза, чтобы предотвратить развитие рака. В настоящем обзоре обсуждаются современные знания об основных молекулярных путях, которые участвуют в канцерогенезе, управляемом ВПЧ, и о способности полифенолов модулировать эти пути. Было продемонстрировано, что полифенолы, действуя на определенных этапах каскада вирусной трансформации, избирательно подавляют рост опухолевых клеток и могут быть многообещающим терапевтическим инструментом для лечения рака шейки матки.Кроме того, обсуждаются недавние результаты, полученные в клинических испытаниях с использованием полифенолов. Эта статья является частью специального выпуска, озаглавленного: Антиоксиданты и лечение антиоксидантами при заболеваниях.
Они могут вмешиваться в каждую стадию инициации, развития и прогрессирования канцерогенеза, чтобы предотвратить развитие рака. В настоящем обзоре обсуждаются современные знания об основных молекулярных путях, которые участвуют в канцерогенезе, управляемом ВПЧ, и о способности полифенолов модулировать эти пути. Было продемонстрировано, что полифенолы, действуя на определенных этапах каскада вирусной трансформации, избирательно подавляют рост опухолевых клеток и могут быть многообещающим терапевтическим инструментом для лечения рака шейки матки.Кроме того, обсуждаются недавние результаты, полученные в клинических испытаниях с использованием полифенолов. Эта статья является частью специального выпуска, озаглавленного: Антиоксиданты и лечение антиоксидантами при заболеваниях.
Основные моменты
► Рак шейки матки является вторым по распространенности раком среди женщин во всем мире и представляет собой серьезную проблему для общественного здравоохранения. ► Окислительный стресс является вероятным фактором патогенеза и прогрессирования рака шейки матки. ► Было обнаружено, что полифенолы являются многообещающими агентами против рака шейки матки.► Помимо того, что полифенолы действуют как антиоксиданты, они обладают широким спектром биологических функций. ► Было продемонстрировано, что полифенолы подавляют пролиферацию ВПЧ-положительных раковых клеток.
Ключевые слова
Рак шейки матки
HPV
Полифенол
Апоптоз
Окислительный стресс
Рекомендуемые статьиЦитирующие статьи (0)
Copyright © 2011 Elsevier B.V. Все права защищены.
Рекомендуемые статьи
Цитирующие статьи
Наноформа куркумина для лечения рака шейки матки
Культура клеток
Клеточные линии рака шейки матки Caski и SiHa были приобретены в Американской коллекции типовых культур (Манассас, Вирджиния).Эти клеточные линии были увеличены, и замороженные аликвоты с малым количеством пассажей хранили в жидком азоте. Для проведения экспериментов клетки размораживали и выращивали в течение <6 месяцев. Клетки SiHa поддерживали в среде Игла, модифицированной Дульбекко (DMEM), содержащей 4,5 г / л глюкозы, 10 нМ заменимых аминокислот, 100 нМ пирувата натрия, 1x антибиотик / антимикотик (Sigma, Сент-Луис, Миссури) и 10% тепла. инактивированный FBS (Atlanta Biologicals, Lawrenceville, GA). Клетки Caski выращивали в среде Roswell Park Memorial Institute (RPMI), содержащей 10% инактивированного нагреванием FBS и 1x антибиотик / антомикотик.Все клетки инкубировали в инкубаторе с 5% CO 2 при 37 ° C.
Приготовление состава Nano-CUR
Наноформа CUR на основе PLGA была синтезирована, как описано ранее 22 . Вкратце, 90 мг раствора PLGA в 10 мл ацетона смешивали с 10 мг CUR в течение 5 минут. Этот раствор по каплям добавляли к 20 мл водного раствора, содержащего 1% мас. / Об. ПВС и 10 мг поли (1-лизина), в течение 10 минут на магнитной мешалке при 800 об / мин. Полученную суспензию частиц Nano-CUR перемешивали при комнатной температуре в течение ~ 24 часов для полного испарения ацетонового растворителя.Более крупные агрегаты и несвязанные полимеры удаляли центрифугированием при 5000 об / мин в центрифуге Eppendorf 5810 R (Eppendorf AG, Гамбург, Германия) в течение 10 мин. Частицы Nano-CUR выделяли ультрацентрифугированием при 30 000 об / мин с использованием ротора 30,50 в центрифуге Avanti J-30I (Beckman Coulter, Фуллертон, Калифорния, США). Частицы дважды промывали и затем лиофилизировали с использованием системы сублимационной сушки Labconco (-48 ° C, 133 × 10 –3 мбар; Labconco, Канзас-Сити, Миссури). Контрольные наночастицы PLGA были приготовлены аналогичным образом путем растворения полимера в органическом растворителе без CUR, остальная часть метода была такой же.
Клеточное поглощение
Чтобы определить эффективность поглощения и интернализации Nano-CUR, мы использовали флуоресцентную микроскопию и проточную цитометрию. Для качественной оценки клетки Caski и SiHa (2 × 10 5 клеток / лунка в 2 мл среды) помещали в 6-луночные планшеты и оставляли для прикрепления в течение ночи. Затем клетки обрабатывали 5, 10 и 20 мкМ CUR или Nano-CUR и их контрольными носителями (НЧ ДМСО и PLGA, соответственно) в течение 6 часов. Через 6 часов клетки дважды промывали PBS и заменяли средой, не содержащей фенолового красного.Живые прилипшие клетки исследовали под флуоресцентным микроскопом (Nikon Eclipse Ti Microscope, Мелвилл, Нью-Йорк), и изображения получали при 200X. Для количественного измерения клетки (2 × 10 5 клеток на лунку в 2 мл среды) помещали в 6-луночные планшеты и оставляли для прикрепления в течение ночи. Затем клетки обрабатывали 5, 10 и 20 мкМ CUR или Nano-CUR и их контрольными носителями (ДМСО и PLGA-NP соответственно) в течение 6 часов. Через 6 часов клетки промывали PBS, трипсинизировали и собирали в 2 мл среды.Далее эти клетки центрифугировали, дважды промывали PBS и собирали в 2 мл среды без фенолового красного для анализа проточной цитометрии. Около 10000 клеток в среде вводили в проточный цитометр Accuri C6 (BD Biosciences, Сан-Хосе, Калифорния, США) для определения уровней флуоресценции в канале FL1 (возбуждение 488, синий лазер, 530 ± 15 нм, FITC / GFP). Канал FL1 измеряет зеленую флуоресценцию, генерируемую куркумином или Nano-CUR.
Анализ пролиферации клеток
Эффект CUR и Nano-CUR на рост клеток определяли анализом пролиферации клеток с использованием реагента CellTiter96 A Water One Solution (MTS) (Promega, Madison, WI).Вкратце, клетки рака шейки матки (5000 клеток / лунку) высевали в 100 мкл среды DMEM / RPMI в 96-луночные планшеты для тканевых культур и инкубировали в течение ночи. CUR растворяли в ДМСО и разводили в среде для культивирования клеток. Клетки обрабатывали различными концентрациями CUR / Nano-CUR или эквивалентными количествами контрольных носителей (ДМСО / PLGA) в течение 48 часов. Пролиферацию клеток определяли путем добавления 20 мкл реагента MTS, инкубации в течение 2 часов при 37 ° C и измерения поглощения при 490 нм с использованием планшетного ридера SPECTRA Max Plus (Molecular Devices, Саннивейл, Калифорния).Процент пролиферации в клетках, обработанных CUR / Nano-CUR, определяли путем нормализации клеток без обработки (считая 100%).
Анализ образования колоний
Для этого анализа клетки рака шейки матки высевали по 500 клеток на лунку в 2 мл среды в 6-луночный планшет и оставляли на 24 часа для прикрепления. После этого клетки обрабатывали концентрациями 2,5, 5 и 10 мкМ CUR / Nano-CUR в течение дополнительных 12–14 дней. Клетки промывали, фиксировали холодным метанолом и окрашивали гематоксилином.Видимые колонии (~ 50 клеток) подсчитывали вручную и представляли как отношение количества колоний в обработанных клетках к количеству колоний в контроле носителя (ДМСО / PLGA).
Анализ клеточного цикла
Остановка клеточного цикла анализировалась методом Телфорда. Клетки рака шейки матки Caski и SiHa (1 × 10 6 ) помещали в чашки диаметром 100 мм и оставляли для прикрепления в течение ночи. На следующий день клетки подвергали воздействию 10 или 25 мкМ CUR, Nano-CUR или эквивалентных количеств контролей в течение 24 часов, трипсинизировали, промывали, фиксировали 70% этанолом, хранили при 4 ° C в течение часа, окрашивали йодидом пропидия. (Сигма-Олдрич, Св.Луи, Миссури; 50 мкг в 1 мл реагента Телфорда) в темноте в течение 4 часов при 4 ° C и анализировали проточным цитометром Accuri C6 в канале FL2.
Окрашивание аннексином V-7AAD
Обнаружение апоптоза определяли с использованием окрашивания аннексином V-7AAD. Клетки рака шейки матки Caski и SiHa (1 × 10 6 ) помещали в чашку диаметром 100 мм и оставляли на ночь. На следующий день клетки обрабатывали 10, 20 и 25 мкМ CUR, Nano-CUR или эквивалентными количествами контролей в течение 24 часов. По истечении указанного времени как прикрепленные, так и плавающие клетки собирали и окрашивали аннексином V и 7-AAD (BD Biosciences) в количестве 5 мкл каждого на 100 мкл суспензии клеток.Клетки инкубировали в течение 20 минут в темноте при комнатной температуре и анализировали с помощью проточного цитометра Accuri C6 в каналах FL2 и FL3.
Ортотопическая модель рака шейки матки у мышей NSG.
Шестинедельных самок мышей NSG (Cancer Research Animal Core, UTHSC, Мемфис, Теннесси) использовали для создания ортотопической модели рака шейки матки. Мышей содержали в среде, свободной от патогенов, и все процедуры выполнялись в соответствии с одобрением Институционального комитета по уходу и использованию животных UTHSC (UTHSC-IACUC).Все процедуры и методы были выполнены в «соответствии» с утвержденными руководящими принципами UTHSC-IACUC. Вкратце, клетки Caski (4 × 10 6 клеток / на мышь) диспергировали в 100 мкл 1X PBS и 100 мкл Matrigel (BD Biosciences) и вводили непосредственно в шейку матки мышей. За животными периодически наблюдали на предмет развития опухоли, и объем опухоли измеряли с 5 дня после инъекции с помощью цифрового штангенциркуля Вернье. Когда объем опухоли достигал ~ 200 мм 3 , внутри опухоли вводили CUR, Nano-CUR (100 мкг / мышь) и их соответствующие контрольные носители (PBST и PLGA NP соответственно).Объем опухоли рассчитывали по формуле объема эллипсоида: объем опухоли (мм 3 ) = π / 6 × L × W × H , где L — длина, W — ширина и H — высота. За опухолью регулярно наблюдали и давали возможность расти до тех пор, пока объем опухоли не достигал максимального объема 1100 мм 3 . Во время умерщвления опухоли мышей удаляли, фиксировали в формалине, заливали парафином и разрезали на 5-микронные срезы для дальнейшей обработки и анализа.
Количественная полимеразная цепная реакция с обратной транскрипцией в реальном времени (qRT-PCR)
Клетки рака шейки матки Caski высевали в 6-луночный планшет, позволяли прикрепиться и обрабатывали различными концентрациями CUR / Nano-CUR и их контрольными носителями ( ДМСО / PLGA) и BaP в их соответствующих комбинациях в течение 4 дней. Тотальную РНК экстрагировали из обработанных клеток с использованием реагента TRIzol (Invitrogen, Life Technologies, Grand Island, NY). Целостность РНК измеряли с помощью набора RNA 6000 Nano Assay и 2100 Bioanalyzer (Agilent Technologies, Санта-Клара, Калифорния).Для обнаружения миРНК 100 нг общей РНК подвергали обратной транскрипции в кДНК с использованием специфических праймеров, разработанных для анализа миРНК (Applied Biosystems, Foster City, CA). Уровни экспрессии miRNA определяли с помощью qRT-PCR с использованием основной смеси Taqman PCR (без AmpErase UNG) и специфических праймеров, разработанных для обнаружения зрелых miRNA (Applied Biosystems). Экспрессию miRNA нормализовали экспрессией эндогенного контроля U6snRNA.
Измерение IL-6.
Клетки рака шейки матки Caski обрабатывали с использованием модифицированной культуральной среды (RPMI-1640 + 2% FBS).Вкратце, после обработки одним BaP или в комбинации (BaP и CUR / Nano-CUR) в течение 48 часов культуральную среду центрифугировали при 10000 g в течение 10 минут при 4 ° C. OD измеряли при 450 нм. Измерение IL-6 (eBioscience, Сан-Диего, Калифорния, США) выполняли в соответствии с инструкциями производителя. Количественное определение IL-6 выполняли с помощью стандартной кривой, построенной для рекомбинантного человеческого IL-6 (входит в комплект) и нормализованной для живых клеток. Все эксперименты были выполнены в трех экземплярах и повторены не менее трех раз.
Анализ миграции
Анализ миграции клеток выполняли в 96-луночном HTS transwell от Corning в соответствии с инструкциями производителя с небольшими изменениями. Вкратце, клетки Caski (50000 клеток / лунку) высевали в верхние камеры планшета, содержащие бессывороточную культуральную среду. Клетки дополнительно обрабатывали одним BaP или их комбинацией (BaP и CUR / Nano-CUR) в течение 18 часов. Клеткам позволяли мигрировать из верхней камеры (5% FBS) в нижнюю камеру, которая содержала 10% FBS. Клетки в верхней камере полностью удаляли ватной палочкой.Клетки фиксировали 4% параформальдегидом, приготовленным в PBS, в течение 30 мин. Эти клетки окрашивали красителем Гимза, и мигрировавшие клетки наблюдали с помощью светового микроскопа. Мигрировавшие клетки подсчитывали в шести случайных полях зрения, и эксперименты проводили в трех повторностях.
Вестерн-блоттинг
Активно растущие клетки рака шейки матки Caski использовали для Вестерн-блоттинга. Вкратце, клетки Caski промывали ледяным фосфатным буферным солевым раствором (PBS) и лизировали в буфере для анализа 2Х радиоиммунопреципитации (RIPA) после соответствующих обработок.Содержание белка анализировали с помощью Nanodrop 2000 (Thermo Scientific, Wilmington, DE), и эквивалентное количество образцов белка разделяли электрофоретически на 4-20% гелях для электрофореза в полиакриламидном геле с додецилсульфатом натрия (SDS-PAGE) и переносили в поливинилидендифторид (PVDF). мембрана (Bio-Rad Laboratories, Геркулес, Калифорния). После блокирования 5% бычьим сывороточным альбумином (BSA; 5 мл в течение одного часа) мембраны зондировали в течение ночи при 4 ° C на различные белки с использованием специфических первичных антител (все от Cell Signaling Technologies, Danvers, MA).Вестерн-блоты инкубировали с вторичным антителом, меченным HRP, и полосы белка проявляли с использованием хемилюминесцентного реагента Lumi-Light Plus (Roche, Indianapolis, IN).
Иммунофлуоресценция и конфокальная микроскопия
Иммунофлуоресцентное окрашивание проводили для определения влияния BaP на ядерную транслокацию β-катенина. 80 000 клеток Caski засевали в течение ночи на предметных стеклах с 4-луночной камерой (Nalgene Nunc Intl .., Rochester, NY), затем обрабатывали одним BaP и в комбинации с CUR / Nano-CUR в течение 24 часов.Впоследствии они были зафиксированы и обработаны для иммуноокрашивания. Вкратце, клетки фиксировали в 2% параформальдегиде, пермеабилизировали, блокировали и затем инкубировали с первичным антителом против β-катенина Ab (Cell Signaling Technologies). После промывания клетки инкубировали с меченным Cy3 вторичным антителом (Jackson Immunoresearch Labs, Westgrove, PA). После дополнительной промывки покровные стекла помещали на предметные стекла, используя водную среду против выцветания (Vector Laboratories, Burlingame, CA). Слайды исследовали под лазерным конфокальным микроскопом (Nikon Corporation).
Гибридизация in situ для miRNA-21
Гибридизация in situ была проведена в соответствии с протоколом производителя для тканей FFPE контрольных и обработанных ортотопических мышей для обнаружения экспрессии miRNA-21 с использованием набора Biochain (Biochain, San Франциско, Калифорния). DIG-меченные олигонуклеотиды LNA (Exiqon, Woburn, MA) использовали для гибридизации в течение ночи при 50 ° C. Окрашивание проводили в соответствии с инструкциями руководства пользователя Exiqon. Вкратце, после депарафинизации образцы фиксировали в 4% параформальдегиде в DEPC-PBS в течение 20 мин и подвергали расщеплению с использованием двукратного стандартного цитрата физиологического раствора и 0.1% Triton-X в течение следующих 25 мин. Предметные стекла предварительно гибридизовали с раствором для предварительной гибридизации в течение 4 часов при 48 ° C с последующей гибридизацией слайдов с гибридизационным буфером и зондом (меченным дигоксигенином) при 45 ° C в течение ночи. После тщательной промывки предметных стекол стандартным цитратом физиологического раствора различных сортов предметные стекла были заблокированы с помощью 1X блокирующего раствора, входящего в комплект. Затем ткани инкубировали в течение ночи с АР-конъюгированным антителом против дигоксигенина. Предметные стекла дважды промывали в течение 5 мин 1X буфером щелочной фосфатазы.Окончательную визуализацию проводили с помощью NBT / BCIP в течение ночи с последующим ядерно-быстрым контрастным окрашиванием в красный цвет. Слайды были установлены, отображены и проанализированы в системе ScanScope® XT / XT2 (Aperio, Vista, CA). Все реагенты, использованные для анализа, были предоставлены в наборе от Biochain.
Иммуногистохимический анализ ортотопических опухолей шейки матки
Был проведен ИГХ анализ белков HPV E6 / E7, Ki67 и PTEN на фиксированных формалином, залитых парафином ортотопических опухолях мышей (срезы размером 5 микрон).Вкратце, опухолевые ткани депарафинизировали, регидратировали, обрабатывали 0,3% перекисью водорода и обрабатывали для извлечения антигена с использованием метода индуцирования тепла. После блокировки фоновым снайпером (Biocare Medical, Concord, CA) образцы обрабатывали для окрашивания E6 (Abcam, Cambridge MA), E7 (Invitrogen), Ki67 и антителами PTEN (Cell Signaling Technologies). Экспрессию этих белков детектировали с использованием набора для обнаружения универсального полимера HRP MACH 4 (Biocare Medical) и 3,39-диаминобензидина (набор субстратов DAB, Vector Laboratories, Burlingame, CA).
