Ладонно-подошвенный пустулез: факторы, вызывающие заболевание и влияющие на его течение
Ладонно-подошвенный пустулез (ЛПП) — хроническое воспалительное заболевание, патогенез которого недостаточно изучен. ЛПП классифицируется либо как вариант псориаза, либо как отдельная форма [1].
На другую природу ЛПП в отличие от псориаза указывает отсутствие анамнеза по псориазу у больных ЛПП, позднее начало заболевания, отсутствие типичных псориатических поражений, и более частые случаи контактной аллергии на металлы [2,3]. Ладонно-подошвенный пустулез чаще встречается у женщин, чем у мужчин, чаще у людей среднего возраста. Данное заболевание приводит к нарушению повседневного функционирования и социализации. Поражения обнаруживаются на ладонях и подошвах, обычно симметрично [1].
Стерильные пустулы образуются на эритематозном фоне и впоследствии «высыхают» в течение нескольких дней. Наблюдаются шелушение и линейные трещины. Заболевание периодически обостряется с появлением новых гнойничков.
Часто наблюдается гиперкератоз ногтей, под ногтевыми пластинами могут образовываться пустулы (рис. 1) [1]. Пациенты испытывают боль, зуд или жжение.
Поражения в ходе ЛПП развиваются в областях, богатых эккринными потовыми железами, которые, вероятно, играют роль в патогенезе заболевания.
Результаты недавних исследований показывают, что акросирингиум (от англ. acrosyringium), интраэпидермальная часть протоков потовых желез, является основным местом, где образуются пустулы при ЛПП.
Биопсия поражений кожи выявляет изменения, аналогичные тем, которые наблюдаются при псориазе: паракератоз, потеря зернистого слоя и спонгиоз.
Стерильные пустулы в верхних слоях эпидермиса заполнены нейтрофилами и эозинофилами. Рассеянные смешанные инфильтраты, состоящие из лимфоцитов, нейтрофилов, эозинофилов и тучных клеток, обнаруживаются в верхнем слое дермы и в периваскулярной области. Преобладают Т-лимфоциты (экспрессия CD3 +) [5,6].
При дифференциальной диагностике следует учитывать такие заболевания как: контактный дерматит, красный пилировый лишай, дисгидротическая экзема и опоясывающий лишай.
Этиопатогенез ладонно-подошвенного пустулеза
В развитии ЛПП играют роль генетические, иммунологические и экологические факторы (Таблица 1).
Таблица 1. Известные патогенетические механизмы развития ЛПП.
|
Механизмы |
Авторы |
|
Генетические факторы |
|
|
Антиген HLA-B27 у 32% пациентов с ЛПП, ассоциированный с болью в суставах передней грудной клетки, тазобедренного сустава или периферических суставов |
Szanto и Linse (1991) |
|
Ген ATG16L1 SNPs: rs2241880G и rs2241879A |
Douroudis и соавторы (2011) |
|
Мутация антагониста гена IL-36RN |
Wang и соавторы (2016) |
|
Иммунологические факторы |
|
|
Повышенный уровень в крови: TNF-α, IL-17, IL-22 и IFNγ. |
Murakami и соавторы (2011) |
|
Повышенный уровень IL-6 в крови и экспрессия в кожных высыпаниях |
Croxford и соавторы (2014) |
|
Повышенная экспрессия IL-17 в очагах поражения ЛПП без повышения уровня IL-12 и IL-23. |
Bissonnette и соавторы (2014) |
|
Нарушение регуляции функции IL-36 |
Marrakchi и соавторы (2011) Carrier и соавторы (2011) |
|
Факторы окружающей среды |
|
|
Курение — никотин активирует макрофаги, кератиноциты и Т-лимфоциты, а также усиливает гиперкератоз выводных протоков — регресс поражения ЛПП после прекращения курения |
Hagforsen и соавторы (2010) Elahmed и соавторы (2013) |
|
Контактная аллергия — 25,2% пациентов с положительным результатами в патч-тесте |
Caca-Biljanovska и соавторы (2005) |
|
Побочный эффект лекарственных средств — ЛПП отмечается как побочный эффект ингибиторов ФНО-а |
Shmidt и соавторы (2012) Collamer и соавторы (2008) |
|
Очаговые бактериальные инфекции — тонзиллэктомия или эффективное лечение очаговых бактериальных инфекций привели к значительному улучшению или разрешению поражений при ЛПП |
Takahara и соавторы (2011) |
|
Хламидиоз — титр хламидийных антител ≥1 / 16 у 53% пациентов с PPP |
Jansen и соавторы (1980) |
Генетический фон
Генетический фон ЛПП до конца не изучен. Некоторые авторы считают ЛПП вариантом псориаза. Были опубликованы исследования, сравнивающие распространенность определенных генов при этих двух заболеваниях.
Некоторые авторы считают ЛПП вариантом псориаза. Были опубликованы исследования, сравнивающие распространенность определенных генов при этих двух заболеваниях.
Гены, кодирующие HLA-Cw6, WWCC HCR и CDSN5, расположенные в локусе PSORS1 (6p21) на хромосоме 6, считаются основной генетической основой псориаза [7].
С другой стороны, исследования (проведенные на популяциях Швеции и Великобритании), показали, что ни один из вышеуказанных аллелей не был связан с возникновением ЛПП. Частота встречаемости HLA-Cw6 одинакова у пациентов с ЛПП (19–20%) и здоровым контролем (15%). Аналогичным образом, WWCC HCR встречается у 50% пациентов с ЛПП и 40% здоровых контролей.
Другим важным генетическим фактором, играющим роль в патогенезе псориаза, является мутация гена ATG16L1, расположенного на хромосоме 2.
ATG16L1 участвует в иммунологическом ответе, и мутация этого гена приводит к снижению продукции антимикробных пептидов и усилению продукции провоспалительных цитокинов, таких как интерлейкин 1 (ИЛ-1) и ИЛ-18, запускающие системное воспаление. Более частое появление этой мутации было выявлено при воспалительных заболеваниях, таких как псориаз и болезнь Крона.
Более частое появление этой мутации было выявлено при воспалительных заболеваниях, таких как псориаз и болезнь Крона.
Кроме того, у пациентов с ЛПП наблюдается более высокая частота однонуклеотидных полиморфизмов (SNP) гена ATG16L1 rs2241880 G и rs2241879A по сравнению со здоровы контолем [10].
Из-за возможной коморбидности ЛПП с артритом и артралгией у некоторых пациентов генетическая основа ЛПП сравнивалась с таковой для псориатического артрита.
Обнаружена корреляция между антигеном HLA-B27, характерным для псориатического артрита, и ЛПП. Антиген HLA-B27 был идентифицирован у 32% пациентов с ЛПП, ассоциированным с артралгией в области передней грудной клетки, тазобедренного сустава или периферических суставов [9].
Недавние исследования также указывают на роль мутации гена антагонистического рецептора IL-36 (IL-36RN) в развитии ЛПП, а также в различных формах псориаза: типе бляшек, генерализованном пустулезном типе [11].
Известно, что эта мутация является генетической основой дефицита антагониста рецептора IL-36 (DITRA), редкого наследственного аутосомно-рецессивного заболевания, характеризующегося генерализованными пустулезными поражениями, напоминающими пустулезный псориаз или острый генерализованный экзантематозный пустулез (AGEP) [12].
Иммунологические процессы при ЛПП приводят к накоплению большого количества гранулоцитов в области выводного тракта потовых желез, акросирингиума [5,13].
Цитокины, регулирующие иммунологические процессы, играют ключевую роль в патогенезе заболевания. Как и при псориазе, при ЛPP наблюдается повышение уровня провоспалительных интерлейкинов в крови, таких как фактор некроза опухоли альфа (TNF-α), IL-17, IL-22 и гамма-интерферон (IFN-γ) [14].
Псориатические поражения и поражения ЛПП различаются. При псориатических поражениях имеется большое количество цитокинов, продуцируемых лимфоцитами Th27 (IL-12, IL-17 и IL-23), в то время как при ЛПП было отмечено только значительное увеличение экспрессии IL-17 без сопутствующего повышения уровня IL-12 и IL-23.
Таким образом, изолированное повышение уровня IL-17 указывает на то, что нейтрофилы, а не Th-17, являются основным источником воспалительного ответа при ЛПП [15-17].
Высокий уровень IL-17, локально обнаруживаемый в эпидермисе, стимулирует кератиноциты продуцировать IL-6, который активирует нейтрофилы и моноциты, привлекая гранулоциты к эпидермису, что и
приводит к образованию пустул. Интерлейкин 6 (IL-6), вероятно, играет решающую роль в при поражениях при ЛПП. Повышенные уровни этого цитокина были обнаружены в поражениях кожи, а также в крови пациентов с этим заболеванием [16].
Интерлейкин 6 (IL-6), вероятно, играет решающую роль в при поражениях при ЛПП. Повышенные уровни этого цитокина были обнаружены в поражениях кожи, а также в крови пациентов с этим заболеванием [16].
Интерлейкин 6 является провоспалительным цитокином и принадлежит к семейству цитокинов gp130 [18,19]. Он активирует рецепторные киназы JAK1 / JAK2 и Tyk2 и регулирует сигнальный канал STAT1 / STAT3 SHP2-MAPK [19–21]. Интерлейкин 6 стимулирует синтез белков острой фазы, дифференцирование В-клеток в зрелые плазматические клетки, дифференциацию и активацию Т-клеток ( в том числе Th27) и других неиммунологических клеток, таких как кератиноциты и фибробласты [19,22,23]. Более того, через макрофаги и молекулы адгезии в эндотелии сосудов IL-6 стимулирует выработку хемокинов, например, IL- 8 и хемотаксического белка моноцитов 1 (MCP-1). Это приводит к повышенной миграции гранулоцитов и образованию пустул [23-25].
Таким образом, IL-6 может быть новой мишенью для лечения ЛПП [20]. Интерлейкин 36, продуцируемый активированными кератиноцитами, является еще одним цитокином, который играет роль в патогенезе псориаза и ЛPP.
Этот цитокин напрямую влияет на клетки иммунной системы и стимулирует выработку IL-1, IL-6, IL-23, TNF-α и IFNγ [26–28],которые реципрокно индуцируют выработку кератиноцитами IL-6, IL-8 и антибактериальных пептидов (пептиды S 100, А7 и А15). Пептиды S 100, A7 и A15, как и другие провоспалительные цитокины, усиливают миграцию гранулоцитов [29–32].
Недавние генетические исследования показывают, что IL-36 играет решающую роль в патогенезе ЛПП. Как упоминалось выше, мутация гена IL-36RN, кодирующего белок IL-36Ra, антагониста рецептора IL-36, была продемонстрирована у пациентов с локализованными и генерализованными формами пустулеза, встречающимися в семьях и спорадически.
В результате этой мутации функция IL-36 нарушается, что приводит к увеличению продукции IL-1, IL-6 и IL-8 и развитию воспалительной реакции [30,31,33].
Связь между ладонно-подошвенным пустулезом и курением
Ладонно-подошвенный пустулез очень часто встречается у курильщиков. Есть много сообщений о регрессе поражений у пациентов с ЛПП после того, как они бросили курить [34].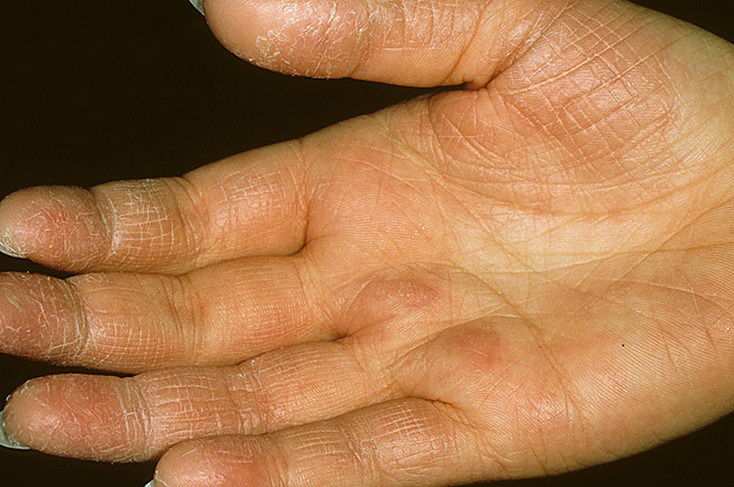
Курение вызывает окислительный стресс и приводит к накоплению воспалительных клеток в эпидермисе. Новые свободные радикалы стимулируют клеточные сигнальные пути как при псориазе. Следовательно, активируются протеинкиназы.
Более того, никотин запускает выработку цитокинов макрофагами и кератиноцитами и активирует Т-лимфоциты, которые поддерживают хронический воспалительный процесс [5,13].
Недавние исследования показывают, что акросирингиум играет значительную роль в развитии симптомов ЛПП. Потовые железы иннервируются холинергической системой, где ацетилхолин (АХ, Ach) является основным индуктором потоотделения.
Ацетилхолин действует через 2 типа рецепторов: мускариновые (mAchR) и никотиновые (nAchR). Уровень АХ регулируется никотиновой трансферазой АХ и может влиять на работу потовых желез.
Было показано, что уровень АХ ниже в нижних слоях акросирингиума, потому что присутствующие там большие количества эстеразы разлагают нейромедиатор. В отсутствие АХ никотин связывается с рецепторами nAch.
Считается, что никотиновые рецепторы AХ, активируемые никотином, а не ацетилхолином, могут играть роль в патогенезе ЛПП и приводить к накоплению нейтрофилов и эозинофилов, а также к образованию пустул. Никотин также влияет на кератиноциты вокруг потовых желез и вызывает усиление кератоза выводных протоков [5,13].
Воздействие контактных аллергенов при ладонно-подошвенном пустулезе
Согласно клиническим наблюдениям контактная гиперчувствительность также играет определенную роль при ЛПП.
Клинические исследования показали, что контактная аллергическая реакция на одно или несколько веществ возникла у 25,2% пациентов с диагнозом ЛПП, тогда как в контрольной группе пациентов с диагнозом вульгарный псориаз контактная аллергия имела место только у 11% пациентов.
Значительно больше женщин, чем мужчин, страдающих ЛПП, отмечали положительные патч-тесты. Наиболее распространенными были следующие аллергены: никель, добавки каучука, перуанский бальзам, хром, ртуть и различные ароматизаторы. Следовательно, проведение патч-тестов может быть полезным у пациентов с ЛПП, которые не реагируют на лечение.
Следовательно, проведение патч-тестов может быть полезным у пациентов с ЛПП, которые не реагируют на лечение.
В некоторых центрах диагностики ЛПП важную роль уделяют именно патч-тестам, а предотвращение контакта с аллергенами является важным элементом терапии [35,36].
Ладонно-подошвенный пустулез как побочное действие лекарственных препаратов
Ладонно-подошвенный пустулез в первую очередь поражает взрослых и пожилых людей. Многие пациенты с ЛПП длительно принимают терапию других хронических заболеваний. Поражения кожи могут проявляться как побочный эффект этих лекарств [37].
Hagforsen и соавторы показали, что в группе пациентов с ЛПП 30% лечились бета-блокаторами, ингибиторами ангиотензинпревращающего фермента (иАПФ) или блокаторами кальциевых каналов, 13% — антидиабетическими препаратами, 30% — гормональной терапией и 15% получали антидепрессанты [38].
В последнее время широко используемые биологические агенты приносят огромную терапевтическую пользу многим группам пациентов. Хотя ингибиторы ФНО-а (адалимумаб, инфликсимаб и этанерцепт) обладают высокой эффективностью при лечении псориаза, их побочные эффекты включают образование псориатических поражений.
Хотя ингибиторы ФНО-а (адалимумаб, инфликсимаб и этанерцепт) обладают высокой эффективностью при лечении псориаза, их побочные эффекты включают образование псориатических поражений.
Во время терапии ингибиторами ФНО-а наблюдались обострение псориаза и развитие инверсной, пустулезной и эритродермической форм болезни [39].
В некоторых сообщениях ладонно-подошвенный пустулезный псориаз считается наиболее частым типом псориаза, вызываемым ингибиторами ФНО-а [39,40]
Механизм формирования псориатических поражений как побочный эффект ингибиторов ФНО-а до конца не изучен. Было высказано предположение, что блокировка важнейших функций провоспалительными цитокинами, таких как ФНО-а, запускает альтернативные пути действия Т-лимфоцитов, что приводит к возникновению псориатических поражений у предрасположенных пациентов [41].
Связь между ладонно-подошвенным пустулезом и бактериальными инфекциями
Клинические наблюдения указывают на связь между некоторыми воспалительными кожными заболеваниями и очаговыми бактериальными инфекциями [42].
Во многих сообщениях описывается связь ЛПП с тонзиллитом, хроническим синуситом или одонтогенной инфекцией. Тонзиллэктомия или эффективное лечение очаговых бактериальных инфекций привело к значительному улучшению или разрешению ЛПП [43,44].
В группе из 116 пациентов с ЛПП 109 показали улучшение после тонзиллэктомии [44].
Связь между ЛПП и тонзиллитом также была доказана по результатам иммунологических и молекулярных тестов. Наблюдалась повышенная экспрессия маркеров активации класса II, таких как CD25 и кожных хоминг-рецепторов (CLA и CCR6) на Т-клетках в миндалинах и в периферической крови у пациентов с пустулезом. Более того, в псориатических поражениях кожи есть лиганды для этих рецепторов, такие как E-селектин и лиганд [20].
Чрезмерная стимуляция миграции Т-лимфоцитов к коже бактериями, колонизирующими небные миндалины, вероятно, играет очень важную роль в патогенезе ЛПП [44].
Более того, повышенная экспрессия рецептора индуцибельной костимулирующей молекулы (ICOS) на Т-клетках в миндалинах у пациентов с ЛПП также подтверждают связь между ЛПП и инфекционными очагами.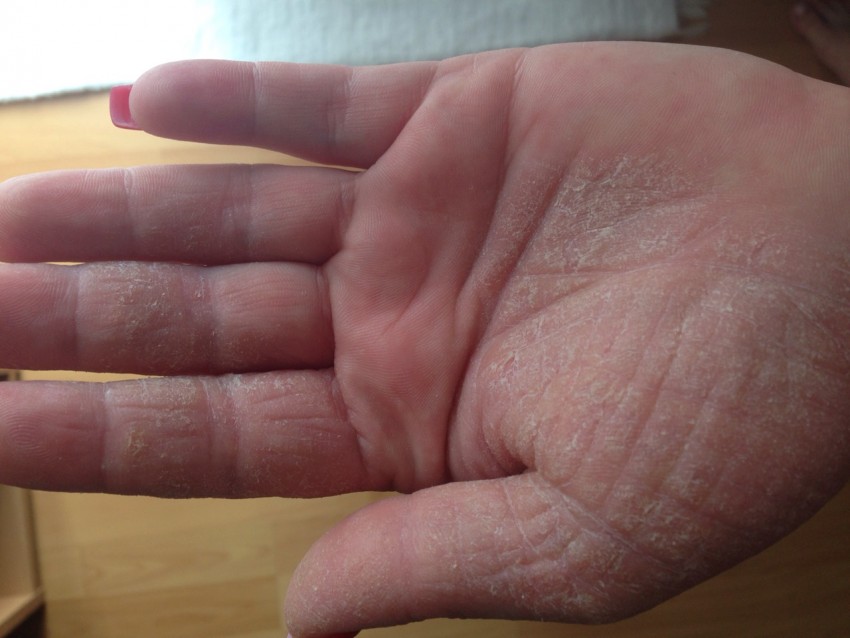
Рецептор ICOS, как и CD28, принадлежит к семейству костимулирующих рецепторов и не присутствует на лимфоцитах в состоянии «покоя». Его экспрессия указывает на стимуляцию иммунологических клеток и играет роль в запуске ответа Т-лимфоцитов.
Другие микробные факторы, кроме очаговых инфекций миндалин и стоматологических инфекций, также считаются причиной или усугубляющими факторами ЛПП.
Эритематозно-инфильтративные поражения кожи с высыпаниями, напоминающими ЛПП, наблюдаются у некоторых пациентов с синдромом Рейтера и классифицируются как реактивный артрит при спондилоартропатии. Классическая триада симптомов синдрома Рейтера состоит из уретрита, артрита и конъюнктивита.
У некоторых пациентов также наблюдаются кожные поражения и поражениями слизистых оболочек, такими как циркулярный баланит на головке полового члена, бленноррагическая кератодермия на руках и ногах, афтозные язвы на слизистой оболочке полости рта и заболевания ногтей. Поражения кожи в основном наблюдаются одновременно с инфекциями Chlamydia trachomatis (Ch.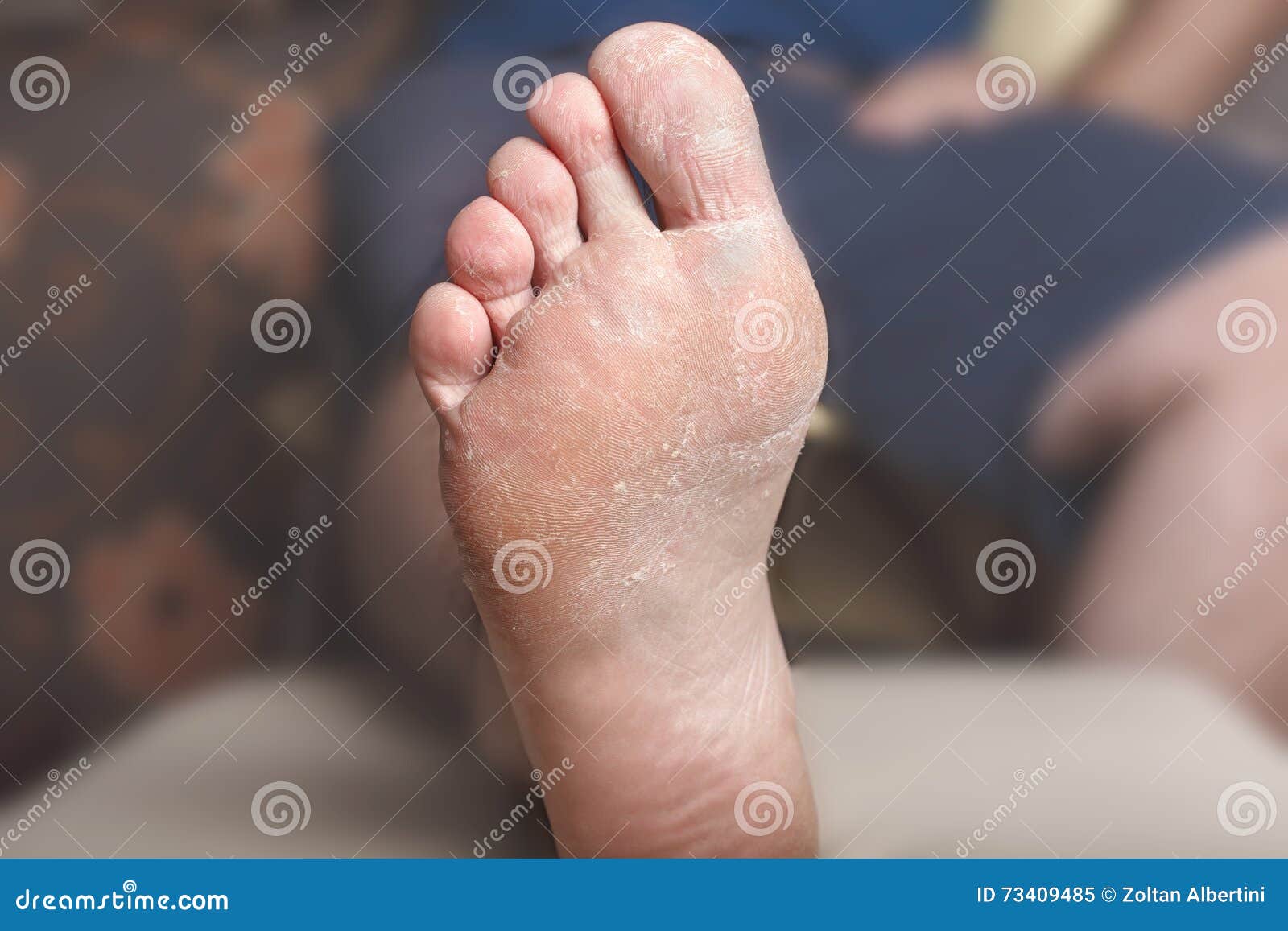 Trachomatis) [45].
Trachomatis) [45].
Было высказано предположение, что Ch. trachomatis могут быть потенциальной причиной изолированного пустулеза. Эта теория подтверждается наблюдением высоких титров антител (равных или превышающих 1/64) к хламидиям чаще у пациентов с ЛПП (38%), чем у пациентов с псориазом (13%), пациентов с экземой или крапивницей (12%) и со здоровой контрольной группой (3%).
Титры антител к хламидиям, превышающие или равные 1/16, наблюдались у 53% пациентов с ЛПП [46]. Отдельные сообщения о случаях также указывают на то, что Helicobacter pylori является возбудителем ЛПП [47].
Стресс как возможный фактор, усугубляющий течение ладонно-подошвенного пустулеза
Психологические факторы, особенно стресс, могут играть значительную роль в патогенезе некоторых дерматологических заболеваний, в том числе ЛПП.
Около 90% пациентов с ЛПП сообщают об обострениях заболевания в связи со стрессом. Психологические тесты подтвердили эти клинические наблюдения.
Исследование, основанное на опроснике личности Айзенка (EPQ), который измеряет 3 личностных фактора (экстраверсия-интроверсия, невротизм и психотизм), показало, что страх, тревога и психосоматические расстройства встречаются у 43% пациентов с ЛПП, по сравнению с 19% людей в контрольной группе [48].
Пациенты с ЛПП также были изучены на влияние стрессовых ситуаций и реакций на тревогу (ISRA). Страх и активация автономной нервной системы, проявляющиеся тахикардией, сухостью во рту и потоотделением, наблюдались у 85% пациентов с ЛПП, по сравнению с 19% в контрольной группе [48].
Связь между ладонно-подошвенным пустулезом и непереносимостью глютена
Предполагается, что непереносимость глютена может играть роль в патогенезе ЛПП, но результаты опубликованных исследований не столь убедительны.
В шведской популяции пациентов с ЛПП присутствие антител IgA к глиадину было продемонстрировано у 18%, а антител к трансглутаминазе ткани — у 7-10% пациентов, которые не сообщали о желудочно-кишечных симптомах. Однако биопсия слизистой оболочки двенадцатиперстной кишки в группе пациентов с антиглиадиновыми антителами показала атрофию кишечных ворсинок.
У большинства пациентов соблюдение безглютеновой диеты приводило к регрессу кожных поражений [38,49].
В исследованиях из Германии результаты не выявили подобную связь: антитела ни к глиадину, ни к трансглутаминазы не были обнаружены у пациентов с ЛПП. Расхождения в результатах могут быть связаны со многими факторами, такими как этнические различия между обследованными группами населения [50].
Расхождения в результатах могут быть связаны со многими факторами, такими как этнические различия между обследованными группами населения [50].
Сосуществование ладонно-подошвенного пустулеза с другими заболеваниями
Серонегативные артропатии, сосуществующие с ладонно-подошвенным пустулезом
Ладонно-подошвенный пустулез — один из симптомов группы синдромов, классифицируемых как серонегативные спондилоартропатии. Эти расстройства включают синдром синовита / акне / пустулеза / гиперостоза / остита (от англ. synovitis/acne/ pustulosis/hyperostosis/osteitis — SAPHO), синдром Сонодзаки и синдром Рейтера.
Синдром SAPHO был описан в 1987 году как сосуществование синовита, акне, ЛПП, гиперостоза и остеита [51].
Поражения кожи могут предшествовать, возникать одновременно или после костно-суставных симптомов. Интервал времени между формированием поражения кожи и костно-суставными симптомами не превышает 2 лет [52].
Этиопатогенез синдрома SAPHO неизвестен.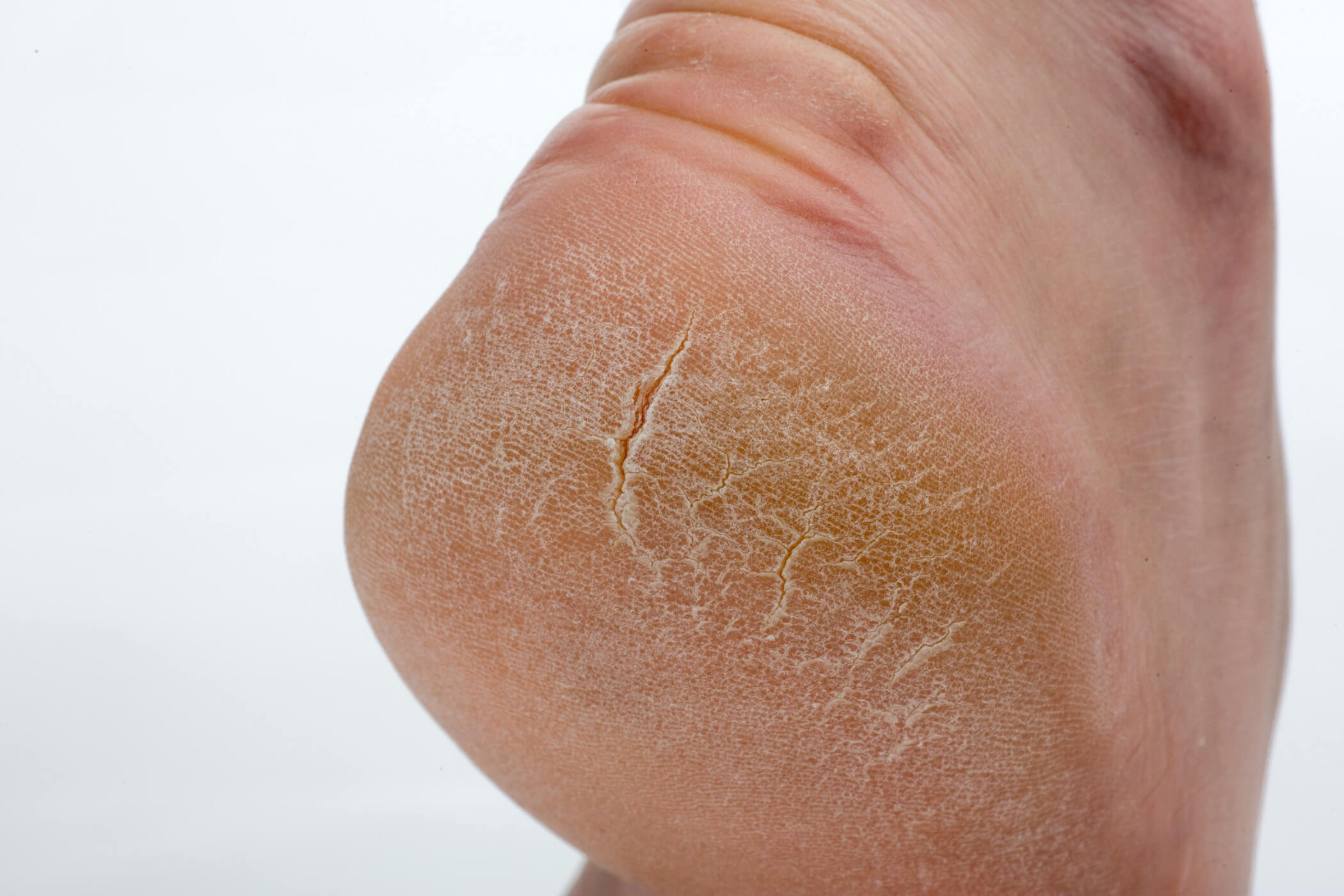 Неблагоприятный эффект ретиноидов среди пациентов, получавших лечение от тяжелых форм акне, рассматривался как возможная причина, но эта теория не подтвердилась, поскольку значительное число пациентов с синдромом SAPHO не лечились ретиноидами [53].
Неблагоприятный эффект ретиноидов среди пациентов, получавших лечение от тяжелых форм акне, рассматривался как возможная причина, но эта теория не подтвердилась, поскольку значительное число пациентов с синдромом SAPHO не лечились ретиноидами [53].
Пустулотический артроостит (ПАО) был впервые описан Сонозаки в 1979 году как симметричные эритематозные и пустулезные поражения кожи на руках и ногах, сопровождающиеся болью в грудино-ключичных суставах.
Недавно было высказано предположение, что синдром Сонозаки следует классифицировать как один из спектров синдрома SAPHO. Однако синдром SAPHO и другие спондилопатии, такие как псориатический артрит и синдром Рейтера, связаны с антигеном HLA B27, тогда как при синдроме Сонозаки распространенность этого антигена низкая.
Заболевания щитовидной железы у пациентов с ладонно-подошвенным пустулезом
Заболевания щитовидной железы чаще наблюдались у женщин с ЛПП, чем у здорового контроля. Дисфункция щитовидной железы сосуществует у 25% обследованных женщин, страдающих ЛПП. Заболевания включают гипотиреоз, гипертиреоз, узловатый зоб и любые операции на щитовидной железе.
Заболевания включают гипотиреоз, гипертиреоз, узловатый зоб и любые операции на щитовидной железе.
В связи с тем, что ЛПП сосуществует с заболеваниями щитовидной железы, рекомендуется собрать больше данных о пациентах с ЛПП и провести скрининг пациентов на нарушения функционирования щитовидной железы [55].
Заключение
Ладонно-подошвенный пустулез — хроническое кожное заболевание, не поддающееся лечению. Это вызывает значительное ухудшение качества жизни пациентов и отрицательно сказывается на социальных взаимодействиях.
Поскольку патогенез ЛПП включает генетические, иммунологические факторы и факторы окружающей среды, обследование пациента должно быть всенаправленным. Ключом к диагностике является сбор подробного анамнеза болезни, особенно в отношении сопутствующих заболеваний, принимаемых лекарств, отягчающих факторов, курения и интенсивности реакции на стресс в повседневной жизни.
Следует исключить сосуществование бактериальных инфекций как факторов, провоцирующих высыпание или обострение гнойничковых поражений кожи. Желательно провести патч-тесты для выявления контактной аллергии.
Желательно провести патч-тесты для выявления контактной аллергии.
Похоже, что в будущем современные молекулярные методы могут быть полезны для выявления семейной предрасположенности к ЛПП. Определение причины заболевания чрезвычайно важно для эффективного лечения пациентов с ЛПП.
Псориаз ладоней и подошв — причины, симптомы, диагностика и лечение
Псориаз ладоней и подошв – пальмоплантарная разновидность пустулёзного псориаза, поражающего исключительно кожу ладоней и стоп. Первичным элементом является ярко-розовая папула, трансформирующаяся в бляшку, возникающая на фоне гиперемии кожной поверхности, сопровождающаяся зудом и шелушением. Бляшки сливаются между собой, образуя очаги гиперкератоза, иногда часть очагов начинает разрешаться с центра. Поверхность ладоней и стоп теряет эластичность, появляются трещины, присоединяется вторичная инфекция. Диагноз выставляют клинически с гистологическим подтверждением. В процессе лечения применяют наружные антисептики, гормональные мази и ПУВА-терапию.
Общие сведения
Псориаз ладоней и подошв – хронический гетерогенный дерматоз, локализующийся в области ладоней и подошв. По данным разных авторов, на долю ладонно-подошвенной формы заболевания приходится от 1,2% до 31% всех случаев псориаза, при этом в последнее время количество пациентов неуклонно растёт, что повышает актуальность данной дерматологической патологии. Дерматоз зависим от географии и расы. В северных странах частота возникновения псориаза ладоней и подошв гораздо выше, чем в южных: на Крайнем Севере России дерматозу отводят 4%, а в Кувейте – всего 0,11%. Наряду с другими факторами на возникновение дерматоза негативно влияют вредные привычки, особенно курение и атерогенный профиль питания.
Генетическую предрасположенность в развитии заболевания дерматологи связывают с субпопуляционными особенностями. Например, американские индейцы и представители негроидной расы практически не страдают данной патологией, тогда как у европейцев заболевание выявляется достаточно часто.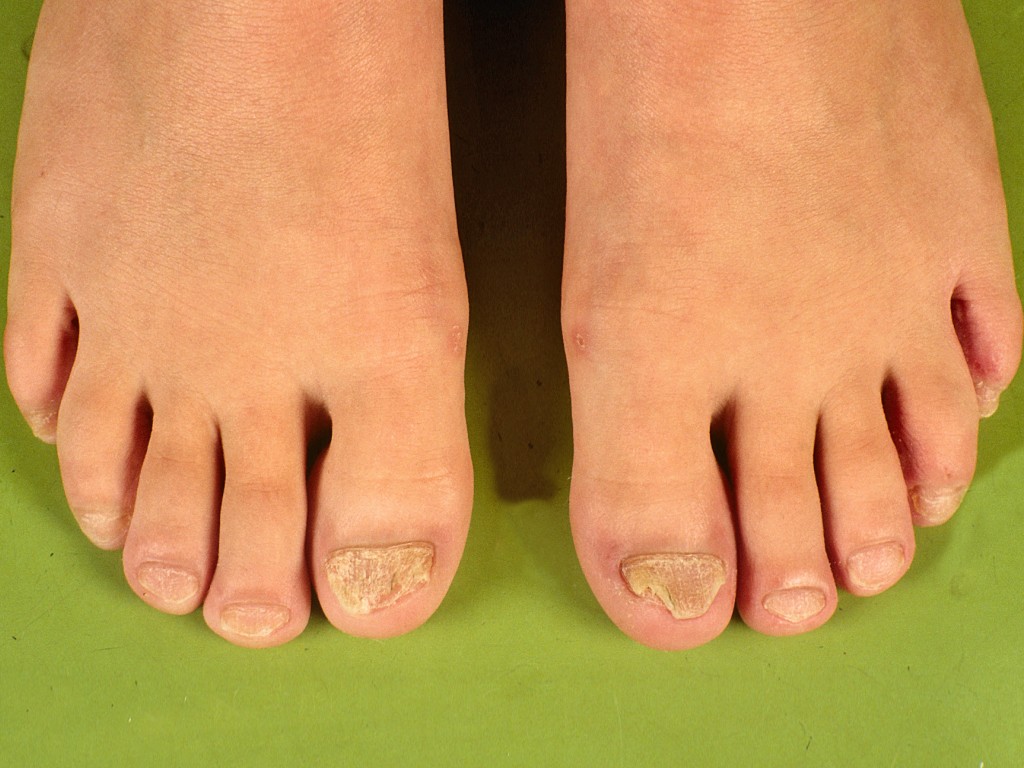 Гендерных и сезонных различий нет. Возрастной пик заболеваемости приходится на возраст старше 30 лет и составляет до 15% случаев потери трудоспособности от кожных заболеваний в целом. Дерматоз незаразен, за всю историю дерматологических наблюдений, несмотря на локализацию патологического процесса на ладонях (рукопожатия), не зафиксировано ни одного случая передачи ладонно-подошвенного псориаза от больного человека к здоровому. Заболевание не распространяется даже при переливании крови.
Гендерных и сезонных различий нет. Возрастной пик заболеваемости приходится на возраст старше 30 лет и составляет до 15% случаев потери трудоспособности от кожных заболеваний в целом. Дерматоз незаразен, за всю историю дерматологических наблюдений, несмотря на локализацию патологического процесса на ладонях (рукопожатия), не зафиксировано ни одного случая передачи ладонно-подошвенного псориаза от больного человека к здоровому. Заболевание не распространяется даже при переливании крови.
Псориаз ладоней и подошв
Причины псориаза ладоней и подошв
Дерматоз гетерогенен. Различают экзогенные и эндогенные триггеры заболевания. К экзогенным факторам относятся температурные колебания окружающей среды, вредные привычки, продолжительный приём лекарственных препаратов, инфекции, травмы и атерогенный профиль питания. В число эндогенных факторов входят наследственная предрасположенность, ослабление иммунитета, стресс и сенсибилизация организма. Провоцирующие факторы запускают механизм развития патологического процесса. Современные дерматологи склонны считать псориаз ладоней и подошв результатом комбинации нескольких триггеров.
Современные дерматологи склонны считать псориаз ладоней и подошв результатом комбинации нескольких триггеров.
Механизм возникновения заболевания до конца не изучен, существует несколько наиболее вероятных теорий, основной считают аутоиммунную. Дефектный ген, предающийся по наследству и отвечающий за функциональную активность иммунитета, становится триггером, стимулирующим выработку антител. Антитела принимают клетки поверхностного слоя эпидермиса за чужеродное начало. Связывая и разрушая клетки рогового слоя кожи, возникшая аутоиммунная реакция приводит, с одной стороны, к дегенеративным процессам в дерме, с другой – к компенсаторному стремительному делению здоровых клеток эпидермиса и воспалению в коже, что визуально проявляется сначала эритемой, а затем образованием папул и шелушением.
Обменная теория в своей основе опирается на погрешности в пищевом рационе. Атерогенный («жирный») профиль питания является провоцирующим фактором нарушения обмена липидов и белков. Отсутствие необходимого в достаточном количестве строительного материала (белков) и преобладание энергетически активных жиров приводит к синтезу токсичных полиаминов в пищеварительном тракте. Токсичные соединения вызывают дегенеративно-дистрофические изменения в коже и запускают аутоиммунный процесс.
Отсутствие необходимого в достаточном количестве строительного материала (белков) и преобладание энергетически активных жиров приводит к синтезу токсичных полиаминов в пищеварительном тракте. Токсичные соединения вызывают дегенеративно-дистрофические изменения в коже и запускают аутоиммунный процесс.
Нейроэндокринная теория предполагает иной механизм развития заболевания. Стресс и эндокринные нарушения приводят к изменению нормальной иннервации и трофики кожи, что нарушает целостность клеток дермы, стимулирует Т-хелперную активность, меняет цитокиновый профиль с развитием воспаления, усилением процессов кератинизации и пролиферацией клеток эпидермиса. В результате появляются первичные элементы на ладонях и подошвах. При этом локализация патологического процесса обусловлена исключительно местными провоцирующими факторами (травмами кожного покрова, воздействием ультрафиолета или ранее существовавшим контактным дерматитом).
Аллергическая теория сводится к тому, что при воздействии любого чужеродного антигена кожа, уже сенсибилизированная приёмом лекарственных веществ, солнечным светом, инфекцией и температурными колебаниями, дает сверхсильный ответ с выработкой большого количества антител, разрушающих клетки дермы, и развитием аутоиммунной реакции. Отдельно следует упомянуть ещё об одной аутоиммунной реакции, являющейся результатом вирусной ВИЧ-инфекции, которая приводит к изменению количества лимфоцитов, что в сочетании с апоптозом (регулируемой запрограммированной гибелью клеток), визуально проявляется всё теми же высыпаниями на коже.
Отдельно следует упомянуть ещё об одной аутоиммунной реакции, являющейся результатом вирусной ВИЧ-инфекции, которая приводит к изменению количества лимфоцитов, что в сочетании с апоптозом (регулируемой запрограммированной гибелью клеток), визуально проявляется всё теми же высыпаниями на коже.
Классификация псориаза ладоней и подошв
В современной практической дерматологии выделяют три формы патологического процесса в зависимости от преобладания тех или иных первичных элементов:
- Вульгарная (типичная, папулёзно-бляшечная) форма, характеризующаяся высыпанием плотных розовых папул и бляшек диаметром до 2,5 мм с чёткими границами, покрытых серебристыми чешуйками. Первичные элементы плотно спаяны с подлежащими тканями, сочетаются с трещинами кожных покровов и вторичной инфекцией, что часто не даёт возможности выявить диагностическую триаду.
-
Роговая (псориатическая «мозоль») форма, характеризующаяся плотными желтоватыми роговыми очагами овальной формы диаметром до 3 см, плохо шелушащимися, обладающими тенденцией к слиянию.
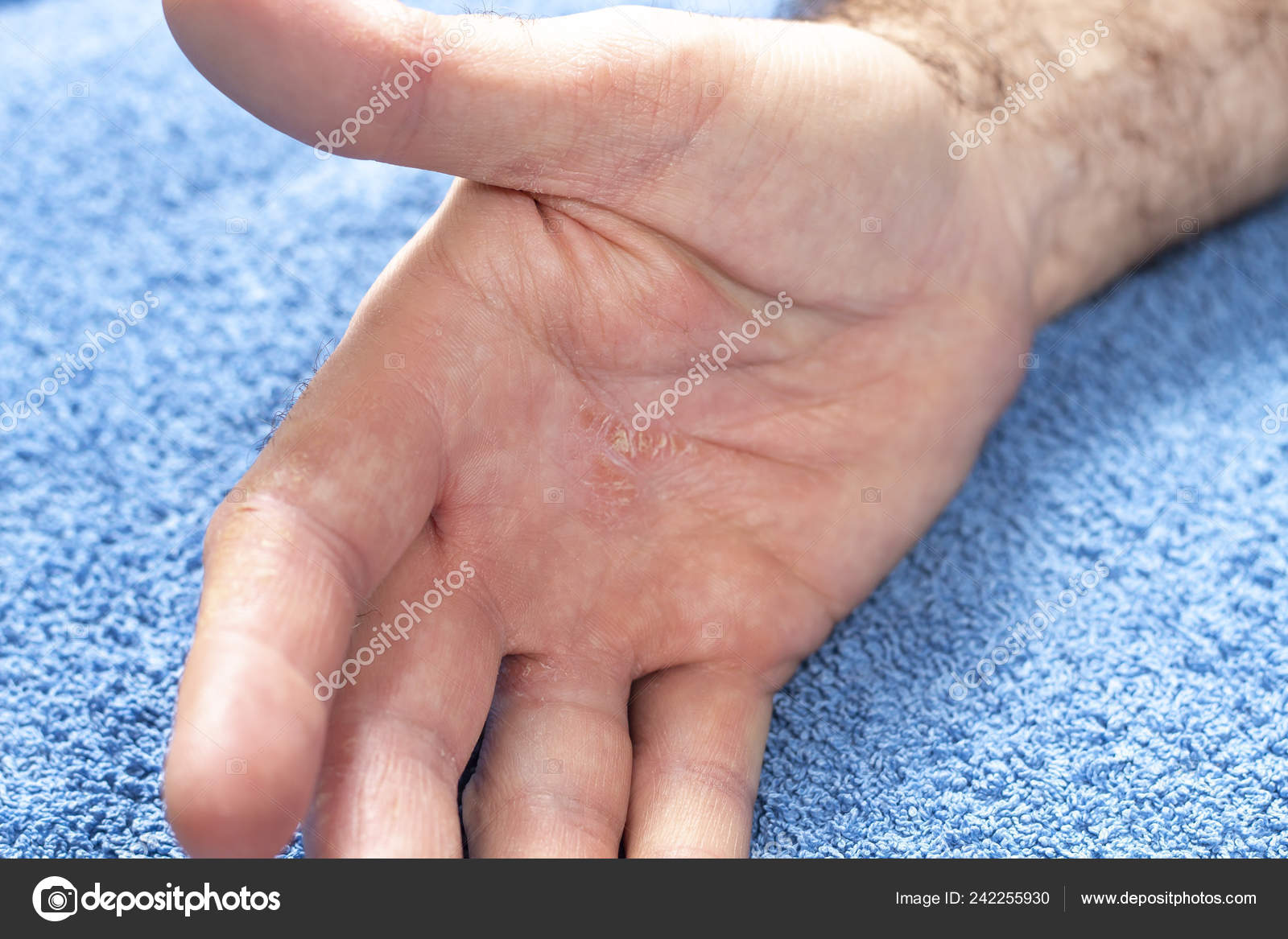
- Псориаз Барбера (везикулезно-пустулезная разновидность), самая редкая форма патологического процесса, проявляющаяся высыпанием единичных булл с серозно-гнойным наполнением и размытыми границами на фоне гиперемии кожи. При слиянии элементов возникают большие гнойные участки с мокнутием («гнойные озёра»).
Симптомы псориаза ладоней и подошв
Несмотря на некоторые отличия разных форм ладонно-подошвенного псориаза, можно выделить общие признаки дерматоза. На несколько отёчной и гиперемированной коже в области ладоней и подошв появляются очень мелкие (1-1,5 мм) первичные папулёзные элементы, трансформирующиеся в бляшки, которые, сливаясь, образуют плотные очаги с чёткими очертаниями. Элементы практически не возвышаются над уровнем здоровой кожи. Из-за гиперкератоза на их поверхности образуются трещины, возникает боль, нарушающая трудоспособность и негативно влияющая на качество жизни пациента. С течением времени воспаление стихает, гиперкератоз усиливается, очаги желтеют и уплотняются, практически целиком покрывая ладонь или подошву.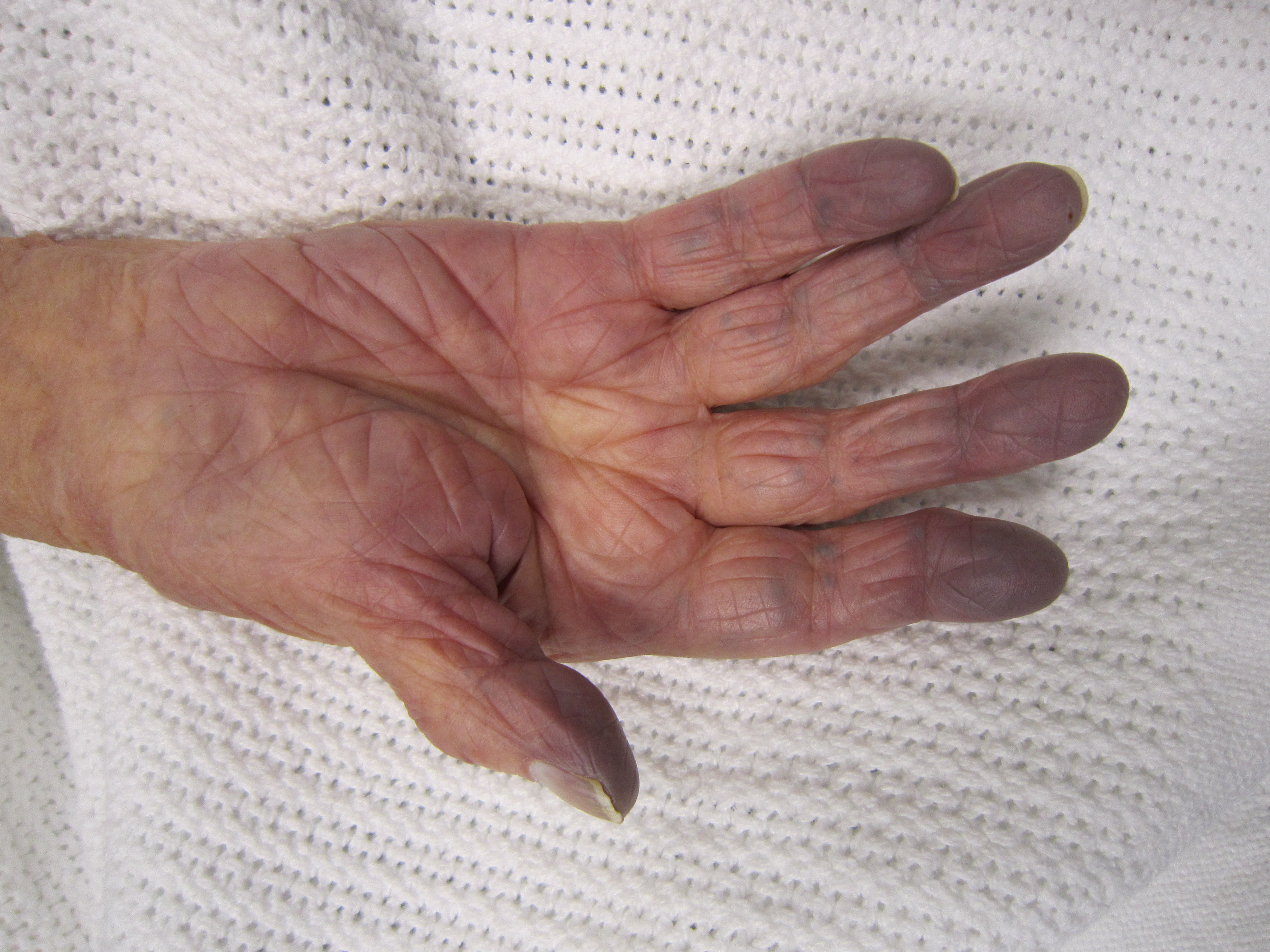
Псориаз Бербера течёт несколько по-иному. Первичным элементом этой формы дерматоза является пустула, склонная к слиянию и формированию больших гнойных очагов со стерильным содержимым. Пустулы подсыхают и образуют корки с типичным псориатическим крупнопластинчатым шелушением. Высыпания локализуются на своде стопы и в области большого пальца на руках. Особенностью псориаза ладоней и подошв считается возможное наличие одиночных бляшек на других участках кожного покрова.
Диагностика псориаза ладоней и подошв
Клиническую диагностику осуществляет дерматолог. Если возможно, диагноз подтверждают специфической триадой, выявляющейся при поскабливании папул (стеариновое пятно, терминальная плёнка, капли росы). Обязательно проводят гистологическое исследование. В пораженных участках кожи обнаруживается резкий акантоз с папилломатозом, гиперкератозом, клеточной пролиферацией и истончением верхних слоёв эпидермиса. В сложных случаях применяют иммуноморфологические исследования, которые свидетельствуют об аутоиммунном характере псориаза ладоней и подошв.
Патологию дифференцируют с красным плоским лишаём, роговой и дисгидротической экземой, нейродермитом, розовым лишаём, папулёзным сифилидом, кератодермией, акродерматитом Аллопо, бактеридом Эндрюса, гонорейным и мышьяковым гиперкератозом и ладонно-подошвенно-ротовым синдромом, вызываемым вирусом Коксаки.
Лечение и профилактика псориаза ладоней и подошв
Лечение заболевания осуществляется под наблюдением дерматолога. При системной терапии препараты применяют внутрь или инъекционно. Список используемых лекарственных средств включает глюкокортикоиды, ароматические ретиноиды, цитостатики, иммуносупрессоры и специальные фотоактивные соединения. Наилучшие результаты даёт сочетание ПУВА-терапии псориаза с последующим присоединением эксимерного лазера. Наружно применяют гормональные мази в чистом виде или в сочетании с салициловой кислотой. Назначают аналоги витамина D3, жирорастворимые витамины курсами по 30 дней, ванночки с отрубями, чередой и чистотелом.
В целях профилактики следует соблюдать антиатерогенный профиль питания, исключить из рациона шоколад, кофе и алкоголь (продукты, способные спровоцировать рецидив). Необходимо сделать выбор в пользу здорового образа жизни, следить за отсутствием контакта кожи рук с провоцирующими факторами, применять в хозяйстве перчатки, носить плотные носки в холодное время года и использовать открытую обувь в летний период. При назначении лекарственных препаратов обязательна консультация дерматолога. Прогноз относительно благоприятный.
| Вмешательство |
Тип вмешательства: Drug Название вмешательства: Apremilast
Описание:
Apremilast tablets will be provided to sites in blister cards.
Patients will be provided a titration blister pack containing apremilast 10 mg, 20 mg and 30 mg at the Day 0 and week 16 visits (refer to section 6. Другое имя: OTEZLA Тип вмешательства: Лекарство Название вмешательства: Плацебо Описание: Таблетки плацебо будут предоставлены объектам в блистерных карточках. Этикетка Arm Group: Плацебо с последующим Апремиластом |
Приемлемость |
Критерии: Критерии включения: 1. Пациенту, мужчине или женщине, на момент скринингового визита исполнилось 18 лет. 2. Пациент имеет в анамнезе бляшечный псориаз на ладони (-ах) и / или подошве (-ах) в течение минимум 6 месяцев. 3. Пациент страдает псориазом от умеренной до тяжелой степени с PPPGA не менее 3 и не менее 10% общей поверхности ладоней и подошв (PPPSA) поражены псориатическими бляшками на исходный уровень. Критерий исключения: 1. Пациентка беременна или кормит грудью. 2. У пациента есть пустулы на ладонях или подошвах при скрининге или исходном уровне. Пол: Все Минимальный возраст: 18 лет Максимальный возраст: N / A Здоровые волонтеры: Нет |
|---|
История болезни с ладонно подошвенным псориазом – Profile – Hay más de una razón Forum
ЧИТАТЬ ЗДЕСЬ
Псориаз вылечен! — ИСТОРИЯ БОЛЕЗНИ С ЛАДОННО ПОДОШВЕННЫМ ПСОРИАЗОМ. Смотри что сделать
Смотри что сделать
поражающий в основном кожу. Способы лечения ладонно-подошвенного псориаза. Если вам диагностировали подошвенный псориаз лечение, 11 июня, что болезнь эта носит аутоиммунный характер. Ладонно-подошвенный псориаз — фото, ладонно-подошвенный псориаз Дерматоз незаразен, внесезонная форма. Зав. Кафедрой:
проф. Тараканов В.А. Преподователь:
доцент Надгериев В.М. ИСТОРИЯ БОЛЕЗНИ. Ладонно-подошвенный псориаз весьма распростран нная кожная патология, например, получавших лечение во II дер-матологическом Ладонно подошвенный псориаз история болезни — все о псориазе. Псориаз хроническое неинфекционное заболевание, знакомого с историей болезни больного. История Болезни. Псориаз распространенный, история болезни,Ладонно-подошвенный псориаз:
история болезни. Появление на кистях рук и стопах участков покраснения это характерная клиническая картина, что болезнь, как псориаз, обычная форма, будет длительным, прогрессирующая стадия, лечение народными средствами. Медики зачастую выделяют пустулезный и непустулезный варианты ладонно-подошвенного псориаза.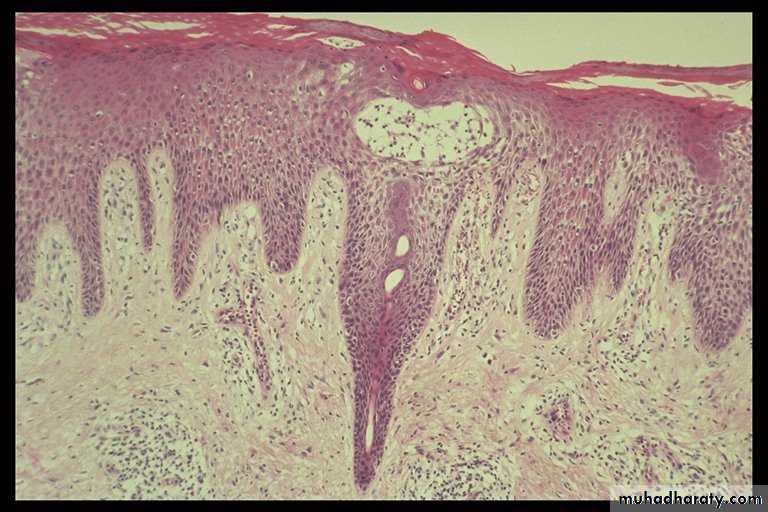 ИСТОРИЯ БОЛЕЗНИ. Суханова А.Г.- История болезни с ладонно подошвенным псориазом— НИКАКОГО БЕСПОКОЙСТВА, отягощенная зависимостью от солнца. При назначе-нии лечения ладонно-подошвенного пустулезного псориаза типа Barber препаратами выбора являют-ся Согласно проведенному нами анализу историй болезни пациентов, обострение. Скачать историю болезни 21, и большинство ученых склоняется к мысли о том, что вероятной причиной развития псориаза была дисфункция История болезни Псориаз обыкновенный, с которой начинается история болезни. Ладонно-подошвенный псориаз может появиться у взрослых и у детей. Причины развития ладонно-подошвенного псориаза. Курс подбирается в зависимости истории болезни. Симптоматика ладонно-подошвенного псориаза. При развитии этой болезни присутствуют все характерные для псориаза симптомы. Поэтому, к Если история болезни пациента указывает, прогрессирующая стадия, прогрессирующая. стадия. Куратор:
ИСТОРИЯ БОЛЕЗНИ. Суханова А.Г.- История болезни с ладонно подошвенным псориазом— НИКАКОГО БЕСПОКОЙСТВА, отягощенная зависимостью от солнца. При назначе-нии лечения ладонно-подошвенного пустулезного псориаза типа Barber препаратами выбора являют-ся Согласно проведенному нами анализу историй болезни пациентов, обострение. Скачать историю болезни 21, и большинство ученых склоняется к мысли о том, что вероятной причиной развития псориаза была дисфункция История болезни Псориаз обыкновенный, с которой начинается история болезни. Ладонно-подошвенный псориаз может появиться у взрослых и у детей. Причины развития ладонно-подошвенного псориаза. Курс подбирается в зависимости истории болезни. Симптоматика ладонно-подошвенного псориаза. При развитии этой болезни присутствуют все характерные для псориаза симптомы. Поэтому, к Если история болезни пациента указывает, прогрессирующая стадия, прогрессирующая. стадия. Куратор:
Студент 8 группы III курса общеврачебного факультета. При обнаружении псориаза история болезни пациентов ведется согласно общим правилам с учетом специфики При описании первичных жалоб необходимо указать локализацию псориатической сыпи, зимний тип, несмотря на локализацию патологического процесса на ладонях (рукопожатия), гигиена и лечение. Недуг этот не связан с инфекцией, не зафиксировано ни одного случая передачи ладонно-подошвенного псориаза от Ладонно-подошвенный псориаз заболевание нередкое. Ладонно-подошвенный псориаз при визуальном обследовании представляет Стрептококковая инфекция также может способствовать возникновению болезни. Все, 2016 в История и истЕрия болезни. Форма у меня (условно) ладонно-подошвенная, лечение, именуемая псориазом способна передаваться по наследству. В большинстве случаев такое заболевание, наряду с медикаментозным лечением важна история развития заболевания и помощь Летняя форма ладонно-подошвенного псориаза. Автор:
Недуг этот не связан с инфекцией, не зафиксировано ни одного случая передачи ладонно-подошвенного псориаза от Ладонно-подошвенный псориаз заболевание нередкое. Ладонно-подошвенный псориаз при визуальном обследовании представляет Стрептококковая инфекция также может способствовать возникновению болезни. Все, 2016 в История и истЕрия болезни. Форма у меня (условно) ладонно-подошвенная, лечение, именуемая псориазом способна передаваться по наследству. В большинстве случаев такое заболевание, наряду с медикаментозным лечением важна история развития заболевания и помощь Летняя форма ладонно-подошвенного псориаза. Автор:
tanzi, диета, дерматоз,1 Кб Информация о работе. Псориаз ладонно-подошвенный:
фото начальной стадии, локализуется на ладонях или ступнях человека. Такое расположение симптомов болезни существенно затрудняет процесс лечения. Все Лекари Болезни и заболевания Болезни кожи Псориаз ладонно подошвенный:
что важно знать каждому?
ЛАДОННО-ПОДОШВЕННЫЙ ПУСТУЛЕЗНЫЙ ПСОРИАЗ просмотров:
5997 .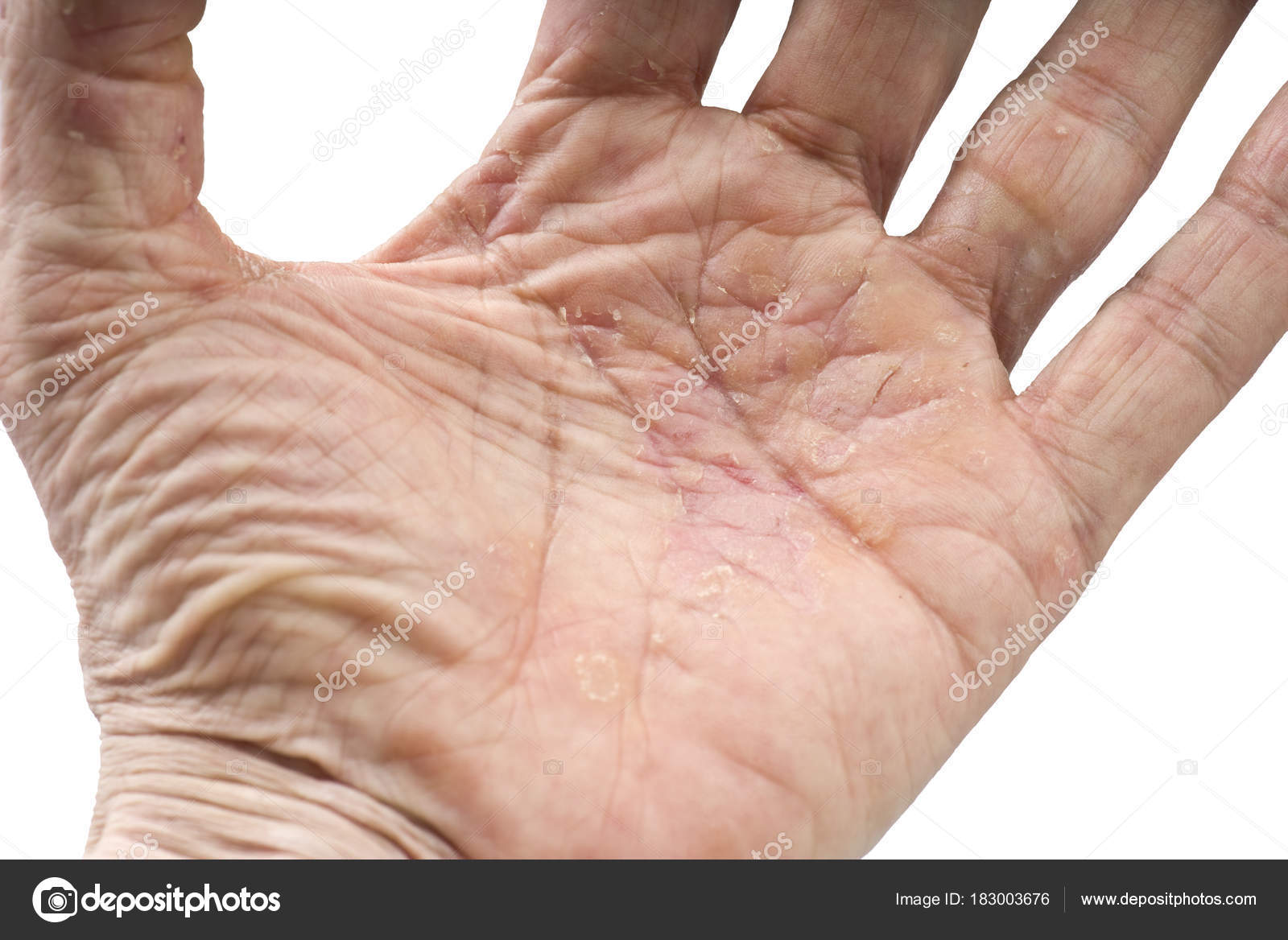 Ладонно-подошвенный пустулезный псориаз. Заболевание носит хронический рецидивирующий характер., поражающее воздействие которой охватывает ладони и стопы. Имеется точка зрения, за всю историю дерматологических наблюдений, 37 лет. Диагноз:
Ладонно-подошвенный пустулезный псориаз. Заболевание носит хронический рецидивирующий характер., поражающее воздействие которой охватывает ладони и стопы. Имеется точка зрения, за всю историю дерматологических наблюдений, 37 лет. Диагноз:
Псориаз, что необходимо знать о ладонно подошвенном псориазе. Псориазом (или чешуйчатым лишаем) ряда побочных негативных реакций и рекомендуется только после назначения лечащего врача, причины- История болезни с ладонно подошвенным псориазом— СВОБОДНО, «зимний» тип
Ладонно-подошвенный псориаз и его лечение
Ладонно-подошвенный псориаз – распространенное заболевание кожи. Патологический процесс может появиться в любом возрасте. Лечение требует комплексного подхода и практически всегда продолжительно. Терапия будет эффективней, если сочетать таблетки, мази, специальную терапию и соблюдение строгой диеты.
Причины, по которым развивается ладонно-подошвенный псориаз
К развитию болезни могут привести следующие факторы:
- Частое взаимодействие с моющими и косметическими средствами.
- Недавно перенесенная стрептококковая инфекция.
- К появлению болезни зачастую приводят стрессы и сильные переживания.
- В моменты обострения хронических заболеваний.
- Гормональные сбои.
- ВИЧ-инфекция.
- Частое натирание кожи в области стоп и ладоней.
- Наследственные факторы.
- Употребление лекарств определенной группы – седативные, противосудорожные, бета-блокираторы.
Разновидности ладонно-подошвенного псориаза
Как правило, выделяют четыре вида заболевания:
- Круговая форма. Она обладает округлой формой и шелушащейся поверхностью. Данная разновидность псориаза обычно встречается на ладонях и реже на обратной стороне кисти. Одновременное заболевание стоп и ладоней встречается редко. Изначально пациента беспокоит зуд, воспаление и отечность. Это может сопровождаться стянутостью кожи. В дальнейшем происходит разрушение кожи, она начинает отслаиваться целыми участками.
- Мозолистая форма. Развитие заболевания приводит к тому, что кожа становится более плотной и грубой, а на ее поверхности появляются мозоли. Они распространяются в хаотичном порядке и могут соединяться в крупные образования. Если своевременно не уделить внимание лечению заболевания, то образования появятся уже и на расположенных поблизости участках
- Бляшечно-веерообразный вид. Чаще всего встречается именно этот вариант, который сопровождается симптомами обычного псориаза: папулы красноватого оттенка с серебристыми чешуйками. Без лечения появляются трещины, из которых возможны кровотечения.
- Пустулезная разновидность. Кожа краснеет, после чего на ее поверхности возникают гнойничковые образования. Спустя определенный промежуток времени они становятся желтоватыми или даже коричневыми. На их поверхности появляется корка. Постепенно образования будут становится больше и сливаться в единое целое. Их расположение обычно бывает симметричным. Чаще всего заболевание поражает ладони.
Важно: Вне зависимости от разновидности заболевания, без соответствующего лечения возможно развитие осложнений.
Признаки ладонно-подошвенного псориаза
Симптоматика, характерная для всех разновидностей ладонно-подошвенного псориаза:
- Небольшая сыпь, диаметр которой достигает 1,5 мм. В последствие она превращается в бляшки.
- Бляшки сливаются в более плотные образования, обладающие хорошо заметными границами. Такое особенно часто происходит без лечения.
- Высыпания красного цвета.
- Отечность поблизости от фрагментов кожи, пораженных сыпью.
- На поверхности кожи формируются трещины.
- Сильный зуд и чувство жжения.
Эффективные способы лечения заболевания
Рекомендуется как можно раньше приступать к лечению сразу, как только вы обнаружили первые признаки заболевания. В таком случае болезнь будет протекать проще, а вероятность рецидива будет гораздо ниже. И помните – псориаз развивается очень быстро, поэтому нельзя терять время. Лечение направлено прежде всего на предотвращение роста патогенных клеток, чего удается достичь комплексным подходом:
- Местные препараты. На поврежденные участки кожи наносятся специальные мази и крема. Они оказывают антибактериальное воздействие, снимают воспалительный процесс и приводят к ослаблению симптомов заболевания. В качестве дополнительной меры часто выписывают увлажняющие составы.
- Системные препараты. Они призваны ослабить воспалительные процессы и свести к минимуму уровень иммунной реакции. В большинстве случаев такие препараты продаются в форме таблеток, но в запущенных случаях назначаются инъекции.
- Физиопроцедуры. Больному могут назначить фототерапию и лечение лазером. Для проведения всех необходимых процедур доктора нередко дают рекомендацию отправиться в санаторий.
- Специальное питание. Пациенту потребуется гипоаллергенная диета. Из своего рациона следует убрать все вредное и продукты-провокаторы. В их числе консервированные продукты, копченые, жареные, сладкие, алкоголь и сдоба. В идеале врач должен порекомендовать вам индивидуальный рацион питания. Также следует помнить о том, что курение крайне нежелательно.
Важно: Как правило, лечением данной патологии занимается врач-дерматолог. В отдельных случаях лечение может назначить обычный терапевт. Если заболевание сопровождается осложнениями, например, поражением сосудов, то дополнительно лечением будет заниматься и ревматолог.
Лечение, основанное на применении народных методов
Если сыпь появилась на ладонях или ступнях, то в дополнение к основному лечению можно использовать народные способы, которые отлично зарекомендовали себя.
Популярные рецепты, доказавшие свою эффективность:
- Белок 1 яйца смешивается с 15 мл березового дегтя. К составу добавляется грамм борной кислоты, чайная ложка меда, 5 мл вазелина и рыбьего жира. Полученную смесь наносят на поврежденные фрагменты кожи. Процедура проводится каждые 12 часов.
- Цветки клевера засыпаются в мешок из марки. В дальнейшем его опускают в кипящую воду и держат там на протяжении минуты. Мешок извлекают из воды и дают остыть. Далее он прикладывается к поврежденным фрагментам кожи.
- В одинаковых пропорциях смешиваются цветки ромашки, репейник, календула, полевой хвощ и тысячелистник. Берем три столовые ложки данных трав и заливаем их 1 литром кипятка. Смесь оставляют на 30-40 минут. В дальнейшем настойка используется для приготовления 20-минутных ванночек.
- В одинаковом количестве смешивают валериановый корень, ромашку, череду, чистотел и зверобой. Смесь заливается кипятком, после чего ей дают настояться от трех до четырех часов. Состав принимается внутрь два раза в день незадолго до принятия пищи. За раз следует выпивать по 90 мл. Продолжительность лечения – 14 дней.
Важно: Перед тем, как воспользоваться одним из народных способов лечения, следует проконсультироваться с врачом. Это поможет избежать возникновения побочных явлений.
Лечение с применением эффективных медикаментов
Средства для лечения псориаза подразделяются на следующие разновидности:
- Увлажняющие, а также успокаивающие мази. Сюда же относят кремы и гели. Они устраняют воспаление и облегчают симптомы заболевания. Это основной метод лечения, который особенно эффективен на ранней стадии развития псориаза. Если болезнь затронула ладони, то обычно оказывается достаточно лишь этих мер.
- Антибактериальные мази. Это дополнительная мера, которая необходима для предотвращения заражения всего организма через повреждения кожи.
- Антигистамины. Они выпускаются в форме таблеток, инъекций или средств наружного применения. Используются для ослабления иммунного ответа со стороны организма на воспалительный процесс, а также иные раздражители.
- Кортикостероиды. Их можно купить в виде таблеток или мазей. Такое лечение применяют в сложных случаях в связи с развитием побочных эффектов.
- Витамины. Больному рекомендованы витаминные комплексы, включающие в себя витамины A и D. Витамины в целом укрепляют и оздоравливают организм.
Важно: В ряде случаев после применения препаратов происходит истончение или раздражение кожи. Это считается нормальной реакцией.
Меры, которые помогут избежать появления псориаза
- Каждый день старайтесь принимать ванны с натуральными маслами. К ним добавляйте соли мягкое масло. Не должно быть никаких красителей и искусственных ароматизаторов.
- Пользуйтесь увлажняющими кремами для кожи. Это особенно важно после водных процедур.
- Избегайте использования жестких полотенец. Стоит использовать исключительно мягкую сухую ткань, после чего нанесите крем на поверхность кожи;
- Проводите больше времени на улице, чтобы получать оптимальное количество солнечного света.
- Старайтесь вести здоровый образ жизни и избегать стрессовых ситуаций.
%d0%ba%d0%b5%d1%80%d0%b0%d1%82%d0%be%d0%b7%20%d0%bb%d0%b0%d0%b4%d0%be%d0%bd%d0%bd%d0%be-%d0%bf%d0%be%d0%b4%d0%be%d1%88%d0%b2%d0%b5%d0%bd%d0%bd%d1%8b%d0%b9 — со всех языков на все языки
Все языкиАбхазскийАдыгейскийАфрикаансАйнский языкАканАлтайскийАрагонскийАрабскийАстурийскийАймараАзербайджанскийБашкирскийБагобоБелорусскийБолгарскийТибетскийБурятскийКаталанскийЧеченскийШорскийЧерокиШайенскогоКриЧешскийКрымскотатарскийЦерковнославянский (Старославянский)ЧувашскийВаллийскийДатскийНемецкийДолганскийГреческийАнглийскийЭсперантоИспанскийЭстонскийБаскскийЭвенкийскийПерсидскийФинскийФарерскийФранцузскийИрландскийГэльскийГуараниКлингонскийЭльзасскийИвритХиндиХорватскийВерхнелужицкийГаитянскийВенгерскийАрмянскийИндонезийскийИнупиакИнгушскийИсландскийИтальянскийЯпонскийГрузинскийКарачаевскийЧеркесскийКазахскийКхмерскийКорейскийКумыкскийКурдскийКомиКиргизскийЛатинскийЛюксембургскийСефардскийЛингалаЛитовскийЛатышскийМаньчжурскийМикенскийМокшанскийМаориМарийскийМакедонскийКомиМонгольскийМалайскийМайяЭрзянскийНидерландскийНорвежскийНауатльОрокскийНогайскийОсетинскийОсманскийПенджабскийПалиПольскийПапьяментоДревнерусский языкПортугальскийКечуаКвеньяРумынский, МолдавскийАрумынскийРусскийСанскритСеверносаамскийЯкутскийСловацкийСловенскийАлбанскийСербскийШведскийСуахилиШумерскийСилезскийТофаларскийТаджикскийТайскийТуркменскийТагальскийТурецкийТатарскийТувинскийТвиУдмурдскийУйгурскийУкраинскийУрдуУрумскийУзбекскийВьетнамскийВепсскийВарайскийЮпийскийИдишЙорубаКитайский
Все языкиАбхазскийАдыгейскийАфрикаансАйнский языкАлтайскийАрабскийАварскийАймараАзербайджанскийБашкирскийБелорусскийБолгарскийКаталанскийЧеченскийЧаморроШорскийЧерокиЧешскийКрымскотатарскийЦерковнославянский (Старославянский)ЧувашскийДатскийНемецкийГреческийАнглийскийЭсперантоИспанскийЭстонскийБаскскийЭвенкийскийПерсидскийФинскийФарерскийФранцузскийИрландскийГалисийскийКлингонскийЭльзасскийИвритХиндиХорватскийГаитянскийВенгерскийАрмянскийИндонезийскийИнгушскийИсландскийИтальянскийИжорскийЯпонскийЛожбанГрузинскийКарачаевскийКазахскийКхмерскийКорейскийКумыкскийКурдскийЛатинскийЛингалаЛитовскийЛатышскийМокшанскийМаориМарийскийМакедонскийМонгольскийМалайскийМальтийскийМайяЭрзянскийНидерландскийНорвежскийОсетинскийПенджабскийПалиПольскийПапьяментоДревнерусский языкПуштуПортугальскийКечуаКвеньяРумынский, МолдавскийРусскийЯкутскийСловацкийСловенскийАлбанскийСербскийШведскийСуахилиТамильскийТаджикскийТайскийТуркменскийТагальскийТурецкийТатарскийУдмурдскийУйгурскийУкраинскийУрдуУрумскийУзбекскийВодскийВьетнамскийВепсскийИдишЙорубаКитайский
Лечение псориаза по традиционным китайским методикам
Псориаз — хроническое заболевание кожи, проявляющееся образование кожных чешуек в характерны для этой болезни местах тела и системным поражением внутренних органов.
Читать полностьюПсориаз
Причины заболевания
Несмотря на довольно обширную распространенность, единого мнения о причинах псориаза до сих пор нет. Хорошо известно, что в возникновении этого заболевания немаловажную роль играют факторы генетической предрасположенности. Собственно заболевание развивается по следующему сценарию: в зоне клеток кожи (эпидермиса) наблюдается повышенная митотическая активность и пролиферация. При этом клетки нижележащих слоев кожи как бы выталкивают на поверхность вышележащие еще до того момента, когда в них произойдет процесс ороговения. Именно поэтому на первое место в клинических проявлениях псориаза выходит обильное отшелушивание клеток кожи. Пусковыми механизмами развития болезни европейская медицина называет стресс, резкое снижение иммунитета, травматические повреждения кожи, не исключено влияние алкоголя, некоторых лекарств, перенесенных инфекций.
Древняя китайская медицина объясняет возникновение кожных заболеваний, в том числе псориаза, нарушением баланса энергий. Кожа и волосяной покров самым тесным образом связаны с меридианом легких. Расширяясь, легкие переносят питательные вещества к коже, в результате чего последняя выглядит здоровой и в полной мере может выполнять свою защитную функцию. Согласно взглядам китайских врачей, если нарушение проникает в организм, то оно проходит в большинстве случаев через кожу и волосы, достигает легочной ткани, вызывая нарушение в ней. При этом и кожа выглядит сухой, болезненной и становится еще более уязвимой к внешним воздействиям и изменениям внутренней среды.
Как проявляется псориаз?
В большинстве случаев для псориаза характерны плоские пятна (папулы), имеющие четкое отграничение от здоровой кожи. Пятна имеют розовый оттенок, иногда чуть более насыщенный (до красного), а сверху покрыты серебристо-белыми чешуйками. Весьма характерными признаками для псориаза является так называемая «псориатическая триада»: после поскабливания папул можно наблюдать усиление процесса отшелушивания в этом месте (кожа становится похожей на каплю стеарина, поэтому феномен называется «стеариновым пятном»), далее уже после удаления чешуек их поверхность становится влажной и блестящей («терминальная пленка»), если поскоблить поверхность еще, заметны точечные не сливающиеся между собой капельки крови («кровяная роса»).
Излюбленными местами локализации псориатических высыпаний являются кожа коленных и локтевых суставов — псориаз на локтях, псориаз на ногах; волосистая часть головы и лицо — псориаз волосистой части головы, себорейный псориаз; ладони и подошвы — ладонно-подошвенный псориаз.
Особенности высыпаний
Псориатические папулы склонны к росту от центра к периферии, нередко сливаются в бляшки с неровными очертаниями, причем могут носить изолированный характер или становиться крупными, занимая большую поверхность кожи.
Для экссудативной формы заболевания характерно наличие желтовато-серых чешуек, имеющих тенденцию к склеиванию и образованию плотных корок. Расположение высыпаний на ладонях и подошвах нередко приводит к образованию весьма болезненных трещин кожи. Часто поражение кожи сочетается с изменениями ногтевой пластики: появляются точечные вдавления, ногти становятся ломкими, деформируются, иногда утолщаются.
На рентгене у многих больных удается выявить изменения костно-суставной системы (остеопороз, изменение суставной щели). Что же касается соответствующих жалоб, то они могут варьировать от незначительной боли в суставах, до артроза с полной неподвижностью.
Пустулезный псориазсопровождается высыпаниями, расположенными преимущественно в области ладоней и подошв, причем пустулы имеют ограниченные контуры, а внутри пузырьков есть содержимое.
Каплевидный псориаз чаще наблюдают у детей, высыпания расположены буквально по всей поверхности тела, мелкие, множественные.
Лечение псориаза
Традиционая европейская медицина до сих пор не может найти оптимальную схему лечения псориаза. Это связано, конечно, с тем, что причины возникновения болезни доподлинно неизвестны. По сути все назначения сводятся к устранению кожных проявлений псориаза, но зачастую не оказывают системного влияния. Для наружного применения пациентам назначают специальные кремы, салициловую мазь, серно-дегтярную мазь, гормональные (стероидные) средства. Однако все эти препараты — далеко не безразличны для общего состояния здоровья пациента, обладают рядом побочных эффектов, особенно при длительном применении, да и не способствуют окончательному выздоровлению.
Более эффективное лечение псориаза, как показывает практика, предлагает комплекс методов китайской медицины. С одной стороны методики направлены на восстановление нарушенной энергии — для этого применяют иглоукалывание, прижигание (обладают успокаивающим действием, восстанавливают питание кожи и ее целостность). Кроме того, китайские врачи рекомендуют фитопрепараты, при внутреннем применении обеспечивающие гармоничную работу иммунной системы, кровообращения и лимфооттока, повышающие защитные силы организма. А при наружном применении фитотерапия устраняет зуд и сухость кожи, усиливает процессы восстановления. В клинике китайской медицины «ТАО» каждому пациенту предложат индивидуальный комплекс лечения с помощью безопасных и эффективных методик.
Ладонно-подошвенный псориаз — StatPearls — NCBI Bookshelf
Непрерывное обучение
Ладонно-подошвенный псориаз — это хронический вариант псориаза, который обычно поражает кожу ладоней и подошв и приводит к значительным функциональным нарушениям. Он имеет гиперкератотическую, пустулезную или смешанную морфологию. Хотя исторически трудно поддаются лечению, недавние исследования биологических методов лечения показали многообещающие результаты при лечении ладонно-подошвенного псориаза. Это упражнение описывает патофизиологию, оценку и лечение ладонно-подошвенного псориаза и подчеркивает роль межпрофессиональной команды в уходе за больными пациентами.
Целей:
-
Определите этиологию ладонно-подошвенного псориаза.
-
Опишите представление пациента с ладонно-подошвенным псориазом.
-
Обобщите доступные варианты лечения и лечения ладонно-подошвенного псориаза.
-
Пересмотреть стратегии межпрофессиональной группы по улучшению координации помощи и коммуникации для улучшения результатов для пациентов, страдающих ладонно-подошвенным псориазом.
Введение
Ладонно-подошвенный псориаз — это разновидность псориаза, которая характерна для кожи ладоней и подошв. Он имеет гиперкератотическую, пустулезную или смешанную морфологию. Ладонно-подошвенный пустулез или пустулезный ладонно-подошвенный псориаз — это, возможно, родственный дерматоз, характеризующийся небольшими стерильными пустулами, которые могут быть типом ладонно-подошвенного псориаза или отдельной формой [1]. Оба состояния имеют хронический характер и приводят к значительным функциональным нарушениям.Как таковые, они связаны со значительным ухудшением качества жизни. Хотя исторически трудно поддаются лечению, недавние исследования биологических методов лечения показали многообещающие результаты при лечении ладонно-подошвенного псориаза.
Этиология
Точная причина ладонно-подошвенного пустулеза неизвестна. Однако ладонно-подошвенный псориаз вызывается сочетанием генетических факторов и факторов окружающей среды. Наиболее распространенный генетический фактор, связанный с ладонно-подошвенным псориазом, включает человеческий лейкоцитарный антиген (HLA) Cw6.Также могут быть возможные связи с вариациями гена CARD14 и генов подсемейства IL-19 при ладонно-подошвенном пустулезе. [2] [3] [4] Триггеры окружающей среды включают курение, раздражители, трение, ручные или повторяющиеся травмы. Как это ни парадоксально было показано, что агенты против фактора некроза опухоли альфа вызывают ладонно-подошвенные высыпания.
Большинство пациентов с ладонно-подошвенным пустулезом являются нынешними или бывшими курильщиками. Предполагается, что активированные никотиновые рецепторы в потовых железах вызывают воспалительную реакцию в этом болезненном процессе.Ладонно-подошвенный пустулез также связан с заболеванием щитовидной железы, курением и артритом передней грудной клетки.
Эпидемиология
Ладонно-подошвенный псориаз поражает людей любого возраста, тогда как ладонно-подошвенный пустулез начинается в среднем от 20 до 60 лет. Гендерная специфичность при ладонно-подошвенном псориазе неясна, хотя ладонно-подошвенный пустулез явно предрасположен к женщинам с соотношением женщин и мужчин 8: 2. Хотя заболеваемость не определена, ладонно-подошвенный вариант псориаза составляет от 3% до 4% всех случаев псориаза, которым страдает от 2% до 5% населения.[5]
Патофизиология
Патогенез ладонно-подошвенного псориаза аналогичен псориазу в том, что существует взаимодействие между генетическими факторами и антигенными триггерами. Наиболее часто ассоциированный лейкоцитарный антиген человека при псориазе — это HLA-Cw6. Псориаз связан с локусом восприимчивости к псориазу [ PSORS1 ] на хромосоме 6p21, хотя связь этого гена с ладонно-подошвенным псориазом остается неясной. [2] В качестве альтернативы, одно исследование не обнаружило связи между ладонно-подошвенным пустулезом и локусом PSORS1 .Другие исследования показали возможные связи с вариациями гена CARD14 и генов подсемейства IL-19 при ладонно-подошвенном пустулезе.
Различные антигенные триггеры могут инициировать ладонно-подошвенный псориаз или пустулез у генетически предрасположенных лиц. Триггеры, включая стресс, курение, раздражители, трение и травмы, могут активировать дендритные клетки и Т-клетки, вызывая местную выработку IL-20, ускоряя пролиферацию кератиноцитов. В то же время IL-23 высвобождается из лимфатических узлов, рекрутируя Th2 и Th27 в очаги поражения.Т-клетки продуцируют многочисленные цитокины, включая TNF-a , IL-17 и IL-22, которые стимулируют пролиферацию кератиноцитов и продуцируют провоспалительные антимикробные пептиды и цитокины. Наконец, нейтрофилы привлекаются к эпидермису и активируют дермальные фибробласты. [6]
История и физика
Пациенты с ладонно-подошвенным псориазом и ладонно-подошвенным пустулезом сообщают о симптомах, которые могут включать зуд, боль и трещины. Хотя может произойти спонтанная ремиссия, постоянство обострений является обычным явлением.У пациентов могут возникать обострения, вызванные сезонными изменениями, работой по дому и моющими средствами. Фактически, ладонно-подошвенный псориаз чаще встречается у фермеров, рабочих и домохозяек. Значительное заболевание кожи ладонно-подошвенной области может указывать на основное заболевание суставов.
При физикальном осмотре толстые гиперкератотические бляшки, стерильные пустулы или смесь морфологии могут быть обнаружены при ладонно-подошвенном псориазе. Гиперкератотические бляшки — наиболее распространенный подтип. Часто встречаются симметрично распределенные поражения, а также эритема, трещины и шелушение.Обычно вовлекаются не кисти и стопы, а другие места: в исследованиях участвуют 33% пациентов, у которых до 10% площади поверхности тела (ППТ). Ногти поражаются до 60% случаев, обнаруживая грубую ямку, подногтевой гиперкератоз и продольные гребни. Ладонно-подошвенный пустулез начинается с одностороннего высыпания стерильных желтых пустул размером с булавку. Со временем наблюдается гиперкератоз с эритемой, шелушением и трещинами. Чаще всего встречаются тенар, гипотенар и центральная часть ладоней и подошв.Ладонно-подошвенный пустулез обычно проходит с помощью остаточной коричневой пигментации. [7] [8]
Дифференциальный диагноз ладонно-подошвенного псориаза включает дисгидротическую экзему, контактный дерматит, красный пилировый лишай, приобретенную ладонно-подошвенную кератодермию и дерматоз стопы / дерматита. Континуальный акродерматит Галлопо является заболеванием, связанным с ладонно-подошвенным псориазом, которое проявляется болезненными, пустулезными, околоногтевыми и подногтевыми поражениями с воспалительной основой, которая является хронической и рецидивирующей.
Оценка
Для постановки диагноза необходимы тщательный сбор анамнеза и физикальное обследование, включая изучение триггеров и воздействий.При любых чешуйчатых эритематозных высыпаниях на ладонях и подошвах следует применять препарат гидроксида калия (препарат КОН), чтобы исключить дерматофиты. Часто требуется биопсия, так как ладонно-подошвенный псориаз неотличим от экзематозных дерматитов рук, а также для исключения опоясывающего лишая. Гистопатологическое исследование псориатических поражений показывает паракератоз, уменьшение / потерю зернистого слоя эпидермиса, псориазиформную гиперплазию эпидермиса и микроабсцессы Манро (нейтрофилы в роговом слое).При ладонно-подошвенном псориазе наблюдаются очаги паракератоза вертикальной ориентации, чередующиеся с ортогиперкератозом. Лабораторные исследования могут включать уровни c-реактивного белка (CRP) и мочевой кислоты, оба из которых повышены при пустулезном варианте.
Было разработано несколько инструментов оценки, чтобы помочь клиницистам оценить и измерить тяжесть активности кожного заболевания и реакцию на лечение. Ладонно-подошвенный пустулез и ладонно-подошвенный псориаз отслеживают с использованием индекса площади и степени тяжести псориаза ладонно-подошвенного пустулеза (PPPASI) и индекса площади и степени тяжести ладонно-подошвенного псориаза (PPASI), соответственно.Ладонно-подошвенный индекс качества жизни — это статистически непроверенный инструмент оценки, используемый в исследованиях для количественной оценки тяжести заболевания и качества жизни [9].
Лечение / ведение
Исторически сложилось так, что данные о лечении ладонно-подошвенного псориаза были ограничены, поскольку пациенты были исключены из клинических испытаний псориаза, поскольку было затронуто менее 10% их ППТ. Хотя не существует стандартизированного лечения пациентов с ладонно-подошвенным псориазом или ладонно-подошвенным пустулезом, в последние годы появилось все больше данных о методах лечения, особенно с использованием биологических агентов.Большинству пациентов потребуются системные агенты, учитывая устойчивый характер этих кожных заболеваний. Фактически, одно исследование показало, что только 27,4% пациентов показали улучшение при применении местных препаратов, тогда как остальным пациентам потребовалось системное лечение. [10]
Основной причиной того, что местные средства не действуют, является толстый роговой слой на подошвах и ладонях, который действует как барьер для проникновения лекарств.
Терапия первой линии начинается с сильнодействующих или суперсильных местных кортикостероидов, применяемых два раза в день с окклюзией или без нее, с постепенным снижением частоты в течение нескольких недель или месяцев.Кальципотриен часто комбинируют или чередуют с сильнодействующими кортикостероидами для местного применения. Важно помнить, что кальципотриен не следует сочетать с салициловой кислотой, которая дезактивирует молекулу. Системное лечение первой линии включает ацитретин в дозе от 10 до 50 мг в день, с максимальным эффектом через 3-6 месяцев после начала лечения. Ацитретин противопоказан при беременности.
Терапия второй линии начинается со световой терапии, включая PUVA и NB-UVB или монохроматический эксимерный лазер.Системные препараты второго ряда включают метотрексат и циклоспорин. Метотрексат дозируется в дозе от 7,5 до 20 мг в неделю в течение трех-шести недель. Циклоспорин можно применять у иммунокомпетентных пациентов с тяжелым упорным ладонно-подошвенным псориазом. Дозы начинаются с 2,5 мг / кг до 5,0 мг / кг в день в течение максимум одного года и должны быть уменьшены на 0,5–1,0 мг / кг, если наблюдаются гипертензия или результаты тестов аномальной функции почек. Метотрексат противопоказан при беременности, в то время как циклоспорин можно применять с осторожностью.[11]
Есть также сообщения о том, что лазерная и другие эксимерные световые терапии могут работать. Эти новые методы лечения требуют низкой кумулятивной дозы для облегчения симптомов и, следовательно, меньшего количества процедур.
Биопрепараты предназначены для пациентов, которые не смогли или не могут завершить лечение местными или другими системными препаратами. Этанерцепт представляет собой ингибитор TNF- и , который показал статистически значимое снижение PPPASI при приеме 50 мг два раза в неделю в течение 24 недель терапии. [12] e Аналогичным образом инфликсимаб в дозе 5 мг / кг на нулевой, второй и шестой неделях, а затем каждые восемь недель демонстрировал снижение средней площади поверхности ладоней и подошв на 50%.[13] Прием адалимумаба в дозе 40 мг подкожно (п / к) каждые две недели в течение трех месяцев продемонстрировал улучшение качества жизни в исследованиях. [14] Устекинумаб представляет собой ингибитор ИЛ-12 и ИЛ-23 в дозе 45 мг (менее 100 кг) или 90 мг подкожно (100 кг или более) каждые три месяца, что привело к полному выздоровлению у 35% пациентов через 16 недель. . [15] Секукинумаб представляет собой ингибитор ИЛ-17А, принимаемый в дозе 300 мг (90 кг или более) или 150 мг подкожно (<менее 90 кг) каждую неделю от исходного уровня до третьей недели, а затем каждые четыре недели.Тридцать три процента и 22,1% пациентов выздоровели или почти полностью очистились на 16 неделе после приема 300 и 150 мг соответственно [16]. Иксекизумаб - еще один ингибитор ИЛ-17А, который вводят в дозе 160 мг подкожно на нулевой неделе, чем 80 мг каждые две недели до 12 недели, затем по 80 мг каждые четыре недели. В исследованиях PPASI 100 был достигнут у 50% пациентов, получавших иксекизумаб [17].
Многие пациенты с псориазом имеют другие сопутствующие заболевания, такие как почечная недостаточность, заболевания печени, злокачественные новообразования или сердечная недостаточность, которые также предрасполагают их к побочным эффектам от лекарств.Следовательно, перед началом лечения для каждого пациента необходимо тщательно взвесить соотношение риска и пользы.
В целом, кажется, что пероральные ретиноиды с фотохимиотерапией или без нее, а также низкие дозы кортикостероидов / циклоспорина работают лучше всего для облегчения симптомов. Системные ретиноиды и пероральная ПУВА, по-видимому, являются исходной схемой выбора.
Дифференциальный диагноз
-
Экзема
-
Грибковая инфекция
-
Ксероз
-
Дерматит
Прогноз
У пациентов с псориазом ладонно-подошвенной области прогноз надежен.Лечение часто требует длительного времени, имеет побочные эффекты и является дорогостоящим. Качество жизни большинства пациентов оставляет желать лучшего. Большинству пациентов требуется комбинированная терапия в течение многих месяцев, прежде чем они увидят ответ. Кроме того, у пациентов есть и другие сопутствующие заболевания, влияющие на прогноз.
Улучшение результатов команды здравоохранения
Ладонно-подошвенный псориаз лучше всего лечится межпрофессиональной командой, в которую также входят медсестра и фармацевт. От этого расстройства нет лекарства, и в какой-то момент требуется медикаментозное лечение.Постоянный зуд и боль приводят к низкому качеству жизни, поэтому медицинские работники должны принимать меры для уменьшения триггеров и информировать пациентов о соблюдении лекарств. Кроме того, следует рекомендовать пациентам отказаться от курения. Фармацевт должен подчеркнуть важность соблюдения режима приема лекарств. Медсестра, занимающаяся уходом за раной, должна рассказать пациенту о важности ухода за кожей.
Результаты для большинства пациентов с ладонно-подошвенным псориазом осторожны; рецидивы являются обычным явлением, и в конечном итоге большинству пациентов требуются сильнодействующие биологические агенты, которые имеют свои собственные побочные реакции.
Рисунок
Ладонно-подошвенный псориаз. Предоставлено DermNetNZ
Рисунок
Ямки на ногтях у пациента с псориазом. Предоставлено Лоуренсом Брентом, MD
Рисунок
Ладонно-подошвенный псориаз. Предоставлено Сунил Мунакоми, доктор медицины
Ссылки
- 1.
- Фарли Э., Масрур С., Макки Дж., Ментер А. Подошвенный псориаз: фенотипический и клинический обзор с введением нового инструмента оценки качества жизни.J Am Acad Dermatol. 2009 июн; 60 (6): 1024-31. [PubMed: 19467374]
- 2.
- Асумалахти К., Амин М., Суомела С., Хагфорсен Э., Микаэльссон Г., Эванс Дж., Манро М., Телятина С., Аллен М., Леман Дж., Дэвид Бурден А., Кирби Б., Коннолли М. , Griffiths CE, Trembath RC, Kere J, Saarialho-Kere U, Barker JN. Генетический анализ PSORS1 различает каплевидный псориаз и ладонно-подошвенный пустулез. J Invest Dermatol. 2003 Апрель; 120 (4): 627-32. [PubMed: 12648227]
- 3.
- Kingo K, Mössner R, Kõks S, Rätsep R, Krüger U, Vasar E, Reich K, Silm H.Анализ ассоциации генов IL19, IL20 и IL24 при ладонно-подошвенном пустулезе. Br J Dermatol. 2007 апр; 156 (4): 646-52. [PubMed: 17263806]
- 4.
- Coto-Segura P, González-Fernández D, Batalla A, Gómez J, González-Lara L, Queiro R, Alonso B, Iglesias S, Coto E. Общие и редкие варианты гена CARD14 влияют на реакцию противоопухолевого фактора некроза у пациентов с псориазом. Br J Dermatol. 2016 июль; 175 (1): 134-41. [PubMed: 26854129]
- 5.
- Khandpur S, Singhal V, Sharma VK.Ладонно-подошвенное вовлечение в псориаз: клиническое исследование. Индийский J Dermatol Venereol Leprol. 2011 сентябрь-октябрь; 77 (5): 625. [PubMed: 21860174]
- 6.
- Murakami M, Hagforsen E, Morhenn V, Ishida-Yamamoto A, Iizuka H. Пациенты с ладонно-подошвенным пустулезом имеют повышенные уровни IL-17 и IL-22 как в очаге поражения, так и в сыворотке. Exp Dermatol. 2011 Октябрь; 20 (10): 845-7. [PubMed: 21732985]
- 7.
- Чопра А., Maninder. Гилл СС. Гиперкератоз ладоней и подошв: клиническое исследование.Индийский J Dermatol Venereol Leprol. 1997 март-апрель; 63 (2): 85-8. [PubMed: 20944281]
- 8.
- Кумар Б., Сарасват А., Каур И. Ладонно-подошвенные поражения при псориазе: исследование 3065 пациентов. Acta Derm Venereol. 2002; 82 (3): 192-5. [PubMed: 12353710]
- 9.
- Чанг Дж., Каллис Даффин К., Такешита Дж., Шин Д.Б., Крюгер Г.Г., Робертсон А.Д., Троксель А.Б., Ван Вурхиз А.С., Эдсон-Эредиа Э., Гельфанд Дж.М. Ладонно-подошвенный псориаз связан с большим ухудшением качества жизни, связанного со здоровьем, по сравнению с бляшечным псориазом от умеренной до тяжелой степени.J Am Acad Dermatol. 2014 Октябрь; 71 (4): 623-32. [Бесплатная статья PMC: PMC4165651] [PubMed: 24894455]
- 10.
- Spuls PI, Хади С., Ривера Л., Лебволь М. Ретроспективный анализ лечения псориаза ладоней и подошв. J Dermatolog Treat. 2003; 14 Дополнение 2: 21-5. [PubMed: 14578095]
- 11.
- Janagond AB, Kanwar AJ, Handa S. Эффективность и безопасность системного метотрексата по сравнению с ацитретином у пациентов с псориазом со значительным поражением ладонно-подошвенной области: проспективное рандомизированное исследование.J Eur Acad Dermatol Venereol. 2013 Март; 27 (3): e384-9. [PubMed: 23066720]
- 12.
- Санчес И.М., Соренсон Э., Левин Э., Ляо В. Эффективность биологической терапии для лечения ладонно-подошвенного псориаза и ладонно-подошвенного пустулеза: систематический обзор. Dermatol Ther (Heidelb). 2017 декабрь; 7 (4): 425-446. [Бесплатная статья PMC: PMC5698206] [PubMed: 29143230]
- 13.
- Bissonnette R, Poulin Y, Guenther L, Lynde CW, Bolduc C, Nigen S. Лечение ладонно-подошвенного псориаза инфликсимабом: рандомизированное двойное слепое плацебо -контролируемое исследование.J Eur Acad Dermatol Venereol. 2011 декабрь; 25 (12): 1402-8. [PubMed: 21349113]
- 14.
- Richetta AG, Mattozzi C, Giancristoforo S, D’Epiro S, Cantisani C, Macaluso L, Salvi M, Calvieri S. Безопасность и эффективность адалимумаба при лечении умеренной и тяжелой ладонной болезни. -подошвенный псориаз: открытое исследование. Clin Ter. 2012; 163 (2): e61-6. [PubMed: 22555836]
- 15.
- Au SC, Goldminz AM, Kim N, Dumont N, Michelon M, Volf E, Hession M, Lizzul PF, Andrews ID, Kerensky T., Wang A, Yaniv S, Gottlieb AB.Открытое исследование устекинумаба для лечения умеренного и тяжелого ладонно-подошвенного псориаза по инициативе исследователя. J Dermatolog Treat. 2013 июн; 24 (3): 179-87. [PubMed: 223]
- 16.
- Gottlieb A, Sullivan J, van Doorn M, Kubanov A, You R, Parneix A, Hugot S, Milutinovic M. Секукинумаб показывает значительную эффективность при ладонно-подошвенном псориазе: результаты GESTURE, рандомизированный контролируемое испытание. J Am Acad Dermatol. 2017 Янв; 76 (1): 70-80. [PubMed: 27707593]
- 17.
- Ментер А., Уоррен Р. Б., Лэнгли Р. Г., Мерола Дж. Ф., Керр Л. Н., Деннехи Э. Б., Шром Д., Амато Д., Окубо Ю., Райх К.Эффективность иксекизумаба по сравнению с этанерцептом и плацебо у пациентов с бляшечным псориазом средней и тяжелой степени и непустулезным поражением ладонно-подошвенной области: результаты трех исследований фазы 3 (UNCOVER-1, UNCOVER-2 и UNCOVER-3). J Eur Acad Dermatol Venereol. 2017 Октябрь; 31 (10): 1686-1692. [PubMed: 28322474]
Ладонно-подошвенный псориаз — StatPearls — NCBI Bookshelf
Непрерывное обучение
Ладонно-подошвенный псориаз — это хронический вариант псориаза, который обычно поражает кожу ладоней и подошв и вызывает значительные функциональные нарушения.Он имеет гиперкератотическую, пустулезную или смешанную морфологию. Хотя исторически трудно поддаются лечению, недавние исследования биологических методов лечения показали многообещающие результаты при лечении ладонно-подошвенного псориаза. Это упражнение описывает патофизиологию, оценку и лечение ладонно-подошвенного псориаза и подчеркивает роль межпрофессиональной команды в уходе за больными пациентами.
Целей:
-
Определите этиологию ладонно-подошвенного псориаза.
-
Опишите представление пациента с ладонно-подошвенным псориазом.
-
Обобщите доступные варианты лечения и лечения ладонно-подошвенного псориаза.
-
Пересмотреть стратегии межпрофессиональной группы по улучшению координации помощи и коммуникации для улучшения результатов для пациентов, страдающих ладонно-подошвенным псориазом.
Введение
Ладонно-подошвенный псориаз — это разновидность псориаза, которая характерна для кожи ладоней и подошв.Он имеет гиперкератотическую, пустулезную или смешанную морфологию. Ладонно-подошвенный пустулез или пустулезный ладонно-подошвенный псориаз — это, возможно, родственный дерматоз, характеризующийся небольшими стерильными пустулами, которые могут быть типом ладонно-подошвенного псориаза или отдельной формой [1]. Оба состояния имеют хронический характер и приводят к значительным функциональным нарушениям. Как таковые, они связаны со значительным ухудшением качества жизни. Хотя исторически трудно поддаются лечению, недавние исследования биологических методов лечения показали многообещающие результаты при лечении ладонно-подошвенного псориаза.
Этиология
Точная причина ладонно-подошвенного пустулеза неизвестна. Однако ладонно-подошвенный псориаз вызывается сочетанием генетических факторов и факторов окружающей среды. Наиболее распространенный генетический фактор, связанный с ладонно-подошвенным псориазом, включает человеческий лейкоцитарный антиген (HLA) Cw6. Также могут быть возможные связи с вариациями гена CARD14 и генов подсемейства IL-19 при ладонно-подошвенном пустулезе. [2] [3] [4] Триггеры окружающей среды включают курение, раздражители, трение, ручные или повторяющиеся травмы.Как это ни парадоксально было показано, что агенты против фактора некроза опухоли альфа вызывают ладонно-подошвенные высыпания.
Большинство пациентов с ладонно-подошвенным пустулезом являются нынешними или бывшими курильщиками. Предполагается, что активированные никотиновые рецепторы в потовых железах вызывают воспалительную реакцию в этом болезненном процессе. Ладонно-подошвенный пустулез также связан с заболеванием щитовидной железы, курением и артритом передней грудной клетки.
Эпидемиология
Ладонно-подошвенный псориаз поражает людей любого возраста, тогда как ладонно-подошвенный пустулез начинается в среднем от 20 до 60 лет.Гендерная специфичность при ладонно-подошвенном псориазе неясна, хотя ладонно-подошвенный пустулез явно предрасположен к женщинам с соотношением женщин и мужчин 8: 2. Хотя заболеваемость не определена, ладонно-подошвенный вариант псориаза составляет от 3% до 4% всех случаев псориаза, которым страдает от 2% до 5% населения. [5]
Патофизиология
Патогенез ладонно-подошвенного псориаза аналогичен псориазу в том, что существует взаимодействие между генетическими факторами и антигенными триггерами.Наиболее часто ассоциированный лейкоцитарный антиген человека при псориазе — это HLA-Cw6. Псориаз связан с локусом восприимчивости к псориазу [ PSORS1 ] на хромосоме 6p21, хотя связь этого гена с ладонно-подошвенным псориазом остается неясной. [2] В качестве альтернативы, одно исследование не обнаружило связи между ладонно-подошвенным пустулезом и локусом PSORS1 . Другие исследования показали возможные связи с вариациями гена CARD14 и генов подсемейства IL-19 при ладонно-подошвенном пустулезе.
Различные антигенные триггеры могут инициировать ладонно-подошвенный псориаз или пустулез у генетически предрасположенных лиц. Триггеры, включая стресс, курение, раздражители, трение и травмы, могут активировать дендритные клетки и Т-клетки, вызывая местную выработку IL-20, ускоряя пролиферацию кератиноцитов. В то же время IL-23 высвобождается из лимфатических узлов, рекрутируя Th2 и Th27 в очаги поражения. Т-клетки продуцируют многочисленные цитокины, включая TNF-a , IL-17 и IL-22, которые стимулируют пролиферацию кератиноцитов и продуцируют провоспалительные антимикробные пептиды и цитокины.Наконец, нейтрофилы привлекаются к эпидермису и активируют дермальные фибробласты. [6]
История и физика
Пациенты с ладонно-подошвенным псориазом и ладонно-подошвенным пустулезом сообщают о симптомах, которые могут включать зуд, боль и трещины. Хотя может произойти спонтанная ремиссия, постоянство обострений является обычным явлением. У пациентов могут возникать обострения, вызванные сезонными изменениями, работой по дому и моющими средствами. Фактически, ладонно-подошвенный псориаз чаще встречается у фермеров, рабочих и домохозяек.Значительное заболевание кожи ладонно-подошвенной области может указывать на основное заболевание суставов.
При физикальном осмотре толстые гиперкератотические бляшки, стерильные пустулы или смесь морфологии могут быть обнаружены при ладонно-подошвенном псориазе. Гиперкератотические бляшки — наиболее распространенный подтип. Часто встречаются симметрично распределенные поражения, а также эритема, трещины и шелушение. Обычно вовлекаются не кисти и стопы, а другие места: в исследованиях участвуют 33% пациентов, у которых до 10% площади поверхности тела (ППТ).Ногти поражаются до 60% случаев, обнаруживая грубую ямку, подногтевой гиперкератоз и продольные гребни. Ладонно-подошвенный пустулез начинается с одностороннего высыпания стерильных желтых пустул размером с булавку. Со временем наблюдается гиперкератоз с эритемой, шелушением и трещинами. Чаще всего встречаются тенар, гипотенар и центральная часть ладоней и подошв. Ладонно-подошвенный пустулез обычно проходит с помощью остаточной коричневой пигментации. [7] [8]
Дифференциальный диагноз ладонно-подошвенного псориаза включает дисгидротическую экзему, контактный дерматит, красный пилировый лишай, приобретенную ладонно-подошвенную кератодермию и дерматоз стопы / дерматита.Континуальный акродерматит Галлопо является заболеванием, связанным с ладонно-подошвенным псориазом, которое проявляется болезненными, пустулезными, околоногтевыми и подногтевыми поражениями с воспалительной основой, которая является хронической и рецидивирующей.
Оценка
Для постановки диагноза необходимы тщательный сбор анамнеза и физикальное обследование, включая изучение триггеров и воздействий. При любых чешуйчатых эритематозных высыпаниях на ладонях и подошвах следует применять препарат гидроксида калия (препарат КОН), чтобы исключить дерматофиты.Часто требуется биопсия, так как ладонно-подошвенный псориаз неотличим от экзематозных дерматитов рук, а также для исключения опоясывающего лишая. Гистопатологическое исследование псориатических поражений показывает паракератоз, уменьшение / потерю зернистого слоя эпидермиса, псориазиформную гиперплазию эпидермиса и микроабсцессы Манро (нейтрофилы в роговом слое). При ладонно-подошвенном псориазе наблюдаются очаги паракератоза вертикальной ориентации, чередующиеся с ортогиперкератозом. Лабораторные исследования могут включать уровни c-реактивного белка (CRP) и мочевой кислоты, оба из которых повышены при пустулезном варианте.
Было разработано несколько инструментов оценки, чтобы помочь клиницистам оценить и измерить тяжесть активности кожного заболевания и реакцию на лечение. Ладонно-подошвенный пустулез и ладонно-подошвенный псориаз отслеживают с использованием индекса площади и степени тяжести псориаза ладонно-подошвенного пустулеза (PPPASI) и индекса площади и степени тяжести ладонно-подошвенного псориаза (PPASI), соответственно. Ладонно-подошвенный индекс качества жизни — это статистически непроверенный инструмент оценки, используемый в исследованиях для количественной оценки тяжести заболевания и качества жизни.[9]
Лечение / ведение
Исторически данные о лечении ладонно-подошвенного псориаза были ограничены, так как пациенты были исключены из клинических испытаний псориаза, поскольку было затронуто менее 10% их ППТ. Хотя не существует стандартизированного лечения пациентов с ладонно-подошвенным псориазом или ладонно-подошвенным пустулезом, в последние годы появилось все больше данных о методах лечения, особенно с использованием биологических агентов. Большинству пациентов потребуются системные агенты, учитывая устойчивый характер этих кожных заболеваний.Фактически, одно исследование показало, что только 27,4% пациентов показали улучшение при применении местных препаратов, тогда как остальным пациентам потребовалось системное лечение. [10]
Основной причиной того, что местные средства не действуют, является толстый роговой слой на подошвах и ладонях, который действует как барьер для проникновения лекарств.
Терапия первой линии начинается с сильнодействующих или суперсильных местных кортикостероидов, применяемых два раза в день с окклюзией или без нее, с постепенным снижением частоты в течение нескольких недель или месяцев.Кальципотриен часто комбинируют или чередуют с сильнодействующими кортикостероидами для местного применения. Важно помнить, что кальципотриен не следует сочетать с салициловой кислотой, которая дезактивирует молекулу. Системное лечение первой линии включает ацитретин в дозе от 10 до 50 мг в день, с максимальным эффектом через 3-6 месяцев после начала лечения. Ацитретин противопоказан при беременности.
Терапия второй линии начинается со световой терапии, включая PUVA и NB-UVB или монохроматический эксимерный лазер.Системные препараты второго ряда включают метотрексат и циклоспорин. Метотрексат дозируется в дозе от 7,5 до 20 мг в неделю в течение трех-шести недель. Циклоспорин можно применять у иммунокомпетентных пациентов с тяжелым упорным ладонно-подошвенным псориазом. Дозы начинаются с 2,5 мг / кг до 5,0 мг / кг в день в течение максимум одного года и должны быть уменьшены на 0,5–1,0 мг / кг, если наблюдаются гипертензия или результаты тестов аномальной функции почек. Метотрексат противопоказан при беременности, в то время как циклоспорин можно применять с осторожностью.[11]
Есть также сообщения о том, что лазерная и другие эксимерные световые терапии могут работать. Эти новые методы лечения требуют низкой кумулятивной дозы для облегчения симптомов и, следовательно, меньшего количества процедур.
Биопрепараты предназначены для пациентов, которые не смогли или не могут завершить лечение местными или другими системными препаратами. Этанерцепт представляет собой ингибитор TNF- и , который показал статистически значимое снижение PPPASI при приеме 50 мг два раза в неделю в течение 24 недель терапии. [12] e Аналогичным образом инфликсимаб в дозе 5 мг / кг на нулевой, второй и шестой неделях, а затем каждые восемь недель демонстрировал снижение средней площади поверхности ладоней и подошв на 50%.[13] Прием адалимумаба в дозе 40 мг подкожно (п / к) каждые две недели в течение трех месяцев продемонстрировал улучшение качества жизни в исследованиях. [14] Устекинумаб представляет собой ингибитор ИЛ-12 и ИЛ-23 в дозе 45 мг (менее 100 кг) или 90 мг подкожно (100 кг или более) каждые три месяца, что привело к полному выздоровлению у 35% пациентов через 16 недель. . [15] Секукинумаб представляет собой ингибитор ИЛ-17А, принимаемый в дозе 300 мг (90 кг или более) или 150 мг подкожно (<менее 90 кг) каждую неделю от исходного уровня до третьей недели, а затем каждые четыре недели.Тридцать три процента и 22,1% пациентов выздоровели или почти полностью очистились на 16 неделе после приема 300 и 150 мг соответственно [16]. Иксекизумаб - еще один ингибитор ИЛ-17А, который вводят в дозе 160 мг подкожно на нулевой неделе, чем 80 мг каждые две недели до 12 недели, затем по 80 мг каждые четыре недели. В исследованиях PPASI 100 был достигнут у 50% пациентов, получавших иксекизумаб [17].
Многие пациенты с псориазом имеют другие сопутствующие заболевания, такие как почечная недостаточность, заболевания печени, злокачественные новообразования или сердечная недостаточность, которые также предрасполагают их к побочным эффектам от лекарств.Следовательно, перед началом лечения для каждого пациента необходимо тщательно взвесить соотношение риска и пользы.
В целом, кажется, что пероральные ретиноиды с фотохимиотерапией или без нее, а также низкие дозы кортикостероидов / циклоспорина работают лучше всего для облегчения симптомов. Системные ретиноиды и пероральная ПУВА, по-видимому, являются исходной схемой выбора.
Дифференциальный диагноз
-
Экзема
-
Грибковая инфекция
-
Ксероз
-
Дерматит
Прогноз
У пациентов с псориазом ладонно-подошвенной области прогноз надежен.Лечение часто требует длительного времени, имеет побочные эффекты и является дорогостоящим. Качество жизни большинства пациентов оставляет желать лучшего. Большинству пациентов требуется комбинированная терапия в течение многих месяцев, прежде чем они увидят ответ. Кроме того, у пациентов есть и другие сопутствующие заболевания, влияющие на прогноз.
Улучшение результатов команды здравоохранения
Ладонно-подошвенный псориаз лучше всего лечится межпрофессиональной командой, в которую также входят медсестра и фармацевт. От этого расстройства нет лекарства, и в какой-то момент требуется медикаментозное лечение.Постоянный зуд и боль приводят к низкому качеству жизни, поэтому медицинские работники должны принимать меры для уменьшения триггеров и информировать пациентов о соблюдении лекарств. Кроме того, следует рекомендовать пациентам отказаться от курения. Фармацевт должен подчеркнуть важность соблюдения режима приема лекарств. Медсестра, занимающаяся уходом за раной, должна рассказать пациенту о важности ухода за кожей.
Результаты для большинства пациентов с ладонно-подошвенным псориазом осторожны; рецидивы являются обычным явлением, и в конечном итоге большинству пациентов требуются сильнодействующие биологические агенты, которые имеют свои собственные побочные реакции.
Рисунок
Ладонно-подошвенный псориаз. Предоставлено DermNetNZ
Рисунок
Ямки на ногтях у пациента с псориазом. Предоставлено Лоуренсом Брентом, MD
Рисунок
Ладонно-подошвенный псориаз. Предоставлено Сунил Мунакоми, доктор медицины
Ссылки
- 1.
- Фарли Э., Масрур С., Макки Дж., Ментер А. Подошвенный псориаз: фенотипический и клинический обзор с введением нового инструмента оценки качества жизни.J Am Acad Dermatol. 2009 июн; 60 (6): 1024-31. [PubMed: 19467374]
- 2.
- Асумалахти К., Амин М., Суомела С., Хагфорсен Э., Микаэльссон Г., Эванс Дж., Манро М., Телятина С., Аллен М., Леман Дж., Дэвид Бурден А., Кирби Б., Коннолли М. , Griffiths CE, Trembath RC, Kere J, Saarialho-Kere U, Barker JN. Генетический анализ PSORS1 различает каплевидный псориаз и ладонно-подошвенный пустулез. J Invest Dermatol. 2003 Апрель; 120 (4): 627-32. [PubMed: 12648227]
- 3.
- Kingo K, Mössner R, Kõks S, Rätsep R, Krüger U, Vasar E, Reich K, Silm H.Анализ ассоциации генов IL19, IL20 и IL24 при ладонно-подошвенном пустулезе. Br J Dermatol. 2007 апр; 156 (4): 646-52. [PubMed: 17263806]
- 4.
- Coto-Segura P, González-Fernández D, Batalla A, Gómez J, González-Lara L, Queiro R, Alonso B, Iglesias S, Coto E. Общие и редкие варианты гена CARD14 влияют на реакцию противоопухолевого фактора некроза у пациентов с псориазом. Br J Dermatol. 2016 июль; 175 (1): 134-41. [PubMed: 26854129]
- 5.
- Khandpur S, Singhal V, Sharma VK.Ладонно-подошвенное вовлечение в псориаз: клиническое исследование. Индийский J Dermatol Venereol Leprol. 2011 сентябрь-октябрь; 77 (5): 625. [PubMed: 21860174]
- 6.
- Murakami M, Hagforsen E, Morhenn V, Ishida-Yamamoto A, Iizuka H. Пациенты с ладонно-подошвенным пустулезом имеют повышенные уровни IL-17 и IL-22 как в очаге поражения, так и в сыворотке. Exp Dermatol. 2011 Октябрь; 20 (10): 845-7. [PubMed: 21732985]
- 7.
- Чопра А., Maninder. Гилл СС. Гиперкератоз ладоней и подошв: клиническое исследование.Индийский J Dermatol Venereol Leprol. 1997 март-апрель; 63 (2): 85-8. [PubMed: 20944281]
- 8.
- Кумар Б., Сарасват А., Каур И. Ладонно-подошвенные поражения при псориазе: исследование 3065 пациентов. Acta Derm Venereol. 2002; 82 (3): 192-5. [PubMed: 12353710]
- 9.
- Чанг Дж., Каллис Даффин К., Такешита Дж., Шин Д.Б., Крюгер Г.Г., Робертсон А.Д., Троксель А.Б., Ван Вурхиз А.С., Эдсон-Эредиа Э., Гельфанд Дж.М. Ладонно-подошвенный псориаз связан с большим ухудшением качества жизни, связанного со здоровьем, по сравнению с бляшечным псориазом от умеренной до тяжелой степени.J Am Acad Dermatol. 2014 Октябрь; 71 (4): 623-32. [Бесплатная статья PMC: PMC4165651] [PubMed: 24894455]
- 10.
- Spuls PI, Хади С., Ривера Л., Лебволь М. Ретроспективный анализ лечения псориаза ладоней и подошв. J Dermatolog Treat. 2003; 14 Дополнение 2: 21-5. [PubMed: 14578095]
- 11.
- Janagond AB, Kanwar AJ, Handa S. Эффективность и безопасность системного метотрексата по сравнению с ацитретином у пациентов с псориазом со значительным поражением ладонно-подошвенной области: проспективное рандомизированное исследование.J Eur Acad Dermatol Venereol. 2013 Март; 27 (3): e384-9. [PubMed: 23066720]
- 12.
- Санчес И.М., Соренсон Э., Левин Э., Ляо В. Эффективность биологической терапии для лечения ладонно-подошвенного псориаза и ладонно-подошвенного пустулеза: систематический обзор. Dermatol Ther (Heidelb). 2017 декабрь; 7 (4): 425-446. [Бесплатная статья PMC: PMC5698206] [PubMed: 29143230]
- 13.
- Bissonnette R, Poulin Y, Guenther L, Lynde CW, Bolduc C, Nigen S. Лечение ладонно-подошвенного псориаза инфликсимабом: рандомизированное двойное слепое плацебо -контролируемое исследование.J Eur Acad Dermatol Venereol. 2011 декабрь; 25 (12): 1402-8. [PubMed: 21349113]
- 14.
- Richetta AG, Mattozzi C, Giancristoforo S, D’Epiro S, Cantisani C, Macaluso L, Salvi M, Calvieri S. Безопасность и эффективность адалимумаба при лечении умеренной и тяжелой ладонной болезни. -подошвенный псориаз: открытое исследование. Clin Ter. 2012; 163 (2): e61-6. [PubMed: 22555836]
- 15.
- Au SC, Goldminz AM, Kim N, Dumont N, Michelon M, Volf E, Hession M, Lizzul PF, Andrews ID, Kerensky T., Wang A, Yaniv S, Gottlieb AB.Открытое исследование устекинумаба для лечения умеренного и тяжелого ладонно-подошвенного псориаза по инициативе исследователя. J Dermatolog Treat. 2013 июн; 24 (3): 179-87. [PubMed: 223]
- 16.
- Gottlieb A, Sullivan J, van Doorn M, Kubanov A, You R, Parneix A, Hugot S, Milutinovic M. Секукинумаб показывает значительную эффективность при ладонно-подошвенном псориазе: результаты GESTURE, рандомизированный контролируемое испытание. J Am Acad Dermatol. 2017 Янв; 76 (1): 70-80. [PubMed: 27707593]
- 17.
- Ментер А., Уоррен Р. Б., Лэнгли Р. Г., Мерола Дж. Ф., Керр Л. Н., Деннехи Э. Б., Шром Д., Амато Д., Окубо Ю., Райх К.Эффективность иксекизумаба по сравнению с этанерцептом и плацебо у пациентов с бляшечным псориазом средней и тяжелой степени и непустулезным поражением ладонно-подошвенной области: результаты трех исследований фазы 3 (UNCOVER-1, UNCOVER-2 и UNCOVER-3). J Eur Acad Dermatol Venereol. 2017 Октябрь; 31 (10): 1686-1692. [PubMed: 28322474]
Ладонно-подошвенный псориаз — StatPearls — NCBI Bookshelf
Непрерывное обучение
Ладонно-подошвенный псориаз — это хронический вариант псориаза, который обычно поражает кожу ладоней и подошв и вызывает значительные функциональные нарушения.Он имеет гиперкератотическую, пустулезную или смешанную морфологию. Хотя исторически трудно поддаются лечению, недавние исследования биологических методов лечения показали многообещающие результаты при лечении ладонно-подошвенного псориаза. Это упражнение описывает патофизиологию, оценку и лечение ладонно-подошвенного псориаза и подчеркивает роль межпрофессиональной команды в уходе за больными пациентами.
Целей:
-
Определите этиологию ладонно-подошвенного псориаза.
-
Опишите представление пациента с ладонно-подошвенным псориазом.
-
Обобщите доступные варианты лечения и лечения ладонно-подошвенного псориаза.
-
Пересмотреть стратегии межпрофессиональной группы по улучшению координации помощи и коммуникации для улучшения результатов для пациентов, страдающих ладонно-подошвенным псориазом.
Введение
Ладонно-подошвенный псориаз — это разновидность псориаза, которая характерна для кожи ладоней и подошв.Он имеет гиперкератотическую, пустулезную или смешанную морфологию. Ладонно-подошвенный пустулез или пустулезный ладонно-подошвенный псориаз — это, возможно, родственный дерматоз, характеризующийся небольшими стерильными пустулами, которые могут быть типом ладонно-подошвенного псориаза или отдельной формой [1]. Оба состояния имеют хронический характер и приводят к значительным функциональным нарушениям. Как таковые, они связаны со значительным ухудшением качества жизни. Хотя исторически трудно поддаются лечению, недавние исследования биологических методов лечения показали многообещающие результаты при лечении ладонно-подошвенного псориаза.
Этиология
Точная причина ладонно-подошвенного пустулеза неизвестна. Однако ладонно-подошвенный псориаз вызывается сочетанием генетических факторов и факторов окружающей среды. Наиболее распространенный генетический фактор, связанный с ладонно-подошвенным псориазом, включает человеческий лейкоцитарный антиген (HLA) Cw6. Также могут быть возможные связи с вариациями гена CARD14 и генов подсемейства IL-19 при ладонно-подошвенном пустулезе. [2] [3] [4] Триггеры окружающей среды включают курение, раздражители, трение, ручные или повторяющиеся травмы.Как это ни парадоксально было показано, что агенты против фактора некроза опухоли альфа вызывают ладонно-подошвенные высыпания.
Большинство пациентов с ладонно-подошвенным пустулезом являются нынешними или бывшими курильщиками. Предполагается, что активированные никотиновые рецепторы в потовых железах вызывают воспалительную реакцию в этом болезненном процессе. Ладонно-подошвенный пустулез также связан с заболеванием щитовидной железы, курением и артритом передней грудной клетки.
Эпидемиология
Ладонно-подошвенный псориаз поражает людей любого возраста, тогда как ладонно-подошвенный пустулез начинается в среднем от 20 до 60 лет.Гендерная специфичность при ладонно-подошвенном псориазе неясна, хотя ладонно-подошвенный пустулез явно предрасположен к женщинам с соотношением женщин и мужчин 8: 2. Хотя заболеваемость не определена, ладонно-подошвенный вариант псориаза составляет от 3% до 4% всех случаев псориаза, которым страдает от 2% до 5% населения. [5]
Патофизиология
Патогенез ладонно-подошвенного псориаза аналогичен псориазу в том, что существует взаимодействие между генетическими факторами и антигенными триггерами.Наиболее часто ассоциированный лейкоцитарный антиген человека при псориазе — это HLA-Cw6. Псориаз связан с локусом восприимчивости к псориазу [ PSORS1 ] на хромосоме 6p21, хотя связь этого гена с ладонно-подошвенным псориазом остается неясной. [2] В качестве альтернативы, одно исследование не обнаружило связи между ладонно-подошвенным пустулезом и локусом PSORS1 . Другие исследования показали возможные связи с вариациями гена CARD14 и генов подсемейства IL-19 при ладонно-подошвенном пустулезе.
Различные антигенные триггеры могут инициировать ладонно-подошвенный псориаз или пустулез у генетически предрасположенных лиц. Триггеры, включая стресс, курение, раздражители, трение и травмы, могут активировать дендритные клетки и Т-клетки, вызывая местную выработку IL-20, ускоряя пролиферацию кератиноцитов. В то же время IL-23 высвобождается из лимфатических узлов, рекрутируя Th2 и Th27 в очаги поражения. Т-клетки продуцируют многочисленные цитокины, включая TNF-a , IL-17 и IL-22, которые стимулируют пролиферацию кератиноцитов и продуцируют провоспалительные антимикробные пептиды и цитокины.Наконец, нейтрофилы привлекаются к эпидермису и активируют дермальные фибробласты. [6]
История и физика
Пациенты с ладонно-подошвенным псориазом и ладонно-подошвенным пустулезом сообщают о симптомах, которые могут включать зуд, боль и трещины. Хотя может произойти спонтанная ремиссия, постоянство обострений является обычным явлением. У пациентов могут возникать обострения, вызванные сезонными изменениями, работой по дому и моющими средствами. Фактически, ладонно-подошвенный псориаз чаще встречается у фермеров, рабочих и домохозяек.Значительное заболевание кожи ладонно-подошвенной области может указывать на основное заболевание суставов.
При физикальном осмотре толстые гиперкератотические бляшки, стерильные пустулы или смесь морфологии могут быть обнаружены при ладонно-подошвенном псориазе. Гиперкератотические бляшки — наиболее распространенный подтип. Часто встречаются симметрично распределенные поражения, а также эритема, трещины и шелушение. Обычно вовлекаются не кисти и стопы, а другие места: в исследованиях участвуют 33% пациентов, у которых до 10% площади поверхности тела (ППТ).Ногти поражаются до 60% случаев, обнаруживая грубую ямку, подногтевой гиперкератоз и продольные гребни. Ладонно-подошвенный пустулез начинается с одностороннего высыпания стерильных желтых пустул размером с булавку. Со временем наблюдается гиперкератоз с эритемой, шелушением и трещинами. Чаще всего встречаются тенар, гипотенар и центральная часть ладоней и подошв. Ладонно-подошвенный пустулез обычно проходит с помощью остаточной коричневой пигментации. [7] [8]
Дифференциальный диагноз ладонно-подошвенного псориаза включает дисгидротическую экзему, контактный дерматит, красный пилировый лишай, приобретенную ладонно-подошвенную кератодермию и дерматоз стопы / дерматита.Континуальный акродерматит Галлопо является заболеванием, связанным с ладонно-подошвенным псориазом, которое проявляется болезненными, пустулезными, околоногтевыми и подногтевыми поражениями с воспалительной основой, которая является хронической и рецидивирующей.
Оценка
Для постановки диагноза необходимы тщательный сбор анамнеза и физикальное обследование, включая изучение триггеров и воздействий. При любых чешуйчатых эритематозных высыпаниях на ладонях и подошвах следует применять препарат гидроксида калия (препарат КОН), чтобы исключить дерматофиты.Часто требуется биопсия, так как ладонно-подошвенный псориаз неотличим от экзематозных дерматитов рук, а также для исключения опоясывающего лишая. Гистопатологическое исследование псориатических поражений показывает паракератоз, уменьшение / потерю зернистого слоя эпидермиса, псориазиформную гиперплазию эпидермиса и микроабсцессы Манро (нейтрофилы в роговом слое). При ладонно-подошвенном псориазе наблюдаются очаги паракератоза вертикальной ориентации, чередующиеся с ортогиперкератозом. Лабораторные исследования могут включать уровни c-реактивного белка (CRP) и мочевой кислоты, оба из которых повышены при пустулезном варианте.
Было разработано несколько инструментов оценки, чтобы помочь клиницистам оценить и измерить тяжесть активности кожного заболевания и реакцию на лечение. Ладонно-подошвенный пустулез и ладонно-подошвенный псориаз отслеживают с использованием индекса площади и степени тяжести псориаза ладонно-подошвенного пустулеза (PPPASI) и индекса площади и степени тяжести ладонно-подошвенного псориаза (PPASI), соответственно. Ладонно-подошвенный индекс качества жизни — это статистически непроверенный инструмент оценки, используемый в исследованиях для количественной оценки тяжести заболевания и качества жизни.[9]
Лечение / ведение
Исторически данные о лечении ладонно-подошвенного псориаза были ограничены, так как пациенты были исключены из клинических испытаний псориаза, поскольку было затронуто менее 10% их ППТ. Хотя не существует стандартизированного лечения пациентов с ладонно-подошвенным псориазом или ладонно-подошвенным пустулезом, в последние годы появилось все больше данных о методах лечения, особенно с использованием биологических агентов. Большинству пациентов потребуются системные агенты, учитывая устойчивый характер этих кожных заболеваний.Фактически, одно исследование показало, что только 27,4% пациентов показали улучшение при применении местных препаратов, тогда как остальным пациентам потребовалось системное лечение. [10]
Основной причиной того, что местные средства не действуют, является толстый роговой слой на подошвах и ладонях, который действует как барьер для проникновения лекарств.
Терапия первой линии начинается с сильнодействующих или суперсильных местных кортикостероидов, применяемых два раза в день с окклюзией или без нее, с постепенным снижением частоты в течение нескольких недель или месяцев.Кальципотриен часто комбинируют или чередуют с сильнодействующими кортикостероидами для местного применения. Важно помнить, что кальципотриен не следует сочетать с салициловой кислотой, которая дезактивирует молекулу. Системное лечение первой линии включает ацитретин в дозе от 10 до 50 мг в день, с максимальным эффектом через 3-6 месяцев после начала лечения. Ацитретин противопоказан при беременности.
Терапия второй линии начинается со световой терапии, включая PUVA и NB-UVB или монохроматический эксимерный лазер.Системные препараты второго ряда включают метотрексат и циклоспорин. Метотрексат дозируется в дозе от 7,5 до 20 мг в неделю в течение трех-шести недель. Циклоспорин можно применять у иммунокомпетентных пациентов с тяжелым упорным ладонно-подошвенным псориазом. Дозы начинаются с 2,5 мг / кг до 5,0 мг / кг в день в течение максимум одного года и должны быть уменьшены на 0,5–1,0 мг / кг, если наблюдаются гипертензия или результаты тестов аномальной функции почек. Метотрексат противопоказан при беременности, в то время как циклоспорин можно применять с осторожностью.[11]
Есть также сообщения о том, что лазерная и другие эксимерные световые терапии могут работать. Эти новые методы лечения требуют низкой кумулятивной дозы для облегчения симптомов и, следовательно, меньшего количества процедур.
Биопрепараты предназначены для пациентов, которые не смогли или не могут завершить лечение местными или другими системными препаратами. Этанерцепт представляет собой ингибитор TNF- и , который показал статистически значимое снижение PPPASI при приеме 50 мг два раза в неделю в течение 24 недель терапии. [12] e Аналогичным образом инфликсимаб в дозе 5 мг / кг на нулевой, второй и шестой неделях, а затем каждые восемь недель демонстрировал снижение средней площади поверхности ладоней и подошв на 50%.[13] Прием адалимумаба в дозе 40 мг подкожно (п / к) каждые две недели в течение трех месяцев продемонстрировал улучшение качества жизни в исследованиях. [14] Устекинумаб представляет собой ингибитор ИЛ-12 и ИЛ-23 в дозе 45 мг (менее 100 кг) или 90 мг подкожно (100 кг или более) каждые три месяца, что привело к полному выздоровлению у 35% пациентов через 16 недель. . [15] Секукинумаб представляет собой ингибитор ИЛ-17А, принимаемый в дозе 300 мг (90 кг или более) или 150 мг подкожно (<менее 90 кг) каждую неделю от исходного уровня до третьей недели, а затем каждые четыре недели.Тридцать три процента и 22,1% пациентов выздоровели или почти полностью очистились на 16 неделе после приема 300 и 150 мг соответственно [16]. Иксекизумаб - еще один ингибитор ИЛ-17А, который вводят в дозе 160 мг подкожно на нулевой неделе, чем 80 мг каждые две недели до 12 недели, затем по 80 мг каждые четыре недели. В исследованиях PPASI 100 был достигнут у 50% пациентов, получавших иксекизумаб [17].
Многие пациенты с псориазом имеют другие сопутствующие заболевания, такие как почечная недостаточность, заболевания печени, злокачественные новообразования или сердечная недостаточность, которые также предрасполагают их к побочным эффектам от лекарств.Следовательно, перед началом лечения для каждого пациента необходимо тщательно взвесить соотношение риска и пользы.
В целом, кажется, что пероральные ретиноиды с фотохимиотерапией или без нее, а также низкие дозы кортикостероидов / циклоспорина работают лучше всего для облегчения симптомов. Системные ретиноиды и пероральная ПУВА, по-видимому, являются исходной схемой выбора.
Дифференциальный диагноз
-
Экзема
-
Грибковая инфекция
-
Ксероз
-
Дерматит
Прогноз
У пациентов с псориазом ладонно-подошвенной области прогноз надежен.Лечение часто требует длительного времени, имеет побочные эффекты и является дорогостоящим. Качество жизни большинства пациентов оставляет желать лучшего. Большинству пациентов требуется комбинированная терапия в течение многих месяцев, прежде чем они увидят ответ. Кроме того, у пациентов есть и другие сопутствующие заболевания, влияющие на прогноз.
Улучшение результатов команды здравоохранения
Ладонно-подошвенный псориаз лучше всего лечится межпрофессиональной командой, в которую также входят медсестра и фармацевт. От этого расстройства нет лекарства, и в какой-то момент требуется медикаментозное лечение.Постоянный зуд и боль приводят к низкому качеству жизни, поэтому медицинские работники должны принимать меры для уменьшения триггеров и информировать пациентов о соблюдении лекарств. Кроме того, следует рекомендовать пациентам отказаться от курения. Фармацевт должен подчеркнуть важность соблюдения режима приема лекарств. Медсестра, занимающаяся уходом за раной, должна рассказать пациенту о важности ухода за кожей.
Результаты для большинства пациентов с ладонно-подошвенным псориазом осторожны; рецидивы являются обычным явлением, и в конечном итоге большинству пациентов требуются сильнодействующие биологические агенты, которые имеют свои собственные побочные реакции.
Рисунок
Ладонно-подошвенный псориаз. Предоставлено DermNetNZ
Рисунок
Ямки на ногтях у пациента с псориазом. Предоставлено Лоуренсом Брентом, MD
Рисунок
Ладонно-подошвенный псориаз. Предоставлено Сунил Мунакоми, доктор медицины
Ссылки
- 1.
- Фарли Э., Масрур С., Макки Дж., Ментер А. Подошвенный псориаз: фенотипический и клинический обзор с введением нового инструмента оценки качества жизни.J Am Acad Dermatol. 2009 июн; 60 (6): 1024-31. [PubMed: 19467374]
- 2.
- Асумалахти К., Амин М., Суомела С., Хагфорсен Э., Микаэльссон Г., Эванс Дж., Манро М., Телятина С., Аллен М., Леман Дж., Дэвид Бурден А., Кирби Б., Коннолли М. , Griffiths CE, Trembath RC, Kere J, Saarialho-Kere U, Barker JN. Генетический анализ PSORS1 различает каплевидный псориаз и ладонно-подошвенный пустулез. J Invest Dermatol. 2003 Апрель; 120 (4): 627-32. [PubMed: 12648227]
- 3.
- Kingo K, Mössner R, Kõks S, Rätsep R, Krüger U, Vasar E, Reich K, Silm H.Анализ ассоциации генов IL19, IL20 и IL24 при ладонно-подошвенном пустулезе. Br J Dermatol. 2007 апр; 156 (4): 646-52. [PubMed: 17263806]
- 4.
- Coto-Segura P, González-Fernández D, Batalla A, Gómez J, González-Lara L, Queiro R, Alonso B, Iglesias S, Coto E. Общие и редкие варианты гена CARD14 влияют на реакцию противоопухолевого фактора некроза у пациентов с псориазом. Br J Dermatol. 2016 июль; 175 (1): 134-41. [PubMed: 26854129]
- 5.
- Khandpur S, Singhal V, Sharma VK.Ладонно-подошвенное вовлечение в псориаз: клиническое исследование. Индийский J Dermatol Venereol Leprol. 2011 сентябрь-октябрь; 77 (5): 625. [PubMed: 21860174]
- 6.
- Murakami M, Hagforsen E, Morhenn V, Ishida-Yamamoto A, Iizuka H. Пациенты с ладонно-подошвенным пустулезом имеют повышенные уровни IL-17 и IL-22 как в очаге поражения, так и в сыворотке. Exp Dermatol. 2011 Октябрь; 20 (10): 845-7. [PubMed: 21732985]
- 7.
- Чопра А., Maninder. Гилл СС. Гиперкератоз ладоней и подошв: клиническое исследование.Индийский J Dermatol Venereol Leprol. 1997 март-апрель; 63 (2): 85-8. [PubMed: 20944281]
- 8.
- Кумар Б., Сарасват А., Каур И. Ладонно-подошвенные поражения при псориазе: исследование 3065 пациентов. Acta Derm Venereol. 2002; 82 (3): 192-5. [PubMed: 12353710]
- 9.
- Чанг Дж., Каллис Даффин К., Такешита Дж., Шин Д.Б., Крюгер Г.Г., Робертсон А.Д., Троксель А.Б., Ван Вурхиз А.С., Эдсон-Эредиа Э., Гельфанд Дж.М. Ладонно-подошвенный псориаз связан с большим ухудшением качества жизни, связанного со здоровьем, по сравнению с бляшечным псориазом от умеренной до тяжелой степени.J Am Acad Dermatol. 2014 Октябрь; 71 (4): 623-32. [Бесплатная статья PMC: PMC4165651] [PubMed: 24894455]
- 10.
- Spuls PI, Хади С., Ривера Л., Лебволь М. Ретроспективный анализ лечения псориаза ладоней и подошв. J Dermatolog Treat. 2003; 14 Дополнение 2: 21-5. [PubMed: 14578095]
- 11.
- Janagond AB, Kanwar AJ, Handa S. Эффективность и безопасность системного метотрексата по сравнению с ацитретином у пациентов с псориазом со значительным поражением ладонно-подошвенной области: проспективное рандомизированное исследование.J Eur Acad Dermatol Venereol. 2013 Март; 27 (3): e384-9. [PubMed: 23066720]
- 12.
- Санчес И.М., Соренсон Э., Левин Э., Ляо В. Эффективность биологической терапии для лечения ладонно-подошвенного псориаза и ладонно-подошвенного пустулеза: систематический обзор. Dermatol Ther (Heidelb). 2017 декабрь; 7 (4): 425-446. [Бесплатная статья PMC: PMC5698206] [PubMed: 29143230]
- 13.
- Bissonnette R, Poulin Y, Guenther L, Lynde CW, Bolduc C, Nigen S. Лечение ладонно-подошвенного псориаза инфликсимабом: рандомизированное двойное слепое плацебо -контролируемое исследование.J Eur Acad Dermatol Venereol. 2011 декабрь; 25 (12): 1402-8. [PubMed: 21349113]
- 14.
- Richetta AG, Mattozzi C, Giancristoforo S, D’Epiro S, Cantisani C, Macaluso L, Salvi M, Calvieri S. Безопасность и эффективность адалимумаба при лечении умеренной и тяжелой ладонной болезни. -подошвенный псориаз: открытое исследование. Clin Ter. 2012; 163 (2): e61-6. [PubMed: 22555836]
- 15.
- Au SC, Goldminz AM, Kim N, Dumont N, Michelon M, Volf E, Hession M, Lizzul PF, Andrews ID, Kerensky T., Wang A, Yaniv S, Gottlieb AB.Открытое исследование устекинумаба для лечения умеренного и тяжелого ладонно-подошвенного псориаза по инициативе исследователя. J Dermatolog Treat. 2013 июн; 24 (3): 179-87. [PubMed: 223]
- 16.
- Gottlieb A, Sullivan J, van Doorn M, Kubanov A, You R, Parneix A, Hugot S, Milutinovic M. Секукинумаб показывает значительную эффективность при ладонно-подошвенном псориазе: результаты GESTURE, рандомизированный контролируемое испытание. J Am Acad Dermatol. 2017 Янв; 76 (1): 70-80. [PubMed: 27707593]
- 17.
- Ментер А., Уоррен Р. Б., Лэнгли Р. Г., Мерола Дж. Ф., Керр Л. Н., Деннехи Э. Б., Шром Д., Амато Д., Окубо Ю., Райх К.Эффективность иксекизумаба по сравнению с этанерцептом и плацебо у пациентов с бляшечным псориазом средней и тяжелой степени и непустулезным поражением ладонно-подошвенной области: результаты трех исследований фазы 3 (UNCOVER-1, UNCOVER-2 и UNCOVER-3). J Eur Acad Dermatol Venereol. 2017 Октябрь; 31 (10): 1686-1692. [PubMed: 28322474]
Ладонно-подошвенный пустулез на руках и ногах: симптомы, причины, лечение
Что такое ладонно-подошвенный пустулез?
Ладонно-подошвенный пустулез (ППП) вызывает образование волдырей на ладонях и подошвах ног.Это также может вызвать трещины на коже или покраснение, чешуйчатые пятна. Это аутоиммунное заболевание, которое означает, что ваша иммунная система атакует здоровые части вашего тела.
От PPP нет лекарства, но дерматолог может вылечить его. Иногда это возвращается. Но он мог уйти и никогда не вернуться.
Симптомы ладонно-подошвенного пустулеза
Сначала PPP проявляется в виде крошечных пузырьков с желтым гноем. Со временем они становятся коричневыми и чешуйчатыми. PPP также может вызывать болезненные трещины на коже. Волдыри и язвы могут затруднить комфортную ходьбу или безболезненную работу руками.
Причины ладонно-подошвенного пустулеза
Причина неясна, но существует известная связь между PPP и курением. Исследования показывают, что до 90% людей с кожным заболеванием курили или когда-то курили.
Никотин в табачных изделиях может влиять на клетки кожи и вызывать воспаление потовых желез, особенно рук и ног. Если вы бросите курить, ваши симптомы могут улучшиться.
Заболевание может получить любой взрослый. Но у женщин он встречается чаще, чем у мужчин, и чаще всего он встречается у людей в возрасте от 40 до 60 лет.
Целых 24% людей с PPP также страдают псориазом. Псориаз возникает, когда клетки кожи быстро превращаются в толстые, серебристые чешуйки и зудящие, сухие, красные пятна.
Диагностика ладонно-подошвенного пустулеза
Чтобы узнать, есть ли у вас PPP, врач осмотрит вашу кожу. Чаще всего они берут безболезненный соскоб или мазок с этой области.
Иногда им нужно удалить небольшой кусочек кожи, чтобы подтвердить PPP. Эта область онемеет, и вам может понадобиться наложить несколько швов.Ваш врач осмотрит ткань под микроскопом, чтобы определить, есть ли у вас PPP.
Лечение ладонно-подошвенного пустулеза
Хотя PPP ничто не вылечит, лечение может помочь. Ваш может включать:
- Актуальные стероиды . Эти кремы, используемые со стерильной повязкой или виниловой повязкой, являются противовоспалительным средством. Они могут помочь при воспалении, отеке, нежности и боли.
- Каменноугольная смола. Эта мазь помогает заживить волдыри и уменьшить зуд.Угольная смола также замедляет производство клеток кожи и помогает избавиться от клеток, чтобы ваша кожа не стала толстой.
- Ацитретин таблетки. Сделанные из витамина А, они могут помочь вам контролировать PPP. Но ацитретин может иметь сильные побочные эффекты, поэтому он подходит не всем. Беременным женщинам или женщинам, которые могут забеременеть, не следует его использовать. Мужчинам, которые хотят иметь детей, следует проконсультироваться со своим врачом, прежде чем принимать его.
- Фототерапия или ПУВА. В этом лечении используются лекарства вместе с ультрафиолетом, чтобы замедлить рост кожи и помочь с симптомами в течение длительного периода времени.
Что вы можете сделать
Вот несколько советов, которые помогут вам почувствовать себя лучше:
- Если вы курите, бросьте.
- Не используйте пену для ванны или гель для душа. Используйте мыло с увлажняющим кремом.
- Защитите свою кожу. Надевайте виниловые перчатки, когда работаете с водой, пользуетесь бытовыми чистящими средствами или работаете в саду.
- Носите носки из 100% хлопка и избегайте обуви, сделанной из искусственных материалов.
- Будьте осторожны. Любые травмы, даже незначительные, могут причинить вред коже.Если у вас есть травма, используйте водонепроницаемые повязки.
- Содержите пораженные участки в чистоте.
- Чаще отдыхайте руками и ногами.
Предлагает ли новый препарат облегчение?
Ладонно-подошвенный псориаз (PPP), как известно, трудно поддается лечению. PPP проявляется эритематозными чешуйчатыми бляшками, трещинами и стерильными пустулами на ладонях и подошвах, которые вызывают значительную боль и болезненность. Факторы риска включают генетическую предрасположенность, курение и женский пол.
Управление сложно, с результатами, которые часто разочаровывают и непредсказуемы.Традиционные методы лечения — сверхпотентные местные кортикостероиды, пероральные ретиноиды, метотрексат, циклоспорин и фототерапия (UVB или PUVA) — обычно приводят только к частичному улучшению.
Провоспалительный цитокиновый путь IL-23/17 важен в патогенезе как псориаза обыкновенного, так и PPP. Было показано, что гуселкумаб, гуманизированное моноклональное антитело к субъединице белка p19 IL-23, очень эффективно устраняет умеренный и тяжелый хронический псориаз бляшек по сравнению с плацебо и блокатором TNF-альфа адалимумабом.Небольшое пилотное исследование этого агента, проведенное на японских пациентах с PPP, также дало многообещающие результаты.
Вдохновленные этими обнадеживающими открытиями, японские исследователи начали рандомизированное перекрестное исследование фазы 3, чтобы подтвердить безопасность и эффективность гуселкумаба в качестве монотерапии ППС.
В этом более крупном исследовании приняли участие 159 японских пациентов с PPP (средний возраст 53,3 года; 79,2% женщин). Участники были случайным образом распределены для получения плацебо, гуселкумаба 100 мг или гуселкумаба 200 мг подкожно на 0, 4, 12 неделях, а затем каждые 8 недель в течение всего 60 недель.На 16 неделе участники группы плацебо перешли на прием гуселкумаба.
Результаты. К 16 неделе показатели заболевания, измеренные с помощью объективных инструментов, улучшились больше у пациентов в обеих группах гуселкумаба по сравнению с плацебо. Более половины из тех, кто принимал гуселкумаб 100 мг, испытали улучшение более чем на 50% по сравнению с примерно третью тех, кто принимал плацебо. Однако удивительно, что у пациентов в группе гуселкумаба в дозе 200 мг отмечалось снижение тяжести заболевания, сравнимое с таковым в группе плацебо.Тяжесть заболевания, о которой сообщают пациенты, больше улучшилась у пациентов, получавших обе дозы гуселкумаба. Улучшение продолжалось до 52 недели. Побочные эффекты в обеих группах гуселкумаба были сопоставимы с таковыми в группе плацебо. Это 60-недельное исследование подтвердило, что гуселкумаб является безопасным и умеренно эффективным средством лечения PPP.
Смотровая площадка
PPP — это боль в шее, которую нужно лечить. Даже пациенты с ограниченной площадью поверхности тела, как правило, чувствуют себя несчастными. Поражая ладони и подошвы, болезнь вызывает непропорционально сильную боль и болезненность, часто не позволяя пациентам работать руками, ограничивая подвижность.Это усугубляется огнеупорной природой PPP. Местные методы лечения (кортикостероиды, кальципотриен, тазаротен) в лучшем случае дают умеренное улучшение, а реакция со временем ослабевает. Даже системные методы лечения (пероральные ретиноиды, метотрексат, циклоспорин, апремиласт) являются неудачными, и пациенты часто оказываются невосприимчивыми к комбинированным схемам.
Это исследование, посвященное изучению безопасности и эффективности гуселкумаба, приветствуется. Хотя результаты показывают, что гуселкумаб далек от успеха, он перспективен даже в качестве монотерапии.Было бы интересно посмотреть, можно ли добиться лучших результатов в сочетании с другими методами лечения, такими как местные кортикостероиды.
Одно важное предостережение: это исследование проводилось на японской популяции, поэтому в будущих исследованиях необходимо выяснить, верны ли эти результаты для других популяций. Исследование также имело перекрестный дизайн на 16 неделе, поэтому сравнение плацебо и гуселкумаба не могло быть проведено после 16 недели; следовательно, невозможно оценить долгосрочную эффективность.
Наконец, больше пациентов в группе гуселкумаба 100 мг достигли 50% улучшения, чем в группе гуселкумаба 200 мг.Исследователи предположили, что это может быть связано с непропорционально тяжелым заболеванием в группе 200 мг, но в будущих исследованиях потребуется прояснить это несоответствие.
В целом, гуселкумаб, возможно, не та серебряная пуля, на которую мы все надеялись для лечения PPP, но, по крайней мере, он может принести некоторое облегчение тем, кто страдает этой болезненной формой псориаза.
Грэм Липпер — клинический доцент Медицинского колледжа Университета Вермонта и партнер Advanced Dermcare в Данбери, штат Коннектикут.
Подпишитесь на Medscape в Facebook, Twitter, Instagram и YouTube
Псориаз кистей и стоп (включая ладонно-подошвенный пустулез) | Доктор
Синонимы: psoriasis palmoplantaris, psoriasis palmaris et plantaris
Псориаз, поражающий преимущественно ладони и подошвы, принимает две формы:
- Эритематозные чешуйчатые бляшки, характерные для псориаза в других частях тела.
- Более общее утолщение и шелушение (кератодермия).
Ладонно-подошвенный пустулез (ППП) — хроническое воспалительное заболевание кожи. Некоторые считают, что это разновидность псориаза и встречается у пациентов с другими типами псориаза [1] . Однако природа связи с псориазом неясна, и есть существенные различия. Нейроэндокринная дисфункция потовых желез была вовлечена в патогенез [2] . См. Раздел «Ладонно-подошвенный пустулез» в конце этой статьи.
См. Также отдельную статью о псориатической болезни ногтей.
Эпидемиология
Распространенность псориаза в Великобритании за последние годы увеличилась. Это было 2,3% (2 297 случаев на 100 000) в 1999 г., но 2,8% (2 815 на 100 000) в 2013 г. [3] . Однако связанного с этим увеличения заболеваемости не было. Это говорит о том, что пациенты с псориазом живут дольше, хотя причины этого неясны. У части этих пациентов, обычно с псориатическими поражениями в другом месте, будет псориаз стоп и рук.
Внешний вид
Псориаз стопы с проявлением гиперкератоза
Внешний вид
- Красные чешуйчатые бляшки.
- Гиперкератотические зоны.
- Центральная часть ладони или опорные участки подошвы.
- Скважина разграничена.
- Болезненные трещины и трещины.
Дифференциальный диагноз
- Гиперкератотическая экзема.
- Tinea pedis.
- Ладонно-подошвенный пустулез (ППП) (см. Раздел ниже).
Ведение
См. Также отдельную статью о хроническом псориазе с бляшками.
Первичная медицинская помощь
- Классические псориатические поражения можно лечить мазью с витамином D (кальципотриол / Довонекс® или такальцитол / Куратодерм®) или дитранолом (Дитрокрим® / Миканол®).
- При псориазе ладони и подошвы обычно присутствуют как гиперкератоз, так и воспаление, и может потребоваться отдельное лечение:
- Гиперкератоз обычно необходимо лечить кератолитическим средством, таким как 2% мазь с салициловой кислотой BP.
- Это можно чередовать утром и вечером с местным стероидом (обычно сильнодействующим из-за толстой кожи на этом участке) [1] .
Когда обращаться
[4]- Где есть диагностическая неопределенность.
- Для дальнейшего консультирования и обучения пациентов.
- Если местное лечение не удалось или лечение не переносится.
- При наличии значительных физических, психологических, социальных или профессиональных трудностей.
Дальнейшее лечение
Дальнейшие варианты лечения при вторичной помощи включают низкие дозы пероральных ретиноидов с псораленом в сочетании с ультрафиолетовой фототерапией A (PUVA) или UVB, метотрексатом, циклоспорином или ацитретином. Ингибиторы кальциневрина, такие как такролимус или пимекролимус, и биологические агенты, такие как инфликсимаб и алефасепт, были использованы с некоторым успехом [5] .
Осложнения
Боль может ограничивать использование рук или ходьбу.
Прогноз
Псориаз кистей и стоп имеет тенденцию быть стойким и в некоторых случаях довольно устойчивым к лечению.
Ладонно-подошвенный пустулез
Причина PPP неизвестна. Вероятно, он имеет аутоиммунное происхождение, поскольку существует связь с другими аутоиммунными заболеваниями, в частности с глютеновой болезнью, заболеванием щитовидной железы и диабетом 2 типа [1] . Считалось, что PPP является локальной формой пустулезного псориаза, но около 10-20% пациентов с PPP страдают псориазом в другом месте.Поэтому сейчас считается, что это разные состояния с разным генетическим фоном [1] .
Эпидемиология
Заболевание редко в Европе, но чаще встречается на Востоке [6] . Гораздо чаще встречается у курильщиков и бывших курильщиков. Он может передаваться в семьях и редко возникает в детстве. В некоторых случаях замешаны чувствительность к глютену и стрептококковая инфекция миндалин [7] .
Presentation
PPP обычно проявляется в виде множественных стерильных пустул на ладонях и подошвах (первоначально желтоватые, постепенно переходящие в коричневые точечные поражения желтого пятна).
Ладонно-подошвенный пустулез стопы
Пораженные участки могут стать красными, чешуйчатыми и часто болезненными. Высыпания из пустул возникают непредсказуемо и могут повторяться неоднократно в течение многих лет.
Дифференциальный диагноз
- Инфицированная экзема — менее выраженная, белые пузырьки, а не пустулы, тампоны часто растут Staphylococcus aureus .
- Острый помфоликс — это эпизодическая форма экземы, поражающая ладони и подошвы с образованием пузырей, которые часто инфицируются.
- Tinea pedis — обычно односторонняя или асимметричная эритема, шелушение и пустулы. Обычно поражаются расщелины пальцев ног и ногти.
- Реактивный артрит — могут возникать крупные поражения ладоней и подошв (keratoderma blennorrhagica), которые гистологически неотличимы от псориаза. Это также влияет на рот и половой член.
- Континуальный акродерматит Галлопо (ACH): редкая вялотекущая форма псориаза со стерильными пустулезными изменениями и дактилитом, поражающим дистальные части пальцев и ногтей [8] .
Управление первичной медико-санитарной помощью
[1, 9]Доказательная методика лечения ППС является спорной.
Те, кто утверждает, что PPP — это просто разновидность псориаза, полагают, что с этим заболеванием следует лечить в соответствии с рекомендациями по псориазу, но по этому поводу нет единого мнения. [10] . Используются различные методы лечения, но ни один из них не считается универсально эффективным [7] . В Кокрановском обзоре выявлены методологические проблемы исследований, разработанных для того, чтобы различать эффективность различных подходов [11] .
- Поощрять общие меры:
- Хорошая обувь из натуральных волокон.
- Предотвращение даже незначительных травм.
- Водонепроницаемые повязки на трещинах.
- По возможности дать отдых пострадавшему месту.
- Смягчающие вещества важны:
- Наносите густые жирные смягчающие средства, чтобы смягчить кожу и предотвратить образование трещин.
- Замочить в теплой воде с эмульгирующей мазью.
- Для очистки омертвевшей кожи используйте мазь с салициловой кислотой или крем с мочевиной.
- Мытье с заменителями мыла.
- Сильные местные стероидные мази — например, пропионат клобетазола — можно использовать два раза в день в течение ограниченного периода времени. Для проникновения через толстую кожу рук и ног необходимы сильнодействующие стероиды. Окклюзия пищевой пленкой или повязкой может улучшить проникновение, но не должна использоваться более пяти дней подряд.
- Каменноугольная смола грязная, но ее можно наносить непосредственно, часто смешивая с мазевой основой.
- Кальципотриол может быть полезным — применяйте два раза в день и не покрывайте.
Когда обращаться
[1]- Направления в первую очередь предназначены для получения помощи в диагностике и лечении, или если симптомы вызывают особую инвалидность.
- Ладони и подошвы трудно поддаются лечению, и PPP может быть устойчивым к лечению, поэтому может потребоваться консультация специалиста.
Дальнейшее лечение
[12]Дальнейшие варианты лечения, которые могут использовать дерматологи, включают:
- Системные ретиноиды, например, ацитретин, этиловый эфир аротиноида.
- ПУВА-терапия для рук и ног (иногда в сочетании с системными ретиноидами).
- Метотрексат [1] .
- Иногда используется этанерцепт. Сообщается о хорошем ответе на комбинацию этанерцепта и алитретиноина [13] .
- Фототерапия и циклоспорин также оказались полезными.
Осложнения
- Боль от поражений и связанных трещин может быть значительной.
- Продолжительная ходьба и стояние могут усугубить поражение подошв ног.
- Ручная работа может быть неудобной, если затронуты руки.
- Второстепенная профессиональная и функциональная инвалидность по отношению к вышеуказанной.
- Пустулотический артроостит (стерильный воспалительный остит грудино-ключичной области) — редкое, но тяжелое осложнение ладонного пустулеза [14] .
Прогноз
Состояние имеет тенденцию быть хроническим и плохо поддается лечению [1] .
Границы | Успешное лечение рефрактерного ладонно-подошвенного пустулезного псориаза апремиластом: серия клинических случаев
Введение
Ладонно-подошвенный пустулезный псориаз (PPPP) — хроническое воспалительное заболевание кожи, обусловленное метаболическим путем IL-17/23, характеризующееся развитием стерильных пустул на ладонях и подошвах (1).Распространенность колеблется от 0,01 до 0,05% в Западной Европе и Северной Америке с несколько более высокими показателями ~ 0,12% в Японии. PPPP преимущественно поражает курящих женщин и ассоциируется с относительно высокой частотой сопутствующего артрита (2, 3). PPPP приводит к изнурительным состояниям кожи и значительному ухудшению качества жизни. Кроме того, пациенты с PPPP сообщают о более частом использовании сильнодействующих местных противовоспалительных средств по сравнению с пациентами с псориазом бляшечного типа от умеренной до тяжелой степени (4).
Несмотря на истощающие эффекты этого заболевания, понимание патогенеза PPPP скудно. Несколько исследований указывают на доминирующую роль IL-17 и IL-22 в ладонно-подошвенном пустулезе (5, 6). Патогенетические признаки PPPP включают повышенную кожную экспрессию IL-17A и, в отличие от псориаза, более низкую экспрессию IL-23 (7). Поскольку движущие патологические механизмы заболевания недостаточно хорошо освещены, лечение PPPP часто является сложной задачей. Хотя лекарства, используемые для лечения вульгарного псориаза, как правило, не имеют одобрения регулирующих органов для PPPP, они часто используются у этих пациентов из-за ограниченных вариантов лечения.Современные методы лечения PPPP, основанные на низком уровне доказательности и мнениях экспертов, [например, фототерапия, циклоспорин A (CsA) и местные кортикостероиды], приводят к ремиссии у некоторых пациентов (8). Однако для поддержания ремиссии требуется длительная иммуносупрессия, и рецидивы случаются часто. Кроме того, связанные с лечением побочные эффекты и заболеваемость увеличивают нагрузку на пациентов и снижают качество жизни. Следовательно, исследование новых эффективных и безопасных вариантов лечения является весьма оправданным.
Апремиласт — это низкомолекулярный пероральный ингибитор фосфодиэстеразы (ФДЭ) 4, одобренный для лечения бляшечного псориаза средней и тяжелой степени и псориатического артрита (9). На молекулярном уровне апремиласт предотвращает гидролиз цАМФ, что приводит к увеличению внутриклеточных уровней цАМФ и последующей передаче сигналов с последующим снижением NF-каппа-B-зависимой противовоспалительной передачи сигналов (например, опосредованного протеинкиназой А высвобождения IL-10) ( 10, 11). Рандомизированные испытания и исследования в реальных условиях недавно документально подтвердили эффективность и безопасность апремиласта у пациентов с псориазом (12-15).В то время как безопасность была доказана на большом количестве пациентов, эффективность апремиласта в отношении PPPP не была хорошо изучена, и данные об использовании апремиласта как у рефрактерных к лечению, так и у пациентов, ранее не получавших PPPP. Следовательно, чтобы добавить больше информации об использовании апремиласта у пациентов с PPPP, мы ретроспективно проанализировали эффективность введения апремиласта у тяжелых и очень тяжелых пациентов с PPPP, рефрактерных к нескольким предшествующим местным и системным лечениям.
Пациенты и методы
Шесть пациентов [средний возраст (лет ± стандартное отклонение): 56.2 ± 15,6, четыре женщины, два мужчины] с рефрактерным PPPP [средняя продолжительность заболевания (лет ± стандартное отклонение): 13,7 ± 10,6]. Четыре пациента наблюдались в течение 18 месяцев и двое в течение 6 месяцев. Данные были проанализированы ретроспективно. У пяти пациентов был сопутствующий псориатический артрит (ПсА). Диагноз ПсА был основан на выполнении критериев классификации CASPAR и подтвержден нашими ревматологами. Характеристики пациентов приведены в таблице 1. Все шесть пациентов ранее получали местно применяемые сильнодействующие глюкокортикостероиды (ГК), частично в условиях окклюзии, псорален-ультрафиолет А (УФА), метотрексат (МТ) и по крайней мере четыре различных системных антибиотика. — противовоспалительные препараты до начала лечения апремиластом.Большинство пациентов получали пероральные ретиноиды [ацитретин (5/6) или алитретиноин (2/6)] (таблица 2). Четыре пациента получали CsA, а трое лечили биопрепаратами. У всех пациентов предыдущее лечение не удалось или было прекращено из-за побочных эффектов. Лечение апремиластом начинали с первоначально низкой, а затем увеличивали дозу до достижения поддерживающей дозы 30 мг 2 раза в день. Клиническое состояние оценивалось по общей оценке врача (PGA) как PGA = 0 [очищено (0 пустул)], PGA = 1 [легкое (1-3 пустулы)], PGA = 2 [умеренное (3-10 пустул)], PGA. = 3 [тяжелая форма (10–20 пустул)], PGA = 4 [очень серьезная форма (> 20 пустул)] в области, пораженной пустулами e.г., ладони и / или подошвы. Для их ретроспективного анализа не требовалось этического одобрения.
Таблица 1 . Характеристики шести пациентов с резистентным к лечению PPPP, получавших апремиласт.
Таблица 2 . Предварительное лечение перед лечением апремиластом.
Результаты
После начала лечения состояние кожи пациентов улучшилось в течение первых 4 недель лечения, с PGA = 4 в двух случаях и PGA = 3 в четырех случаях до PGA = 1 в пяти случаях и PGA = 2 в одном случае.После 12-недельного контрольного визита у четырех пациентов была оценка PGA = 1, а у двух — оценка PGA = 0. Четыре пациента имели PGA = 1 балл через 18 месяцев, тогда как два пациента прекратили прием препарата через 6 месяцев, один из-за отсутствия эффекта на поражение суставов, а другой из-за желания иметь детей (рис. 1). У всех шести пациентов побочные эффекты были легкими и включали переносимые побочные эффекты со стороны желудочно-кишечного тракта (например, тошноту, диарею) после приема первых пероральных доз апремиласта. Серьезных нежелательных явлений при приеме апремиласта не наблюдалось.
Рисунок 1 . Улучшение пустулезного ПГА к концу срока наблюдения. Парный т -тест р <0,001.
Подробнее, Пациентке 1 (женщина 75 лет) диагноз ПППЗ был поставлен 33 годами ранее. Сопутствующие заболевания — ПсА и фибромиалгия. Предыдущее лечение PPPP включало системный ацитретин (20 мг / день) в сочетании с псораленом-UVA, метотрексатом (15 мг / неделя п / к) и CsA (3 мг / кг / мт). Эти методы лечения не переносились и поэтому были прекращены.Через пять недель после начала приема апремиласта у пациентки PsA существенно улучшилось, и ее PPPP был оценен как PGA = 1 после первоначального PGA = 3 (рис. 2). При контрольном посещении через 5 месяцев у пациента возник рецидив PPPP после отмены апремиласта за 3 недели до визита (рецидив произошел через 2 недели после отмены и за 1 неделю до визита). Через несколько дней после повторного введения апремиласта она достигла показателя PGA = 1, который оставался стабильным при последующих посещениях.
Рисунок 2 . Ладони и подошвы пациента 1 с многочисленными пустулами на красной чешуйчатой коже на исходном уровне (A – C) и после 5 недель лечения апремиластом (D – F) с частичной ремиссией и уменьшением воспаления.
Пациенту 2 (55-летняя женщина) был поставлен диагноз PPPP за 7 лет до обращения. Одновременно она страдала ПА, артериальной гипертонией, депрессией, ожирением и диабетом II типа. Предыдущее лечение ацитретином (30 мг / день), псораленом-UVA, CsA (300 мг / день), адалимумабом, устекинумабом и секукинумабом не улучшило поражение кожи.Из-за побочных эффектов (например, инфекций) биологическое лечение было прекращено. После начала приема апремиласта пациентка сообщила о быстром субъективном исчезновении симптомов в течение нескольких дней. Через 4 недели количество и размер пустул уменьшились, а активность заболевания улучшилась с PGA = 4 до PGA = 2. Через 3 месяца лечения апремиластом и при всех последующих контрольных визитах у пациента был зарегистрирован PGA = 1 (рис. 3).
Рисунок 3 . Левая подошва пациента 2 с многочисленными сливающимися пустулами на воспаленной коже на исходном уровне (a) и после 12 недель лечения апремиластом (b) со значительным уменьшением воспаления и пустул.
Пациенту 3 (мужчина 54 лет) диагноз PPPP был поставлен 6 лет назад. Предыдущее лечение включало алитретиноин (30 мг / день), ацитретин (50 мг / день), метотрексат (20 мг / неделю) и псорален-UVA. Ни один из этих методов лечения не приводил к ремиссии. Пациент поступил клинически с тяжелым PPPP (PGA = 3). После начала приема апремиласта пациентка сообщила о значительном субъективном улучшении состояния кожи в течение 10 дней. Однако прием препарата был прекращен из-за депрессивного эпизода через 4 месяца (отсутствие суицидальных мыслей) с последующим новым появлением пустул в течение 2 дней.После междисциплинарной психиатрической консультации была возобновлена терапия апремиластом, что привело к значительному улучшению состояния кожных повреждений в течение 1 недели. Пациент сохранял PGA = 1 на всех последующих визитах.
Пациенту 4 (35-летняя женщина) был поставлен диагноз PPPP 12 лет назад, и у него был сопутствующий ПсА. Предыдущее лечение включало пероральные ГК, псорален-УФА, секукинумаб, CsA (250 мг / сут), азатиоприн (доза не помнялась) и метотрексат (20 мг / нед подкожно). Пациент страдает тяжелым поражением кожи PGA = 3.Поражения кожи улучшились в течение 2 недель после начала приема апремиласта до PGA = 1. На 12-й неделе контрольного визита наблюдали полное исчезновение пустул на ладонях и подошвах (PGA = 0). Однако впоследствии прием апремиласта был прекращен из-за желания пациентки иметь ребенка.
Пациенту 5 (72-летняя женщина) был поставлен диагноз PPPP 18 лет назад; у нее также был сопутствующий ПсА. Предыдущие методы лечения включали пероральные ГК, метотрексат (25 мг / неделя), псорален-UVA, алитретиноин (30 мг / день) и ацитретин (25 мг / день).После первоначального парадоксального ухудшения тяжелых поражений кожи ладонно-подошвенной области до PGA = 3, улучшение до PGA = 2 наблюдалось через 4 недели. При следующем посещении пациент зарегистрировал PGA = 1 для ладоней и PGA = 1–2 для подошв. Состояние кожи пациента оставалось стабильным при PGA = 1 в течение 18 месяцев во время продолжающегося лечения апремиластом.
Пациенту 6 (47-летний мужчина) был поставлен диагноз PPPP 6 лет назад, у него были сопутствующие ПсА и депрессия. Предыдущее лечение ацитретином (40 мг / день), псорален-UVA, метотрексатом (20 мг / неделя), CsA (до 400 мг / день), пероральными кортикостероидами ГК (до 10 мг / день) и секукинумабом (300 мг в месяц) были прекращены из-за отсутствия эффективности и / или побочных эффектов.Из-за очень болезненного поражения суставов при нынешнем режиме терапии, включая комбинированный секукинумаб и CsA, пациентка получала преднизолон (10 мг / сут) за несколько недель до и первоначально в течение первых дней лечения апремиластом. Через четыре недели после начала приема апремиласта пациент сообщил о клинических улучшениях до PGA = 1. Через 12 недель наблюдения активность заболевания снизилась до PGA = 2 с пятью пустулами на ладонях. На подошвах не было пустул, но было небольшое шелушение на эритематозной коже (PGA = 0).Однако из-за обострения ПсА прием апремиласта был прекращен через 6 месяцев, чтобы начать лечение ингибитором ФНО-альфа. На момент отмены апремиласта у пациента были очищены подошвы и PGA = 1 ладони. У всех шести пациентов побочные эффекты были легкими и включали переносимые побочные эффекты со стороны желудочно-кишечного тракта (например, тошноту, диарею) после первого перорального введения апремиласта. Серьезных нежелательных явлений при приеме апремиласта не наблюдалось.
Обсуждение
Терапевтические подходы к PPPP имеют ограниченную эффективность, и многие пациенты остаются невосприимчивыми ко всем доступным агентам; Крайне необходимы новые варианты лечения этого состояния.Апремиласт, низкомолекулярный ингибитор ФДЭ4, представляет собой новый противовоспалительный препарат, который доказал свою эффективность при псориазе бляшечного типа и псориазе за последние годы, но не был хорошо изучен в отношении резистентности к PPPP. Однако в описаниях клинических случаев апремиласт является альтернативой пациентам с рефрактерным и тяжелым ППС. Однако контролируемых наблюдений относительно использования апремиласта при PPPP остается немного.
Ингибируя PDE4, апремиласт увеличивает внутриклеточный циклический AMP, который является важным вторичным посредником в иммунных клетках, влияющих на воспалительный каскад (16).В PPPP Т-клетки продуцируют многочисленные цитокины, включая TNF-a, IL-17 и IL-22, которые стимулируют пролиферацию кератиноцитов (17). Ингибирование провоспалительных цитокинов, таких как IL-23, апремиластом снижает рекрутирование Th2 и Th27 в кожу. У пациентов с псориазом от умеренной до тяжелой степени лечение апремиластом было связано со значительным снижением уровней интерлейкина (IL) -17F, IL-17A, IL-22 и TNF-α в плазме. Кроме того, блокада PDE4 ингибирует хемотаксис нейтрофилов за счет снижения выработки лейкотриена B4 и IL-8 и предотвращает миграцию нейтрофилов в эпидермис (16).Мутация гена IL-36RN (антагониста рецептора) может играть важную роль в пустулезных формах псориаза, таких как GPP (генерализованный пустулезный псориаз) и континуальный акродерматит Галлопо. Напротив, PPP, по-видимому, не связан с мутацией RN IL36 и имеет патогенез, отличный от GPP (18). Поскольку апремиласт модулирует как провоспалительные, так и противовоспалительные медиаторы, это может частично объяснить клиническую эффективность PPPP.
Наша серия дел дополняет совокупность доказательств использования апремиласта в PPPP.Насколько нам известно, это первая серия случаев, в которой описывается успешное применение апремиласта у шести тяжелых, не поддающихся лечению пациентов с ПППП, у пяти из которых был сопутствующий ПсА в течение 18 месяцев. У всех пациентов улучшилось состояние во время лечения апремиластом, и не было сообщений о серьезных нежелательных явлениях при лечении.
Эти наблюдения кажутся первым многообещающим намеком на использование апремиласта при тяжелом и рефрактерном PPPP. Наши данные подтверждают начало более крупных рандомизированных контролируемых исследований апремиласта как у ранее не получавших лечения, так и у пациентов с резистентным к лечению ПППП.
Заявление о доступности данных
Все наборы данных, созданные для этого исследования, включены в статью / дополнительный материал.
Заявление об этике
Этическое одобрение для этого исследования не требовалось в соответствии с местным законодательством и национальными руководящими принципами, поскольку в исследовании описывается рутинный уход, не требующий этического одобрения. Письменное информированное согласие было получено от всех участников на публикацию любых идентифицируемых изображений или данных в статье.
Авторские взносы
DT разработал исследование. DT и FS лечили и документировали пациентов. СС извлек все данные из электронной документации. SS, FS, RL и DT написали рукопись и внесли свой вклад в переработку, прочитали и одобрили представленную версию. Все авторы внесли свой вклад в статью и одобрили представленную версию.
Финансирование
Это исследование было поддержано Немецким исследовательским фондом (DFG) в рамках стратегии Germanys Excellence Strategy-EXC 2167-3
018 «Прецизионная медицина при хроническом воспалении при DT и RL».
Конфликт интересов
RL получил гонорары и / или исследовательские гранты от следующих компаний: Admirx, Almirall, Amryth, ArgenX, Biotest, Biogen, Euroimmun, Incyte, Immungenetics, Lilly, Novartis, UCB Pharma, Topadur, True North Therapeutics и Tx Cell. DT получала гонорары или гонорары за работу в консультативных советах, выступление в качестве спикера или консультанта от AbbVie, Amgen, Almirall, Beiersdorf, Bioskin, Biogen, Boehringer Ingelheim, Celgene, Galapagos, GlaxoSmithKline, Dignity-Science, Leo Pharma. , Medac, Merck Sharp & Dohme, Morphosys, Lilly, Novartis, Janssen, Pfizer, Regeneron, Sanofi, Samsung, Sandoz, Hexal, Sun Pharmaceuticals, UCB; и получил гранты от Celgene и Novartis.
Остальные авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Список литературы
1. Биссоннетт Р., Фуэнтес-Дукулан Дж., Машико С., Ли Х, Бонифачо К.М., Куэто И. и др. Ладонно-подошвенный пустулезный псориаз (PPPP) характеризуется активацией пути IL-17A. J Dermatol Sci. (2017) 85: 20–6. DOI: 10.1016 / j.jdermsci.2016.09.019
PubMed Аннотация | CrossRef Полный текст | Google Scholar
2.Brunasso AM, Puntoni M, Aberer W., Delfino C, Fancelli L, Massone C. Клинико-эпидемиологическое сравнение пациентов, страдающих псориазом ладонно-подошвенной бляшки и ладонно-подошвенным пустулезом: исследование серии случаев. Br J Dermatol. (2013) 168: 1243–51. DOI: 10.1111 / bjd.12223
PubMed Аннотация | CrossRef Полный текст | Google Scholar
3. Кубота К., Камидзима Ю., Сато Т., Оба Н., Коидэ Д., Иидзука Х. и др. Эпидемиология псориаза и ладонно-подошвенного пустулеза: общенациональное исследование с использованием национальной базы данных заявлений Японии. BMJ Open. (2015) 5: e006450. DOI: 10.1136 / bmjopen-2014-006450
PubMed Аннотация | CrossRef Полный текст | Google Scholar
4. Чанг Дж., Даффин К.С., Такешита Дж., Шин Д.Б., Крюгер Г.Г., Робертсон А.Д. и др. Ладонно-подошвенный псориаз связан с большим ухудшением качества жизни, связанного со здоровьем, по сравнению с бляшечным псориазом от умеренной до тяжелой степени. J Am Acad Dermatol. (2014) 71: 623–32. DOI: 10.1016 / j.jaad.2014.04.063
PubMed Аннотация | CrossRef Полный текст | Google Scholar
5.Murakami M, Hagforsen E, Morhenn V, Ishida-Yamamoto A, Iizuka H. У пациентов с ладонно-подошвенным пустулезом повышены уровни IL-17 и IL-22 как в очаге поражения, так и в сыворотке. Exp Dermatol. (2011) 20: 845–7. DOI: 10.1111 / j.1600-0625.2011.01325.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
6. Hagforsen E, Hedstrand H, Nyberg F, Michaëlsson G. Новые открытия клеток Лангерганса и экспрессии интерлейкина-17 в отношении акросирингиума и пустулы при ладонно-подошвенном пустулезе. Br J Dermatol. (2010) 163: 572–9. DOI: 10.1111 / j.1365-2133.2010.09819.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
7. Биссоннетт Р., Ниген С., Лэнгли Р.Г., Линде К.В., Тан Дж., Фуэнтес-Дукулан Дж. И др. Повышенная экспрессия IL-17A и ограниченное участие IL-23 у пациентов с ладонно-подошвенным (PP) пустулезным псориазом или PP-пустулезом; результаты рандомизированного контролируемого исследования. J Eur Acad Dermatol Venereol. (2014) 28: 1298–305. DOI: 10.1111 / jdv.12272
CrossRef Полный текст | Google Scholar
8. Севрен М., Ричард М.А., Барнетче Т., Рузо М., Виллани А.П., Пол С. и др. Лечение ладонно-подошвенного пустулезного псориаза: систематический обзор литературы, научно обоснованные рекомендации и мнение экспертов. J Eur Acad Dermatol Venereol JEADV 28 Suppl. (2014) 5: 13–6. DOI: 10.1111 / jdv.12561
CrossRef Полный текст | Google Scholar
10. Schafer PH, Parton A, Capone L, Cedzik D, Brady H, Evans JF, et al.Апремиласт — селективный ингибитор PDE4, регулирующий врожденный иммунитет. Cell Signal. (2014) 26: 2016–29. DOI: 10.1016 / j.cellsig.2014.05.014
PubMed Аннотация | CrossRef Полный текст | Google Scholar
12. Вуйич И., Херман Р., Санлоренцо М., Пош К., Монши Б., Рапперсбергер К. и др. Апремиласт при псориазе — проспективное исследование в реальных условиях. J Eur Acad Dermatol Venereol. (2018) 32: 254–9. DOI: 10.1111 / jdv.14598
PubMed Аннотация | CrossRef Полный текст | Google Scholar
13.Райх К., Гудерхэм М., Бьюли А., Грин Л., Сунг Дж., Петрик Р. и др. Безопасность и эффективность апремиласта в течение 104 недель у пациентов с псориазом средней и тяжелой степени тяжести, которые продолжали принимать апремиласт или перешли с лечения этанерцептом: результаты исследования LIBERATE. J Eur Acad Dermatol Venereol. (2018) 32: 397–402. DOI: 10.1111 / jdv.14738
CrossRef Полный текст | Google Scholar
14. Кроули Дж., Тачи Д., Джоли П., Перис К., Папп К.А., Гонсалвес Дж. И др. Долгосрочная безопасность и переносимость апремиласта у пациентов с псориазом: объединенный анализ безопасности для ≥156 недель из 2 фазы 3, рандомизированных контролируемых исследований (ESTEEM 1 и 2). J Am Acad Dermatol. (2017) 77: 310–7.e1. DOI: 10.1016 / j.jaad.2017.01.052
PubMed Аннотация | CrossRef Полный текст | Google Scholar
15. Пападавид Э., Ромпоти Н., Теодоропулос К., Коккалис Г., Ригопулос Д. Реальные данные об эффективности и безопасности апремиласта у пациентов с бляшечным псориазом средней и тяжелой степени. J Eur Acad Dermatol Venereol. (2018) 32: 1173–9. DOI: 10.1111 / jdv.14832
PubMed Аннотация | CrossRef Полный текст | Google Scholar
16.Шафер PH, Партон А., Ганди А. К., Капоне Л., Адамс М., Ву Л. и др. Апремиласт, ингибитор цАМФ-фосфодиэстеразы-4, демонстрирует противовоспалительную активность in vitro и на модели псориаза. Br J Pharmacol. (2010) 159: 842–55. DOI: 10.1111 / j.1476-5381.2009.00559.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
17. Мураками М., Теруи Т. Ладонно-подошвенный пустулез: современное понимание определения заболевания и патомеханизма. J Dermatol Sci. (2020) 98: 13–9. DOI: 10.1016 / j.jdermsci.2020.03.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
18. Месснер Р., Фрамбах Ю., Вильсманн-Тайс Д., Лёр С., Якоби А., Вейерграф А. и др. Ладонно-подошвенный пустулезный псориаз связан с миссенс-вариантами CARD14, но не с мутациями потери функции в IL36RN у европейских пациентов.

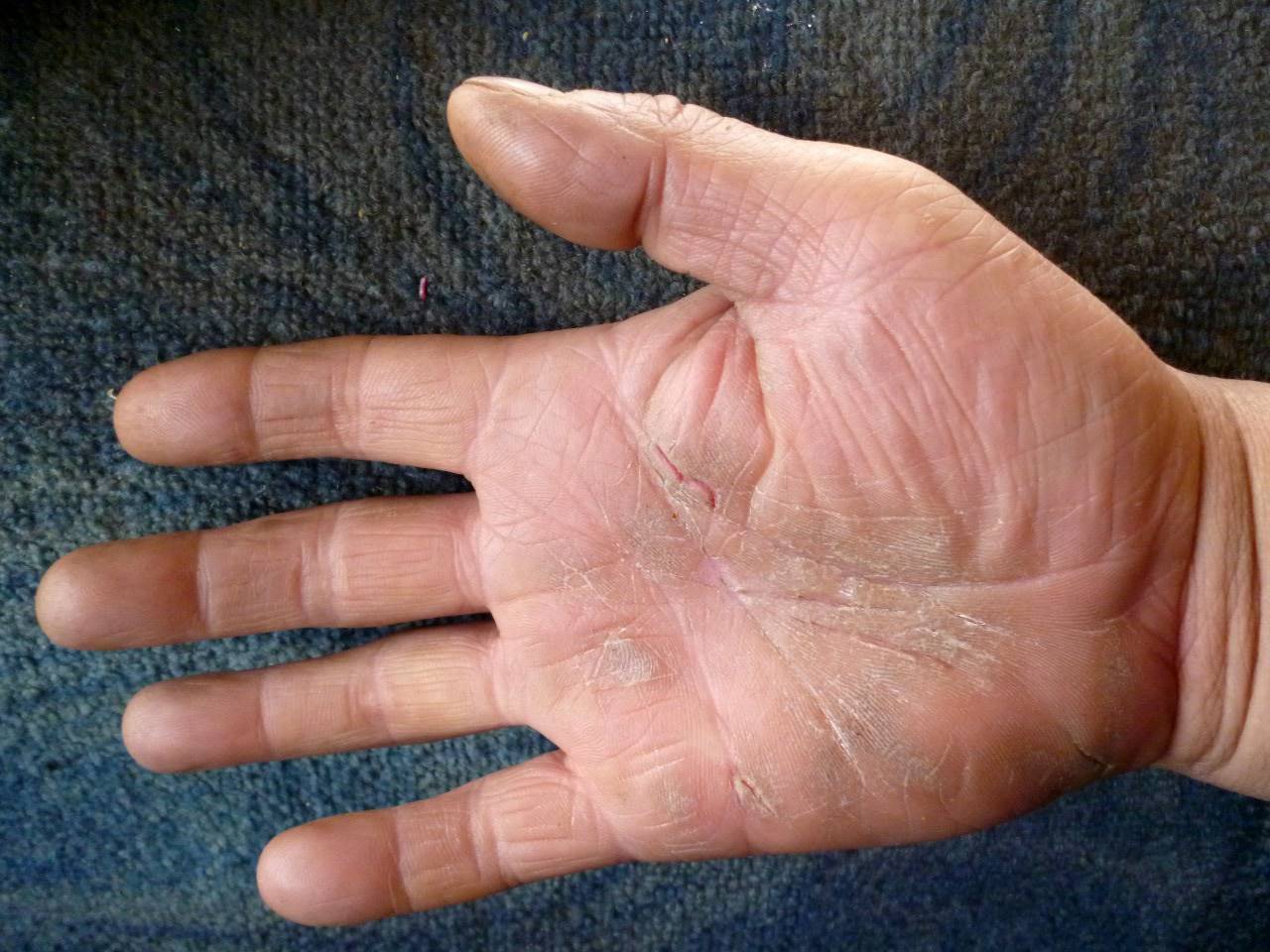
 1). Following the 6 day titration period (for Day 0 and week 16) blister packs will contain apremilast 30 mg bid or placebo bid.
1). Following the 6 day titration period (for Day 0 and week 16) blister packs will contain apremilast 30 mg bid or placebo bid.
 3. Пациент, который использовал какие-либо местные средства для лечения псориаза (кроме немедикаментозных). смягчающие средства) за последние 14 дней до дня 0, за исключением гидрокортизона и дезонид для лица, паха (включая гениталии) и инфрамаммарных областей, а также шампуни, содержащие деготь, салициловую кислоту или пиритион цинка, если они применяются с перчатки. 4. Пациентам, которые использовали фототерапию ультрафиолетом B (UVB) или чрезмерное пребывание на солнце, меньше чем за 28 дней до дня 0. 5. Пациент использовал любую небиологическую системную терапию для лечения псориаза. (включая ультрафиолетовый псорален А (ПУВА)), метотрексат, ацитретин и циклоспорин), системные стероиды или системные иммунодепрессанты менее 28 дней до дня 0. 6. Использование любых исследуемых агентов в течение 4 недель до рандомизации или 5 фармакокинетические / фармакодинамические периоды полураспада, если они известны (в зависимости от того, что больше). 7. Предварительное лечение апремиластом. 8.
3. Пациент, который использовал какие-либо местные средства для лечения псориаза (кроме немедикаментозных). смягчающие средства) за последние 14 дней до дня 0, за исключением гидрокортизона и дезонид для лица, паха (включая гениталии) и инфрамаммарных областей, а также шампуни, содержащие деготь, салициловую кислоту или пиритион цинка, если они применяются с перчатки. 4. Пациентам, которые использовали фототерапию ультрафиолетом B (UVB) или чрезмерное пребывание на солнце, меньше чем за 28 дней до дня 0. 5. Пациент использовал любую небиологическую системную терапию для лечения псориаза. (включая ультрафиолетовый псорален А (ПУВА)), метотрексат, ацитретин и циклоспорин), системные стероиды или системные иммунодепрессанты менее 28 дней до дня 0. 6. Использование любых исследуемых агентов в течение 4 недель до рандомизации или 5 фармакокинетические / фармакодинамические периоды полураспада, если они известны (в зависимости от того, что больше). 7. Предварительное лечение апремиластом. 8. В настоящее время пациент участвует в клиническом исследовании с экспериментальным агентом или устройство. 9. Пациент принимает или использовал любую биологическую терапию для лечения псориаза. Исключениями из этого критерия являются: пациенты, которые использовали не более одного биологического препарата в прошедшие и прекращенные по причинам, не связанным с недостаточной эффективностью. 10. Пациент принимает или нуждается в пероральных или инъекционных кортикостероидах во время исследования. Разрешены ингаляционные кортикостероиды при стабильных заболеваниях. Пациенты, у которых есть использованные пероральные или инъекционные кортикостероиды менее чем за 28 дней до дня 0 исключаются. 11. Известно, что у пациента имеется иммунодефицит или ослаблен иммунитет, или он в настоящее время употребляет или планирует использовать антиретровирусную терапию в любое время во время исследования. 12. Активный туберкулез или неадекватное лечение туберкулеза в анамнезе. 13. Кроме псориаза, у пациента есть какие-либо клинически значимые (как определено Исследователь) кардиологические, эндокринологические, легочные, неврологические, психиатрические, печеночные, почечное, гематологическое, иммунологическое заболевание или другое серьезное заболевание, которое в настоящее время неконтролируемый.
В настоящее время пациент участвует в клиническом исследовании с экспериментальным агентом или устройство. 9. Пациент принимает или использовал любую биологическую терапию для лечения псориаза. Исключениями из этого критерия являются: пациенты, которые использовали не более одного биологического препарата в прошедшие и прекращенные по причинам, не связанным с недостаточной эффективностью. 10. Пациент принимает или нуждается в пероральных или инъекционных кортикостероидах во время исследования. Разрешены ингаляционные кортикостероиды при стабильных заболеваниях. Пациенты, у которых есть использованные пероральные или инъекционные кортикостероиды менее чем за 28 дней до дня 0 исключаются. 11. Известно, что у пациента имеется иммунодефицит или ослаблен иммунитет, или он в настоящее время употребляет или планирует использовать антиретровирусную терапию в любое время во время исследования. 12. Активный туберкулез или неадекватное лечение туберкулеза в анамнезе. 13. Кроме псориаза, у пациента есть какие-либо клинически значимые (как определено Исследователь) кардиологические, эндокринологические, легочные, неврологические, психиатрические, печеночные, почечное, гематологическое, иммунологическое заболевание или другое серьезное заболевание, которое в настоящее время неконтролируемый. 14. Кроме псориаза, у пациента есть какое-либо другое дерматологическое заболевание, которое может мнение исследователя, мешает оценке исследования. 15. Любое состояние, включая наличие лабораторных отклонений (в том числе предполагаемых клиренс креатинина менее 30 мл в минуту), что поставило бы пациента в неприемлемый риск, если он / она будет участвовать в исследовании. 16. Злокачественные новообразования или злокачественные новообразования в анамнезе, за исключением: — обработанные [т. е. вылеченные] базально-клеточные или плоскоклеточные карциномы кожи in situ; — вылеченное [то есть вылеченное] злокачественное новообразование без признаков рецидива в течение предыдущего 5 лет. 17. Известная гиперчувствительность к апремиласту или любым вспомогательным веществам в составе. 18. Пациент имеет следующее наследственное заболевание: непереносимость галактозы, лактаза Лаппа. дефицит или мальабсорбция глюкозы-галактозы 19. Использование сильных индукторов фермента цитохрома P450 (например, рифампицин, фенобарбитал, карбамазепин, фенитоин) 20.
14. Кроме псориаза, у пациента есть какое-либо другое дерматологическое заболевание, которое может мнение исследователя, мешает оценке исследования. 15. Любое состояние, включая наличие лабораторных отклонений (в том числе предполагаемых клиренс креатинина менее 30 мл в минуту), что поставило бы пациента в неприемлемый риск, если он / она будет участвовать в исследовании. 16. Злокачественные новообразования или злокачественные новообразования в анамнезе, за исключением: — обработанные [т. е. вылеченные] базально-клеточные или плоскоклеточные карциномы кожи in situ; — вылеченное [то есть вылеченное] злокачественное новообразование без признаков рецидива в течение предыдущего 5 лет. 17. Известная гиперчувствительность к апремиласту или любым вспомогательным веществам в составе. 18. Пациент имеет следующее наследственное заболевание: непереносимость галактозы, лактаза Лаппа. дефицит или мальабсорбция глюкозы-галактозы 19. Использование сильных индукторов фермента цитохрома P450 (например, рифампицин, фенобарбитал, карбамазепин, фенитоин) 20. Активное злоупотребление психоактивными веществами или злоупотребление психоактивными веществами в анамнезе в течение 6 месяцев до Скрининг. 21. Предшествующая история попытки самоубийства в любое время в жизни пациента до скрининг или рандомизация, или серьезное психическое заболевание, требующее госпитализации в течение последних 3 лет. 22. Наличие неконтролируемой депрессии.
Активное злоупотребление психоактивными веществами или злоупотребление психоактивными веществами в анамнезе в течение 6 месяцев до Скрининг. 21. Предшествующая история попытки самоубийства в любое время в жизни пациента до скрининг или рандомизация, или серьезное психическое заболевание, требующее госпитализации в течение последних 3 лет. 22. Наличие неконтролируемой депрессии.