Детский артрит – причины, лечение
Причины артрита у детей – основные сведения
Так как артрит бывает в трех вариантах, в зависимости от происхождения, то следует выделить 3 основные виды артрита, возникающие у детей и подростков:
- Травматический артрит – возникает после ушиба или удара суставом об твердую поверхность. Обычно болезнь проходит самостоятельно, если дать ребенку покой. Осложнения возникают тогда, когда в открытую рану попадает инфекция, что может вызвать гнойный артрит. Также плохо на состоянии сустава сказываются переломы.
- Деструктивный остеоартрит – результат хронической перегрузки или постоянной травмы сустава. Такое явление наблюдается у детей, которые усиленно занимаются профессиональным и травматическим спортом (легкая атлетика, художественная гимнастика, балет). Если мелкие суставы подвержены хроническим перегрузкам, то это вызывает длительное, вялотекущее воспаление, проводящее к деструкции сустава. Лечение заключается в длительном отдыхе и проведении реабилитации.
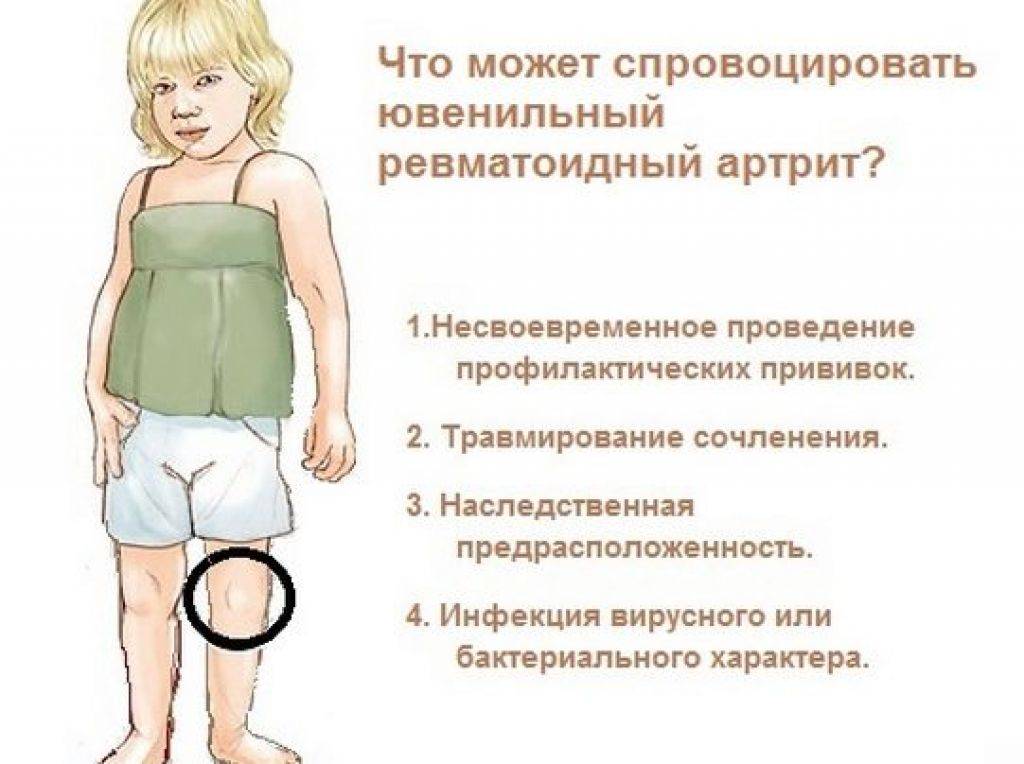
- Аутоиммунный артрит – результат ранее перенесенной инфекции, которая вызвала сбой в работе иммунной системы. У некоторых детей бурная реакция иммунитета провоцирует ответную реакцию, поражающую суставную ткань, что приводит к развитию ревматоидного артрита, ревматизма, ЮРА, реактивного инфекционного артрита, болезни Бехтерева, синдрому Стилла.
Ревматический артрит связан с кардиологическими, дерматологическими и суставными проявлениями, которые возникают на фоне перенесенной инфекции верхних дыхательных путей, спровоцированной гемолитическим стрептококком. Обычно состояние связано с перенесенной ангиной, скарлатиной и фарингитом.
Ювениальный ревматоидный артрит обычно возникает у детей, младше 16 лет и имеет прогрессирующее течение. Если не начать вовремя терапию заболевания, то аутоиммунная реакция необратимо затронет внутренние органы и несовершеннолетний пациент рискует умереть. Заболевание может протекать как в суставной форме, так и поражать внутренние органы по висцеральному типу, что затрагивает сердце, легкие, кожу, глаза.
Болезнь Бехтерева у детей также характеризуется острым течением с преимущественным поражением периферических и аксиальных суставов, в зависимости от формы заболевания. В 20% случаев патология дебютирует до 18 лет, поэтому анкилозирующий спондилоартрит нередко обнаруживают в подростковом возрасте.
Причины детского артрита
Реактивные артриты также являются результатом аутоиммунной реакции после перенесенного инфекционного заболевания внутренних органов. В отличие от других типов аутоиммунных артритов, при своевременно начатом лечении реактивный артрит удается полностью излечить в большинстве случаев. Если же патология протекает тяжело, то это может привести к развитию другого ревматологического заболевания – ревматоидного артрита, анкилозирующего спондилоартрита.
Если возбудитель проник в полость сустава, то это инфекционный артрит, который требует мощной терапии антибиотиками и хирургического вмешательства для удаления гнойных масс.
Причины возникновения артрита у детей
Точные причины симптомов артрита у детей не установлены. Обычно к приступам ювенильного артрита склонны дети с отягощенной семейной наследственностью либо ранее перенесшие тяжелое вирусное или инфекционное заболевание. Триггером в появлении аутоиммунного процесса может стать травма или удар. Механизм развития детского артрита связан с синтезом антител, которые организм воспринимает как чужеродные патогены, в ответ на которые выделяются провоспалительные цитокины (фактор некроза опухоли и различные виды интерлейкинов). В результате возрастает показатель аутоиммунных комплексов в организме, что приводит к воспалительной реакции. Так и возникает ювенильный артрит у детей.
Обычно к приступам ювенильного артрита склонны дети с отягощенной семейной наследственностью либо ранее перенесшие тяжелое вирусное или инфекционное заболевание. Триггером в появлении аутоиммунного процесса может стать травма или удар. Механизм развития детского артрита связан с синтезом антител, которые организм воспринимает как чужеродные патогены, в ответ на которые выделяются провоспалительные цитокины (фактор некроза опухоли и различные виды интерлейкинов). В результате возрастает показатель аутоиммунных комплексов в организме, что приводит к воспалительной реакции. Так и возникает ювенильный артрит у детей.
Также с учетом наследственной предрасположенности и ранее перенесенной инфекционной атаки, в организме могут произойти патологические процессы, способствующие появлению ювенильного анкилозирующего спондилоартрита. Реактивный артрит – результат перенесенной урогенитальной или кишечной инфекции. Причина инфекционного артрита у детей – попадание в асептические условия патогенного микроорганизма, который мигрирует с током крови или лимфы в сустав, из-за чего он воспаляется.
Если обобщить имеющуюся информацию, то в большинстве случаев причина воспаления суставов у детей связана с ранее перенесенным заболеванием бактериального или вирусного происхождения. Чаще всего осложнения вызывают такие заболевания:
- Краснуха.
- Аденовирусы.
- Грипп.
- Паротит.
- Вирусный гепатит.
- Последствия вакцинации.
- Хронический тонзиллит, фарингит, гайморит.
- Гонорея,
- Туберкулез.
- Инфекционные поражения кожи и слизистых оболочек.
Также риск появления артритов у детей повышается при переохлаждении, из-за сниженного иммунитета и проживания в неблагоприятных социальных условиях.
Как у детей проявляется артрит, частые симптомы
 Чаще в дебюте болезни поражается один или несколько суставов одновременно, не более. Сначала в патологический процесс вовлекаются крупные суставы (колени, локти), реже страдают мелкие суставы пальцев рук и ног.
Чаще в дебюте болезни поражается один или несколько суставов одновременно, не более. Сначала в патологический процесс вовлекаются крупные суставы (колени, локти), реже страдают мелкие суставы пальцев рук и ног.
Может возникать утренняя скованность в коленных, голеностопных суставах и изменение походки, если ребенок старше 3 лет. Обычно дети до двух лет перестают ходить вообще. В период обострения температура тела повышается до 39 градусов, а суставная форма может сопровождаться дополнительным течением увеита, иридоциклита, лимфаденией и сыпью, что часто сопровождается увеличением печени и селезенки. При длительном течении болезни без лечения развивается анемия хронического воспаления, артралгия, амилоидоз почек, перикардит, поражения других внутренних органов. ЮРА может привести к ранней инвалидности и даже летальному исходу.
При ювенильном анкилозирующем спондилоартрите преимущественно симптоматика проявляется в виде артралгии крупных суставов (преимущественно ног) с асимметрическим поражением.
Артрит колена у ребенка
Характерный признак реактивного артрита у ребенка – развитие после ранее перенесенной инфекции, с момента течения которой прошло несколько недель. Как и при ЮАС, реактивный артрит характеризуется асимметрическим поражением нескольких крупных суставов в дебюте болезни. Ребенок страдает от артрита, тендовагинита, бурсита и сильной суставной боли. Часто наблюдается поражение глаз и внутренних органов, если не начать вовремя лечение..gif) Обычно синдром Рейтера проходит самостоятельно, но при длительном и запущенном течении может перейти в анкилозирующий спондилоартрит или ревматоидный артрит у взрослого пациента.
Обычно синдром Рейтера проходит самостоятельно, но при длительном и запущенном течении может перейти в анкилозирующий спондилоартрит или ревматоидный артрит у взрослого пациента.
Симптоматика при появлении детского инфекционного артрита развивается быстро. Организм страдает при заболевании сильно, так как проявляется выраженная лихорадка, ухудшается общее самочувствие, наблюдается слабость и пропадает аппетит. Воспаленный сустав сильно увеличивается в объеме, становится красным и отечным. Боль в суставе наблюдается как в покое, так и при движении. Признаки у детей артрита инфекционной природы настолько выражены, что ребенок не может спать от боли, а прием обезболивающих средств оказывается малоэффективным. При извлечении гнойных масс болезнь проходит быстро. Требуется прием антибиотиков и операционное вмешательство.
Методы диагностики артрита у детей
Так как заболевание затрагивает много систем организма, то терапией и диагностикой болезни могут заниматься педиатры, ревматологи, офтальмологи, нефрологи, кардиологи.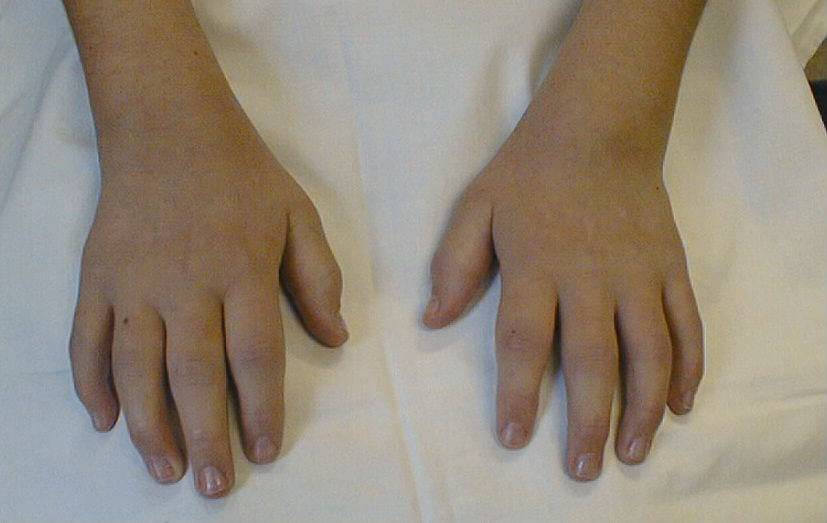 Обычно диагноз ставит детский ревматолог. Признаки поражения суставов трудно не заметить при внешнем осмотре, ведь у ребенка они болят, распухают, он не может передвигаться без обезболивающих средств или кортикостероидов. Основные методы диагностики заключаются в проведении инструментальных методов исследовании и лабораторных анализов.
Обычно диагноз ставит детский ревматолог. Признаки поражения суставов трудно не заметить при внешнем осмотре, ведь у ребенка они болят, распухают, он не может передвигаться без обезболивающих средств или кортикостероидов. Основные методы диагностики заключаются в проведении инструментальных методов исследовании и лабораторных анализов.
Какие анализы проводят с целью точной установки диагноза:
- Общий анализ крови. При активном воспалении наблюдается повышение уровня скорости оседания эритроцитов, снижение гемоглобина и эритроцитарных индексов (вторичная анемия, вызванная хроническим воспалением), а лейкоцитарная формула сдвигается влево.
- Общий анализ мочи. Проводят для выявления осложнений со стороны почек. Должен насторожить повышенный уровень белка, наличие эритроцитов.
- Биохимический анализ крови. Проверяют состояние печени, почек. При активном воспалении повышается уровень С-реактивного белка.
- Ревматологические пробы. Требуется выявить уровень ревматоидного фактора, АСЛ-О, Anti-MCV, ACC-P.
 Если повышен уровень стрептолизина-О, то это может указывать на реактивный артрит или ревматизм. При повышении РФ ставят диагноз серопозитивный ЮРА, если остальные маркеры, то серонегативный ЮРА.
Если повышен уровень стрептолизина-О, то это может указывать на реактивный артрит или ревматизм. При повышении РФ ставят диагноз серопозитивный ЮРА, если остальные маркеры, то серонегативный ЮРА. - Анализ на антигены. Если у малыша положительный результат на HLA-B27, то это достоверный диагностический маркер реактивного артрита или ювенильного анкилозирующего спондилоартрита.
- Анализ на патогенные возбудители, вирусы. Врач может назначить исследование на антитела к ерсиниям, хламидии, цитомегаловирусу, герпесу. Если имеются положительные реакции, то можно заподозрить реактивный или инфекционный артрит.
Для инструментального исследования воспалительного процесса пораженных суставов требуется провести рентгенографию. Если имеются рентгенологические суставные эрозивные изменения с сужением субхондральной щели, то моноартрит или олигоартрит подтверждается. Некоторые специалисты иногда советуют дополнительно провести МРТ, чтобы увидеть более детальную диагностическую картину. В большинстве случаев функциональные нарушения видны на рентгеновском снимке, поэтому рентгенографии оказывается достаточно.
В большинстве случаев функциональные нарушения видны на рентгеновском снимке, поэтому рентгенографии оказывается достаточно.
Лечение и симптомы артрита у детей
Лечение артрита у детей заключается в модификации образа жизни и приема медикаментов, подавляющих аутоиммунную реакцию. Если артрит связан с травмой, то он лечится щадящим образом жизни. В клинической практике в данном случае не следует использовать медикаменты, за исключением кратковременной симптоматической терапии с помощью НПВС. После заживления травмы требуется восстановить важные двигательные функции, поэтому во время реабилитации проводится ЛФК, чтобы мышцы пришли в тонус и ребенок не испытывал ухудшений из-за возможных последствий острого повреждения.
Особенности лечения полиартритов аутоиммунной группы заключаются в том, что ребенок регулярно принимает препараты, модифицирующие течение заболевания. Важное место занимает симптоматическая терапия. Если нет стойкой ремиссии при использовании базисных или биологических средств, то допустимо использовать в качестве симптоматического лечения НПВС, реже – кортикостероиды. Курс лечения и дозировки препаратов подбирает врач индивидуально.
Курс лечения и дозировки препаратов подбирает врач индивидуально.
В лечении артрита у детей используют такие медикаменты с высокой эффективностью:
- Метотрексат. Это базисный иммунодепрессант, являющийся антагонистом фолиевой кислоты. Медикамент в небольших дозировках проявляет антипролиферативные и иммуносупрессивные эффекты, поэтому его следует назначать при активной аутоиммунной реакции. При правильном администрировании медикаментозной терапии лекарство безопасное и хорошо переносится. Лечебные дозировки варьируют от 7.5 до 20 мг в неделю у детей. Важно контролировать тщательно анализы на фоне терапии, так как Метотрексат проявляет гепатотоксические и нефротоксические свойства.
- Сульфасалазин. Этот медикамент назначают при неэффективности или непереносимости Метотрексата, как средство второй линии выбора. Препарат помогает при наличии болевых ощущений, локализирующихся в крупных периферических суставах – стопы, колени, локти. Длительность терапии минимум составляет 3-4 месяца с целью оценки результата.
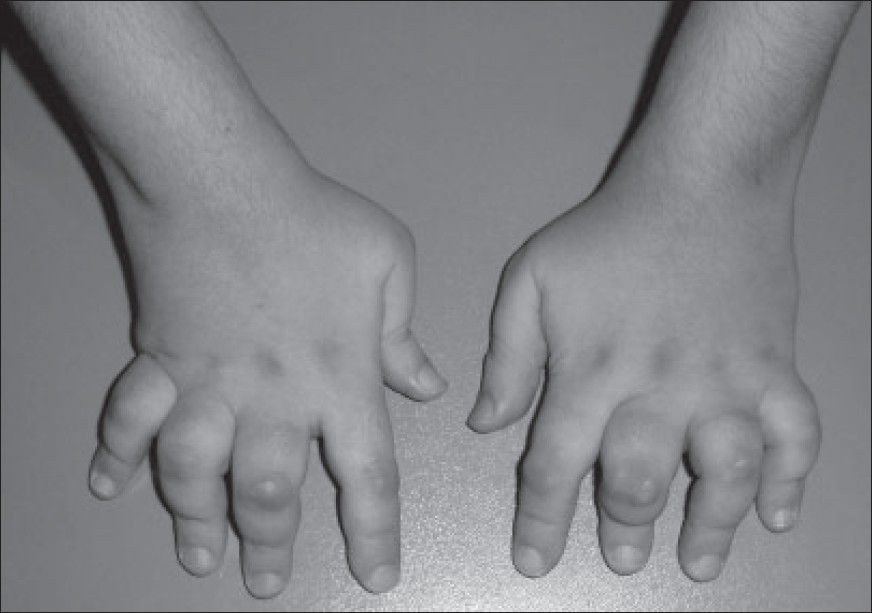 Это препарат накопительного действия. Во время терапии контролируют показатели печени и почек. Терапевтическая дозировка – 1.5 – 3 г.
Это препарат накопительного действия. Во время терапии контролируют показатели печени и почек. Терапевтическая дозировка – 1.5 – 3 г. - Хумира. Действующее вещество – адалимумаб. Это препарат биоинженерной терапии, ингибитор фактора некроза опухоли. Лекарство избирательно подавляет провоспалительный цитокин, вызывающий бурную аутоиммунную реакцию в теле. Средство обладает высокой эффективностью, проявляющейся с первой инъекции. Во время лечения тщательно контролируют анализы и проверяют ребенка на скрытый туберкулез. При наличии онкологии использовать Хумиру запрещено.
- Ремикейд. Действующее вещество – инфликсимаб. Это первое моноклональное антитело, ингибитор ФНО-а, синтезированный из мышиных белков. Преимущество – высокая эффективность. Недостатки – повышенный риск аллергической реакции и необходимость проведения инфузии в условиях стационара раз в 6-8 недель (Хумиру вводят подкожно в домашних условиях). Препарат имеет повышенный риск образования аутоантител при лечении, поэтому часто терапию комбинируют с применением Метотрексата, замедляющего выведение инфликсимаба из организма.
 Во время лечения необходимо учитывать все риски, связанные использованием Ремикейда (появление признаков оппортунистических инфекций, риск возникновения онкологии).
Во время лечения необходимо учитывать все риски, связанные использованием Ремикейда (появление признаков оппортунистических инфекций, риск возникновения онкологии).
Медикаменты выбирает врач в зависимости от реакции на терапию.
Мнение редакции
При детском полиартрите важно оперативно определить диагноз, чтобы правильно подобрать базисную терапию. Если воспаление суставов является результатом травмы, то нужен отдых и реабилитация.
Лечение артрита в Москве | Институт Физической Реабилитации
О болезни
Воспаление сустава и вызванная этим болезнь называется артритом. При заболевание артритом Вы будете ощущать боль в первую очередь при ходьбе. Также в этом случае возможно покраснение на коже.
Артрит можно разделить на: моноартрит – это когда подвергается болезни один сустав и полиартрит – соответственно, когда болезнь поражает два и более сустава. По локациям поражения артрит бывает: коленный, плечевой, тазобедренный, голеностопный и челюстно-лицевой.
По локациям поражения артрит бывает: коленный, плечевой, тазобедренный, голеностопный и челюстно-лицевой.
Принято выделять 4 степени артрита:
Во время первой степени происходит инфицирование организма, она протекает бессимптомно, человека ничего не беспокоит.
Вторая степень характеризуется появлением небольших припухлостей в районе больного сустава, покраснением кожи вокруг него, появление хруста. Также возникают боли во время сна.
Третья степень артрита уже проявляется постоянными болями, если поражены нижние конечности, то человеку будет сложно передвигаться, а если поражены руки, то больному будет трудно выполнять элементарные вещи, чаще всего на этой стадии присваивается инвалидность.
Рентген показывает очевидную деформацию сустава, происходит деформация конечности из-за болевых спазмов, человек ощущает боль даже в состоянии покоя.
Четвертая степень характеризуется необратимостью процессов, которые разрушают сустав. Артрит нижних конечностей не позволит человеку передвигаться без помощи посторонних. Частые и интенсивные боли становятся постоянным спутником.
Артрит нижних конечностей не позволит человеку передвигаться без помощи посторонних. Частые и интенсивные боли становятся постоянным спутником.
Потенциальная группа риска, которая может быть подвержена артриту – взрослые пенсионного возраста. Но бывают исключения, и заболеть могут более молодые люди, или даже дети.
Высокий процент болеющих артритом можно аргументировать тем, что на первых шагах болезни происходит бессимптомно, а при дальнейшем развитии люди чаще всего занимаются самолечением. Попытки самостоятельно вылечить недуг вряд ли увенчаются успехом.
Причины
Весь список причин, которые могут вызвать это заболевание неизвестен врачам до сих пор. Большинство считают, что основными причинами могут стать: генетическая предрасположенность, травмы, аллергия, вирусная или грибковая инфекции. Помимо этого, к причинам, вызывающим артрит, можно отнести:
- Избыточный вес
- Занятия спортом, особенно профессиональным
- Проблемы с эндокринной системой
- Переохлаждение
- Недостаток витаминов и питательных веществ
- Дизентерия, подагра и другие болезни
- Несбалансированное питание и употребление алкоголя
- Плохая экология
- Также постоянные стрессы – тоже могут спровоцировать развитие артрита, особенно у женщин в среднем возрасте, поскольку на их плечи взваливаются бытовые проблемы, работа, взаимоотношение с мужем и детьми.
 Не всегда стресс проходит в обостренной форме, но такой образ жизни откладывает заметный отпечаток на здоровье женщины.
Не всегда стресс проходит в обостренной форме, но такой образ жизни откладывает заметный отпечаток на здоровье женщины.
Симптомы
Если боли в суставах незначительные, то это называется хронический артрит. Если же боли возникают внезапно и носят резкий характер, то такой артрит называется острым. К основным симптомам можно отнести:
- Скованность в суставах, особенно утром. Руки «не слушаются» и человеку довольно-таки сложно сделать даже элементарные вещи, либо скованность в поясничном отделе на протяжении нескольких дней.
- Ночные боли. В этом случае суставы не ноют, как от усталости, а болят. Ну а если человеку боль мешает спать – это верный знак обратиться к врачу.
- Воспаление суставов, на руках, ступнях, локтях.
- Суставы воспаляются по очереди, в определенной последовательности, каждый друг за другом.
- Деформация пальцев (длительные покраснения и опухлости)
- Высокая температура, озноб, потовыделение, воспаленные глаза –признаки реактивного артрита.

Лечение
Наиболее раннее выявление артрита залог быстрейшего лечения. На первой и второй стадии обнаружить его достаточно сложно, поскольку деформация сустава еще не произошла.
Нужно запомнить, что производить лечение этой болезни нужно комплексно и запастись терпением, поскольку одной неделей артрит не вылечишь.
Лечение артрита можно разделить на медикаментозное и немедикаментозное. К первой группе можно отнести различные гели, мази, уколы, антибиотики назначаются в случае инфекционного артрита.
Вторая группа:
Не стоит забывать о правильном питании и строгом распорядке дня. Диету больному врач назначает в индивидуальном порядке.
Паротит симптомы причины лечение » Государственное Бюджетное Учреждение Здравоохранения МО Орехово-Зуевский районный Центр Общей Врачебной Семейной Практики
Первые случаи паротита были описаны ещё в V веке до н. э. Гиппократом. Но обобщить всю информацию о болезни и выявить её истинную вирусную природу получилось лишь в XX веке. В середине прошлого столетия впервые была применена вакцина, но более удачные её варианты против паротита синтезировали немного позже.
В середине прошлого столетия впервые была применена вакцина, но более удачные её варианты против паротита синтезировали немного позже.
Название — эпидемический паротит (parotitis epidemica) не совсем верное, ведь давно не было случаев массовой инфекции. Несмотря на это с каждым годом заболеваемость паротитом растёт, что привело к необходимости наблюдать за циркуляцией вируса в природе.
В чём особенность вируса?
- Он неустойчив в окружающей среде, паротит легко обезвредить с помощью ультрафиолетового облучения, кипячения и обработки дезинфектантами.
- Вирус долго сохраняется на предметах при низких температурах до минуса 70 ºC.
- Период активного размножения микроорганизма — конец зимы и начало весны.
- Несмотря на то что иммунитет после перенесённого острого заболевания считается пожизненным, бывают случаи повторного заражения со всеми вытекающими последствиями.
- Типичное проявление инфекционного паротита — увеличение с одной или с двух сторон околоушных слюнных желёз.
 Но нередко заболевание протекает бессимптомно, что способствует быстрому распространению вируса среди людей.
Но нередко заболевание протекает бессимптомно, что способствует быстрому распространению вируса среди людей. - Инфекция часто регистрируется у детей от 3 лет и до 15, но нередко заболевают и взрослые.
- Мальчики паротитом болеют практически в полтора раза чаще девочек.
Это заболевание характерно для детского возраста, но его проявления часто напоминают течение самых тяжёлых взрослых болезней.
Паротит — это острое инфекционное вирусное заболевание, развивающееся чаще в детском возрасте, характерной чертой которого является воспаление слюнных желёз. Излюбленное место обитания вируса — железистые органы и нервная система, то есть, другими словами, такие проявления, как панкреатит, менингит — это закономерные процессы из-за особенностей микроорганизма.
воспаление слюнных желёз
В природе вирус циркулирует только среди людей, поэтому источником заражения может быть больной человек.
Основной путь передачи — воздушно-капельный, кроме слюны, вирус может передаваться через заражённые предметы посредством мочи. Паротит у новорождённых бывает при вертикальном пути заражения или внутриутробном от больной матери. Но в случае если женщина переболела данной вирусной инфекцией до беременности — малышу передаются антитела, которые защищают его в течение шести месяцев.
Паротит у новорождённых бывает при вертикальном пути заражения или внутриутробном от больной матери. Но в случае если женщина переболела данной вирусной инфекцией до беременности — малышу передаются антитела, которые защищают его в течение шести месяцев.
Это одна из самых частых вирусных инфекций, которая распространена во всём мире, нет региона или страны, где полностью отсутствуют случаи заражения.
Свинка относится к классу инфекционных и паразитарных болезней. Согласно классификации по МКБ 10 код паротита — В 26.
По течению болезни инфекция подразделяется на следующие степени:
- лёгкую;
- среднюю;
- тяжёлую.
Заболевание может протекать с осложнениями или без них. Известны случаи бессимптомного течения, когда нет типичных классических клинических проявлений, такая форма инфекции носит название — инаппарантная.
В литературе можно встретить ещё один, казалось бы, нелогичный термин — неинфекционный паротит, который не имеет ничего общего с вирусным заболеванием. Встречается он в случае травмы или длительного переохлаждения с последующим воспалением околоушных слюнных желёз одной либо двух.
Встречается он в случае травмы или длительного переохлаждения с последующим воспалением околоушных слюнных желёз одной либо двух.
Попав на слизистую оболочку верхних дыхательных путей и ротовой полости, вирус постепенно здесь накапливается, после чего проникает в кровяное русло. С током крови он разносится в железистые органы. Околоушные слюнные железы — это первое место накопления, где паротит обосновывается и начинает активно размножаться. Здесь, как правило, на первом этапе развития инфекции максимальное скопление клеток.
Часть микроорганизма попадает в другие железистые органы и нервную ткань, но их воспаление развивается не всегда и не сразу. Чаще происходит поэтапное поражение сразу слюнные железы, затем поджелудочная, яички, нервная ткань и так далее. Это обусловлено размножением вируса в слюнных железах и дополнительным их поступлением оттуда в кровь.
Инкубационный период паротита составляет по разным источникам от 11 дней до трёх с небольшим недель (23 дня самый максимальный). Особенность заболевания в том, что отсутствует продромальный период или длится он всего 1–3 дня.
Особенность заболевания в том, что отсутствует продромальный период или длится он всего 1–3 дня.
Классический вариант острого паротита протекает со следующими симптомами.
- Короткий продромальный период сопровождается типичными для любой инфекции симптомами: слабость, недомогание, вялость, апатия, постоянная беспричинная сонливость, в этот период развития паротита может снизиться аппетит, появляются периодические боли в области суставов, редкие головные боли.
- Во время попадания и размножения вируса в околоушных слюнных железах происходит резкое повышение температуры, которая может колебаться в пределах 38–40 ºC.
- Максимально высокая температура наблюдается на второй день болезни и длится не более недели с постепенным её снижением. Но вовлечение в воспаление других органов снова приводит к повышению температуры тела.
- К признакам паротита относится увеличение околоушных слюнных желёз из-за чего заболевание и носит название свинка, сразу воспаляется одна слюнная железа, затем вторая, в редких случаях наблюдается одностороннее поражение, ещё реже заболевание протекает без этого признака.
/GettyImages-146593677-566ba8003df78ce1616bf967.jpg)
- Одновременно с припуханием слюнных желёз больной чувствует их болезненность, воспаляются не только околоушные, но ещё и подъязычные, и подчелюстные.
- В этот момент развития паротита появляется болезненность при дотрагивании впереди и сзади мочки уха — это типичный признак инфекции, который носит название «Симптом Филатова».
- Воспаляются окружающие ткани — наблюдается покраснение и отёчность миндалин.
- К симптомам паротита у детей относится припухлость, которая заметна не только в области выводных протоков слюнных околоушных желёз, но и на всей шее, где кожа напряжена и лоснится.
- Появляется боль при жевании, а из-за сильного отёка немного наклоняется голова в сторону поражения (в случае одностороннего воспаления слюнных желёз).
Это первая линия атаки вируса паротита или видимые симптомы, которые развиваются в большинстве случаев и способствуют правильной постановке диагноза. Воспаление желёз постепенно уменьшается и к концу первой, середине второй недели при нормальном течении заболевания уже не беспокоит человека. В случае лёгкого течения (в том числе и бессимптомного) всех вышеперечисленных симптомов не будет, а паротит по своим проявлениям напоминает лишь лёгкую острую вирусную инфекцию.
В случае лёгкого течения (в том числе и бессимптомного) всех вышеперечисленных симптомов не будет, а паротит по своим проявлениям напоминает лишь лёгкую острую вирусную инфекцию.
По мере увеличения количества вирусных клеток в крови повышается вероятность вовлечения в воспаление других желёз. Поочерёдно при тяжёлом и осложнённом течении паротита происходит заражение важных органов, что может отразиться на функциях организма человека в будущем.
Тяжёлое течение эпидемического паротита у детей сопровождается:
- выраженной слабостью;
- учащением сердцебиения;
- снижением артериального давления;
- отсутствием аппетита у больного паротитом и истощением всего организма;
- приблизительно на пятые сутки может развиться острый панкреатит и менингит;
- немного позже на 6–8 день появляются признаки воспаления половых желёз.
Что происходит с другими органами?
- Частым осложнением паротита является серозный менингит.
Воспаление оболочек головного мозга случается практически сразу после поражения слюнных желёз или спустя некоторое время. В среднем это явление наблюдается на 4–10 сутки инфекционного паротита. Для менингита характерен озноб, повторное повышение температуры, которая может доходить до 39 ºC. Вместе с этим, больного беспокоит постоянная головная боль, тошнота, рвота, не приносящая облегчения, повышенный тонус затылочных мышц — один из важных диагностических симптомов менингита, когда человек в процессе обследования не может дотронуться подбородком грудной клетки. Окончательный диагноз помогает поставить исследование спинномозговой жидкости.
- Менингоэнцефалит, вызванный паротитом, протекает намного тяжелее. Здесь уже речь идёт не только о воспалении оболочек, но и самого головного мозга. При этом у человека нарушается сознание, он вялый, сонный. По тяжести проявления заболевание не уступает менингиту, у человека наблюдаются парезы мышц лицевого нерва (нарушения работы из-за воспаления нервов), параличи мышц, вялость рефлексов.

-
орхит
К последствиям паротита у мальчиков и подростков относится орхит и эпидидимит. Это воспаление яичек и их придатков. Возникает заболевание приблизительно через неделю, на 5–8 сутки. Это может быть единственным признаком инфекции. Человека беспокоит выраженные боли в области мошонки, покраснение яичка, припухлость, увеличиваются паховые лимфоузлы. Всё это сопровождается повышенной температурой тела. Боли отдают вниз живота, иногда напоминают картину аппендицита. Такие симптомы проходят через неделю.
- У женщин и девочек возникает оофорит — воспаление яичников. Это одно из редких осложнений паротита и протекает более благоприятно, чем орхит. Проявляется болями внизу живота справа или слева, бывает двухсторонним.
- Одним из частых осложнений паротита у взрослых является панкреатит. Воспаление поджелудочной происходит из-за проникновения вируса в ослабленную погрешностями в диете железу. В среднем заболевание развивается на 4–7 сутки начала болезни.
 Признаки панкреатита: тошнота, урчание и резкие боли в животе, отдающие в спину или опоясывающие, повышение температуры тела, неоднократная рвота, запор, сменяющийся послаблением стула.
Признаки панкреатита: тошнота, урчание и резкие боли в животе, отдающие в спину или опоясывающие, повышение температуры тела, неоднократная рвота, запор, сменяющийся послаблением стула.
В основе поражения желёз лежит не только воспаление самой ткани органа, но и загустевание её секрета, того что вырабатывает железа. Дополнительно воспаляются выводные протоки, что затрудняет сам процесс выделения секрета. Это влияет на окружающие системы. Поэтому один из опасных моментов, связанных с паротитом, является поражение соседних органов и тяжёлые осложнения в последующем.
Какие проблемы возникают через длительное время после перенесения паротита?
- Смертельные случаи бывают, но редко, приблизительно 1 на 100 000, что нередко связано с присоединением вторичной инфекции и тяжелейшим течением заболевания.
- Один из самых надёжных методов профилактики — прививки, привели к снижению заболеваемости среди детей, но возрастанию её у людей до 30 лет, поэтому паротит называют казарменной болезнью — ей легче заразиться в местах большого скопления людей.
 Паротит у мужчин приводит к бесплодию из-за воспаления и атрофии яичка, что случается приблизительно через месяц после перенесённой инфекции.
Паротит у мужчин приводит к бесплодию из-за воспаления и атрофии яичка, что случается приблизительно через месяц после перенесённой инфекции. - Очередное тяжёлое, но редкое осложнение паротита — глухота. Происходит поражение слухового нерва, в большинстве случаев одностороннее, проявляется чаще в детском возрасте. К первым признакам относится шум в ушах, позже появляется выраженное головокружение, тошнота и рвота, нарушается координация, что свидетельствует о вовлечении в процесс воспаления внутреннего уха (лабиринт).
- Заболевания сердца — миокардит.
- Воспалительный процесс почек — нефрит.
- Паротит затрагивает многие железы, в том числе молочную, из-за чего развивается мастит, щитовидную, что является причиной возникновения тиреоидита, в более позднее время, у женщин могут воспаляться железы половых органов — бартолинит.
- Вирус поражает суставы — артрит.
- В редких случаях перенесённое заболевание является пусковым механизмом в развитии диабета.

Заболевание острое с осложнениями, о хроническом паротите идёт речь чаще при других причинах поражения околоушных слюнных желёз (неинфекционной природы или иными вирусными инфекциями).
Казалось бы, выставить диагноз свинка сможет абсолютно каждый врач. После инкубационного периода он не представляет никаких сложностей. Увеличенные околоушные железы — это уже половина точного диагноза. Но не всё так просто. Воспаление слюнных желёз может быть признаком других заболеваний, а лёгкое или бессимптомное течение паротита помешает правильной и своевременной диагностике.
Что помогает выставить диагноз?
-
анализы
Кроме осмотра больного, нужен тщательный анамнез и уточнение наличия контактов с больными паротитом за последние дни.
- Общий анализ крови неинформативен, так как выявляются лишь стандартные признаки наличия инфекции в организме.
- В последние дни инкубационного периода и первые 4 дня активного развития заболевания вирус может быть выделен с помощью бактериологического метода из слюны, мочи, спинномозговой жидкости.

- Самым информативным методом диагностики паротита считается иммунофлюоресцентный метод.
- В серодиагностике используют нарастание титра антител в сыворотке крови.
Дополнительно обследуют поражённые органы, применяя специальные инструментальные методы.
Главное правило лечения — это изоляция человека от окружающих и домашний режим. Это поможет избежать дополнительного инфицирования. Госпитализация проводится лишь в случае тяжёлой формы инфекционного паротита либо при появлении осложнений.
В лечении паротита, главное, соблюсти несколько правил.
- Лечение паротита у взрослых и детей с нетяжелыми формами заключается в назначении противовоспалительных препаратов от простых нестероидных до гормональных при необходимости.
- Нет лекарств, направленных против возбудителя, поэтому во многих случаях лечение симптоматическое.
- Важным этапом лечения является диета — в еде приходится ограничивать острые блюда, преимущества отдают щадящему питанию отварным и тушёным блюдам, полностью исключаются экстрактивные продукты, возбуждающие аппетит (сладости, кофе и чай, алкоголь, окрашенные напитки, копчения и соленья).
- Используют жаропонижающие лекарственные средства и обезболивающие исходя из показаний.
- Если развился панкреатит в лечении врачи руководствуются тремя правилами: холод, голод и покой, стараясь минимизировать нагрузку на поражённый орган.
- Чтобы снизить вероятность такого последствия паротита для мужчин, как бесплодие применяют гормональные препараты в стандартных дозах, назначают сухое тепло и покой.
- Антибиотики не назначают, но прибегают к использованию физиопроцедур на поражённые органы.
- В случае тяжёлого течения лекарства вводят внутривенно в капельницах.
Кроме стандартных правил, по временной изоляции больного на 9 дней, всем детям в качестве профилактики делают прививку от паротита. Это активная профилактика заболеваний, вызванных вирусом.
Применяется вакцина — живая, ослабленная, которую вводят подкожно под лопатку либо в наружную часть плеча в дозе 0,5 мл однократно.
Когда делают прививку от паротита? В нормальных условиях вакцинацию проводят детям в 12 месяцев. Вакцина включает антитела против кори и краснухи. Ревакцинацию назначают в 6 лет, что способствует выработке защитных клеток против паротита практически на 100%. В случае нарушения графика или отказа от вакцинации в детском возрасте прививку делают всем желающим, а ревакцинация моновакциной должна проводиться не менее чем через 4 года.
Вакцина включает антитела против кори и краснухи. Ревакцинацию назначают в 6 лет, что способствует выработке защитных клеток против паротита практически на 100%. В случае нарушения графика или отказа от вакцинации в детском возрасте прививку делают всем желающим, а ревакцинация моновакциной должна проводиться не менее чем через 4 года.
Какие есть вакцины от паротита?
- Моновакцины — «Имовакс Орейон», «Вакцина паротитная культуральная живая».
- Дивакцина — «Вакцина паротитно-коревая культуральная живая».
- Трёхкомпонентные вакцины — ММR, «Приорикс», «Эрвевакс», «Тримовакс».
Септический артрит у детей: диагностика и лечение
Pediatric Health Med Ther. 2017; 8: 65–68.
Маркус Пяэкконен
1 Отделение детской ортопедической хирургии
2 Отделение хирургии кисти, Университетская больница Турку и Университет Турку, Турку, Финляндия
1 Отделение детской ортопедической хирургии
2 Отделение хирургии кисти, Университетская больница Турку и Университет Турку, Турку, Финляндия
Для корреспонденции: Маркус Пяакконен, Отделение детской ортопедической хирургии, Университетская больница Турку и Университет Турку, Kiinamyllynkatu 4-8, PL 52, 20521 Турку, Финляндия, тел. + 358 2313 0000, факс: +358 2313 3613, электронная почта, если[email protected] Авторские права © 2017 Pääkkönen. Эта работа опубликована и лицензирована Dove Medical Press Limited. Полные условия этой лицензии доступны по адресу https://www.dovepress.com/terms.php и включают лицензию Creative Commons Attribution — Non Commercial (unported, v3.0) License ( https://creativecommons.org/licenses/by-nc/3.0/). Получая доступ к работе, вы тем самым принимаете Условия. Некоммерческое использование работы разрешено без какого-либо дополнительного разрешения Dove Medical Press Limited при условии надлежащей атрибуции работы.Эта статья цитировалась в других статьях в PMC.
+ 358 2313 0000, факс: +358 2313 3613, электронная почта, если[email protected] Авторские права © 2017 Pääkkönen. Эта работа опубликована и лицензирована Dove Medical Press Limited. Полные условия этой лицензии доступны по адресу https://www.dovepress.com/terms.php и включают лицензию Creative Commons Attribution — Non Commercial (unported, v3.0) License ( https://creativecommons.org/licenses/by-nc/3.0/). Получая доступ к работе, вы тем самым принимаете Условия. Некоммерческое использование работы разрешено без какого-либо дополнительного разрешения Dove Medical Press Limited при условии надлежащей атрибуции работы.Эта статья цитировалась в других статьях в PMC. Abstract
Острый септический артрит у детей обычно гематогенный. Чаще встречается у мальчиков, и чаще всего поражает крупные суставы нижних конечностей. Диагноз ставится на основании культур, полученных из инфицированного сустава, и подтверждается анализом крови на С-реактивный белок или ультразвуковой визуализацией. Золотистый стафилококк является наиболее частым возбудителем и является основной мишенью для эмпирического лечения. Подходящими антибиотиками являются цефалоспорины первого поколения и клиндамицин.Ванкомицин используется в районах с высоким уровнем устойчивости к клиндамицину и метициллину S. aureus . После короткого внутривенного введения в течение 2–4 дней в неосложненных случаях достаточно 2-недельного курса. Раннее лечение антибиотиками значительно улучшило прогноз в странах с высоким уровнем дохода, но неосложненное выздоровление затрудняется, если лечение откладывается. Такие осложнения, как симптоматический остеоартрит или аваскулярный некроз головки бедренной кости, развиваются медленно.Для выявления всех возможных последствий требуется длительное наблюдение в течение 1-2 лет.
Золотистый стафилококк является наиболее частым возбудителем и является основной мишенью для эмпирического лечения. Подходящими антибиотиками являются цефалоспорины первого поколения и клиндамицин.Ванкомицин используется в районах с высоким уровнем устойчивости к клиндамицину и метициллину S. aureus . После короткого внутривенного введения в течение 2–4 дней в неосложненных случаях достаточно 2-недельного курса. Раннее лечение антибиотиками значительно улучшило прогноз в странах с высоким уровнем дохода, но неосложненное выздоровление затрудняется, если лечение откладывается. Такие осложнения, как симптоматический остеоартрит или аваскулярный некроз головки бедренной кости, развиваются медленно.Для выявления всех возможных последствий требуется длительное наблюдение в течение 1-2 лет.
Ключевые слова: ребенок, септический артрит, сепсис, Staphylococcus aureus
Введение
Острый септический артрит (СА) у детей чаще всего является гематогенной инфекцией. 1 , 2 Вялый кровоток в метафизарных капиллярах делает растущие кости восприимчивыми к инфекции из-за гематогенного посева при любой травме или инфекции.СА чаще встречается у мальчиков, чем у девочек, в соотношении 2: 1. 1 , 2 Заболеваемость в развитых странах составляет 4–5 случаев на 100 000 детей в год. 1 Чаще всего поражаются крупные суставы нижних конечностей — тазобедренные, коленные и голеностопные. Золотистый стафилококк и респираторные патогены являются наиболее распространенными возбудителями. Kingella kingae — региональный патоген, который все чаще идентифицируется как частый возбудитель, особенно у детей в возрасте 6–36 месяцев. 3 Роль травмы в патогенезе остается неясной. 4 У новорожденных в родовых путях часто встречаются такие бактерии, как Escherichia coli .
1 , 2 Вялый кровоток в метафизарных капиллярах делает растущие кости восприимчивыми к инфекции из-за гематогенного посева при любой травме или инфекции.СА чаще встречается у мальчиков, чем у девочек, в соотношении 2: 1. 1 , 2 Заболеваемость в развитых странах составляет 4–5 случаев на 100 000 детей в год. 1 Чаще всего поражаются крупные суставы нижних конечностей — тазобедренные, коленные и голеностопные. Золотистый стафилококк и респираторные патогены являются наиболее распространенными возбудителями. Kingella kingae — региональный патоген, который все чаще идентифицируется как частый возбудитель, особенно у детей в возрасте 6–36 месяцев. 3 Роль травмы в патогенезе остается неясной. 4 У новорожденных в родовых путях часто встречаются такие бактерии, как Escherichia coli .
Диагноз
Несмотря на то, что острая СА может проявляться по-разному, классическим проявлением является резко опухший, красный, болезненный сустав с ограниченными движениями и лихорадкой. Ребенок отказывается от несения веса, если задействована нижняя конечность. Новорожденные с септическим тазобедренным суставом принимают характерное положение с согнутым и отведенным тазобедренным суставом при внутренней ротации.Лихорадка особенно высока в случаях, вызванных устойчивым к метициллину S. aureus (MRSA). 5 Случаи, вызванные K. kingae , протекают легче, и лихорадка может даже отсутствовать. 6 Заболевание может быть коварным, так как поражен любой сустав в организме, а иммунодефицит, подавление иммунитета или недавнее применение антибиотиков могут изменить клинический и лабораторный вид септического сустава. Дифференциальный диагноз включает остеомиелит, вирусные артриты и ювенильный ревматоидный артрит ().С-реактивный белок (СРБ) в сыворотке крови, количество лейкоцитов (WBC) и скорость оседания эритроцитов (СОЭ) используются для дифференциации преходящего синовита тазобедренного сустава от септического артрита тазобедренного сустава, хотя эти состояния частично совпадают.
Ребенок отказывается от несения веса, если задействована нижняя конечность. Новорожденные с септическим тазобедренным суставом принимают характерное положение с согнутым и отведенным тазобедренным суставом при внутренней ротации.Лихорадка особенно высока в случаях, вызванных устойчивым к метициллину S. aureus (MRSA). 5 Случаи, вызванные K. kingae , протекают легче, и лихорадка может даже отсутствовать. 6 Заболевание может быть коварным, так как поражен любой сустав в организме, а иммунодефицит, подавление иммунитета или недавнее применение антибиотиков могут изменить клинический и лабораторный вид септического сустава. Дифференциальный диагноз включает остеомиелит, вирусные артриты и ювенильный ревматоидный артрит ().С-реактивный белок (СРБ) в сыворотке крови, количество лейкоцитов (WBC) и скорость оседания эритроцитов (СОЭ) используются для дифференциации преходящего синовита тазобедренного сустава от септического артрита тазобедренного сустава, хотя эти состояния частично совпадают. 6 , 7
6 , 7
Таблица 1
Условия, которые необходимо учитывать при дифференциальной диагностике септического артрита в детском возрасте
| Асептический синовит бедра | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вирусный артрит | 900омиелит90 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Юношеский ревматоидный артрит | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Болезнь Легга-Кальве-Пертеса | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Болезнь Лайма (боррелиоз) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Эпифиз соскальзывания головки бедренной кости | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Реактивный артрит | 901 клеточная||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Сикл 90 Диагностический алгоритм для SA показан на. Алгоритм диагностики септического артрита у детей. Сокращения: CRP, С-реактивный белок; СОЭ, скорость оседания эритроцитов. Лечение Лечение начинают без промедления после получения образцов синовиальной жидкости и крови. Эмпирическое лечение в первую очередь нацелено на S. aureus и учитывает его устойчивость к антибиотикам (). Подходят и цефалоспорины первого поколения, и клиндамицин, но их следует вводить в больших дозах и 4 раза в день, поскольку это антибиотики, зависящие от времени. 10 В регионах, где распространенность штаммов MRSA превышает 10%, клиндамицин является допустимым вариантом лечения, если распространенность устойчивых к клиндамицину штаммов остается <10%.Если устойчивость к клиндамицину распространена, ванкомицин является первым вариантом лечения, несмотря на опасения по поводу плохого проникновения в кости. 11 Монотерапия пенициллином подходит для Streptococcus pyogenes и S. Таблица 2Рекомендуемое эмпирическое лечение антибиотиками
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 Если у ребенка с острыми симптомами повышен уровень СРБ (> 20 мг / л) 8 или СОЭ (> 20 мм / ч), выполняется пункция сустава для выявления гнойного аспирата и получения образца для бактериологического исследования. Получают посевы крови. Находки в синовиальной жидкости неспецифичны, но образец синовиальной жидкости с лейкоцитами> 50 000 / мкл, из которых> 75% составляют полиморфно-ядерные клетки, считается признаком СК. 8 Посевы могут оставаться отрицательными даже в 30–70% случаев. 1 , 9 В дополнение к чашкам с агаром рекомендуется культивировать синовиальную жидкость в аэробных флаконах для культивирования крови, чтобы улучшить обнаружение K.Королева . Обычный рентген не очень полезен в диагностике, но он может обнаружить опухоль суставов или хронический остеомиелит. Ультразвук можно использовать для обнаружения отека суставов и для направления их пункции. Магнитно-резонансная томография действительно показывает отек и особенно полезна при диагностике соседнего остеомиелита или абсцесса, но у младенцев требуется анестезия.
Если у ребенка с острыми симптомами повышен уровень СРБ (> 20 мг / л) 8 или СОЭ (> 20 мм / ч), выполняется пункция сустава для выявления гнойного аспирата и получения образца для бактериологического исследования. Получают посевы крови. Находки в синовиальной жидкости неспецифичны, но образец синовиальной жидкости с лейкоцитами> 50 000 / мкл, из которых> 75% составляют полиморфно-ядерные клетки, считается признаком СК. 8 Посевы могут оставаться отрицательными даже в 30–70% случаев. 1 , 9 В дополнение к чашкам с агаром рекомендуется культивировать синовиальную жидкость в аэробных флаконах для культивирования крови, чтобы улучшить обнаружение K.Королева . Обычный рентген не очень полезен в диагностике, но он может обнаружить опухоль суставов или хронический остеомиелит. Ультразвук можно использовать для обнаружения отека суставов и для направления их пункции. Магнитно-резонансная томография действительно показывает отек и особенно полезна при диагностике соседнего остеомиелита или абсцесса, но у младенцев требуется анестезия.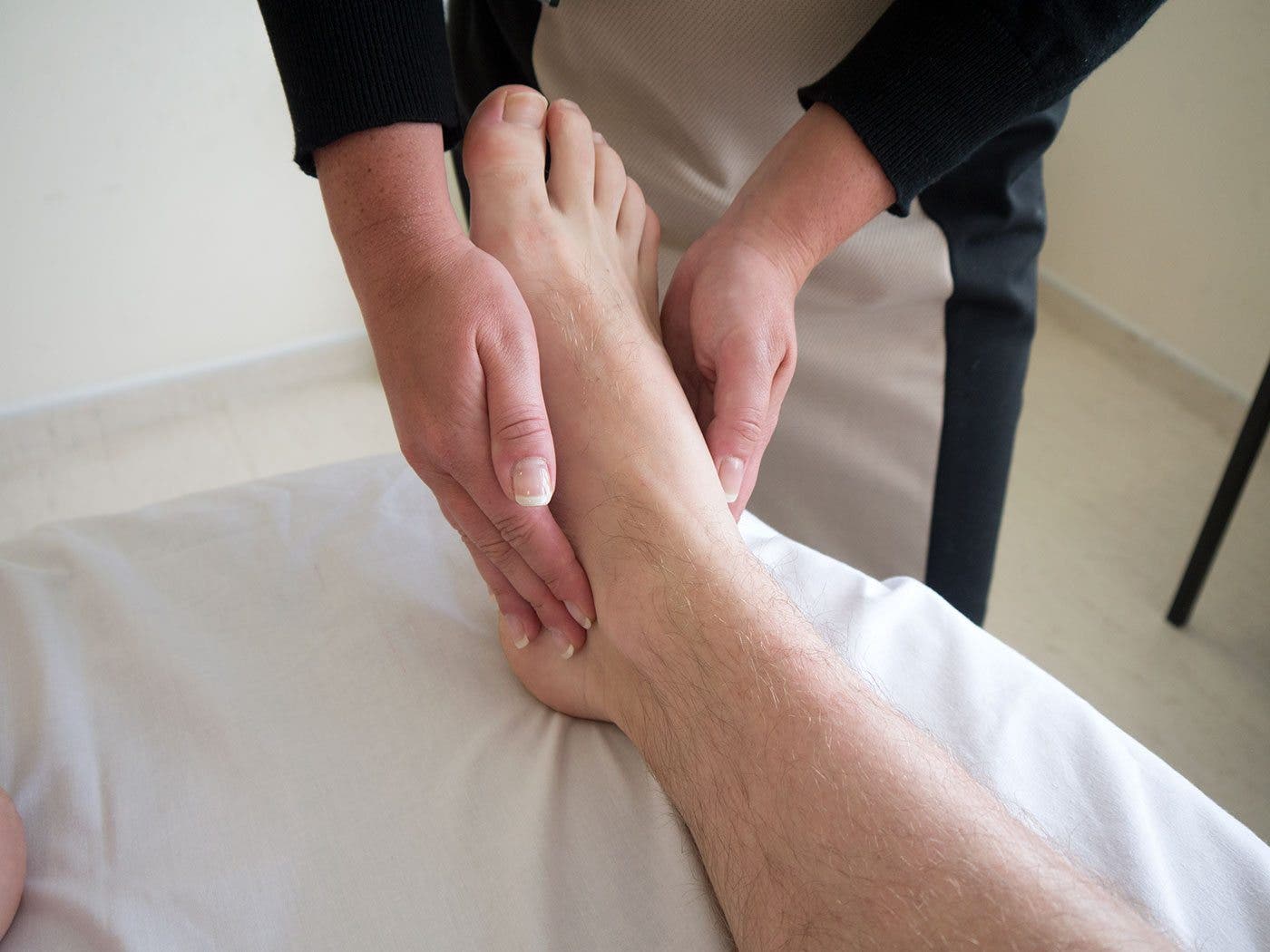
 pneumoniae при условии приема больших доз. 12 Детям, получившим вакцинацию против Haemophilus type b, не требуется адъювантный ампициллин или амоксициллин, которые в эпоху превакцинации часто давали всем детям в возрасте до 5 лет. 13 K. kingae чувствительна к большинству пенициллинов и цефалоспоринов. 14 Фторхинолоны или цефалоспорины третьего поколения являются действенными вариантами против Salmonella spp., Но их стоимость может быть проблемой в странах с низким уровнем дохода. 15 , 16
pneumoniae при условии приема больших доз. 12 Детям, получившим вакцинацию против Haemophilus type b, не требуется адъювантный ампициллин или амоксициллин, которые в эпоху превакцинации часто давали всем детям в возрасте до 5 лет. 13 K. kingae чувствительна к большинству пенициллинов и цефалоспоринов. 14 Фторхинолоны или цефалоспорины третьего поколения являются действенными вариантами против Salmonella spp., Но их стоимость может быть проблемой в странах с низким уровнем дохода. 15 , 16  После короткого 2–4-дневного внутривенного курса антибиотик можно вводить перорально, если пациент выздоравливает и уровень СРБ снижается. 10 В неосложненных случаях достаточно двухнедельного курса. 17 Если поражена соседняя кость, лечение антибиотиками должно быть продлено как минимум на 3 недели. 18 Дексаметазон можно вводить для уменьшения воспаления, что может привести к несколько более короткому пребыванию в больнице. 19 Нестероидные противовоспалительные средства используются для снятия боли.
После короткого 2–4-дневного внутривенного курса антибиотик можно вводить перорально, если пациент выздоравливает и уровень СРБ снижается. 10 В неосложненных случаях достаточно двухнедельного курса. 17 Если поражена соседняя кость, лечение антибиотиками должно быть продлено как минимум на 3 недели. 18 Дексаметазон можно вводить для уменьшения воспаления, что может привести к несколько более короткому пребыванию в больнице. 19 Нестероидные противовоспалительные средства используются для снятия боли.  8 , 10 Считается, что поздняя диагностика, серповидно-клеточная анемия и инфекция, вызванная лейкоцидинпродуцирующими штаммами MRSA Пантона – Валентайна, предрасполагают к ортопедическим последствиям, 20 , 21 и длительное течение 3–4 недели для MRSA SA по-прежнему рекомендуется большинством исследователей. 11 Кроме того, оптимальная продолжительность антибактериальной терапии не изучалась у пациентов с иммунодефицитом и тяжелым основным заболеванием, а также у новорожденных, и в этих случаях терапия может быть индивидуальной.
8 , 10 Считается, что поздняя диагностика, серповидно-клеточная анемия и инфекция, вызванная лейкоцидинпродуцирующими штаммами MRSA Пантона – Валентайна, предрасполагают к ортопедическим последствиям, 20 , 21 и длительное течение 3–4 недели для MRSA SA по-прежнему рекомендуется большинством исследователей. 11 Кроме того, оптимальная продолжительность антибактериальной терапии не изучалась у пациентов с иммунодефицитом и тяжелым основным заболеванием, а также у новорожденных, и в этих случаях терапия может быть индивидуальной.  Артроскопия приобрела популярность при артрите коленного, тазобедренного и плечевого суставов. 24 , 25
Артроскопия приобрела популярность при артрите коленного, тазобедренного и плечевого суставов. 24 , 25  Внутривенный курс продолжают 2–4 дня до выздоровления. В неосложненных случаях достаточно 2-хнедельного курса. Открытая артротомия предназначена для пациентов, которые не отвечают на традиционную терапию. Пациенты с отсроченным диагнозом или инфекцией MRSA имеют худший прогноз, как и дети из неблагополучных семей из малообеспеченных семей. 26
Внутривенный курс продолжают 2–4 дня до выздоровления. В неосложненных случаях достаточно 2-хнедельного курса. Открытая артротомия предназначена для пациентов, которые не отвечают на традиционную терапию. Пациенты с отсроченным диагнозом или инфекцией MRSA имеют худший прогноз, как и дети из неблагополучных семей из малообеспеченных семей. 26  Журнал Педиатр Ортоп Б. 2014; 23 (2): 196–199.[PubMed] [Google Scholar] 5. Ju KL, Zurakowski D, Kocher MS. Дифференциация резистентного к метициллину и чувствительного к метициллину Staphylococcus aureus Остеомиелит у детей: основанный на доказательствах алгоритм клинического прогноза. J Bone Joint Surg Am. 2011. 93 (18): 1693–1701. [PubMed] [Google Scholar] 6. Ягупский П., Дубнов-Раз Г., Джене А., Эфрос М., Израильско-испанская исследовательская группа Kin-gella kingae Дифференциация Kingella kingae септического артрита бедра от преходящего синовита у детей раннего возраста.J Pediatr. 2014; 165 (5): 985–989. [PubMed] [Google Scholar] 7. Султан Дж., Хьюз П. Дж. Септический артрит или преходящий синовит бедра у детей: значение алгоритмов клинического прогноза. J Bone Joint Surg Br. 2010. 92 (9): 1289–1293. [PubMed] [Google Scholar] 8. Pääkkönen M, Kallio MJ, Kallio PE, Peltola H. Чувствительность скорости оседания эритроцитов и С-реактивного белка при инфекциях костей и суставов у детей.
Журнал Педиатр Ортоп Б. 2014; 23 (2): 196–199.[PubMed] [Google Scholar] 5. Ju KL, Zurakowski D, Kocher MS. Дифференциация резистентного к метициллину и чувствительного к метициллину Staphylococcus aureus Остеомиелит у детей: основанный на доказательствах алгоритм клинического прогноза. J Bone Joint Surg Am. 2011. 93 (18): 1693–1701. [PubMed] [Google Scholar] 6. Ягупский П., Дубнов-Раз Г., Джене А., Эфрос М., Израильско-испанская исследовательская группа Kin-gella kingae Дифференциация Kingella kingae септического артрита бедра от преходящего синовита у детей раннего возраста.J Pediatr. 2014; 165 (5): 985–989. [PubMed] [Google Scholar] 7. Султан Дж., Хьюз П. Дж. Септический артрит или преходящий синовит бедра у детей: значение алгоритмов клинического прогноза. J Bone Joint Surg Br. 2010. 92 (9): 1289–1293. [PubMed] [Google Scholar] 8. Pääkkönen M, Kallio MJ, Kallio PE, Peltola H. Чувствительность скорости оседания эритроцитов и С-реактивного белка при инфекциях костей и суставов у детей. Clin Orthop Relat Res. 2010. 468 (3): 861–866. [Бесплатная статья PMC] [PubMed] [Google Scholar] 9.Лион RM, Evanich JD. Культурально-отрицательный септический артрит у детей. J Pediatr Orthop. 1999. 19 (5): 655–659. [PubMed] [Google Scholar] 10. Peltola H, Pääkkönen M, Kallio P, Kallio MJ, Исследовательская группа OM-SA Клиндамицин против цефалоспоринов первого поколения при острых костно-суставных инфекциях у детей — проспективное квази-рандомизированное контролируемое исследование. Clin Microbiol Infect. 2012. 18 (6): 582–589. [PubMed] [Google Scholar] 11. Лю С., Байер А., Косгроув С. Е. и др. Американское общество инфекционных заболеваний. Руководящие принципы клинической практики Американского общества инфекционных болезней по лечению метициллин-резистентных инфекций Staphylococcus aureus у взрослых и детей.Clin Infect Dis. 2011; 52 (3): e18 – e55. [PubMed] [Google Scholar] 12. Мера Р.М., Миллер Л.А., Амрин-Мадсен Х., Сам Д.Ф. Влияние новых стандартов лаборатории клинических испытаний институт Streptococcus pneumoniae контрольных точек чувствительности к пенициллину на зарегистрированные изменения резистентности с течением времени.
Clin Orthop Relat Res. 2010. 468 (3): 861–866. [Бесплатная статья PMC] [PubMed] [Google Scholar] 9.Лион RM, Evanich JD. Культурально-отрицательный септический артрит у детей. J Pediatr Orthop. 1999. 19 (5): 655–659. [PubMed] [Google Scholar] 10. Peltola H, Pääkkönen M, Kallio P, Kallio MJ, Исследовательская группа OM-SA Клиндамицин против цефалоспоринов первого поколения при острых костно-суставных инфекциях у детей — проспективное квази-рандомизированное контролируемое исследование. Clin Microbiol Infect. 2012. 18 (6): 582–589. [PubMed] [Google Scholar] 11. Лю С., Байер А., Косгроув С. Е. и др. Американское общество инфекционных заболеваний. Руководящие принципы клинической практики Американского общества инфекционных болезней по лечению метициллин-резистентных инфекций Staphylococcus aureus у взрослых и детей.Clin Infect Dis. 2011; 52 (3): e18 – e55. [PubMed] [Google Scholar] 12. Мера Р.М., Миллер Л.А., Амрин-Мадсен Х., Сам Д.Ф. Влияние новых стандартов лаборатории клинических испытаний институт Streptococcus pneumoniae контрольных точек чувствительности к пенициллину на зарегистрированные изменения резистентности с течением времени. Microb Drug Resist. 2011; 17 (1): 47–52. [PubMed] [Google Scholar] 13. Пелтола Х., Каллио М.Ю., Ункила-Каллио Л. Снижение заболеваемости септическим артритом у детей с помощью вакцинации против Haemophilus influenza type-b.Значение для лечения. J Bone Joint Surg Br. 1998. 80 (3): 471–473. [PubMed] [Google Scholar] 14. Saphyakhajon P, Joshi AY, Huskins WC, Henry NK, Boyce TG. Эмпирическая антибактериальная терапия при острых костно-суставных инфекциях с подозрением на метициллин-резистентность Staphylococcus aureus или Kingella. Pediatr Infect Dis J. 2008; 27 (8): 765–767. [PubMed] [Google Scholar] 15. Шерман Дж. У., Конте Дж., Младший. Лечение цефтриаксоном полирезистентного сальмонеллезного остеомиелита. Am J Med. 1987. 83 (1): 137–138.[PubMed] [Google Scholar] 16. Брэдли Дж. С., Джексон М. А., Комитет по инфекционным заболеваниям. Американская академия педиатрии. Использование системных и местных фторхинолонов. Педиатрия. 2011; 128 (4): e1034 – e1045. [PubMed] [Google Scholar] 17.
Microb Drug Resist. 2011; 17 (1): 47–52. [PubMed] [Google Scholar] 13. Пелтола Х., Каллио М.Ю., Ункила-Каллио Л. Снижение заболеваемости септическим артритом у детей с помощью вакцинации против Haemophilus influenza type-b.Значение для лечения. J Bone Joint Surg Br. 1998. 80 (3): 471–473. [PubMed] [Google Scholar] 14. Saphyakhajon P, Joshi AY, Huskins WC, Henry NK, Boyce TG. Эмпирическая антибактериальная терапия при острых костно-суставных инфекциях с подозрением на метициллин-резистентность Staphylococcus aureus или Kingella. Pediatr Infect Dis J. 2008; 27 (8): 765–767. [PubMed] [Google Scholar] 15. Шерман Дж. У., Конте Дж., Младший. Лечение цефтриаксоном полирезистентного сальмонеллезного остеомиелита. Am J Med. 1987. 83 (1): 137–138.[PubMed] [Google Scholar] 16. Брэдли Дж. С., Джексон М. А., Комитет по инфекционным заболеваниям. Американская академия педиатрии. Использование системных и местных фторхинолонов. Педиатрия. 2011; 128 (4): e1034 – e1045. [PubMed] [Google Scholar] 17. [PubMed] [Google Scholar] 22. Гивон У., Либерман Б., Шиндлер А., Бланкштейн А., Ганель А. Лечение септического артрита тазобедренного сустава с помощью повторных аспираций под контролем ультразвука. J Pediatr Orthop. 2004. 24 (3): 266–270. [PubMed] [Google Scholar] 23. Пяакконен М., Каллио М.Дж., Пелтола Х., Каллио ЧП. Детский септический тазобедренный сустав с артротомией или без: ретроспективный анализ 62 последовательных неонатальных случаев с положительным посевом.Журнал Педиатр Ортоп Б. 2010; 19 (3): 264–269. [PubMed] [Google Scholar] 24. Agout C, Lakhal W, Fournier J, de Bodman C, Bonnard C. Артроскопическое лечение септического артрита колена у детей. Orthop Traumatol Surg Res. 2015; 101 (8 приложение): S333 – S336. [PubMed] [Google Scholar] 25. Эдмондс EW, Лин C, Фарнсворт CL, Bomar JD, Upasani VV. Медиальный портал для артроскопии тазобедренного сустава у детей с септическим артритом: исследование безопасности. J Pediatr Orthop. 3 сентября 2016 г .; Epub. [PubMed] [Google Scholar]
[PubMed] [Google Scholar] 22. Гивон У., Либерман Б., Шиндлер А., Бланкштейн А., Ганель А. Лечение септического артрита тазобедренного сустава с помощью повторных аспираций под контролем ультразвука. J Pediatr Orthop. 2004. 24 (3): 266–270. [PubMed] [Google Scholar] 23. Пяакконен М., Каллио М.Дж., Пелтола Х., Каллио ЧП. Детский септический тазобедренный сустав с артротомией или без: ретроспективный анализ 62 последовательных неонатальных случаев с положительным посевом.Журнал Педиатр Ортоп Б. 2010; 19 (3): 264–269. [PubMed] [Google Scholar] 24. Agout C, Lakhal W, Fournier J, de Bodman C, Bonnard C. Артроскопическое лечение септического артрита колена у детей. Orthop Traumatol Surg Res. 2015; 101 (8 приложение): S333 – S336. [PubMed] [Google Scholar] 25. Эдмондс EW, Лин C, Фарнсворт CL, Bomar JD, Upasani VV. Медиальный портал для артроскопии тазобедренного сустава у детей с септическим артритом: исследование безопасности. J Pediatr Orthop. 3 сентября 2016 г .; Epub. [PubMed] [Google Scholar]  Симптомы включают боль, отсутствие веса и лихорадку. Маркеры воспаления повышены, а ультразвуковое исследование демонстрирует выпот в сустав.
Симптомы включают боль, отсутствие веса и лихорадку. Маркеры воспаления повышены, а ультразвуковое исследование демонстрирует выпот в сустав. 
 Гематогенное бактериальное распространение — наиболее частая причина септического артрита у детей.Остеомиелит соседних костей также может привести к инфекции суставов ( Рисунок 2 ). Это особенно характерно для суставов с внутрикапсулярным метафизом, например, бедра и плеча. Возможна прямая инокуляция через проникающие ранения или хирургическое вмешательство.
Гематогенное бактериальное распространение — наиболее частая причина септического артрита у детей.Остеомиелит соседних костей также может привести к инфекции суставов ( Рисунок 2 ). Это особенно характерно для суставов с внутрикапсулярным метафизом, например, бедра и плеча. Возможна прямая инокуляция через проникающие ранения или хирургическое вмешательство.