Вмешательства, направленные на предотвращение рецидивов целлюлита и рожи
Актуальность
И целлюлит, и рожа – это бактериальные инфекции кожи, чаще всего поражающие ноги. Рожа затрагивает верхние слои кожи, тогда как целлюлит распространяется на более глубокие слои. Однако, зачастую оказывается достаточно сложно провести между ними четкую границу, поэтому в этом обзоре мы будем рассматривать оба заболевания, используя единый термин «целлюлит». Около половины людей, страдающих целлюлитом, сталкиваются с проблемой его рецидивов. Несмотря на распространенность этого состояния, в настоящее время нет подтвержденной, основанной на доказательствах высокого качества информации об эффективных способах предотвращения рецидивов этого заболевания.
Вопрос обзора
Какой метод лечения, направленный на предотвращение рецидивовов целлюлита, является наиболее эффективным в сравнении с отсутствием лечения, плацебо, другим вмешательством или тем же вмешательством по другой схеме у пациентов старше 16 лет и какие у него побочные эффекты?
Характеристика исследований
Мы провели поиск по базам данных и регистрам вплоть до июня 2016 года.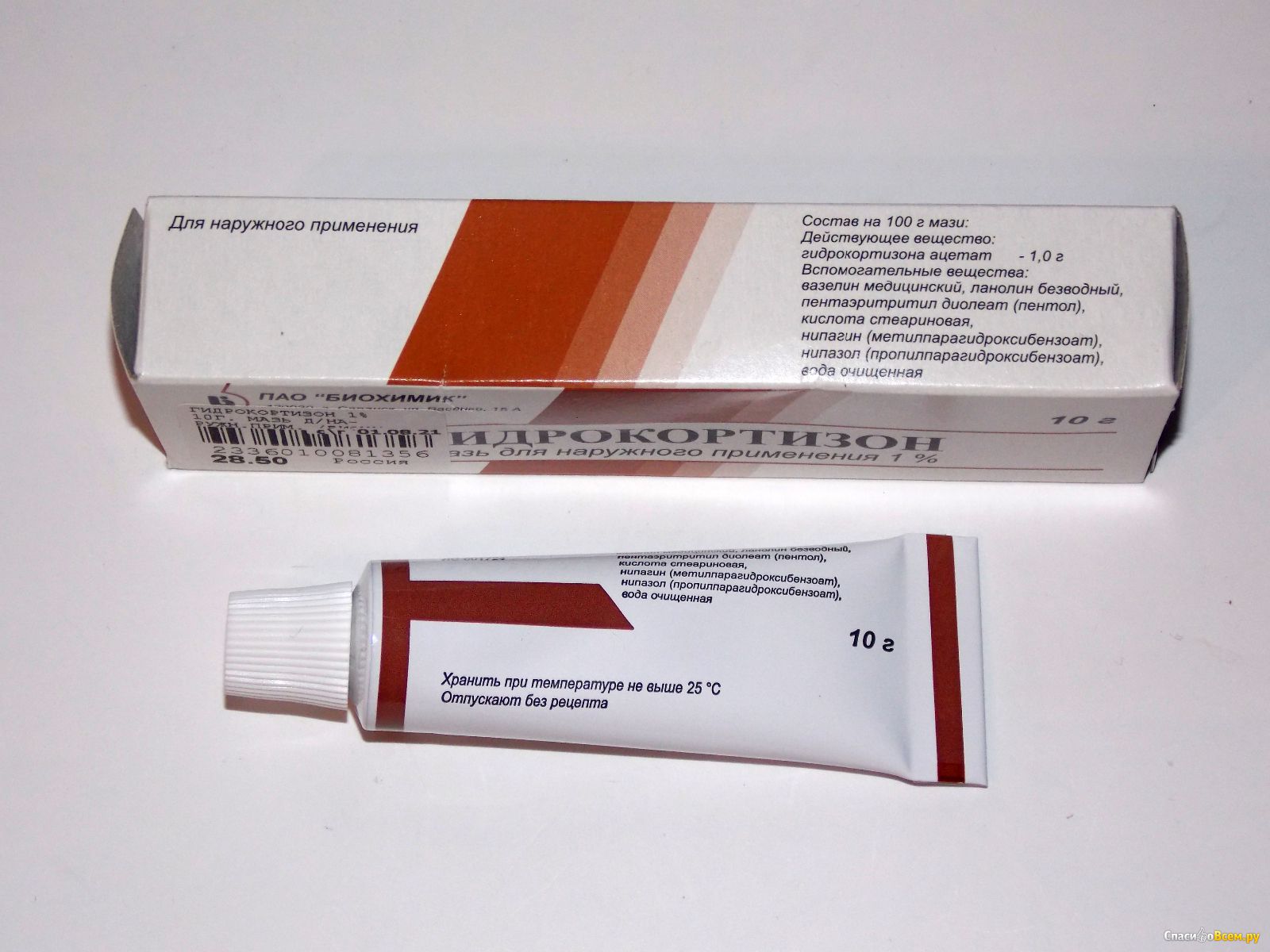
Исследования проводились в Великобритании, Швеции, Тунисе, Израиле и Австрии. В основном, они проводились на базе стационаров, а два исследования были многоцентровыми. В анамнезе участников всех испытаний отмечалось небольшое число (от 1 до 4) эпизодов целлюлита. В испытаниях, в которых изучали профилактику антибиотиками, у участников был целлюлит ног, а в испытании, в котором изучали селен, у участников был целлюлит рук.
Основные результаты
Предотвращение повторных эпизодов целлюлита было основным исходом. Среди других исходов – число рецидивов целлюлита, время между повторными эпизодами, госпитализации, качество жизни, развитие устойчивости к антибиотикам, нежелательные реакции и смертность.
Обобщив результаты всех пяти испытаний, посвященных антибиотикам, мы нашли доказательства умеренного качества, что лечение антибиотиками (в частности, пенициллином) является эффективным и безопасным способом предотвращения рецидивов целлюлита ног, по сравнению с отсутствием лечения или плацебо.
Анализ показал, что в сравнении с отсутствием лечения или плацебо, антибиотики снижали риск рецидивов на 69%, уменьшали их число более чем на 50% и существенно снижали время до наступления следующих эпизодов (доказательства умеренного качества). Однако, мы нашли доказательства низкого качества, что эффект антибиотиков в отношении этих исходов снижался после прекращения лечения. Кроме того, было отмечено, что положительный эффект от применения антибиотиков был соответствующим у пациентов, у которых было, по меньшей мере, два эпизода целлюлита за предшествующие три года.
Доказательства низкого качества свидетельствовали, что значимых различий в развитии побочных эффектов и частоте госпитализации у пациентов, принимавших антибиотики, и тех, кто не принимал ничего или получал плацебо, не было. Имеющиеся данные не позволяют сделать однозначные выводы относительно длительности госпитализации пациентов.
Имеющиеся данные не позволяют сделать однозначные выводы относительно длительности госпитализации пациентов.
В исследованиях не сообщали о каких-либо серьезных нежелательных эффектах. Наиболее часто отмечались следующие побочные эффекты: диарея, тошнота, сыпь (о тяжелых поражениях кожи не сообщалось) и кандидоз. В 3 исследованиях прием антибиотиков был прекращен из-за нежелательных эффектов. У 3 человек, принимавших эритромицин, появились жалобы на боль в животе и тошноту, после чего они были переведены на прием пенициллина. В одном из исследований 2 человека прекратили принимать пенициллин в связи с диареей и тошнотой. Также около 10% участников другого исследования отказались от инъекций бензатина бензилпенициллина из-за боли в месте инъекции.
Ни в одном из исследований не оценивали качество жизни и развитие устойчивости к антибиотикам.
Уверенность в доказательствах
Качество доказательств относительно эффективности антибиотиков в профилактике рецидивов, сокращении их частоты и увеличении времени между повторными эпизодами, в сравнении с плацебо или отсутствием лечения, было умеренным и ограничивалось небольшим числом участников и событий.
Современные методы лечения рожи Текст научной статьи по специальности «Клиническая медицина»
УДК 616.981.21:616-08 © А.Г. Хасанов, Д.Г. Шайбаков, 2013
А.Г. Хасанов, Д.Г. Шайбаков СОВРЕМЕННЫЕ МЕТОДЫ ЛЕЧЕНИЯ РОЖИ
ГБОУ ВПО «Башкирский государственный медицинский университет» Минздрава России, г. Уфа
В обзоре представлены литературные данные по лечению рожи. Отражены современные аспекты этиотропной, имму-нокорригирующей терапии, применение физических методов воздействия на местный очаг поражения. Приводятся данные об особенностях противорецидивной антибактериальной терапии и об ее эффективности. Также описываются особенности лечения больных пожилого возраста, необходимость коррекции сопутствующей соматической патологии, что часто является причиной полипрагмазии.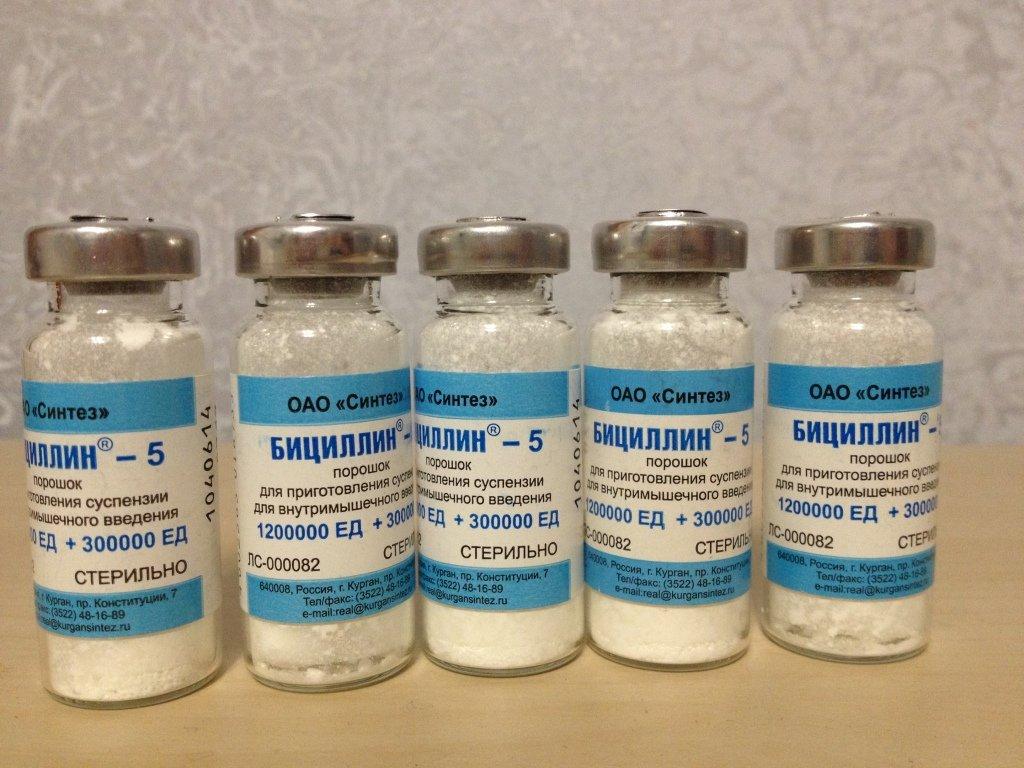
Ключевые слова: рожа, антибактериальная терапия, иммунокоррекция, рецидив рожи.
A.G. Khasanov, D.G. Shaibakov MODERN METHODS OF ERYSIPELAS TREATMENT
The review presents the published data on the treatment of erysipelas. It reflects the modern aspects of etiotropic immunotherapy, the use of physical methods to influence the local lesion. The article gives the data about the features of anti-relapsing antibiotic therapy and its effectiveness. It also describes the features of the treatment of elderly patients, the need for correction of concomitant somatic pathology, which is a frequent cause of polypharmacy. In this paper great attention is paid to immunotropic therapy, it describes different methods of medicinal application and drugs used for immunomodulation.
Key words: erysipelas, antibacterial therapy, immunotherapy, recurrence of erysipelas.
Несмотря на многовековую историю лечения рожи, появление современных антибактериальных препаратов, применение различных физиотерапевтических процедур существенно ситуацию не улучшили.
В последние годы среди больных рожей отмечается резкое увеличение осложненных ее форм — флегмонозной и некротической, которые нуждаются не только в комплексном медикаментозном лечении, но и в операции, что свидетельствует о малой эффективности традиционных способов лечения и профилактики рецидивов [5,9,25,55]. Такое положение, с одной стороны, можно объяснить сложностью патогенеза заболевания, отсутствием экспериментальной модели болезни, поздним поступлением больных, превалированием лиц пожилого и старческого возраста с множественными сопутствующими заболеваниями, с другой стороны, отсутствием единых общепринятых стандартов лечения, основанных на принципах доказательной медицины.
В медицинской практике широко применяются также физиотерапевтические методы воздействия на область местного очага с использованием низкоинтенсивного гелий-
неонового и инфракрасного лазера и внутривенного лазерного облучения крови [1,20, 30,31].
Ведущее место в лечении рожи занимает этиотропная антибактериальная терапия. Большинство авторов подчеркивают необходимость ранней антибактериальной терапии в остром периоде заболевания с учетом характера заболевания, его тяжести, кратности и т. д. Как свидетельствуют литературные данные, пенициллин до сих пор остается «золотым стандартом» лечения [25,31]. Однако в последние годы увеличивается доля пеницил-линорезистентных штаммов стрептококков, которые наблюдаются у 25 % больных рожей [14]. Ряд авторов отмечают высокую чувствительность стрептококка к пенициллину in vitro и ее резкое снижение в организме больного из-за недостаточной экспрессии микробом белков-рецепторов пенициллина либо их экранирования сывороточными, плазменными и лимфатическими белками, обладающими высоким аффинитетом к белкам клеточной стенки микроба [24]. Последние годы в лечении рожи используются полусинтетические пенициллины, цефалоспорины, макролиды, препараты группы линкозамидов, тетрацик-лины, ванкомицин, миноциклин, фторхиноло-ны [40,50,49,52,57]. Однако назначение эритромицина, тетрациклинов и рифампицина при лечении стрептококковых инфекций в последние годы ограничено развитием высокой устойчивости стрептококков к этим препаратам [11,14,22,27,50,53].
д. Как свидетельствуют литературные данные, пенициллин до сих пор остается «золотым стандартом» лечения [25,31]. Однако в последние годы увеличивается доля пеницил-линорезистентных штаммов стрептококков, которые наблюдаются у 25 % больных рожей [14]. Ряд авторов отмечают высокую чувствительность стрептококка к пенициллину in vitro и ее резкое снижение в организме больного из-за недостаточной экспрессии микробом белков-рецепторов пенициллина либо их экранирования сывороточными, плазменными и лимфатическими белками, обладающими высоким аффинитетом к белкам клеточной стенки микроба [24]. Последние годы в лечении рожи используются полусинтетические пенициллины, цефалоспорины, макролиды, препараты группы линкозамидов, тетрацик-лины, ванкомицин, миноциклин, фторхиноло-ны [40,50,49,52,57]. Однако назначение эритромицина, тетрациклинов и рифампицина при лечении стрептококковых инфекций в последние годы ограничено развитием высокой устойчивости стрептококков к этим препаратам [11,14,22,27,50,53].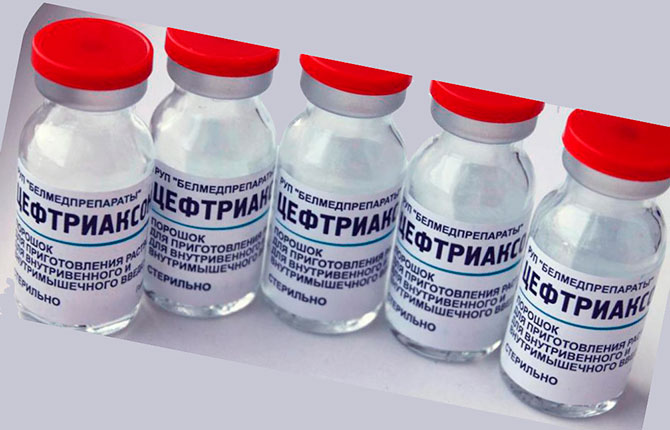
течении — антибиотики более широкого спектра действия [2,12,25,31]. Е.И. Краснова констатировала при рецидивирующей роже высокую эффективность комбинации рифампи-цина и макропена [12]. В.Л. Черкасовым и соавт. предложен метод двухкурсовой антибактериальной терапии, когда вначале назначался у#-лактамный антибиотик, действующий бактерицидно, а второй курс состоял в применении бактериостатика, действующего на L-формы стрептококка А, и при наличии выраженных остаточных явлений рожи назначался через 7-10 дней после окончания первого курса [31].
С целью более полной санации очага поражения разрабатывались различные способы местного использования антибиотиков. Н. Partsch при лечении некротической рожи нижних конечностей предложил ретроградное внутривенное введение этиотропных средств. За рубежом также широко используются внутривенные инъекции пенициллина [34,38,40,43,45,48]. В нашей стране в 80-е годы прошлого века был разработан метод эн-долимфатической антибактериальной терапии, позволяющий создать в лимфатических сосудах и узлах пораженной области оптимальную концентрацию лекарственного вещества «в чистом виде» и обеспечивающий его максимальный контакт с патогенными микроорганизмами в местах их задержки и скопления [2]. Первоначально растворы антибиотиков вводились непосредственно в лимфатическую систему нижних конечностей путем хирургической пункции или катетеризации периферического лимфатического сосуда тыльной поверхности стопы на стороне поражения. Однако из-за технической сложности катетеризации мелких лимфатических сосудов, развития частых осложнений, связанных с действием концентрированного раствора веществ на лимфатическую систему, проявлявшихся усилением отека, развитием лимфаденита, некроза кожи и подкожной клетчатки, данный метод не получил широкого распространения и был вытеснен непрямым эндо-лимфатическим введением лекарственных веществ, доступным для применения в условиях любого стационара.
В нашей стране в 80-е годы прошлого века был разработан метод эн-долимфатической антибактериальной терапии, позволяющий создать в лимфатических сосудах и узлах пораженной области оптимальную концентрацию лекарственного вещества «в чистом виде» и обеспечивающий его максимальный контакт с патогенными микроорганизмами в местах их задержки и скопления [2]. Первоначально растворы антибиотиков вводились непосредственно в лимфатическую систему нижних конечностей путем хирургической пункции или катетеризации периферического лимфатического сосуда тыльной поверхности стопы на стороне поражения. Однако из-за технической сложности катетеризации мелких лимфатических сосудов, развития частых осложнений, связанных с действием концентрированного раствора веществ на лимфатическую систему, проявлявшихся усилением отека, развитием лимфаденита, некроза кожи и подкожной клетчатки, данный метод не получил широкого распространения и был вытеснен непрямым эндо-лимфатическим введением лекарственных веществ, доступным для применения в условиях любого стационара.
К.В. Малых [19] в лечении рожи применял сочетанное внутриартериальное (в наружную бедренную артерию пораженной конечности) и эндолимфатическое введение этиотропных средств с одновременным форсированием лимфовенозного оттока при помощи поэтапного наложения давящих цинк-желатиновых повязок на пораженную конечность. По мнению Хасанова А.Г с соавт., лимфотропная антибиотикотерапия путем иммобилизации цефаперазона с помощью ме-тиленовой синий на эндотелий лимфатического сосуда позволяет достоверно повысить эффективность лечения рецидивирующей формы рожистого воспаления [27,28].
Использование современных антибиотиков, новых комбинаций и путей их введения в остром периоде рожи привело к снижению числа тяжелых форм и осложнений, показателей летальности, однако не решило проблему рецидивов [2,20]. С целью профилактики рецидивов заболевания большинство современных отечественных и зарубежных авторов наиболее часто применяют препараты пенициллина продленного действия длительными курсами [2,12,25,31,34,35,43]. В частности, А. А. Еровиченков [39,40] считает необходимым назначение непрерывной круглогодичной бициллино- или ретарпенопрофилак-тики на протяжении 2 — 3 лет больным с частыми рецидивами рожи для предупреждения реверсии L-форм стрептококка в исходные бактериальные формы. Однако рядом авторов [10] указывалось на недостаточную эффективность бициллинопрофилактики у 13 — 37 % пациентов. Эксперты Американской академии педиатрии считают профилактическое использование антибиотиков нецелесообразным, а эффективность антибиотикопрофилак-тики не доказанной. Allard Р. [34] и А. С. Sjoblom [59] наблюдали рецидивы рожи при продолжительной антибактериальной терапии пенициллином, феноксиметилпенициллином и эритромицином, С.А. Шляпников, М.К. Малютина [20,32] указывают на отсутствие значимого профилактического эффекта различных групп антибиотиков, отмечая при этом развитие дополнительной сенсибилизации и нарастание числа резистентных штаммов микроорганизмов.
С целью профилактики рецидивов заболевания большинство современных отечественных и зарубежных авторов наиболее часто применяют препараты пенициллина продленного действия длительными курсами [2,12,25,31,34,35,43]. В частности, А. А. Еровиченков [39,40] считает необходимым назначение непрерывной круглогодичной бициллино- или ретарпенопрофилак-тики на протяжении 2 — 3 лет больным с частыми рецидивами рожи для предупреждения реверсии L-форм стрептококка в исходные бактериальные формы. Однако рядом авторов [10] указывалось на недостаточную эффективность бициллинопрофилактики у 13 — 37 % пациентов. Эксперты Американской академии педиатрии считают профилактическое использование антибиотиков нецелесообразным, а эффективность антибиотикопрофилак-тики не доказанной. Allard Р. [34] и А. С. Sjoblom [59] наблюдали рецидивы рожи при продолжительной антибактериальной терапии пенициллином, феноксиметилпенициллином и эритромицином, С.А. Шляпников, М.К. Малютина [20,32] указывают на отсутствие значимого профилактического эффекта различных групп антибиотиков, отмечая при этом развитие дополнительной сенсибилизации и нарастание числа резистентных штаммов микроорганизмов. М.П. Королев показал, что, несмотря на применение современных методов антибактериальной терапии, частота рецидивов при роже не снижается [15]. Рецидивирующее течение регистрируется более чем у трети пациентов.
М.П. Королев показал, что, несмотря на применение современных методов антибактериальной терапии, частота рецидивов при роже не снижается [15]. Рецидивирующее течение регистрируется более чем у трети пациентов.
Ряд авторов в качестве этиотропной терапии использовали стрептококковый бакте-
риофаг подкожно и в виде орошений эрозиро-ванных поверхностей при буллезной форме [13].
До сих пор дискутабельными остаются вопросы применения в лечении рожи нестероидных противовоспалительных средств (НПВС), глюкокортикостероидов, антикоагулянтов. Выявлено, что в присутствии эндотоксина стрептококка после назначения НПВС, в частности ибупрофена, наблюдались повышение провоспалительных цитокинов -сывороточной концентрации ИЛ-6, значительное увеличение уровня ФНО-а, что приводило к более тяжелому, агрессивному течению заболевания, развитию осложнений [3,4,]. В ряде случаев применение НПВС может давать парадоксальный эффект, когда воспаление не только не утихает, но даже усиливается в связи со снижением синтеза простагландинов группы Е и простациклина, «сворачивающих» инфильтрацию. Использование глюкокортикоидов системного действия считается оправданным лишь в тяжелых случаях, при развитии осложненных форм [31,42]. А. Oikarinen отмечал положительный эффект местного использования глюкокорти-коидов при буллезной роже. С другой стороны, ряд исследователей справедливо указывают, что назначение данных препаратов вследствие их иммуносупрессивного действия на фоне нарушенного иммунитета повышает риск рецидивирующего течения заболевания. Р.1. Bergkvist при сочетанном применении преднизолона и антибактериальной терапии не выявил неблагоприятного влияния предни-золона на частоту развития рецидивов рожи [36,37].
В ряде случаев применение НПВС может давать парадоксальный эффект, когда воспаление не только не утихает, но даже усиливается в связи со снижением синтеза простагландинов группы Е и простациклина, «сворачивающих» инфильтрацию. Использование глюкокортикоидов системного действия считается оправданным лишь в тяжелых случаях, при развитии осложненных форм [31,42]. А. Oikarinen отмечал положительный эффект местного использования глюкокорти-коидов при буллезной роже. С другой стороны, ряд исследователей справедливо указывают, что назначение данных препаратов вследствие их иммуносупрессивного действия на фоне нарушенного иммунитета повышает риск рецидивирующего течения заболевания. Р.1. Bergkvist при сочетанном применении преднизолона и антибактериальной терапии не выявил неблагоприятного влияния предни-золона на частоту развития рецидивов рожи [36,37].
По мнению ряда авторов, показанием для назначения гепарина при роже является развитие осложнений в виде тромбозов или тромбофлебитов [40, 51, 43,54], другие исследователи рекомендуют широкое назначение антикоагулянтов, особенно при развитии геморрагических форм [31,58].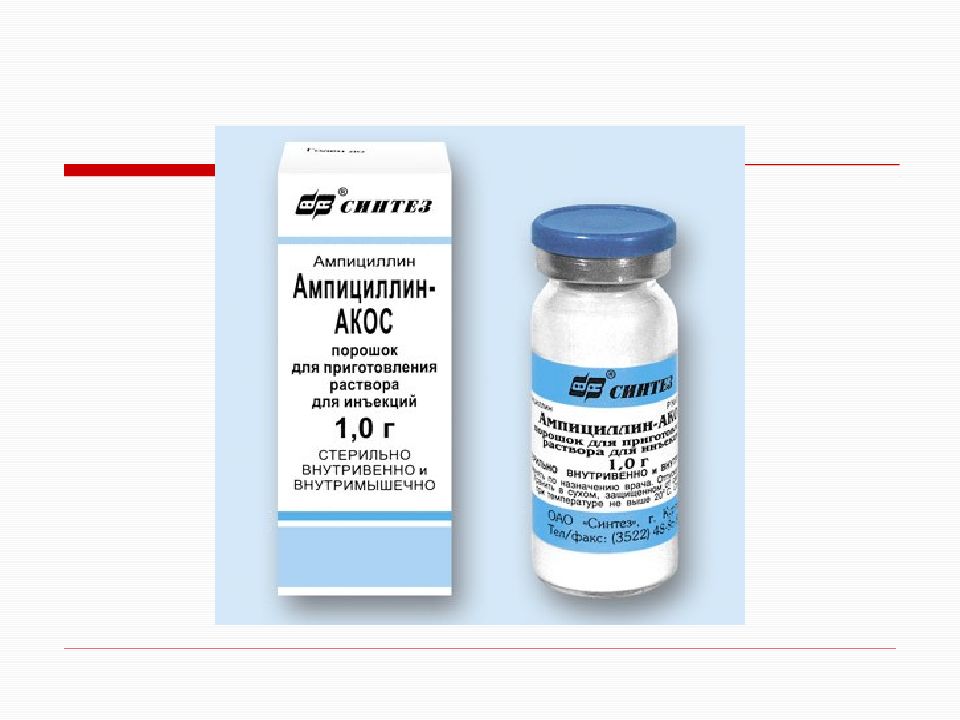 Патогенетически обосновано при роже назначение антиокси-дантов, витаминов Е и С, дезагрегантов, анти-гистаминных средств, ингибиторов протеоли-за [11,12,14,15,21,29]. Учитывая пожилой возраст, большинство пациентов с рожей требуют коррекции сопутствующей соматической патологии и зачастую в лечении данных больных наблюдается полипрагмазия [5]. В настоящее время с целью стимуляции иммунного ответа и предупреждения развития острых стрептококковых инфекций разрабатываются стрептококковые вакцины [56], в частности содержащие эпитопы М-протеинов
Патогенетически обосновано при роже назначение антиокси-дантов, витаминов Е и С, дезагрегантов, анти-гистаминных средств, ингибиторов протеоли-за [11,12,14,15,21,29]. Учитывая пожилой возраст, большинство пациентов с рожей требуют коррекции сопутствующей соматической патологии и зачастую в лечении данных больных наблюдается полипрагмазия [5]. В настоящее время с целью стимуляции иммунного ответа и предупреждения развития острых стрептококковых инфекций разрабатываются стрептококковые вакцины [56], в частности содержащие эпитопы М-протеинов
стрептококка, не вступающие в перекрестную реакцию с тканевыми антигенами человеческого организма. U.F. Haustein [44] считает, что использование стрептококковой вакцины эквивалентно долгосрочной антибиотикопро-филактике рецидивов рожи и является альтернативой этому методу. Ряд авторов для профилактики рецидивов использовали бактериальные липополисахариды (пирогенал и продигиозан), которые вызывают активацию нейтрофильно-макрофагального звена, повышение уровня лизоцима и иммуноглобулинов класса А и М [25,31]. Также применяются различные иммунотропные средства — мети-лурацил, левамизол, нуклеинат натрия, тима-лин, тимоген, спленин, реаферон. Большинство иммуномодуляторов оказывают влияние лишь на определенные звенья иммунитета, поэтому при роже часто назначают сочетание иммуномодуляторов [12,14,19,21,25,26]. М.А. Жаров отмечает высокую эффективность местного применения галавтилина, оказывающего регулирующее воздействие на моно-цитарно-макрофагальное звено. По мнению автора, препарат стимулирует микробицид-ную систему нейтрофилов, усиливая фагоцитоз и повышая неспецифическую резистентность организма к микробным агентам [11]. R.G. Kasseroller, F. Bruns и соавт. рекомендовали использование селенита натрия в лечении лимфедемы, а также при профилактике рецидивов рожи у пациентов с лимфедемой верхней конечности [41,46,47].
Также применяются различные иммунотропные средства — мети-лурацил, левамизол, нуклеинат натрия, тима-лин, тимоген, спленин, реаферон. Большинство иммуномодуляторов оказывают влияние лишь на определенные звенья иммунитета, поэтому при роже часто назначают сочетание иммуномодуляторов [12,14,19,21,25,26]. М.А. Жаров отмечает высокую эффективность местного применения галавтилина, оказывающего регулирующее воздействие на моно-цитарно-макрофагальное звено. По мнению автора, препарат стимулирует микробицид-ную систему нейтрофилов, усиливая фагоцитоз и повышая неспецифическую резистентность организма к микробным агентам [11]. R.G. Kasseroller, F. Bruns и соавт. рекомендовали использование селенита натрия в лечении лимфедемы, а также при профилактике рецидивов рожи у пациентов с лимфедемой верхней конечности [41,46,47].
Ряд авторов в качестве иммунотропной терапии в лечении больных рожей парентерально использовали раствор Лейкинферона [29]. А.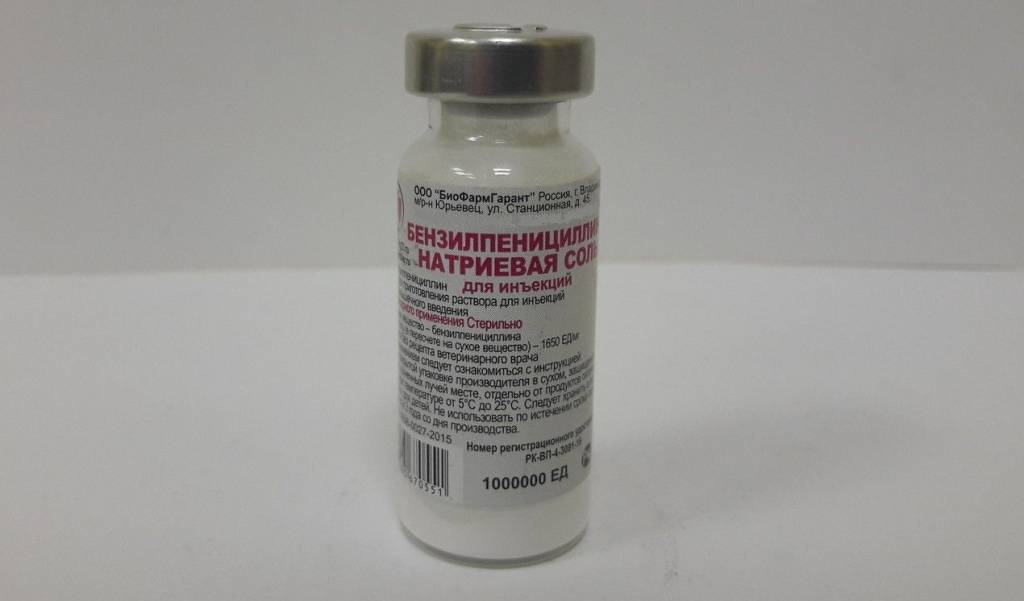 Н. Емельянова в лечении рожи использовала однократные капельные инфузии Рон-колейкина (рекомбинантного ИЛ-2) [8]. Ряд отечественных авторов в лечении рожи и лимфедемы нижних конечностей успешно использовали перфузат ксеноселезенки, который является сбалансированным природным комплексом цитокинов с провоспалительной активностью. Он содержит ИЛ-1, 2, 3, ФНО-а, гранулоцитарно-макрофагальный колоние-стимулирующий фактор (ГМ-КСФ), интерферон, опсонины, лейкотриены, пропердин, бактериолизин, лизоцим [5,18]. К.В. Малых, Л.И. Кутявин [19] использовали местные аппликации перфузата в терапии некротической и флегмонозной форм рожи. Л.В. Титова с соавт. отмечают высокую эффективность внут-риартериальных инъекций перфузата ксено-селезенки в бедренную артерию в комплексной терапии лимфедемы нижних конечностей [23]. Авторы выявили значительное уменьше-
Н. Емельянова в лечении рожи использовала однократные капельные инфузии Рон-колейкина (рекомбинантного ИЛ-2) [8]. Ряд отечественных авторов в лечении рожи и лимфедемы нижних конечностей успешно использовали перфузат ксеноселезенки, который является сбалансированным природным комплексом цитокинов с провоспалительной активностью. Он содержит ИЛ-1, 2, 3, ФНО-а, гранулоцитарно-макрофагальный колоние-стимулирующий фактор (ГМ-КСФ), интерферон, опсонины, лейкотриены, пропердин, бактериолизин, лизоцим [5,18]. К.В. Малых, Л.И. Кутявин [19] использовали местные аппликации перфузата в терапии некротической и флегмонозной форм рожи. Л.В. Титова с соавт. отмечают высокую эффективность внут-риартериальных инъекций перфузата ксено-селезенки в бедренную артерию в комплексной терапии лимфедемы нижних конечностей [23]. Авторы выявили значительное уменьше-
ние инфильтрации в стенке кровеносных и лимфатических сосудов, восстановление нарушений лимфо- и кровообращения, наблюдались быстрое и стойкое уменьшение отека пораженной конечности, увеличение продолжительности ремиссии. По мнению Васильевой Н.Г., свидетельством высокой эффективности метода непрямого эндолимфа-тического введения перфузата ксеноселезенки явились сокращение продолжительности острого периода заболевания (на 4-6 дней), сроков антибактериальной терапии (на 4-7 дней), предупреждение развития лимфостаза. Наиболее убедительным доказательством положительного эффекта цитокинотерапии явилось существенное улучшение отдаленных исходов заболевания: в течение 2-х лет наблюдения рецидивы развивались значительно меньше. Иммуномодулирующее воздействие цитокинов перфузата ксеноселезен-ки проявилось нормализацией уровня CD3+ и CD8+ и более частой в сравнении с общепринятым лечением регистрацией нормальных значений ИРИ, CD72+ и CD 16+-лимфоцитов, более полной реверсией нейтрофилов на макрофаги в «позднем кожном окне».
По мнению Васильевой Н.Г., свидетельством высокой эффективности метода непрямого эндолимфа-тического введения перфузата ксеноселезенки явились сокращение продолжительности острого периода заболевания (на 4-6 дней), сроков антибактериальной терапии (на 4-7 дней), предупреждение развития лимфостаза. Наиболее убедительным доказательством положительного эффекта цитокинотерапии явилось существенное улучшение отдаленных исходов заболевания: в течение 2-х лет наблюдения рецидивы развивались значительно меньше. Иммуномодулирующее воздействие цитокинов перфузата ксеноселезен-ки проявилось нормализацией уровня CD3+ и CD8+ и более частой в сравнении с общепринятым лечением регистрацией нормальных значений ИРИ, CD72+ и CD 16+-лимфоцитов, более полной реверсией нейтрофилов на макрофаги в «позднем кожном окне».
Сведения об авторах статьи: Хасанов Анвар Гиниятович — д.м.н., профессор, зав. кафедрой хирургических болезней ГБОУ ВПО БГМУ Минздрава России. Адрес: 450000, г. Уфа, ул. Ленина, 3. Тел./факс 8(347)264-16-19. Е-шай: [email protected]
Адрес: 450000, г. Уфа, ул. Ленина, 3. Тел./факс 8(347)264-16-19. Е-шай: [email protected]
Шайбаков Данис Габдинурович — к.м.н., доцент кафедры хирургических болезней ГБОУ ВПО БГМУ Минздрава России. Адрес: 450000, г. Уфа, ул. Ленина, 3. Тел./факс 8(347)264-16-19. Е-mail: [email protected]
ЛИТЕРАТУРА
1. Абузярова, Е. Н. Комплексное лечение рожи с использованием низкоинтенсивного инфракрасного лазерного излучения: авто-реф. дис…. канд. мед. наук. — М., 1999. — 23 с.
2. Амбалов Ю.М. [и др.]. Клинико-иммунологическая оценка эффективности непрямой эндолимфатической терапии бициллином-3 у больных рожей// Журнал микробиологии, эпидемиологии и иммунобиологии. — 1993. — № 6. — С. 114-115.
3. Белов, Б.С. Современные аспекты А-стрептококковых инфекций// Инфекции и антимикробная терапия. — 2001. — N° 4. — С. 104108.
— 2001. — N° 4. — С. 104108.
4. Белов, Б.С. Острая ревматическая лихорадка: проблемы и перспективы// Вестник РАМН. — 2003. — № 7. — С. 39-41.
5. Васильева, Н.Г. Эффективность метода непрямого эндолимфатического применения перфузата ксеноселезенки в лечении рожи: автореф. дисс. …канд. мед. наук. — Новосибирск, 2006. — 19 с.
6. Герман, К.М. Оценка эффективности эндолимфатического введения антибиотиков при роже // Материалы съезда врачей-инфекционистов. — Суздаль, 1992. — С. 266-267.
7. Долгош С.С. Л. Петнегази Д.С., Шарапа И.П. Лимфотропная антибиотикотерапия рожистого воспаления// Клиническая хирургия. — 1989. — № 1. — С. 65-66.
8. Емельянова, А. Н. Влияние биорегулирующей терапии на состояние иммунитета и гемостаза при рожистом воспалении: автореф. дис…. канд. мед. наук. — Чита, 1999. — 18 с.
дис…. канд. мед. наук. — Чита, 1999. — 18 с.
9. Еровиченков, А.А. Современные аспекты терапии рожи// Клиническая фармакология и терапия. — 2005. — № 2. — С.73-77.
10. Ермолов, А.С. Эндолимфатическая антибиотикотерапия рожи нижних конечностей// Советская медицина. — 1989. — № 8. — С. 95-99.
11. Жаров, М. А. Клинико-лабораторная характеристика и эффективность лечения рожи с применением галавтилина: автореф. дис…. канд. мед. наук. — М., 2003. — 20 с.
12. Краснова, Е.И. Патогенетические подходы к прогнозированию вариантов течения рожи и совершенствованию ее терапии: автореф. дис…. д-ра мед. наук. — Томск, 1997. — 38 с.
13. Краснова, Е.И. Клинико-иммунологическая характеристика рожи при применении различных методов этиотропной терапии: автореф. дис…. канд. мед. наук. — Новосибирск. — 1987. — 19 с.
дис…. канд. мед. наук. — Новосибирск. — 1987. — 19 с.
14. Краснова, Е.И. Современные аспекты лечения и профилактики рожи// Журнал инфекционной патологии. — 1999. — № 2 — 3 (6). -С. 128-132.
15. Королев, М. П. Комплексное лечение больных с осложненными формами рожи// Вестник хирургии. — 2000. — Т. 159. — № 4. — С. 64-69.
16. Левина, Л.Д. [и др.]. Влияние непрямой эндолимфатической антибиотикотерапии на клинические и иммунологические показатели у больных рожей нижних конечностей Антибиотики и химиотерапия. — 1992. — № 6. — С. 24-26.
17. Левин, Ю.М. Основы лечебной лимфологии. — М.: Медицина, 1986. — 287 с.
18. Любарский, М.С. [и др.]. Непрямые лимфостимулирующие блокады и внутриартериальные введения ксеноперфузата в комплексном лечении лимфедемы нижних конечностей. Эфферентная и иммунокорригирующая терапия в клинической практике// Материалы III Всероссийской научно-практической конференции. — Ижевск, 1998. — С. 134-136.
Эфферентная и иммунокорригирующая терапия в клинической практике// Материалы III Всероссийской научно-практической конференции. — Ижевск, 1998. — С. 134-136.
Таким образом, несмотря на определенные успехи в лечении рожи, многие аспекты патогенеза остаются еще не до конца изученными. В настоящее время отсутствует единая концепция этиотропной терапии рожи. Нет общей точки зрения в отношении профилактического использования антибактериальных препаратов, хотя, исходя из особенностей возбудителя и патогенеза заболевания, факт его нецелесообразности является совершенно очевидным. Большинством авторов признается необходимость этиотропной терапии в остром периоде заболевания. Назначение современных способов антибактериальной терапии предотвращает развитие тяжелых форм и осложнений, однако эти способы малоэффективны в отношении рецидивов болезни.
Рецидивирующее течение рожи отмечается более чем у трети пациентов. Исходя из вышесказанного, следует отметить, что главные усилия в лечении рожи должны быть направлены на полную эрадикацию возбудителя в острой фазе заболевания и на восстановление нарушений иммунного гомеостаза в организме в целом.
Исходя из вышесказанного, следует отметить, что главные усилия в лечении рожи должны быть направлены на полную эрадикацию возбудителя в острой фазе заболевания и на восстановление нарушений иммунного гомеостаза в организме в целом.
19. Малых К. В. Лечение осложненных форм рожистого воспаления нижних конечностей. Эфферентная и иммунокорригирующая терапия в клинической практике // Материалы III Всероссийской научно-практической конференции. — Ижевск, 1998. — С. 137139.
20. Малютина, М.К. Оценка клинической эффективности лазеротерапии больных рожей // Материалы съезда врачей-инфекционистов. — Суздаль, 1992. — Т. 2. — С. 247-248.
21. Навасардян, А. С. Оптимизация комплексного лечения больных с рожистым воспалением на госпитальном этапе: автореф. дис…. канд. мед. наук. — Самара, 2000. — 23 с.
22. Навашин, СМ. Рифампицин в современной химиотерапии бактериальных инфекций// Антибиотики и химиотерапия. -1992. -Т. 37. — № 6. — С. 41-48.
Навашин, СМ. Рифампицин в современной химиотерапии бактериальных инфекций// Антибиотики и химиотерапия. -1992. -Т. 37. — № 6. — С. 41-48.
23. Титова, Л. В. Применение препаратов ксеноселезенки в комплексном лечении лимфедемы нижних конечностей// Проблемы лимфологии и эндоэкологии: материалы межд. симпозиума НИИ клинической и экспериментальной лимфологии СО РАМН. -Новосибирск, 1998. — 271 с.
24. Тотолян А.А., Малеев В.В. Современные проблемы стрептококковой инфекции// Журнал микробиологии, эпидемиологии и иммунобиологии. — 1996. — № 2. — С. 117-120.
25. Фролов, В.М. Патогенез и диагностика рожистой инфекции. — Воронеж: Изд-во ВГУ, 1986. — 160 с.
26. Фролов, В.М. Иммуномодулирующий эффект нуклеината натрия и спленина.
27. Хасанов А. Г., Нуртдинов М.А., Ибрагимов Р.К. Возможности совершенствования хирургического лечения рожистого воспаления// Медицинский вестник Башкортостана. — 2009. — № 3. — С. 46-49.
Г., Нуртдинов М.А., Ибрагимов Р.К. Возможности совершенствования хирургического лечения рожистого воспаления// Медицинский вестник Башкортостана. — 2009. — № 3. — С. 46-49.
28. Хасанов А.Г., Шайбаков Д.Г., Суфияров И.Ф. Способ лечения рожистого воспаления: патент РФ № 2317085 от 20.02.08.
29. Черкасов, В.Л. [и др.]. Опыт применения лейкинферона в лечении и предупреждении рецидивов рожи// Материалы съезда врачей-инфекционистов. — Суздаль, 1992. — Т. 2. — С. 270-272.
30. Черкасов, В.Л. Лазеротерапия геморрагических форм рожи и ее влияние на некоторые показатели гемостаза// Эпидемиология и инфекционные болезни. — 1998. — № 6. — С. 44-47.
31. Черкасов, В. Л. Рожа. — М.: Медицина, 1986. — 199 с.
32. Шляпников, С.А. Рожистое воспаление: взгляд на нестареющую проблему// Вестник хирургии. — 2004. — № 4. — С. 71-74.
— 2004. — № 4. — С. 71-74.
33. Amal S. et al., Epidemiology, clinical features, and evolution of Erysipelas in the Marrakech region (100 cases).Med. Mai. Infect. 2004; Vol. 34, 4: p.l71-176.
34. Allard P. et al. Cyclical intravenous antibiosis as an effective therapy concept in chronic recurrent erysipelas.Hautarzt. 1999; Vol. 50, 1:p. 34-38.
35. Becq-Giraudon B. Primary and secondary prevention for erysipelas.Ann. Dermatol. Venereol. 2001; Vol. 128, 3:pt. 2. p. 368-375.
36. Bergkvist P. I. Antibiotic and prednisolone therapy of erysipelas: a randomized, double blind, placebo-controlled study.Scand. J. Infect. Dis. 1997; Vol. 29, 4:p. 377-382.
37. Bergkvist P.I. Relapse of erysipelas following treatment with prednisolone or placebo in addition to antibiotics: a 1-year follow-up. Scand J Infect Dis. 1998;Vol. 30, 2: p. 206-207.
Scand J Infect Dis. 1998;Vol. 30, 2: p. 206-207.
38. Bernard P. Primary and secondary hospitalization criteria. Ann. Dermatol. Venereol. 2001; Vol. 128, 3: pt 2. p. 363-367.
39. Bishara J. Antibiotic use in patients with erysipelas: a retrospective study Isr. Med. Assoc. J. 2001; Vol. 3, № 10: р. 722-724.
40. Bonnetblanc J.M. Bedane C. Erysipelas: recognition and management Am J. Clin. Dermatol. 2003;Vol. 4, 3: p. 157-163.
41. Bruns F. l Selenium in the treatment of head and neck lymphedema. Med. Princ. Pract. 2004; Vol. 13, 4: p. 185-190.
42. Estines O. et al. Haemorrhagic cellulitis: three cases. Ann. Dermatol. Venereol. 2003;Vol. 130, 5:р. 523-526.
43. Granier F. Management of erysipelas. Ann. Dermatol. Venereol. 2001; Vol. 128, 3:pt 2. p. 429-442.
Ann. Dermatol. Venereol. 2001; Vol. 128, 3:pt 2. p. 429-442.
44. Grosshans E. Erysipelas. Clinicopathological classification and terminol Ogy. Ann. Dermatol. Venereol. 2001; Vol. 128 3: р. 307-311. 317. Haustein U.F.Treatment of chronic recurrent erysipelas with streptococcal vaccine. Hautarzt. 1989;Vol. 40, 4: p. 215-221.
45. Jegou J. Hospitalization criteria for erysipelas: prospective study in 145 cases Ann. Dermatol. Venereol. 2002; Vol. 129, 4: pt. 1. p. 375377.
46. Kasseroller R. Sodium selenite as prophylaxis against erysipelas in secondary lymphedema. Anticancer Res. 1998;Vol. 18, 3: p. 22272230.
47. Kasseroller R. G. Schrauzer G. N. Treatment of secondary lymphedema of the arm with physical decongestive therapy and sodium selenite: a review Am. J. Ther. 2000; Vol. 7, 4: p. 73-279.
73-279.
48. Li H. B, Chen F. Preparative isolation and purification of phillyrin from the medicinal plant Forsythia suspensa by high-speed counter-current chromatography. J. Chromatogr A. 2005; Vol. 1083, 1-2: p. 102-105.
49. Kujala P. Use of oral cephalosporins. Duodecim. 1999;Vol. 115, 20:p. 2241-2247.
50. Lucht F. Which treatment for erysipelas? Antibiotic treatment: drugs and methods of administering. Ann. Dermatol. Venereol. 2001; Vol. 128, 3:pt. 2.p. 345-347.
51. Mahe A. et al. Deep venous thromboses in erysipelas of the leg. A prospective study of 40 cases Presse. Med. 1992;Vol. 21, 22: p. 10221024.
52. Martin S. J., Zeigler D. G. The use of fluoroquinolones in the treatment of skin infections. Expert. Opin. Pharmacother. 2004;Vol. 5, 2:p. 237-246.
2004;Vol. 5, 2:p. 237-246.
53. Nielsen H.U. et al. Beta-hemolytic streptococcal bacteremia: a review of 241 cases. Scand. J. Infect. Dis. 2002;Vol. 34, 7:р. 483-486.
54. Perrot J. L. Is anticoagulant therapy useful when treating erysipelas? Ann. Dermatol. Venereol. 2001; Vol. 128, 3:pt. 2. p. 352-357.
55. Potel G. Value of Synercid in clinical practice: from temporary approval to clinical trial authorization. Presse Med. 2001; Vol. 30, 25, pt. 2 p. 19-22.
56. Rosskopf-Streicher U. Potency testing of inactivated erysipelas vaccines by ELISA-infruence of the adjuvant on antibody develop-ment.Dev. Biol. Basel, 2002; Vol. 111. p. 159-162.
57. Sauer J., Weyer T, Seifert A. Mitigated erysipelas after implantation of foreign material. Zentralbl. Chir. 2004; Vol. 129, 3:p. 220-224.
Zentralbl. Chir. 2004; Vol. 129, 3:p. 220-224.
58. Schmit J. L. A prospective study on erysipelas and infectious cellulitis: how are they dealt within hospital? Ann. Dermatol. Venere-ol.2001; Vol. 128, 3: pt. 2, р. 334-337.
59. Sjoblom A. С. Antibiotic prophylaxis in recurrent erysipelas Infection. 1993; Vol. 21: 6. p. 390-393
Рожистое воспаление (рожа): лечение, симптомы и диагностика
Рожистое воспаление либо просто рожа — это инфекционно-аллергическая болезнь, которая затрагивает кожу и подкожную клетчатку. Заболевание довольно распространено и склонно к рецидивам. Оно занимает четвертое место среди всех инфекционных болезней, а также все чаще встречается с течением времени. Так, за последние двадцать лет количество рецидивов этой болезни увеличилось на 25%. Более того, все чаще встречается тяжелая форма заболевания — теперь это около 80% случаев, хотя еще 50-60 лет назад тяжелую форму ставили лишь 30 процентам пациентов.
Группы риска
Чаще всего такому заболеванию подвержены женщины в возрасте от 50 лет, но оно может встречаться и у младенцев. В их случае заражение происходит после попадания стрептококка в ранку пупочной области. Нет никаких объяснений этому факту, но люди с III группой крови страдают от рожи чаще. Также есть связь с местом проживания. В Южной Азии, а также в Африке это заболевание встречается очень редко.
В зоне риска находятся люди с низким уровнем иммунитета, ослабленные болезнями, стрессами, лечением и другими факторами.
Симптомы
Заметить первые симптомы болезни рожа можно на разных частях тела: ногах, руках, лице, туловище, промежности. Причем многое будет зависеть от того, как именно развивается болезнь. Например, воспаление на лице может локализоваться вокруг глазницы, возле ушной раковины, на волосистой части головы и шеи. Если болезнь начинается с носа, может развиться поражение по типу бабочки — с выходом на щеки. Параллельно возникает отек, который искажает размеры тканей. То же самое касается всех остальных органов — локализация заболевания разная и зависит от ситуации.
Параллельно возникает отек, который искажает размеры тканей. То же самое касается всех остальных органов — локализация заболевания разная и зависит от ситуации.
Симптомы рожи делятся на общие и локальные. К общим относятся такие моменты:
- Озноб, лихорадка. Часто пациентов сильно трясет.
- Высокая температура, вплоть до 40 градусов. Она может держаться до десяти дней.
- Судороги, помутнение сознания, бред.
- Очень сильная слабость, головокружения.
- Тошнота, нередко рвота.
- Боли в мышцах и суставах.
Иными словами, наблюдаются симптомы общего отравления организма.
Локальные симптомы рожи выглядят так:
- Покраснение кожи в месте поражения. Обычно изменения заметны через десять-двадцать часов после того, как начались патологические процессы.
- Отечность, припухлость, боль в том месте, где кожа приподнимается.
 Также участок кожи на ощупь становится более теплым, даже горячим. Больной может чувствовать жжение и ощущение, будто кожу изнутри что-то распирает.
Также участок кожи на ощупь становится более теплым, даже горячим. Больной может чувствовать жжение и ощущение, будто кожу изнутри что-то распирает. - Быстрый рост воспаления, поскольку стрептококки довольно активно размножаются. Края мест поражения неровные, они постоянно меняются по мере роста.
- Увеличение близкорасположенных лимфатических узлов, так как возбудитель распространяется по лимфатической системе.
- Пузыри с прозрачной жидкостью. Сразу они маленькие, но потом растут и объединяются между собой. Такой признак есть не всегда.
- Кровоизлияния. Если не помочь пациенту в первое время, пойдут осложнения, среди которых и повреждения кровеносных сосудов, кровь которых выходит в межклеточное пространство.
- Пузыри с кровью, гноем в окружении участков кровоизлияний. Классификация рожи предполагает разные степени развития болезни — и эти проявления свойственны уже для осложненных форм.
Чем запущеннее ситуация, тем выше риски того, что даже после успешного лечения наступит рецидив. Нередко заболевание возникает на том же месте, что и в первый раз.
Нередко заболевание возникает на том же месте, что и в первый раз.
Причины
Рожистое воспаление вызывается стрептококками — а точнее, одной из разновидностей бактерий данной группы. В организме с ослабленным иммунитетом стрептококк способен вызывать и другие заболевания — например, скарлатину, миокардит, ангину.
Около 15% людей планеты являются носителями стрептококка. То есть их иммунитет довольно сильный, чтобы не заболеть, но при этом они распространяют инфекцию. Она передается через личные контакты, бытовые предметы, воздушно-капельным путем и т. д.
Предрасполагающие факторы для заражения:
- Разные повреждения кожи, включая укусы насекомых, животных, пролежни и язвы. Даже венозные катетеры могут быть в этом смысле опасными.
- Вредные условия работы — когда кожа постоянно подвергается воздействию химических веществ, часто загрязняется. В зоне риска также люди, которые постоянно носят резиновую одежду, обувь.
- Повреждения кожи вирусного характера — ветрянка, опоясывающий лишай, герпес. Они не только нарушают целостность покровов, но и сильно снижают иммунитет.
- Хронические поражения кожи вроде экземы, атопического дерматита, псориаза и т. д.
- Гнойные поражения кожных покровов: фурункул, карбункул и подобные образования.
- Нарушения в системе кровообращения — варикозное расширение вен, тромбофлебит. Если кожа получает кислородное голодание, то она повреждается и становится более восприимчивой к заражению.
- Разные рубцы, клетки которых сам организм может атаковать, из-за чего развивается рожа.
- Грибковые заболевания кожи головы, стоп.
- Серьезные осложнения при рините, отите, конъюнктивите.
- Травмы на коже, вызванные ношением тесной одежды, которая натирает и нарушает процесс кровообращения в тканях.
- Любые причины, угнетающие иммунитет: прием определенных лекарств, серьезные заболевания, истощение в результате недоедания, переохлаждение, вредные привычки, хронический или сильный стресс и многое другое.

Если обобщить, то болезнь развивается на фоне ослабленного иммунитета и заражения стрептококком, которое может произойти разными путями.
Диагностика
Если возникли первые признаки болезни рожа, необходимо обратиться к дерматологу либо терапевту. В зависимости от степени проблемы может потребоваться помощь и таких специалистов, как иммунолог, хирург, инфекционист.
Диагностика заболевания включает опрос пациента, а также его тщательный осмотр. Затем назначаются анализы на уровень Т-лимфоцитов, СОЭ, количество нейтрофилов (это все выясняется через анализ крови).
Факультативно назначается бактериологическое исследование для определения возбудителя — у врачей нет единого мнения по поводу целесообразности такого обследования.
Лечение
В случае развития рожи на ноге, руке или другой части тела, подход всегда будет комплексным — одного местного лечения просто недостаточно. Более того, упор во многом делается на повышение иммунитета, иначе риски того, что болезнь повторится, очень высоки. Для работы с иммунитетом используются специальные препараты, но пациенту важно поменять образ жизни: хорошо отдыхать, тщательно следить за своим здоровьем, правильно питаться, исключить негативные факторы.
При лечении рожистого воспаления используются антибиотики, а также антибактериальные препараты других групп. Лекарственная терапия подбирается индивидуально — самостоятельно назначать себе лекарства нельзя ни в коем случае.
Вместе с приемом медикаментов необходимо обрабатывать пораженную кожу: специальными растворами, присыпками, аэрозолями. А мази, которые люди так любят назначать себе сами — синтомициновая, ихтиоловая, Вишневского — в этом случае категорически запрещены, поскольку они могут спровоцировать осложнения и стать причиной развития абсцесса. Ни в каком виде не допускается и применение народной медицины — при лечении рожистого воспаления это крайне опасно!
С пациентами обязательно проводится профилактическая беседа относительно нюансов гигиены во время лечения. Так, ежедневно нужно менять постельное белье, заботиться о доступе воздуха к пораженному участку, регулярно принимать душ в теплой, очень комфортной воде. Кожу нельзя вытирать — только пропитывать бумажными полотенцами.
При роже используются и физиотерапевтические методы: УФО, магнитотерапия, УВЧ, электрофорез, определенные виды лазеротерапии, аппликации с теплым парафином. На каждом этапе лечения назначаются свои процедуры, причем подбираются они индивидуально — под каждого пациента и его состояние. Здесь также неуместна никакая самодеятельность, иначе можно навредить здоровью.
При очень серьезных осложнениях требуется хирургическое лечение.
Если вы столкнулись с такой проблемой, мы рекомендуем немедленно обратиться в клинику АО «Медицина». Мы находимся в Москве и располагаем большим штатом профессиональных дерматологов, терапевтов и других специалистов, которые могут вам помочь. А современные условия для диагностики и лечения помогут добиться результатов гораздо быстрее.
Если врачи вовремя возьмутся за лечение, а пациент будет соблюдать все рекомендации, болезнь можно вылечить в течение 10-14 дней.
Профилактика
Поскольку заболевание может коснуться каждого, профилактика рожи важна и для тех, кто уже однажды переболел, и для тех, кто только слышал о подобной болезни.
Профилактика заключается в соблюдении следующих советов:
- Своевременно лечите любые воспаления на коже, слизистых.
- Соблюдайте личную гигиену. В том случае, если работа или образ жизни связаны с дополнительными загрязнениями, гигиена должна быть еще более тщательной, но не чрезмерной, чтобы кожа не страдала — иначе эффект будет обратным.
- Используйте для мытья специальные средства (гели и масла), которые не сушат кожу. Обычное мыло для регулярного использования не походит.
- Тщательно следите за состоянием кожи в жару или в том случае, если у вас есть складки, которые постоянно потеют. В таком случае необходимо использовать специальные присыпки.
- Усиленно следите за здоровьем, если наблюдаются проблемы с сосудами, застоем лимфы. Таким людям показаны массажи и разные процедуры, разгоняющие жидкости в организме.
- Сразу же лечите кожу, если вы ее обморозили, обветрили или обожгли на солнце.
- Носите комфортную, дышащую, по возможности натуральную одежду, которая свободно сидит на теле.
- Тщательно следите за иммунитетом и устраняйте все факторы, которые могут его ослабить.
Помните, что от этой болезни нельзя застраховаться, но можно сделать все, чтобы снизить риски ее возникновения.
Вопросы-ответы
Как выглядит рожа?
Как правило, как красный, припухший участок кожи — в зависимости от вида и степени болезни он может покрываться пузырями с жидкостью, кровью или гноем.
Заразна ли рожа на ноге для окружающих?
Если у кого-то из окружающих сниженный иммунитет, есть риски заражения стрептококковой инфекцией. Но она необязательно вызовет такое же заболевание — этот же возбудитель становится причиной многих других неприятных болезней. По этой причине воспаления на ногах и руках рекомендуется прикрывать стерильной повязкой и соблюдать элементарные правила гигиены.
Как лечится рожа?
Рожа всегда лечится комплексно. Для этого нужны медикаменты, методы физиотерапии, иногда хирургическое вмешательство. Но в любой ситуации ставка также будет сделана на повышение иммунитета.
Рожа свиней: симптомы, лечение болезни, профилактика
Заболевание, вызванное бактериями Erysipelothrix insidiosa, относят к наиболее распространенным у свиней. Поражает кожу поросят и способно нанести существенный экономический урон хозяйствам и компаниям. Чаще всего рожу у свиней диагностируют в возрасте до года. Основное проявление — сепсис, который приводит к воспалению и дистрофическим процессам в тканях. При остром течении и отсутствии ветеринарной помощи возможен летальный исход.
Факторы риска и причины
До 3 месяцев особи обычно не болеют, а у взрослых животных вырабатывается резистентность либо они при заражении переболевают бессимптомно. Рожа у поросят появляется в 3–12-месячном возрасте. Болезнь поражает особей со слабым, несформированным иммунитетом. Также к факторам риска относят:
- неполноценное кормление;
- частые перепады температуры и влажности;
- нарушения санитарного режима в помещениях.
Пик заболевания рожей у свиней приходится на теплый весенний, летний, осенний период. Основной источник бактерий — почва. Также возможно заражение инфицированными предметами ухода. Бактерии могут попасть в хозяйство с зараженными особями. Их переносят насекомые, птицы и грызуны.
Что происходит в организме
Если заражение происходит с кормом или питьем, бактерии оседают на миндалинах. Если при контакте с почвой, то инфекция концентрируется на коже в местах, где она повреждена.
У поросят бактерии легко попадают в кровь, печень, селезенку, где активно размножаются. Продукты их жизнедеятельности вызывают интоксикацию и воспаление в тканях органов. В местах скопления инфекции образуются отеки, тромбы. В тканях нарушается обмен веществ.
При остром течении важно своевременно начать лечение рожи свиней, так как при глубоком поражении тканей возможен летальный исход.
Как проявляется рожа у свиней
Возможно подострое развитие — в течение более 7 дней. В этих случаях можно заметить гиперемию тканей и местные воспалительные процессы. Они могут проявляться:
- пятнами, похожими на ромбы;
- артритом;
- повышением температуры тела до 41 °С и выше, слабостью, снижением аппетита и повышенной жаждой, запором, конъюнктивитом.
Чаще всего заболевают молодые особи, и болезнь у них протекает в острой форме (2–5 дней). В данном случае основные симптомы рожи у свиней следующие.
- 1-е сутки. Особи становятся вялыми, слабеют, мало двигаются, отказываются от пищи. При передвижении можно заметить ходульную напряженную походку. Температура повышается до 42 оС, возможен озноб. Заболевшие поросята лежат отдельно от основной группы.
- 2–3-е сутки. На шее, боках, спине заметны ромбовидные пятна, которые в начале болезни светло-розовые, а затем краснеют и становятся плотными, припухлыми. Увеличиваются лимфоузлы. Возникает гипертермия, отек легких, одышка, сердечная недостаточность. Пульс учащается до 100 уд/мин.
- 4–5-е сутки. При отсутствии адекватного лечения рожи примерно у половины свиней наблюдается летальный исход из-за значительного некроза тканей, нарушения дыхательной и сердечной деятельности. Также возможен переход болезни в хроническую форму, сопровождающейся поражением сердца (рожистый эндокардит), суставов и некрозом кожи.
Диагностика
Заболевание имеет явные клинические признаки, поэтому для его определения опытному ветеринару достаточно визуального осмотра животных. Диагноз подтверждают в ходе бактериологического анализа в лаборатории, а также при патологоанатомическом исследовании.
Чем и как лечить рожу у свиней
Терапевтические меры следует применять при первых признаках и поставленном диагнозе. При выборе препарата рекомендуем обратить внимание на продукцию российской компании NITA-FARM — ветеринарный антибиотик нового поколения «Азитронит». Уже через 10–12 часов после введения состояние животных может улучшиться. При научных исследованиях на 700 головах препарат показал высокую эффективность.
Действующее вещество — азитромицин. У него широкий спектр антибактериального действия (действует против более чем 30 патогенов). Эффективен он, в том числе, и против Erysipelothrix insidiosa, что доказано при практических исследованиях. Вещество подавляет синтез белка, что останавливает жизнедеятельность бактерий и приводит к их гибели. При этом препарат абсолютно безопасен для организма животных.
Курс «Азитронита» при роже свиней состоит из 2 введений с периодом 24 часа. Препарат вводят внутримышечно в дозе 1 мл/20 кг веса. Действие начинается уже через полчаса. В тяжелых случаях производитель рекомендует повторить инъекцию спустя 24 часа.
Дополнительная терапия
Для быстрого выздоровления и реабилитации после болезни оптимально стимулировать формирование иммунитета у поросят. Для этого компания NITA-FARM рекомендует витамины для свиней, например «Бутофан» — на основе бутафосфана и цианокобаламина (B₁₂). Его применение способствует:
- сокращению реабилитационного периода;
- повышению обменных процессов;
- быстрому возвращению к нормальным показателям роста, продуктивности.
«Бутофан» применяют в течение 4–5 суток в форме внутримышечной инъекции 1 раз в сутки. Суточная доза — 1–2,5 мл на животное (в зависимости от веса и возраста).
список препаратов, состав, инструкции по применению, показания и противопоказания, дозировки
Рожистое воспаление — это проблема, с которой может столкнуться любой человек. Данное заболевание имеет статус рецидивного и может проявляться в любом возрасте.
Мировая статистика показывает, что болезнь очень распространена и занимает четвертое место после гепатита, кишечных, а также респираторных проблем. Наблюдаемая специалистами тенденция ничуть не радует: за последние 20 лет частота проявления рожистого воспаления выросла на 25 %. Что касается смертности, то рассматриваемая проблема становится причиной ухода из жизни всего лишь 5 % всех больных.
Для борьбы с рассматриваемым заболеванием специалисты в области медицины чаще всего используют антибиотики. Рассмотрим далее перечень наиболее популярных и действенных из них, а также рекомендуемые дозировки.
Основные группы антибиотиков
При роже специалисты в области медицины рекомендуют своим пациентам антибиотики, отнесенные к четырем основным группам: пенициллины, макролиды, тетрациклины и левомицетины. Лекарства, отнесенные к каждой из них, выполняют определенные действия с белком, содержащимся в организме, который в процессе воспаления направлен на образование новых клеток бактерий.
Что касается формы выпуска препаратов, то они могут быть представлены в виде таблеток, капсул, а также растворов для введения инъекций.
Пенициллины
Наиболее распространенной группой антибиотиков, какими лечат рожу, являются пенициллиновые. Средства данного типа могут быть представлены как в виде драже (таблеток), так и в виде растворов для инъекций в капсулах.
Препараты, содержащие пенициллин, попадая в организм, начинают свое взаимодействие с ферментами, из которых состоит клеточная оболочка, в результате чего происходит не только разрушение клетки, но и гибель самого микроорганизма, вызывающего воспаление. Специалисты в области медицины, как правило, назначают данное средство в тех случаях, когда причиной заболевания является бактерия, имеющая свойство роста и размножения. Опытным путем было установлено, что лечение пенициллином становится более эффективным в том случае, когда он используется в сочетании со «Стрептоцидом» или «Фуразолидоном».
Наиболее часто используемым при роже антибиотиками являются «Бензилпенициллин», «Бициллин-5» и «Феноксиметилпенициллин». Первый вариант препарата представлен в виде растворов для инъекций, которые должны вводиться в пораженный участок дважды в день, по 250 000-500 000 ЕД. Продолжительность лечения таким способом может составить до месяца. В такой же форме представлен и «Бициллин-5». Инъекции с данным составом делаются очень редко — раз в месяц, но в течение пары лет. Использование данного лекарственного средства осуществляется для предотвращения возможных рецидивов. Что касается «Феноксиметилпенициллина», то данный препарат предлагается пациентам как в виде сиропа, так и в таблетках. Процесс лечения рожи антибиотиком такого типа должен производиться в течение недели, если заболевание находится на начальном этапе, и около 10 дней, если оно уже начало прогрессировать.
Тетрациклины
Следует отметить, что пенициллиновые антибиотики при роже являются классическим препаратом. Все остальные средства могут назначаться только в том случае, если организм пациента имеет индивидуальную непереносимость пенициллина.
Особенность действия тетрациклинов состоит в том, что указанные компоненты направлены на торможение процесса синтеза белка, который требуется для построения новых клеток бактерий.
Наиболее известным и эффективным препаратом с содержанием тетрациклинов является «Доксициклин». Данное средство представлено в виде драже, которые необходимо употреблять дважды в сутки после еды, запивая водой.
Левомицетины
Какие антибиотики при роже используют для лечения заболевания специалисты в области медицины? При условии индивидуальной непереносимости пенициллина таковыми являются левомицетины, которые замедляют рост количества стрептококков в организме человека, действуя методом, аналогичным тетрациклинам.
Чем лечить рожу? Антибиотики левомицетины представлены в таблетках с одноименным названием. Их необходимо принимать трижды в день, по 250 мг. Общая продолжительность курса лечения данным препаратом составляет 1-2 недели, что зависит от масштабов воспаления.
Макролиды
Что касается особенностей действий препаратов данной серии, то она заключается в полном подавлении активности болезнетворных бактерий в организме человека, в результате чего она полностью стихает, и микроорганизмы начинают погибать. Однако второй эффект возможен только в том случае, если доктор назначает высокую дозу препарата.
Какие антибиотики принимать при роже? Наиболее известным препаратом из серии макролидов является «Эритромицин», который представлен в форме таблеток, предназначенных для перорального приема (по 1/4 г, 4-5 раз в сутки, за час до приема пищи).
Наиболее популярные лекарства
Существует определенный перечень лекарств, которые признаются наиболее эффективными в борьбе с воспалением кожи, именуемым рожей. К числу таковых относятся «Линезолид», «Кубицин» и «Олететрин». Рассмотрим далее более детально каждый из них.
Что касается «Линезолида», то данное средство относится к группе синтетических препаратов, которые имеют особенный механизм действия, заключающийся не только в синтезе белка, но еще и в нарушении процесса образования отдельного комплекса, который впоследствии может предаться будущим поколениям. Отлично помогает данный антибиотик при роже на ноге, эффективность его действия особенно заметна тогда, когда воспаление имеет довольно крупные масштабы. Что касается дозирования, то данное средство необходимо принимать в количестве 600 мг за раз, дважды в день.
«Кубицин» — это еще одно средство нового поколения, которое с самого момента своего появления на рынке фармакологии привлекло внимание специалистов в области медицины, занимающихся лечением рожи и кожных воспалений иного типа. Данное средство обрело свою популярность благодаря моментальному бактерицидному эффекту, который наблюдается уже в первые часы после применения. Рассматриваемый препарат выпускается исключительно в форме растворов, которые необходимо вводить в мышцу с помощью иглы. Курс лечения данным лекарством составляет не более пары недель. Суточная доза препарата для взрослого индивидуума должна быть рассчитана индивидуально — 4 мг вещества на килограмм массы тела.
С помощью каких антибиотиков рожа на ноге устраняется быстрее всего? К числу таковых относится «Олететрин» — вещество, которое обладает бактериостатическим свойством. По своему составу он представляет смесь олеандомицина, тетрациклина и макролида — такие составляющие отлично подходят для тех лиц, которым свойственна индивидуальная непереносимость пенициллина. Лекарство выпускается в форме таблеток, имеющих различную дозировку. Принимать средство необходимо 4 раза в день, по 250 мг (для взрослого человека).
Несмотря на широкое разнообразие лекарственных средств, которые помогают бороться с проблемой, тот антибиотик, с каким лечение рожи окажется наиболее эффективным, должен подбирать именно специалист в области медицины и исключительно после проведения предварительного обследования.
Показания к применению антибиотиков
Какие антибиотики при роже пить можно, а какие нет — это должен определить лечащий доктор. Для этого он проводит осмотр и изучает личную медицинскую карту пациента, а также состояние самого воспаления.
Существуют определенные ситуации, которые выступают прямыми показателями к использованию антибиотиков при роже в процессе лечения. К таковым случаям относятся: диагноз развитого рожистого воспаления, а также отсутствие положительных результатов после проведения лечения другими методами и средствами.
Сочетание с другими препаратами
Для того чтобы более эффективно бороться с возникшей проблемой, практически все специалисты в области медицины назначают своим пациентам комплексное лечение, которое представляет собой употребление антибиотиков в сочетании с другими препаратами. Как правило, в числе таковых встречаются противоаллергические средства, из которых наиболее популярными считаются «Тавегил», «Диазолин» и «Супрастин». Курс лечения антибиотиками в сочетании с лекарствами указанного типа должен продолжаться около 7-10 дней, каждые сутки следует принимать 1-2 таблетки, в зависимости об общих особенностей организма человека. Как правило, в ходе такого лечения у больного проходит болезненная отечность, а также пропадает аллергическая реакция.
Нередко курс лечения антибиотиками сочетают с употреблением препаратов-сульфаниламидов и нитрофуранов. В результате такого сочетания в организме человека нарушатся процессы образования бактерий, развивающих отечность.
Нередко специалисты в области медицины назначают своим пациентам различные биостимуляторы — вещества, которые способствуют укреплению иммунитета. В некоторых случаях больным назначаются глюкокортикоиды — данные компоненты, по мнению многих докторов, наоборот, губительным образом воздействуют на иммунную систему организма человека, хотя и обладают прекрасным противоаллергенным эффектом. Оптимальным решением проблемы многие специалисты в области медицины считают курс, состоящий из антибиотиков и поливитаминов, которые восполняют витаминный запас в тяжелый для организма период.
Некоторые курсы лечения предусматривают сочетание употребления антибиотиков и введения инъекций ферменов тимуса и протеолитических ферментов. Такие методики лечения активизируют питание тканей мышц и улучшают рассасывание инфильтрата.
Обработка кожи
В процессе лечения болезни рожа антибиотики оказывают положительный эффект. Однако следует понимать, что внутреннего лечения проблемы недостаточно для того, чтобы получить желаемый эффект максимально быстро. Для этого необходимо применять и некоторые внешние воздействия. Курс лечения заболевания предусматривает использование некоторых компрессов с различными полезными для кожи растворами. В особенности, это актуально при лечении рожи на ноге.
Какими антибиотиками необходимо смачивать повязки для компрессов? Как правило, для таких целей рекомендуется использование аэрозоля «Оксициклозоля», а также «Фурацилина» и «Микроцида». Оставлять такие компрессы на пораженных участках следует на 3-4 часа — за это время все бактерии, которые успели поселиться в верхних слоях кожи и на ее поверхности, будут уничтожены.
Некоторые специалисты рекомендуют использовать 50%-ый раствор «Димексида», а также присыпку с «Энтеросептолом». Второе средство можно применять, рассыпая небольшим слоем на внутреннюю часть чистой одежды. Данная методика отлично подходит на тот случай, когда рожа на ноге. Антибиотики в таком случае также назначаются — это ускорит выздоровление.
Правила гигиены
В том случае, если у пациента обнаруживается рожистое воспаление, специалист в области медицины обязательно должен порекомендовать ему соблюдение определенных правил личной гигиены, даже несмотря на то, что болезнь не является опасной для окружающих и пациент спокойно может пребывать в домашних условиях. Однако практика соблюдения элементарных правил гигиены позволяет ускорить процесс окончательного выздоровления.
В первую очередь, обратить свое внимание на регулярность приема душа — желательно делать это каждый день. Специалисты не рекомендуют использовать для таких целей ванну, тем более, с горячей водой. Место, пораженное инфекцией, не нужно тереть — его достаточно просто обмыть с применением мыла. После совершения водных процедур желательно улечься на постель с чистым бельем, которое также рекомендуется менять каждый день. Отдельные требования выдвигаются по отношению к материалу, из которого сделано постельное белье — он должен быть натуральным и мягким (желательно, хлопок).
Кроме приема антибиотиков, при роже необходимо делать ежедневные промывания воспаленного места с использованием травяных отваров (рекомендуется брать мать-и-мачеху или лекарственную ромашку). В том случае, если рожа образовалась в области половых органов или на лице, для создания отваров лучше всего использовать календулу или череду, а если воспаление находится на стадии заживления и покрыто шероховатостями, то на данном этапе лучше всего смазывать пораженное место маслом шиповника или соком, выдавленным из каланхоэ.
Профилактика заболевания
Для того чтобы не болеть рожей, следует тщательно следить не только за своим здоровьем, но и за образом жизни. Отдельное внимание необходимо уделять водным процедурам, которые должны проводиться как можно чаще (максимум — раз в день). Это необходимо для того, чтобы человек мог избежать опрелостей в различных местах, которые вызывают образование проблемы. В случае возникновения таковых, после приема душа тело следует обработать присыпкой.
Отдельное внимание следует уделить средствам личной гигиены. Нужно отметить, что для купания лучше всего использовать гель для душа, уровень содержания рН в котором меньше 7. То же самое правило касается и мыла. Наилучшим вариантом окажется то средство, в состав которого входит молочная кислота. Это необходимо для того, чтобы не нарушить защитный слой кожи, наличие которого предотвращает появление различных инфекций.
Для того чтобы избежать проявления рожи и последующего лечения заболевания, необходимо своевременно обрабатывать ранки и повреждения, которые образовываются на теле. Для такой цели лучше всего использовать камфорное масло, «Йоддицирин», а также перекись водорода.
Рожа › Болезни › ДокторПитер.ру
Рожа (erysipelas) — инфекционная болезнь, характеризующаяся очаговым серозным или серозно-геморрагическим воспалением кожи, лихорадкой и интоксикацией.
Рожа распространена повсеместно. Заболеваемость ею составляет 12—20 случаев на 10 тыс. населения в год. Чаще болеют женщины.
Признаки
Инкубационный период — от нескольких часов до 3—5 суток. По характеру местных проявлений различают эритематозную, эритематозно-буллезную, эритематозно-геморрагическую, буллезно-геморрагическую рожу. В зависимости от тяжести заболевания выделяют легкое течение, среднетяжелое и тяжелое. Чаще процесс локализуется на нижних конечностях, реже — на лице, верхних конечностях, очень редко — в области туловища, половых органов. Болезнь начинается остро. При наиболее типичном среднетяжелом течении возникают головная боль, чувство жара общая слабость, озноб, мышечные боли. Температура тела за несколько часов повышается до 38—39,5°. В ряде случаев наблюдаются тошнота и рвота. Более чем у половины больных появление симптомов интоксикации на 12—48 ч опережает развитие очага воспаления, особенно при локализации процесса на нижних конечностях. Основным признаком рожистого воспаления является эритема с четко отграниченными от непораженной кожи неровными краями в виде извилистой линии, дуг и языков. Для эритематозной рожи характерно наличие периферического валика в виде возвышающегося края эритемы. Кожа в области эритемы интенсивно гиперемирована, при пальпации боли обычно незначительны, в основном по периферии эритемы. Кожа напряжена, горячая на ощупь инфильтрирована. Одновременно возникает отек кожи, распространяющийся за пределы эритемы. Отмечается регионарный лимфаденит. При эритематозно-буллезной роже на фоне эритемы появляются пузыри (буллы), содержащие прозрачную желтоватую жидкость. При эритематозно-геморрагической роже возникают геморрагии разных размеров — от мелкоточечных кровоизлияний до обширных и сливных, распространяющихся на всю эритему. Буллезно-геморрагическая рожа характеризуется наличием геморрагического и фибринозного экссудата в пузырях. Пузыри могут содержать и преимущественно фибринозный экссудат, иметь уплощенный характер и быть плотными при пальпации.
При легком течении болезни температура в пределах 38,5°, умеренная головная боль. При тяжелом течении болезни температура достигает 40° и выше, отмечаются потрясающий озноб, рвота, бред, расстройства сознания, менингеальный синдром выраженная тахикардия, гипотония.
Лихорадочный период у больных рожей продолжается в среднем 4—5 суток. Острые воспалительные изменения в очаге исчезают в сроки до 5—7 суток при эритематозной роже, до 10—12 суток и более при буллезно-геморрагической роже. Сохраняющиеся во время реконвалесценции увеличенные регионарные лимфатические узлы, инфильтрация кожи на месте очага воспаления, субфебрильная температура являются прогностически неблагоприятными для развития ранних рецидивов. Повторная рожа возникает спустя 2 года и более после предыдущего заболевания и имеет другую локализацию.
Описание
Возбудитель инфекции — бета-гемолитический стрептококк группы А — находится в организме больных как в бактериальной, так и в L-форме.
Источником возбудителя инфекции может являться больной любым стрептококковым заболеванием (например, ангиной, скарлатиной) и носитель стрептококка. Основной путь передачи возбудителя — контактно-бытовой. Заражение происходит через поврежденную кожу — обычно незначительные микротравмы. Дополнительное значение имеет воздушно-капельный путь передачи (особенно при возникновении рожи на лице). Больные мало заразны. Предрасполагающими факторами являются стойкие нарушения лимфообращения, хроническая венозная недостаточность, грибковые заболевания кожи. Типична летне-осенняя сезонность.
Осложнения обычно носят местный характер: некрозы кожи, абсцессы, флегмоны, тромбофлебиты, лимфангииты, периаденит. При сопутствующих тяжелых заболеваниях и поздно начатом лечении может развиться сепсис, инфекционно-токсический шок. При частых рецидивах возможны лимфатический отек (лимфедема) и вторичная слоновость.
Диагностика
Диагноз устанавливают на основании клинической картины. В крови большинства больных отмечаются умеренный нейтрофильный лейкоцитоз с палочкоядерным сдвигом, незначительно повышенная СОЭ.
Лечение
Лечение в большинстве случаев проводят на дому и амбулаторно. Показаниями для госпитализации являются тяжелое течение болезни, распространенный местный процесс, его буллезно-геморрагический характер и рецидивирующая рожа. При лечении больных на дому и на догоспитальном этапе назначают антибиотики. Курс антибиотикотерапии — 8—10 дней. Патогенетическое лечение включает нестероидные противовоспалительные препараты, аскорутин, комплекс витаминов. При частых рецидивах рожи показана неспецифическая стимулирующая и иммунокорригирующая терапия. При рецидивирующей роже в ряде случаев применяют аутогемотерапию. Местное лечение рожи проводится лишь при ее буллезных формах и локализации процесса на конечностях. Пузыри надрезают у одного из краев и на очаг воспаления накладывают повязки с раствором антибактериального препарата, меняя их несколько раз в день. В остром периоде болезни можно использовать УФ-облучение и УВЧ-терапию. Больных выписывают не ранее 7-го дня после нормализации температуры тела. Перенесшие рожу находятся на учете в кабинете инфекционных болезней в течение 3 месяцев, а страдающие рецидивирующей рожей не менее 2 лет.
Хирургическое лечение осложнений при роже. При некрозах кожи после отграничения очага и улучшения общего состояния пациента производится некрэктомия. Рану покрывают дальцекс-трипсином с антисептиком или химиотерапевтическими средствами. При дефектах больших размеров, после появления плотных зернистых грануляций и ликвидации острых явлений проводят повторную операцию — ауто-дермопластику. При флегмонах и абсцессах разрез проводят по кратчайшему пути, рассекают кожу, подкожную клетчатку и вскрывают полость гнойника. После эвакуации детрита полость промывают антисептиками, осушают, разводят края раны крючками и выполняют ревизию. Иссекают все нежизнеспособные ткани. Рану, как правило, не ушивают, накладывают стерильную повязку. Гнойные лимфадениты, абсцедирующиеся флебиты и парафлебиты и другие очаги гнойно-воспалительного характера лечат по обычной методике — производят вскрытие скоплений гноя, удаление некротизированных тканей, дренирование раны.
Прогноз для жизни благоприятный. Частые рецидивы рожи с формированием вторичной слоновости могут привести к инвалидности.
Профилактика
Профилактика заключается в тщательном соблюдении личной гигиены, предупреждении микротравм, обработке микротравм антисептиками (например, 5 % спиртовым раствором йода, раствором бриллиантового зеленого), санации очагов хронической стрептококковой инфекции. Профилактика рецидивирующей рожи предусматривает лечение предрасполагающих к рецидивам заболеваний (грибковых поражений кожи, лимфовенозной недостаточности).
© Медицинская энциклопедия РАМН
Рожа — Appotek
Рожа — бактериальная инфекция верхнего слоя кожи. Инфекция приводит к большим, припухлым красным пятнам на коже. Иногда сопровождается другими симптомами, включая пузыри, лихорадку и озноб. Рожа чаще всего возникает на лице и ногах. Обычно инфекцию можно эффективно лечить антибиотиками.
В APPOTEK вы можете получить помощь при роже.
Причины
Рожа возникает, когда бактерии стрептококка группы А проникают через внешний барьер кожи. Эти бактерии обычно живут на вашей коже и других поверхностях, не причиняя вреда. Однако они могут попасть в вашу кожу через порез или рану и вызвать инфекцию. Состояния, которые вызывают разрывы кожи, такие как стопа спортсмена и экзема, иногда приводят к возникновению рожи. Также рожа может возникать, когда бактерии распространяются на носовые ходы после инфекции в носу и горле.
К другим причинам рожи относятся:
- язвы на коже
- хирургические разрезы
- укусы насекомых
- укусы собаки
- определенные заболевания кожи, например, псориаз
- отекшие ноги из-за проблем со здоровьем, такие как сердечная недостаточность или диабет
- использование наркотиков
Если у вас возникла рожа, существует риск рецидива.
Симптомы
Типичные симптомы включают высокую температуру, дрожь, озноб, усталость, головные боли, рвоту и общую болезненность в течение 48 часов после начала инфекции. Эритематозное поражения кожи быстро разрастается и имеет резко отграниченный, поднятый край. Он появляется в виде красной, отечной, теплой и болезненной сыпи, похожей по консистенции с кожурой апельсина. Лимфатические узлы могут быть набухшими, может появиться лимфедема.
Инфекция может произойти на любом участке кожи, включая лицо, руки, пальцы, ноги и пальцы ног.
Профилактика и защита
Вы можете принять следующие меры, чтобы снизить риск возникновения рожи:
- Держите раны в чистоте.
- Используйте увлажняющие средства для предотвращения высыхания и растрескивания кожи.
- Старайтесь не царапать кожу.
- Убедитесь, что любые проблемы с кожей, например, экзема, эффективно лечатся.
Вы также можете предупредить возникновение в будущем случаев возникновения рожи, посещая врача. Врач может убедиться, что инфекция не вернулась к другим частям тела.
У детей раннего возраста (особенно от 2 до 6 лет) и взрослых старше 60 лет чаще возникает рожа. Старшие взрослые, имеют слабую иммунную систему или имеют проблемы с накоплением жидкости после операции, имеют высокий риск заболеть рожей.
Лечение
Антибиотики, такие как пенициллин, является самым распространенным вариантом лечением рожи. Вы можете принимать антибиотики в домашних условиях, если у вас легкий случай рожи. Вам, скорее всего, придется принимать лекарства около недели. Более серьезные случаи рожи обычно лечат в больнице, где антибиотики можно вводить через вену. Маленькие дети и старики также могут потребовать лечения в стационаре. Иногда бактерии не реагируют на антибиотик, и нужно попробовать другой тип.
Также вам могут давать обезболивающие средства для уменьшения дискомфорта и лечения лихорадки.
Противогрибковые лекарства для стопы спортсмена могут понадобиться, если это является причиной рожи.
Когда нужно обратиться к врачу
Обратитесь к врачу, если у вас внезапное покраснение кожи с ухудшением общего состояния или повышение температуры — или когда покраснение кожи увеличивается в размерах.
Как APPOTEK может вам помочь
APPOTEK может помочь вам при роже. Медсестра или врач составит индивидуальную оценку на основе ваших симптомов. Тогда вам могут назначить лечение или направить на дальнейшее обследование. Если ваш ребенок пострадал, ему также следует посещать консультации.
Лекарства от рожи: антибиотики, анальгетики-жаропонижающие
Автор
Лоретта С. Дэвис, доктор медицины Профессор и заведующий кафедрой дерматологии, Медицинский колледж Джорджии, Университет Августа
Лоретта С. Дэвис, доктор медицины, является членом следующих медицинских обществ: Американская академия дерматологии
Раскрытие: Ничего не раскрывать .
Соавтор (ы)
Джон А. Коул, доктор медицины Дерматолог, частная практика, Валдоста, Джорджия
Джон А. Коул, доктор медицины, является членом следующих медицинских обществ: Американская академия дерматологии, Американское общество дерматологической хирургии
Раскрытие информации: раскрывать нечего.
Главный редактор
Уильям Д. Джеймс, доктор медицины Пол Р. Гросс, профессор дерматологии, заместитель председателя, директор программы резидентуры, факультет дерматологии, Медицинская школа Университета Пенсильвании
Уильям Д. Джеймс, доктор медицины, является членом следующих медицинских обществ: Американских Академия дерматологии, Общество следственной дерматологии
Раскрытие информации: Полученный доход в размере 250 долларов США или выше от: Elsevier; WebMD
Выступал в качестве спикера для различных университетов, дерматологических обществ и дерматологических факультетов.
Благодарности
Кейт Бенбенисти, MD Консультант, специалисты по дерматологии, доктора медицины, PA
Раскрытие: Ничего не нужно раскрывать.
Фрэнсис Советник, доктор медицинских наук Директор программы, председатель, профессор кафедры неотложной медицины Медицинской школы Восточной Вирджинии
Фрэнсис Советник, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американский колледж врачей неотложной помощи, Ассоциация академических кафедр неотложной медицины (AACEM), Норфолкская медицинская академия и Общество академической неотложной медицины
Раскрытие: Ничего не нужно раскрывать.
Эдди С. Ланг, MDCM, CCFP (EM), CSPQ Адъюнкт-профессор, старший научный сотрудник, отделение неотложной медицины, факультет семейной медицины, Университет Калгари; Доцент кафедры семейной медицины, Университет Макгилла
Эдди С. Ланг, MDCM, CCFP (EM), CSPQ является членом следующих медицинских обществ: Американского колледжа врачей неотложной помощи, Канадской ассоциации врачей неотложной помощи и Общества академической неотложной медицины
Раскрытие: Ничего не нужно раскрывать.
Christen M Mowad, MD Доцент, отделение дерматологии, Медицинский центр Гейзингер
Кристен Мовад, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американская академия дерматологии, Американская дерматологическая ассоциация, Дерматологическое общество Ноя Вустера, Академия дерматологии Пенсильвании и Phi Beta Kappa
.Раскрытие: Ничего не нужно раскрывать.
Роберт А. Шварц, доктор медицины, магистр здравоохранения Профессор и руководитель дерматологии, профессор патологии, педиатрии, медицины, профилактической медицины и общественного здравоохранения, Медицинская школа Рутгерса, Нью-Джерси,
Роберт А. Шварц, доктор медицины, магистр здравоохранения является членом следующих медицинских обществ: Alpha Omega Alpha, Американская академия дерматологии, Американский колледж врачей, Нью-Йоркская медицинская академия и Sigma Xi
.Раскрытие: Ничего не нужно раскрывать.
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Medscape Reference Salary Employment
Майкл Дж. Уэллс, доктор медицины Доцент, кафедра дерматологии, Центр медицинских наук Техасского технологического университета, Медицинская школа Пола Л. Фостера
Майкл Дж. Уэллс, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американской академии дерматологии, Американской медицинской ассоциации и Техасской медицинской ассоциации
Раскрытие: Ничего не нужно раскрывать.
Рассмотрение подхода, фармакологическое лечение, мероприятие
Автор
Лоретта С. Дэвис, доктор медицины Профессор и заведующий кафедрой дерматологии, Медицинский колледж Джорджии, Университет Августа
Лоретта С. Дэвис, доктор медицины, является членом следующих медицинских обществ: Американская академия дерматологии
Раскрытие: Ничего не раскрывать .
Соавтор (ы)
Джон А. Коул, доктор медицины Дерматолог, частная практика, Валдоста, Джорджия
Джон А. Коул, доктор медицины, является членом следующих медицинских обществ: Американская академия дерматологии, Американское общество дерматологической хирургии
Раскрытие информации: раскрывать нечего.
Главный редактор
Уильям Д. Джеймс, доктор медицины Пол Р. Гросс, профессор дерматологии, заместитель председателя, директор программы резидентуры, факультет дерматологии, Медицинская школа Университета Пенсильвании
Уильям Д. Джеймс, доктор медицины, является членом следующих медицинских обществ: Американских Академия дерматологии, Общество следственной дерматологии
Раскрытие информации: Полученный доход в размере 250 долларов США или выше от: Elsevier; WebMD
Выступал в качестве спикера для различных университетов, дерматологических обществ и дерматологических факультетов.
Благодарности
Кейт Бенбенисти, MD Консультант, специалисты по дерматологии, доктора медицины, PA
Раскрытие: Ничего не нужно раскрывать.
Фрэнсис Советник, доктор медицинских наук Директор программы, председатель, профессор кафедры неотложной медицины Медицинской школы Восточной Вирджинии
Фрэнсис Советник, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американский колледж врачей неотложной помощи, Ассоциация академических кафедр неотложной медицины (AACEM), Норфолкская медицинская академия и Общество академической неотложной медицины
Раскрытие: Ничего не нужно раскрывать.
Эдди С. Ланг, MDCM, CCFP (EM), CSPQ Адъюнкт-профессор, старший научный сотрудник, отделение неотложной медицины, факультет семейной медицины, Университет Калгари; Доцент кафедры семейной медицины, Университет Макгилла
Эдди С. Ланг, MDCM, CCFP (EM), CSPQ является членом следующих медицинских обществ: Американского колледжа врачей неотложной помощи, Канадской ассоциации врачей неотложной помощи и Общества академической неотложной медицины
Раскрытие: Ничего не нужно раскрывать.
Christen M Mowad, MD Доцент, отделение дерматологии, Медицинский центр Гейзингер
Кристен Мовад, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американская академия дерматологии, Американская дерматологическая ассоциация, Дерматологическое общество Ноя Вустера, Академия дерматологии Пенсильвании и Phi Beta Kappa
.Раскрытие: Ничего не нужно раскрывать.
Роберт А. Шварц, доктор медицины, магистр здравоохранения Профессор и руководитель дерматологии, профессор патологии, педиатрии, медицины, профилактической медицины и общественного здравоохранения, Медицинская школа Рутгерса, Нью-Джерси,
Роберт А. Шварц, доктор медицины, магистр здравоохранения является членом следующих медицинских обществ: Alpha Omega Alpha, Американская академия дерматологии, Американский колледж врачей, Нью-Йоркская медицинская академия и Sigma Xi
.Раскрытие: Ничего не нужно раскрывать.
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Medscape Reference Salary Employment
Майкл Дж. Уэллс, доктор медицины Доцент, кафедра дерматологии, Центр медицинских наук Техасского технологического университета, Медицинская школа Пола Л. Фостера
Майкл Дж. Уэллс, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американской академии дерматологии, Американской медицинской ассоциации и Техасской медицинской ассоциации
Раскрытие: Ничего не нужно раскрывать.
Использование антибиотиков у больных рожей: ретроспективное исследование
Задний план: Рожа — это кожная инфекция, обычно вызываемая стрептококками группы А. Хотя пенициллин является препаратом выбора, некоторые врачи склонны лечить рожистое воспаление антибиотиками, отличными от пенициллина.
Цели: Определить характер использования антибиотиков, факторы, влияющие на выбор антибиотика, и исход пациентов, получавших пенициллин, по сравнению с пациентами, получавшими другие противомикробные препараты.
Методы: Ретроспективный обзор карт взрослых пациентов с диагнозом рожистое воспаление при выписке был проведен за 1993–1996 годы.
Полученные результаты: В исследуемую группу вошли 365 пациентов (средний возраст 67 лет). В 76% случаев инфекция поражала ногу / ноги.Предрасполагающие условия присутствовали в 82% случаев. Микроорганизмы были выделены из посевов крови только в 6 из 176 случаев (3%), причем Streptococcus spp. выздоровел у четырех из этих шести пациентов. Культуры образцов кожи оказались положительными в 3 из 23 случаев. Только пенициллин был назначен 164 пациентам (45%). Другие антибиотики чаще использовались во второй половине периода исследования (P <0,0001) у пациентов с сопутствующими заболеваниями (P = 0,06) и у пациентов, госпитализированных в дерматологическое отделение (P <0.0001). Госпитализация была значительно короче в группе пенициллина (P = 0,004). Смертей в больницах не было.
Выводы: Мы не обнаружили никаких преимуществ в использовании антибиотиков, кроме пенициллина, для лечения рожи. Низкий результат посевов кожи и крови и их незначительное влияние на лечение, а также отличный результат предполагают, что эту инфекцию, вероятно, можно лечить эмпирически в амбулаторных условиях.
Erysipelas — обзор | Темы ScienceDirect
Рожа
Рожа — это поверхностная инфекция кожи, поражающая верхнюю часть дермы и лимфатическую систему. В большинстве случаев причиной рожи является ГАЗ; 12,13,17,68 однако стрептококки группы B, C и G иногда могут вызывать инфекцию, 12,68 и редко S. aureus, Streptococcus pneumoniae, Klebsiella pneumoniae, Yersinia enterocolitica, и Haemophilus influenzae причастны к патогенам. 68 Рожа имеет бимодальное распространение и чаще всего встречается у маленьких детей и пожилых людей. 12,68 Инфекция возникает, когда нарушение кожного барьера позволяет организмам проникать в кожу, и часто связано с ссадинами, язвами ног, интертригинозными или педальными грибковыми инфекциями, укусами насекомых, венозной или лимфатической обструкцией и хроническим отеком. 12,13,68,69 У новорожденных инфекция может исходить из культи пуповины и распространяться на брюшную стенку. 68
Рожистое воспаление начинается внезапно и характеризуется болезненным, ярко-красным, блестящим отечным налетом с хорошо очерченными и слегка приподнятыми краями. В тяжелых случаях могут возникнуть буллы и некроз. Инфекция обычно возникает на нижней конечности (чаще всего) или на лице и может быть связана с регионарным лимфаденитом. 12,13,17,68 Лихорадка, озноб и недомогание могут предшествовать появлению кожных изменений. Возможные системные осложнения рожи включают сепсис, синдром токсического стрептококкового шока, эндокардит и менингит; однако при своевременной диагностике и соответствующем лечении осложнения возникают редко.Дифференциальный диагноз включает контактный дерматит, ожоги, целлюлит, гангренозную эктиму и крапивницу. 68 Диагноз рожи ставится преимущественно на основании клинических данных. 13,68 Посев крови, биопсия кожи и пункционная аспирация дают низкие результаты. 12
Лечение рожи у иммунокомпетентных пациентов заключается в пероральном приеме пенициллина в течение 10–14 дней с последующим наблюдением через 48–72 часа, чтобы убедиться, что инфекция проходит. Пациентам с тяжелыми инфекциями, младенцам и пациентам с ослабленным иммунитетом изначально может потребоваться госпитализация для парентеральной терапии. 68 Для пациентов с аллергией на пенициллин обычно эффективна терапия макролидами; 12,68 и если наличие стафилококков вызывает беспокойство, следует использовать антистафилококковые антибиотики. 12 Местный уход за раной и внимание к предрасполагающим факторам (лечение опоясывающего лишая стопы, отек ног) также являются важными аспектами лечения. Профилактическая терапия назначается нечасто пациентам с рецидивирующим заболеванием. 12,68
Границы | Внутриклеточное поглощение и сохранение стрептококков: потенциальная причина рецидива рожи
Введение
Определение рожи
Рожа — тяжелая инфекция кожи, вызываемая в основном β-гемолитическими стрептококками группы А ( S.pyogenes , GAS) (1–4). Стрептококковая инфекция при рожистом воспалении в первую очередь поражает лимфатические сосуды (5). Как уже было определено в писаниях Гиппократа, «έρυσίπελαϛ» (красная кожа) представляет собой острое начало местного воспаления с болезненной отечной эритемой, которая имеет резкую границу с прилегающей непораженной кожей. Языковые или нерегулярные разрастания отражают распространение инфекции по лимфатическим сосудам (Рисунки 1A – C). Сопутствующие системные симптомы включают лихорадку, озноб, недомогание и лабораторные признаки воспаления (6, 7).Термины рожа и целлюлит часто используются как синонимы. Они обычно рассматриваются как проявления того же состояния, при этом считается, что рожистое воспаление в первую очередь поражает поверхностные слои кожи, то есть эпидермис, дерму и верхний подкожный слой, в то время как целлюлит считается более диффузной инфекцией кожи, распространяющейся из дермы глубже в подкожную ткань ( 8). Клинически граница между рожей и целлюлитом размыта, и точная дифференциация может быть затруднена. В этом обзоре термины рожа и целлюлит рассматриваются по разным обозначениям для одного и того же заболевания.
Рисунок 1 . Клинические проявления рожистого воспаления и рецидивов рожистого воспаления. Типичное воспалительное (A) или геморрагическое (B) рожистое воспаление голени. (C) Увеличение лимфедемы после нескольких рецидивов буллезного рожистого воспаления, на что указывает периферическое увеличение левой голеностопного сустава и отек переднего отдела стопы без ямок. (D) Первый эпизод рожи и два рецидива, два (E) и три (F) лет после первого эпизода, обычно происходящего в том же месте у пациентки. (G) Поздняя стадия чрезмерной лимфедемы с утолщенной складкой кожи у основания второго пальца, которая не может быть поднята (положительный тест по признаку Штеммера), кожный фиброз и образование многочисленных фиброзных узлов в результате многократных эпизодов рецидивирующего рожистого воспаления. (H, I) Место прививки паутины пальца при первом эпизоде рожи левой голени. Обратите внимание на типичное центростремительное расстояние (стрелка) между местом посева бактерий и рожей.
Рожа — это бремя для здоровья во всем мире.Зарегистрированная заболеваемость рожей колеблется от 19–24 на 10 000 жителей в европейских странах до 24,6 случаев на 1000 пациенто-лет в зависимости от анализируемой популяции (9–11). В Соединенных Штатах Америки около 14,5 миллионов случаев в год вызывают более 650 000 госпитализаций и 3,7 миллиарда долларов США на амбулаторное лечение (12). Согласно строгой классификации, рожа вызывается β-гемолитическими стрептококками группы А ( S. pyogenes , GAS), а также стрептококками не группы А. S. aureus и грамотрицательные бактерии иногда вызывают клинические состояния, напоминающие рожистое воспаление и целлюлит (1–3). Стрептококковая инфекция при рожистом воспалении в первую очередь поражает лимфатические сосуды (5). Согласно первичному месту прививки, наиболее частым местом заражения является нижняя конечность, на которую приходится около 80% всех случаев (рис. 1) (13). Сведения о естественном течении невылеченной рожи неточны. Без адекватного лечения рожистое воспаление может вызвать эндокардит, сепсис и синдром токсического шока, вызванного стрептококками (STSS).В дальнейшем он может прогрессировать до некротического фасциита, затрагивающего все слои кожи, миозита и мионекроза (12, 14–16). Негнойные осложнения возникают редко, но кожные инфекции, вызванные нефритогенными штаммами ГАЗ, предрасполагают пациентов к постстрептококковому гломерулонефриту. Ревматическая лихорадка не связана со стрептококковыми кожными инфекциями (17, 18).
Пенициллин считается препаратом выбора, поскольку он недорогой, а S. pyogenes остается чувствительным к β-лактамным антибиотикам, несмотря на 60 лет широкого применения (19–22).Хотя он использовался в качестве основного лечения стрептококковой инфекции в течение десятилетий, S. pyogenes никогда не приобретал гены бета-лактамаз или резистентность к пенициллин-связывающему белку на основе пенициллина (20). Альтернативой являются макролидные антибиотики, но частота резистентности к ГАЗ возрастает (23–25).
Рецидив рожи: неудовлетворенная потребность в лечении рожи
Наиболее частым осложнением рожи является рецидив с развитием лимфедемы.Рецидивирующие эпизоды рожи возникают примерно в 40% случаев и обычно поражают один и тот же анатомический участок (рисунки 1C – F) (26, 27). Каждый повторный эпизод рожи вызывает прогрессирующее повреждение и облитерацию лимфатических сосудов (28, 29). Это ухудшает лимфодренаж и, в конечном итоге, приводит к необратимой лимфедеме (рис. 1C, E, F), которая может привести к потере трудоспособности и получила название «ностры слоновости» из-за его клинического сходства с поздними стадиями лимфедемы, вызванной лимфатическим филяриозом (рис. 1G).Слоновость представляет собой драматическое и необратимое состояние, характеризующееся деформирующим лимфедематозным отеком и древесным фиброзом пораженной анатомической области. В целом рецидивы рожи связаны со значительной заболеваемостью, социальными нарушениями и снижением затрат на здравоохранение (12, 30).
Для предотвращения рецидива рожи рекомендуется длительный профилактический прием низких доз пенициллина. Продолжающаяся профилактика пенициллином продлевает время до следующего эпизода, хотя иногда пациенты испытывают рецидивы во время антибиотикопрофилактики (26, 31–33).Однако защитный экран не сохраняется после прекращения профилактики, и частота рецидивов снова становится такой же, как и без профилактики (26, 34, 35). Соответственно, остается нерешенным вопрос о предотвращении рецидива рожи. Таким образом, выявление причин и разработка стратегий предотвращения рецидивов представляют собой основные неудовлетворенные медицинские потребности пациентов с рожей.
В этой статье мы рассмотрим механизмы, которые были предложены в качестве объяснения повторения.Обычные факторы риска рецидивов такие же, как и для единичных эпизодов (36). К ним относятся анатомическая локализация, венозная недостаточность, лимфедема, предыдущая операция, продолжающееся нарушение кожного барьера, способствующее повторному проникновению бактерий, ожирение и другие общие факторы риска (34, 35, 37–42). Однако они не дают конкретного обоснования рецидива рожи, помимо факторов риска самого рожистого воспаления. Поскольку резистентность к пенициллину среди стрептококков практически не задокументирована, поэтому другие аспекты должны иметь значение для высокой частоты повторяющихся эпизодов рожистого воспаления.Хотя это очевидно, недавний метаанализ подверг критике, что лишь небольшое количество исследований действительно рассматривало причины рецидивов (35).
В поисках альтернативных объяснений мы идентифицируем внутриклеточную персистенцию S. pyogenes как потенциальную причину рецидивов. Внутриклеточное поглощение стрептококков эпителиальными и эндотелиальными клетками, макрофагами и полиморфно-ядерными клетками создает резервуары для персистенции ГАЗ (43, 44). Поскольку бета-лактамные антибиотики не достигают достаточной бактерицидной внутриклеточной концентрации, эти внутриклеточные резервуары, вероятно, не удаляются во время лечения пенициллином.Эти внутриклеточные резервуары могут служить спящей инфекцией, склонной к реактивации. Следовательно, мы пришли к выводу, что для длительного лечения рожи необходимы схемы антибиотиков с эффективной внутриклеточной антибактериальной эффективностью. Это требует альтернативных стратегий лечения и их потенциальной проверки в испытаниях терапевтических антибиотиков.
Методы
Данные для этого обзора были получены в результате поиска в MEDLINE, Current Contents, PubMed и Cochrane central, а также ссылок из соответствующих статей (Pubmed), посвященных факторам риска рожи и схемам лечения с использованием поисковых терминов «факторы риска рожистого воспаления», «целлюлит нижних конечностей». , »« Целлюлит »,« рожа »,« стрептококк »или их сочетание.Были включены только статьи, опубликованные на английском и французском языках до июня 2017 года. Кроме того, мы суммируем данные об экспериментальных и клинических доказательствах внутриклеточного поглощения ГАЗА и персистенции ГАЗ-инфекций, идентифицированных с помощью поисковых терминов «стрептококковые инфекции», «стойкость стрептококков», «интернализация стрептококков», «стрептококковые тонзиллиты». Стратегии поиска и справочные оценки приведены на рисунках 2, 3.
Рисунок 2 . Условия поиска и блок-схема анализа литературы о рецидиве рожи.N обозначает количество статей.
Рисунок 3 . Условия поиска и блок-схема анализа литературы по внутриклеточному поглощению и персистенции стрептококков. N обозначает количество статей.
Традиционные факторы риска рецидива рожи
Факторы риска рецидива рожи считаются такими же, как и для единичных эпизодов (36). Они относятся к анатомическому строению, венозной недостаточности, лимфедему, предыдущей операции, продолжающемуся нарушению кожного барьера, способствующему повторному проникновению бактерий, ожирению и другим общим факторам риска.
Анатомический сайт
В популяционном когортном исследовании целлюлита нижних конечностей было показано, что анатомическая локализация является самым сильным независимым предиктором двухлетнего рецидива. Фактически, пациенты с целлюлитом большеберцовой области в пять раз чаще испытывали рецидив, чем пациенты с целлюлитом в области стопы или бедра. Незначительные травмы передней большеберцовой области и разреженная претибиальная подкожная клетчатка рассматривались как причины предрасположенности претибиальной области и рецидива рожистого воспаления (39).
Венозная недостаточность и лимфедема
Наличие венозной недостаточности и хронической лимфедемы были независимо связаны с рожистым воспалением во многих исследованиях и поэтому считаются сильным фактором риска повторных эпизодов голени (34, 37, 38, 40, 45–48). Повреждение лимфатических сосудов приводит к неэффективному дренажу и лимфедему, ухудшает поверхностный фагоцитоз полиморфно-ядерными лейкоцитами и значительно увеличивает восприимчивость к инфекции (49). Аномальный лимфатический дренаж наблюдался в здоровой ноге у 79–86% пациентов, перенесших лимфосцинтиграфию после предыдущего эпизода целлюлита.Соответственно, пациенты с целлюлитом ног могут иметь ранее не диагностированные первичные лимфатические аномалии (28, 29). Однако отличить венозный отек от лимфедемы может не хватать диагностической чувствительности, в частности, поскольку хронический венозный отек всегда включает компонент лимфедемы (46). Примерами других причин лимфедемы при рецидивирующем рожистом воспалении являются радикальная мастэктомия с расслоением подмышечных узлов или филяриатоз (50, 51).
Каждый эпизод рожи прогрессивно повреждает лимфатические сосуды, увеличивает лимфатическую недостаточность и способствует остаточному отеку (рисунки 1C, E, F), создавая порочный круг, предрасполагающий к новым эпизодам рожистого воспаления (52, 53).Сильно нарушенный лимфатический дренаж обнаруживается у 80% пациентов с двумя или более эпизодами рожистого воспаления после лечения и разрешения рецидивирующего эпизода (54). Таким образом, отек может быть как причиной, так и следствием первого эпизода рожи, но отчетливую причинную роль рецидива рожи доказать трудно. Поэтому любой отек следует рассматривать как фактор риска рожистого воспаления в целом, а также он связан с рецидивом.
Предыдущая операция
Исследования случай-контроль показали, что пациенты с рецидивирующим рожистым воспалением чаще перенесли операции на ногах (37, 47, 48, 52).Сафенэктомия была определена как один из наиболее значительных факторов риска рецидива рожи (52). Двадцать шесть процентов пациентов, перенесших радикальную вульвэктомию по поводу рака вульвы с иссечением проксимальной части подкожных вен и глубокой паховой лимфаденэктомией, перенесли острый целлюлит ног с частотой рецидивов 81%. Никакого фактора риска, кроме присутствия β-гемолитических стрептококков на различных участках до операции, выявить не удалось (55). Эти результаты были подтверждены другими исследованиями (56, 57) и объяснены нарушением венозного и лимфатического дренажа после операции, что привело к появлению мест проникновения бактерий для колонизации ГАЗ.
Кожные барьерные дефекты
Бактериальным инфекциям требуются входные участки. Дефекты целостности кожи служат воротами для проникновения стрептококков при рожистом воспалении. Исследования случай-контроль показали, что нарушение кожного барьера было наиболее значимым фактором риска рецидива рожи (37). В трех других исследованиях случай-контроль раны ног были определены как потенциальные факторы риска рецидива (47, 48, 58). Язвы на ногах и раздражающие кожные заболевания (экзема, псориаз и неустановленные кожные заболевания) также были связаны с повышенным риском рецидива (37, 47, 48, 58, 59).
Колонизация кожи дерматофитами вызывает разрушение эпидермиса и трещины для инокуляции стрептококков. Tinea pedis — один из наиболее значительных местных факторов риска рецидива (34). Европейское исследование случай-контроль определило дерматомикоз как фактор риска рожистого воспаления с отношением шансов 2,4 при однофакторном анализе (59). Это было подтверждено системным обзором и метаанализом факторов риска целлюлита на ногах и показало связь между наличием опрелостей пальцев и перепонок (рис. 1I), вторичных по отношению к микозу стопы, и целлюлитом (60).Постоянное наличие мест проникновения бактерий считается предрасполагающим фактором для рецидивирующего рожистого воспаления, а лечение опоясывающего лишая является рекомендуемой мерой для снижения риска целлюлита. Интересно, что частота рецидивов 50% в исследовании антибиотикопрофилактики, проведенном Kremer et al. произошел, несмотря на лечение дерматофитии стопы (61). Следовательно, лечения опоясывающего лишая может быть недостаточно для профилактики рецидива. Более того, учитывая повсеместность микозов стопы в общей популяции, был сделан вывод, что в патогенез рецидивирующего рожистого воспаления вовлечены и другие факторы (28).
Общие факторы риска
Местные факторы риска, по-видимому, играют более значительную роль в развитии рецидивирующего целлюлита, чем системные факторы. Из четырех общих факторов (сахарный диабет, ожирение, курение и потребление алкоголя), выявленных в ходе системного обзора, только ожирение (индекс массы тела> 30) было связано с повышенным риском рецидива (60). Это можно объяснить тем фактом, что тяжелое ожирение приводит к венозной и лимфатической недостаточности, а также к большему риску грибковых инфекций и, таким образом, в принципе предрасполагает к рожистому воспалению.
Злокачественные новообразования, в том числе рак груди, рак эндометрия, болезнь Ходжкина, аденокарцинома простаты и семинома, являются другими факторами риска стрептококковых инфекций (62). Фактически, пациенты с раком в анамнезе имеют в 4 раза повышенный риск рецидива по сравнению с пациентами без каких-либо опухолей в анамнезе (39). Это может включать венозную и лимфатическую недостаточность из-за прямого воздействия опухоли, лучевой терапии или лимфаденэктомии (63).
Обычные факторы риска: отсутствие достаточного объяснения рецидивов рожи
В целом, факторы риска, выявленные для рецидивов, отражают факторы риска для рожистого воспаления в целом и не дают конкретного объяснения рецидивам рожистого воспаления.Соответственно, предыдущий эпизод целлюлита является наиболее очевидным фактором риска целлюлита ног (37, 47, 59). Лечение потенциальных мест заражения является основным обоснованием лечения рожи, и необходимо эффективно лечить предрасполагающие состояния, такие как лимфедема или опрелость пальцев стопы. Однако нет достоверных данных о том, что эти меры действительно могут повлиять на частоту рецидивов. Фактически, лечение tinea pedis, по-видимому, не предотвращает второго эпизода рожи (61). Кроме того, защитный эффект длительной антибиотикопрофилактики снижается после прекращения приема (26, 34, 35).Таким образом, высокая частота рецидивов требует альтернативных объяснений. Их можно искать в биологическом поведении стрептококков.
Рецидив рожи: роль внутриклеточной стойкости стрептококков
Стрептококки и способность к внутриклеточному захвату и персистенции
Хотя S. pyogenes в принципе является внеклеточным патогеном, некоторые штаммы обладают способностью к внутриклеточному захвату и сохранению в эпителиальных и эндотелиальных, а также иммунных клетках, включая макрофагоподобные клетки, полиморфноядерные гранулоциты и дендритные клетки (64–75 ).Внутриклеточное выживание, по-видимому, является обычной стрептококковой стратегией. Помимо стрептококков группы A (GAS), стрептококки группы C и G все чаще признаются за их способность проникать в эпителиальные или эндотелиальные клетки (76, 77). После внутриклеточного поглощения жизнеспособными клетками бактерии защищены от действия β-лактамных антибиотиков, поскольку пенициллины не проникают в живые клетки в значительной степени. Различные стратегии способствуют внутриклеточному поглощению и сохранению стрептококков.
Механизмы внутриклеточного поглощения и персистенции ГАЗА
Эффективная внутриклеточная инвазия S. pyogenes в нефагоцитарные эпителиальные клетки была впервые предложена LaPenta et al. с использованием модели инфекции клеточной культуры в 1994 г. Способность к внутриклеточному поглощению была равна или даже выше, чем у классических внутриклеточных патогенов, таких как Listeria или Salmonella (65). После этого в нескольких исследованиях изучали механизм инвазии и выживания стрептококков в клетках горла, включая кератиноциты ротоглотки, для объяснения неэффективности лечения фарингита (65, 78, 79).
Экспрессия широкого и вариабельного спектра адгезинов и инвазинов является одним из отличительных признаков стрептококков (80). Адгезины осуществляют тесный контакт с белками внеклеточного матрикса (ЕСМ) хозяина, такими как фибронектин, в то время как инвазины запускают инвазию в клетки-хозяева. Благодаря репертуару инвазинов и адгезинов, стрептококки разработали многочисленные механизмы для интернализации и выживания в клетках-хозяевах, избегания лечения антибиотиками и иммунной защиты хозяина (рис. 4A – E) (17, 83–87).М-белки и связывающие фибронектин белки (такие как sfbI) действуют как адгезины, которые опосредуют прикрепление как к эпителиальным, так и к эндотелиальным клеткам (81, 82).
Рисунок 4 . Внутриклеточный образ жизни стрептококков группы А. (A) Адгезия к мембране клетки-хозяина клетки HEp-2 через адгезины. (B, C) Проникновение в клетки HEp-2 через инвазины путем кооптации кавеол для образования больших инвагинаций для стрептококков, несущих SfbI. (D) Вторжение через сигнальные события, которые запускают перестройки цитоскелета, такие как взъерошивание мембран. (E) Прилипшие стрептококки разрастаются микроворсинками клетки-хозяина, которые сливаются, образуя мембранные лоскуты, которые впоследствии покрывают стрептококки. (F) Стрептококки, находящиеся внутриклеточно исключительно в мембраносвязанных фагосомоподобных компартментах после короткого времени инфицирования (модель клеточной культуры). (G) Высвобождение стрептококков из окруженного мембраной компартмента в цитоплазму клетки-хозяина после более длительного периода инфицирования, где они реплицируются и сохраняются (модель клеточной культуры). (H) Модель мыши in vivo , обеспечивающая доказательство наличия и репликации стрептококков в цитоплазме в свободном состоянии и подтверждающая наблюдения, полученные в культуре клеток. Полоски представляют 2 мкм в (A) 1 мкм в (F) и G, 0,5 мкм в (B – E, H) . Все изображения были взяты из экспериментов по заражению, проведенных на моделях клеточных культур и на мышах в Центре исследований инфекций им. Гельмгольца. Экспериментальные процедуры были описаны ранее (81, 82). (A – E) представляют собой изображения, полученные с помощью автоэмиссионного сканирующего электронного микроскопа; Рисунки ( F – H ) представляют собой изображения, полученные с помощью просвечивающей электронной микроскопии, ультратонких срезов образцов, залитых смолой.
Описаны два морфологически различных основных механизма инвазии и различные пути внутриклеточного транспорта стрептококков в эпителиальные и эндотелиальные клетки. Белки SfbI и M инициируют процесс, связывая фибронектин, который взаимодействует с рецепторами интегрина.Обширная кластеризация интегринов запускает агрегацию кавеол с образованием больших инвагинаций клеточной мембраны, которые поглощают прикрепленные стрептококки (Фигуры 4B, C). С другой стороны, стрептококки, которые взаимодействуют с фибронектином с белком М, могут вызывать фокальные адгезионные комплексы, которые попадают в организм через механизм, похожий на застежку-молнию или мембранный механизм (рис. 4D) (80). Для механизма захвата, опосредованного кавеолами, ГАЗ предотвращает слияние с лизосомами и вместо этого находится в кавеосомах (82). GAS, проникающий через перестройки цитоскелета, сливается с лизосомами с образованием фаголизосом.Кроме того, в моделях клеточных культур GAS может быть обнаружен свободным в цитоплазме клетки-хозяина после более длительного периода инфицирования, где они могут эффективно реплицироваться (рисунки 4F, G) (70, 88, 89). После того, как они реплицировались и разрушили клетки-хозяева, S. pyogenes выходит наружу и может инфицировать новые клетки и может сохраняться в горле в течение длительного времени, высвобождая стрептококковые антигены любого типа и вызывая постоянство высоких титров антител даже в отсутствие явного заболевания. Помимо своей способности проникать в эпителиальные и эндотелиальные клетки, стрептококки могут ускользать из фагосомы в цитоплазму фагоцитарных клеток, где они выживают благодаря внутриклеточным механизмам уничтожения полимороядерных клеток (рис. 4H) (43).Фагоцитоз стрептококков изменяет программу дифференцировки апоптоза нейтрофилов. Он активирует гены, кодирующие ключевые эффекторы апоптоза, и подавляет рецепторы, критические для функции врожденного иммунитета, что потенциально приводит к выживанию патогенов (90). Взаимодействие некоторых штаммов GAS с плазминогеном способствует опосредованному интегрином прикреплению и инвазии GAS в кератиноциты, создавая специфический для кожи резервуар персистенции стрептококков (91).
Внутриклеточная стойкость стрептококков при инфекциях мягких тканей
При инвазивных острых инфекциях мягких тканей ГАЗ был обнаружен в макрофагах в биоптатах пациентов даже после длительного внутривенного лечения антибиотиками.Внутриклеточная локализация GAS варьировала в зависимости от тяжести инфекции и была наиболее распространенной во вновь пораженных, менее воспаленных тканях с более низкой бактериальной нагрузкой, в то время как чисто внеклеточный GAS или комбинация внутри- и внеклеточного GAS преобладала в сильно воспаленной ткани. In vitro S. pyogenes выжил внутриклеточно в макрофагах, несмотря на терапевтическую концентрацию пенициллина G в культуральной среде, и за удалением антибиотика последовал значительный рост внеклеточных бактерий (92).
Способность GAS проникать в эндотелиальные клетки может способствовать распространению в окружающие мягкие ткани. Помимо локальной инвазии, стрептококки, прячущиеся в эндотелиальном барьере, также могут быть источником транзиторной бактериемии (80). S. dysgalactiae subsp equisimilis (SDSE) вызывал рецидивирующие бактериемические инфекции в течение нескольких лет, несмотря на присутствие опсонизирующих антител против изолята и длительное лечение пенициллином. SDSE был обнаружен в аневризме аорты, и изолят эффективно проникал в эндотелиальные клетки, тем самым подчеркивая механизмы персистенции стрептококков в эндотелиальной выстилке стенок сосудов (77).Это может объяснить, почему у пациентов без видимых участков проникновения бактерий в мягкие ткани были зарегистрированы случаи инвазивных инфекций мягких тканей. При этом М3-серотипы ГАЗ являются одними из наиболее частых бактерий, выделяемых от пациентов с инвазивным заболеванием тканей. Эти изоляты характеризуются высокой способностью проникать в эндотелиальные клетки и сохраняться в них. Эти механизмы, вероятно, способствуют выживанию, тропизму глубоких тканей и повторному распространению инвазивного ГАЗ (93). В целом, эти результаты предполагают, что стрептококки, находящиеся внутри клетки, представляют собой важный резервуар бактерий, которые могут вызывать продолжающуюся инфекцию после выхода из своих клеток-хозяев (92).
Внутриклеточная персистенция стрептококков вызывает рецидивы рецидивирующего стрептококкового фарингита
Анализ рецидивирующего стрептококкового тонзиллита может помочь улучшить патогенетическое понимание высокой частоты рецидивов рожи. S. pyogenes — наиболее частая причина рецидивирующего бактериального тонзиллофарингита. Десятидневный курс пенициллина является общепринятым лечением стрептококковой ангины (94–96). Подобно рожистому воспалению, лечение пенициллином не устраняет стрептококковую инфекцию примерно у 10–30% пациентов, хотя стрептококки остаются чувствительными in vitro к пенициллину (97, 98).Попадание в защищенную внутриклеточную среду, недоступную для пенициллинов, может объяснить неудачи лечения стрептококкового фарингита (66, 68). При рецидивирующем тонзиллите сообщалось о внутриклеточных стрептококковых резервуарах, устойчивых к эрадикации антибиотиками (68, 69). Электронная микроскопия и иммуногистохимия наблюдали внутриклеточные стрептококки в эпителиальных клетках глотки у большинства пациентов с тонзиллитом, а также в макрофагоподобных клетках и эпителиальных клетках бессимптомных носителей ГАЗ (69).После репликации и разрушения клеток-хозяев, S. pyogenes выходит наружу и может инфицировать новые клетки и сохраняться в горле в течение длительного времени, высвобождая стрептококковые токсины и вызывая необратимо повышенные титры антистрептококковых антител даже при отсутствии явного заболевания ( 99). Частота выявления идентичных изолятов S. pyogenes во время начальных эпизодов и рецидива тонзиллита достигает 80% по оценке молекулярного типирования (100), что указывает на то, что рецидив в основном связан с реактивацией стойкой стрептококковой инфекции у бессимптомных носителей, а не с экзогенная реинфекция.Способность к внутриклеточному проникновению в эпителий миндалин или глотки является отличительной особенностью этих штаммов стрептококков. В отличие от штаммов, которые были успешно уничтожены лечением антибиотиками, они эффективно прилипали и были интернализованы эпителиальными клетками человека 2 типа (HEp-2), клеточной линией, происходящей из карциномы гортани человека (66, 101). Таким образом, проникновение в эпителиальные клетки обеспечивает надежное объяснение стойкой колонизации глотки, поскольку оно защищает внутриклеточные стрептококки от иммунных эффекторов и антибиотиков, которые менее проницаемы для мембран, в частности пенициллина (43, 70).
Внутриклеточное поглощение и постоянство — потенциальный механизм рецидива рожи
Данные о биологическом поведении стрептококков дают убедительное обоснование высокой частоты рецидивов рожи, возникающей, несмотря на соответствующее лечение пенициллином и долгосрочную антибиотикопрофилактику. Они предполагают, что способность к внутриклеточному поглощению и персистенции стрептококков представляет собой важный механизм, ответственный за рецидив рожистого воспаления.На сегодняшний день только несколько исследований посвящены этому вопросу напрямую. В биопсиях различных стрептококковых инфекций мягких тканей (миозит, некротический фасциит и два случая целлюлита) наблюдались высокие количества интактных стрептококков, находящихся внутри клетки, даже после длительной терапии антибиотиками. Они сопротивлялись убийству антибиотиками, предположительно из-за внутриклеточной устойчивости в клетках-хозяевах. Внеклеточная и внутриклеточная бактериальная нагрузка при этих инфекциях варьировалась в зависимости от тяжести инфекции и поражения тканей.Более чем в 40% проанализированных случаев наблюдалось чисто внутриклеточное бактериальное распределение, преимущественно в макрофагах (92). Поэтому в стратегиях антибиотиков для предотвращения повторных эпизодов рожи следует, возможно, рассмотреть возможность ликвидации внутриклеточных резервуаров стрептококка.
Стратегии лечения рожи
Устранение внутриклеточной стойкости стрептококков для предотвращения рецидива рожи
Из клинических испытаний и практического опыта очевидно, что существующие схемы лечения антибиотиками с использованием β-лактамных антибиотиков могут контролировать острые стрептококковые инфекции при рожистом воспалении, но недостаточны для предотвращения рецидива рожистого воспаления.Стратегии, направленные на устранение распространенных факторов риска рожистого воспаления, в частности, лечение участков инокуляции от проникновения патогенов, таких как опрелость пальцев стопы, необходимы для предотвращения экзогенного повторного заражения, но, очевидно, не могут снизить риск рецидива. В совокупности эти наблюдения показывают, что как текущие схемы приема антибиотиков, так и меры, направленные на предполагаемые факторы риска, не устраняют фактические причины рецидива рожи и требуют переоценки.
Понимание внутриклеточного поглощения и устойчивости ГАЗ теперь может дать интригующее и правдоподобное объяснение неудачам предотвращения.Пенициллины и цефалоспорины плохо проникают через клеточную мембрану и не достигают достаточных внутриклеточных бактерицидных концентраций. Соответственно, внутриклеточные стрептококки защищены от β-лактамных антибиотиков (102). Каплан и др. не наблюдали деградации внутриклеточных стрептококков после воздействия бактерицидных уровней пенициллина в модели культуры клеток, в то время как воздействие на эпителиальные клетки эритромицина или азитромицина могло эффективно убивать внутриклеточный ГАЗ. Цефалотин и клиндамицин также были более эффективны в уничтожении проглоченного ГАЗ, чем пенициллин, но менее эффективны, чем эритромицин или азитромицин (103, 104).Такие результаты подтверждают гипотезу о том, что высокая частота рецидивов рожи и неспособность пенициллина предотвратить рецидивы рожистого воспаления действительно могут быть связаны с внутриклеточным поглощением стрептококков и отсутствием внутриклеточной активности пенициллина (104).
Текущие рекомендации по лечению рожи
Хотя во многих исследованиях анализировалась реакция рожистого воспаления и целлюлита на различные схемы приема антибиотиков, недавний метаанализ не смог определить «лучшее» лечение (105).Не существует согласованного на международном уровне стандартного лечения для сравнения, и даже подходящую продолжительность лечения антибиотиками нельзя было определить, потому что режимы дозирования и показатели результатов были неоднородными в разных исследованиях (105, 106).
Текущие рекомендации по лечению рожи рекомендуют антибактериальную терапию в зависимости от тяжести заболевания без учета потенциальной персистенции стрептококков. Они предлагают монотерапию бета-лактамными антибиотиками или клиндамицином для легких и умеренных негнойных инфекций кожи и мягких тканей и рекомендуют комбинацию этих антибиотиков только в тяжелых случаях, подтвержденных посевом и тестами на чувствительность (22, 107).Левофлоксацин, ингибитор гиразы с повышенной активностью против грамположительных бактерий, также может быть использован, но возможно появление устойчивости (108). Альтернативы включают линезолид, первый из нового класса оксазолидиноновых антибиотиков с внутриклеточной активностью. Линезолид может проникать в фагоциты и нефагоцитарные клетки. Он был так же эффективен, как кларитромицин или цефподоксим проксетил (цефалоспорин третьего поколения), в лечении пациентов с неосложненными инфекциями мягких тканей и имел лучшие результаты, чем эмпирическое лечение оксациллином (109, 110).Имеются ограниченные доказательства того, что макролид и стрептограмин немного лучше, чем пенициллин, для устранения или уменьшения симптомов в конце лечения целлюлита (105). Частота рецидивов рожи для этих последних антибиотиков систематически не определялась.
Текущие рекомендации по предотвращению рецидивов рожи
Рекомендации по предотвращению рецидива рожи рассмотрены в нескольких национальных руководствах (35). В основном они основаны на наблюдательных исследованиях с низким уровнем доказательности.Устранение предрасполагающих факторов во всех них считается обязательным. Начало антибиотикопрофилактики обычно рекомендуется после второго эпизода. Пациентам с рецидивирующим целлюлитом рекомендуется профилактическое лечение пероральным пенициллином или эритромицином или внутримышечным бензатин-пенициллином до тех пор, пока сохраняются предрасполагающие факторы (22). В пяти контролируемых исследованиях оценивалась реакция на профилактику антибиотиками с использованием пенициллина или эритромицина (35). Во всех исследованиях наблюдалось снижение частоты рецидивов во время профилактики.В группе эритромицина рецидивов в течение 18 месяцев профилактики не наблюдалось. К сожалению, пациенты не наблюдались после прекращения приема эритромицина (61). Профилактические эффекты пенициллина в отношении риска рецидива целлюлита не сохранялись после прекращения профилактики (26, 35). Соответственно, проблема предотвращения рецидива рожи осталась нерешенной.
Выводы из отоларингологии: эрадикация стрептококков в глоточных государствах-носителях
Проблема искоренения широко рассматривалась для состояний глоточного носительства и повторяющихся эпизодов стрептококковой ангины, которую можно рассматривать как состояние, аналогичное рецидивирующему рожистому воспалению.Таким образом, опыт лечения рецидивирующего стрептококкового фарингита может определять направления разработки новых стратегий лечения рецидивирующего рожистого воспаления.
Пенициллин V для перорального применения является препаратом выбора ГАЗ-фарингита (104). Хотя у большинства пациентов клиническое улучшение наблюдается в течение первых нескольких дней лечения, для достижения максимального клиренса GAS из глотки требуется 10 дней для пероральной антибиотикотерапии (111). Однако, как и при рожистом воспалении, пенициллин не устранял ГАЗ из горла почти у 35% пациентов (112).В нескольких исследованиях оценивалась ликвидация состояний носительства стрептококков после неудачного лечения. Они определили уровень эрадикации после лечения одним пенициллином или в комбинации с рифампицином, цефалоспоринами, амоксициллин-клавуланатом, макролидами и клиндамицином. Показатели эрадикации носительства стрептококков в глотке были выше у пациентов, получавших клиндамицин или амоксициллин-клавуланат, по сравнению с лечением пенициллином V (113–115). Более того, несколько исследований подтвердили превосходство цефалоспоринов над пенициллинами в эрадикации ГАЗ (116–118).Цефалоспорины первого поколения (такие как цефалексин и цефадроксил) считаются альтернативой пенициллину, особенно при неэффективности лечения или гиперчувствительности к бета-лактамам (111, 119). Сообщается также, что 5-дневный курс азитромицина позволяет достичь 95% эрадикации ГАЗ (120). Эффективность эритромицина спорно обсуждается из-за растущей распространенности штаммов ГАЗ, устойчивых к эритромицину (121–123). В целом, исследования отоларингологии предполагают, что сочетание пенициллина с клиндамицином имеет самый высокий потенциал для искоренения состояний носительства стрептококков в глотке (124).Комбинация пенициллина с рифампицином также может быть эффективной (125). Основные исследования по искоренению глотки приведены в таблице 1.
Таблица 1 . Скорость эрадикации ГАЗ в глотке.
Комбинации антибиотиков для эрадикации стрептококков при роже
Учитывая клинический опыт глоточного носительства, при попытках искоренить стрептококковую инфекцию и предотвратить рецидив рожи следует в первую очередь рассматривать комбинацию антибиотиков в соответствии с противопоказаниями и потенциальным риском нежелательных явлений у конкретного пациента.Клиндамицин в сочетании с пенициллином является препаратом первого выбора для лечения опасных для жизни инфекций ГАЗ, таких как некротический фасциит, STSS, менингит и пневмония. Клиндамицин достигает достаточных бактериостатических внутриклеточных концентраций, подавляет выработку стрептококковых суперантигенов и других факторов вирулентности, таких как М-белок, а сочетание пенициллина с клиндамицином было более эффективным при лечении глубоких инфекций, таких как миозит ГАЗ, чем только β-лактамные антибиотики (126). Соответственно, такие комбинации были признаны наиболее эффективным средством лечения инвазивного S.pyogenes (127).
Лечение рожи в будущем: необходимость разработки новых стратегий лечения внутриклеточных стрептококковых резервуаров
Стратегии, направленные на устранение распространенных факторов риска рожистого воспаления и снижение предрасполагающих условий, в частности, лечение участков заражения патогенными микроорганизмами, такими как опрелость пальцев стопы, должны оставаться стандартной клинической практикой для предотвращения экзогенной реинфекции, но, очевидно, имеют ограниченное влияние на частоту рецидивов (61).Кроме того, из клинических испытаний и практического опыта очевидно, что текущие схемы приема антибиотиков с использованием β-лактамных антибиотиков могут контролировать острые инфекции ГАЗ, но недостаточны для предотвращения рецидива рожи (26, 35). Даже длительная антибиотикопрофилактика не снижает частоту рецидивов в постпрофилактический период (26, 35). Таким образом, текущие схемы приема антибиотиков и меры, направленные на предполагаемые факторы риска, не устраняют фактических причин рецидива рожи и нуждаются в переоценке.
Понимание внутриклеточного поглощения и персистенции стрептококков теперь может объяснить неэффективность профилактики. Пенициллины, амоксициллин и цефалоспорины плохо проникают через клеточные мембраны и не достигают достаточных внутриклеточных бактерицидных концентраций. Соответственно, внутриклеточные стрептококки защищены от β-лактамных антибиотиков (102). Бактерицидные уровни пенициллина в среде для культивирования клеток не разрушали внутриклеточные стрептококки, в то время как воздействие на эпителиальные клетки эритромицина или азитромицина могло эффективно убивать внутриклеточный ГАЗ в модели культуры клеток (103).Цефалотин и клиндамицин были более эффективны в уничтожении проглоченного ГАЗ, чем пенициллин, но менее эффективны, чем эритромицин или азитромицин (103, 104). Такие данные подтверждают гипотезу о том, что высокая частота рецидивов рожи и неспособность пенициллина предотвратить рецидивы рожистого воспаления действительно связаны с внутриклеточным поглощением стрептококков и отсутствием внутриклеточной активности пенициллина.
Разработка будущих стратегий лечения
Внедрение новых подходов выиграет от дополнительных доклинических и клинических испытаний антибиотиков.Эти испытания должны оценивать внутриклеточную эффективность антибиотиков в отношении грамположительных бактерий. Использование in vitro моделей инфицирования клеточной культурой внутриклеточного поглощения и персистенции стрептококков может дать дополнительную доклиническую информацию об антибиотической эффективности внутриклеточной эрадикации стрептококков, которая затем может быть использована в дальнейшем клиническом применении (103).
Другим подходом может быть разработка стрептококковых вакцин. Вакцинация эффективна для предотвращения инфекций или существенного улучшения течения инфекционных заболеваний, вызванных различными патогенами.М-белки считаются основными кандидатами на вакцину против ГАЗ. Специфические к белку M стрептококки антитела способствуют опсонизации и последующему удалению стрептококков путем фагоцитоза (128). Считается, что специфические к белку М антитела представляют собой основу опосредованного антителами иммунитета от инфекции GAS, однако они защищают только против GAS-организмов того же серотипа M (129). Таким образом, альтернативный подход к разработке вакцины, связанной с М-белком, основан на эпитопах, присутствующих в области С-повтора по направлению к карбоксиконцу М-белка, которые являются консервативными среди всех или большинства штаммов GAS.Однако М-белки могут вызывать перекрестные иммунные ответы против различных белков человека, которые, как считается, способствуют развитию стрептококковых осложнений, включая острую ревматическую лихорадку, постстрептококковые гломерулонефириты, аутоиммунные нейропсихатрические расстройства у детей, связанные со стрептококковыми инфекциями (PANDAS) (17, 18, 99), а также, возможно, псориаз (130). Предыдущие исследования показали, что ГАЗ-вакцина, специфичная для М-типа, может даже предрасполагать реципиентов к развитию острой ревматической лихорадки, а не защищать от последующих ГАЗ-инфекций (131).Следовательно, необходимо будет искать антигены, которые имеют минимальный шанс вызвать аутоиммунные последствия. Вакцины-кандидаты против стрептококков на основе М-белков и не-М-белков в настоящее время проходят доклиническую или предварительную клиническую разработку для профилактики постстрептококковых заболеваний (132). Потенциальный защитный эффект от рецидива рожи в настоящее время является предположительным.
Прогнозирование риска рецидива рожи у отдельного пациента
Было бы желательно провести тесты для анализа персистенции стрептококков и прогнозирования риска рецидивов рожистого воспаления, которые могут помочь определить необходимость дальнейших профилактических мер или схем лечения для каждого отдельного пациента.Измерение специфических к стрептококкам антител, таких как анти-стрептолизин O и анти-ДНКаза B (133), в сыворотке полезно в качестве индикатора недавней стрептококковой инфекции и может указывать на персистентность стрептококков (99, 134). Специфичность и чувствительность серологических тестов для оценки устойчивости стрептококков и прогнозирования рецидивов рожистого воспаления после предшествующего эпизода рожистого воспаления подробно не анализировались. Выращивание стрептококков от острого рожистого воспаления было успешным только в небольшом количестве случаев и, вероятно, не имеет смысла после заживления.Независимые от культивирования молекулярные методы, основанные на гене малой субъединицы рибосомной РНК (16S рРНК) из образцов ткани или крови (135), могут быть более многообещающим подходом для определения оставшегося присутствия стрептококков. Они позволят провести таксономическую дифференциацию, но применение таких молекулярных методов ограничено стоимостью секвенирования по Сэнгеру и будет зарезервировано для специальных показаний и учреждений. Альтернативно, диагностические подходы на основе ПЦР могут быть использованы для идентификации стрептококковой ДНК в ткани (136), но для этого потребуется биопсия кожи, ранее пораженной рожей.Таким образом, первый эпизод рожи в настоящее время является наиболее надежным предиктором рецидива и, вероятно, останется фактическим показанием для рассмотрения профилактических мер.
Соображения относительно внутриклеточной стойкости стрептококков для клинической практики
Внутриклеточная персистенция стрептококков может быть основной причиной пока необъяснимой высокой частоты рецидивов рожи. Поэтому при лечении рожи следует уделять особое внимание устранению возможных внутриклеточных стрептококковых резервуаров.Этот аспект актуален для двух показаний: (1) лечение первых эпизодов рожистого воспаления и (2) лечение рецидивов рожистого воспаления. Цели лечения по обоим показаниям в основном идентичны: борьба с острой инфекцией и предотвращение последующих эпизодов. Для этого потребуются антибиотики с достаточной внутриклеточной активностью. К ним относятся клиндамицин, макролиды и рифампицин. Комбинация клиндамицина или рифампицина с пенициллином в настоящее время является наиболее эффективным средством лечения инфекций ГАЗ. До тех пор, пока не доступна дополнительная информация из доклинических анализов и клинических испытаний по устойчивости и искоренению стрептококков при рожистом воспалении, эти комбинации антибиотиков следует рассматривать как лечение первой линии для предотвращения рецидива рожистого воспаления, либо путем лечения уже первых эпизодов рожистого воспаления, либо — по крайней мере — первый эпизод рецидива рожи.Дополнительные затраты и риски нежелательных явлений от комбинации этих антибиотиков в клинической практике могут быть компенсированы за счет снижения частоты рецидивов рожистого воспаления и избежания высоких затрат на здоровье и ухудшения здоровья в результате лечения рецидивирующего рожистого воспаления и прогрессирующей лимфедемы. Тщательный мониторинг частоты рецидивов будет иметь важное значение для определения эффективности этого подхода.
Взносы авторов
FJ и JP выполнили обзор литературы и оценку данных.JP предоставила клинические фотографии. MR провел эксперименты по внутриклеточному поглощению и персистенции стрептококков и создал фотографии на рисунке 4. FJ, MR и JP сотрудничали в написании рукописи.
Финансирование
FJ был поддержан грантом программы наставничества Международного общества дерматологов.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Благодарности
Эта рукопись посвящена памяти покойного Сингха Чхатвала, который внес большой вклад в современные знания о внутриклеточном поглощении и персистенции стрептококков.
Список литературы
1. Бернар П., Бедан С., Мунье М., Дени Ф., Катанцано Дж., Боннетблан Дж. М.. Стрептококковая причина рожи и целлюлита у взрослых. Микробиологическое исследование с использованием метода прямой иммунофлуоресценции. Arch Dermatol. (1989) 125: 779–82. DOI: 10.1001 / archderm.1989.01670180051004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
2. Эрикссон Б., Йоруп-Ронстром С., Каркконен К., Сджоблом А.С., Холм С.Е. Рожа: клинико-бактериологический спектр и серологические аспекты. Clin Infect Dis. (1996) 23: 1091–8. DOI: 10.1093 / Clinids / 23.5.1091
PubMed Аннотация | CrossRef Полный текст | Google Scholar
3. Сильяндер Т., Карппелин М., Вахакуопус С., Сырджанен Дж., Торопайнен М., Кере Дж. И др. Острый бактериальный ненекротический целлюлит в Финляндии: микробиологические данные. Clin Infect Dis. (2008) 46: 855–61. DOI: 10.1086 / 527388
PubMed Аннотация | CrossRef Полный текст | Google Scholar
4. Дженг А., Бехешти М., Ли Дж., Натан Р. Роль бета-гемолитических стрептококков в возникновении диффузного, некультивируемого целлюлита: перспективное исследование. Медицина (2010) 89: 217–26. DOI: 10.1097 / MD.0b013e3181e8d635
PubMed Аннотация | CrossRef Полный текст | Google Scholar
5. Стивенс Д.Л., Брайант А.Е. Импетиго, рожа и целлюлит.В: Ферретти Дж. Дж., Стивенс Д. Л., Фишетти В. А., редакторы. Streptococcus pyogenes: от фундаментальной биологии до клинических проявлений . Оклахома-Сити, Оклахома: Центр медицинских наук Университета Оклахомы (2016). п. 723–40.
Google Scholar
10. Goettsch WG, Bouwes Bavinck JN, Herings RM. Бремя болезни бактериального целлюлита и рожи голени в Нидерландах. J Eur Acad Dermatol Venereol. (2006) 20: 834–9. DOI: 10.1111 / j.1468-3083.2006.01657.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
11.Эллис Симонсен С.М., ван Орман Е.Р., Хэтч Б.Е., Джонс С.С., Грен Л.Х., Хегманн К.Т. и др. Заболеваемость целлюлитом в определенной популяции. Эпидемиол. Инфекция. (2006) 134: 293–9. DOI: 10.1017 / S095026880500484X
PubMed Аннотация | CrossRef Полный текст | Google Scholar
15. Хэй Р.Дж., Моррис-Джонс Р. Бактериальные инфекции. В: Griffiths CEM, Barker J, Bleiker T, Chalmers R, Creamer D, редакторы. Учебник дерматологии Рока, 9-е изд. . Оксфорд: John Wiley & Sons, Ltd (2016).п. 26.21–26.87.
Google Scholar
16. Пастернак М.С., Шварц М.Н. Целлюлит, некротический фасциит и инфекции подкожной ткани. В: Bennet JE, Dolin R, Blaser M, редакторы. Манделл, Дуглас и Беннеттс Принципы и практика инфекционных болезней , 8-е изд. Филадельфия, Пенсильвания: Elsevier Saunders (2015). п. 1194–215.
Google Scholar
18. Уокер М.Дж., Барнетт Т.К., МакАртур Дж. Д., Коул Дж. Н., Гиллен С. М., Хеннингем А. и др. Проявления заболевания и механизмы патогенеза стрептококков группы А. Clin Microbiol Rev. (2014) 27: 264–301. DOI: 10.1128 / CMR.00101-13
PubMed Аннотация | CrossRef Полный текст | Google Scholar
20. Хорн Д.Л., Забриски Дж. Б., Австрийский Р., Клири П. П., Ферретти Дж. Дж., Фишетти В. А. и др. Почему стрептококки группы А остались чувствительными к пенициллину? Отчет о симпозиуме. Clin Infect Dis. (1998) 26: 1341–5. DOI: 10.1086 / 516375
PubMed Аннотация | CrossRef Полный текст | Google Scholar
21. Чазан Б., Раз Р., Эдельштейн Х., Кеннес И., Гал В., Колоднер Р.Восприимчивость стрептококка группы А к противомикробным препаратам в северном Израиле: эпиднадзорное исследование. Устойчивость к микробным препаратам (2015) 21: 551–5. DOI: 10.1089 / mdr.2015.0040
PubMed Аннотация | CrossRef Полный текст | Google Scholar
22. Стивенс Д.Л., Бисно А.Л., Чемберс Х.Ф., Деллинджер Е.П., Гольдштейн Е.Дж., Горбач С.Л. и др. Практические рекомендации по диагностике и лечению инфекций кожи и мягких тканей: обновление 2014 г., подготовленное обществом инфекционистов Америки. Clin Infect Dis (2014) 59: e10–52. DOI: 10.1093 / cid / ciu296
CrossRef Полный текст | Google Scholar
23. Мартин Дж. М., Грин М., Барбадора К. А., Вальд ER. Устойчивые к эритромицину стрептококки группы А у школьников в Питтсбурге. N Engl. J Med. (2002) 346: 1200–6. DOI: 10.1056 / NEJMoa013169
PubMed Аннотация | CrossRef Полный текст | Google Scholar
24. Лю X, Шен X, Чанг Х, Хуанг Г, Фу З, Чжэн И и др. Высокая устойчивость к макролидам у штаммов Streptococcus pyogenes, выделенных от детей с фарингитом в Китае. Pediatr Pulmonol. (2009) 44: 436–41. DOI: 10.1002 / ppul.20976
PubMed Аннотация | CrossRef Полный текст | Google Scholar
25. Йорк М.К., Гиббс Л., Пердро-Ремингтон Ф., Брукс Г.Ф. Характеристика устойчивости к противомикробным препаратам у изолятов Streptococcus pyogenes из района залива Сан-Франциско в северной Калифорнии. J Clin Microbiol. (1999) 37: 1727–31.
PubMed Аннотация | Google Scholar
26. Томас К.С., Крук А.М., Нанн А.Дж., Фостер К.А., Мейсон Дж. М., Чалмерс Дж. Р. и др.Пенициллин для предотвращения рецидивирующего целлюлита ног. N Engl J Med. (2013) 368: 1695–703. DOI: 10.1056 / NEJMoa1206300
PubMed Аннотация | CrossRef Полный текст | Google Scholar
28. Damstra RJ, van Steensel MA, Boomsma JH, Nelemans P, Veraart JC. Рожа как признак субклинического первичного лимфатического отека: проспективное количественное сцинтиграфическое исследование 40 пациентов с односторонним рожистым воспалением голени. Br J Dermatol. (2008) 158: 1210–5. DOI: 10.1111 / j.1365-2133.2008.08503.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
29. Су Дж. К., Биканик Т. А., Хинан С., Мортимер П. С.. Лимфатические аномалии, выявленные лимфосцинтиграфией после целлюлита нижних конечностей. Br J Dermatol. (2008) 158: 1350–3. DOI: 10.1111 / j.1365-2133.2007.08423.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
30. Левелл, Нью-Джерси, Вингфилд К.Г., Гариох Дж. Дж. Тяжелая форма целлюлита нижних конечностей лучше всего диагностируется дерматологами и лечится совместно с первичной и вторичной медико-санитарной помощью. Br J Dermatol. (2011) 164: 1326–8. DOI: 10.1111 / j.1365-2133.2011.10275.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
31. Костер Дж. Б., Куллберг Б. Дж., Ван дер Меер Дж. В.. Рецидивирующее рожистое воспаление, несмотря на профилактику антибиотиками: анализ конкретных случаев. Нидерланды J Med. (2007) 65: 89–94.
PubMed Аннотация | Google Scholar
35. Далал А., Эскин-Шварц М., Мимуни Д., Рэй С., Дей В., Ходак Е. и др. Вмешательства для профилактики рецидивов рожи и целлюлита. Кокрановская база данных Syst Rev. (2017) 6: CD009758. DOI: 10.1002 / 14651858.CD009758.pub2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
37. Дюпюи А., Бенчихи Х., Ружо Дж. К., Бернар П., Вайллант Л., Чосидоу О. и др. Факторы риска рожистого воспаления ног (целлюлита): исследование случай-контроль. BMJ (1999) 318: 1591–4. DOI: 10.1136 / bmj.318.7198.1591
PubMed Аннотация | CrossRef Полный текст | Google Scholar
38. Cox NH. Отек как фактор риска множественных эпизодов целлюлита / рожи голени: серия с последующим наблюдением в сообществе. Br J Dermatol. (2006) 155: 947–50. DOI: 10.1111 / j.1365-2133.2006.07419.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
39. McNamara DR, Tleyjeh IM, Berbari EF, Lahr BD, Martinez J, Mirzoyev SA, et al. Прогностическая модель рецидивирующего целлюлита нижних конечностей в популяционной когорте. Arch Int Med. (2007) 167: 709–715. DOI: 10.1001 / archinte.167.7.709
PubMed Аннотация | CrossRef Полный текст | Google Scholar
41.Льюис С.Д., Питер Г.С., Гомес-Марин О., Бисно А.Л. Факторы риска рецидивирующего целлюлита нижних конечностей в медицинском центре для ветеранов США. Am J Med Sci. (2006) 332: 304–7. DOI: 10.1097 / 00000441-200612000-00002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
43. Медина Е., Роде М., Чхатвал Г.С. Внутриклеточное выживание пиогенов Streptococcus в полиморфно-ядерных клетках приводит к повышенной бактериальной вирулентности. Infect Immun. (2003) 71: 5376–80. DOI: 10.1128 / IAI.71.9.5376-5380.2003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
44. Медина Е., Гольдманн О., Топпель А.В., Чхатвал Г.С. Выживание Streptococcus pyogenes в фагоцитарных клетках хозяина: патогенный механизм персистенции и системной инвазии. J Infect Dis. (2003) 187: 597–603. DOI: 10.1086 / 373998
PubMed Аннотация | CrossRef Полный текст | Google Scholar
47. Халперн Дж., Холдер Р., Лэнгфорд, штат Нью-Джерси.Этническая принадлежность и другие факторы риска острого целлюлита нижних конечностей: проспективное исследование случай-контроль, проведенное в Великобритании. Br J Dermatol. (2008) 158: 1288–92. DOI: 10.1111 / j.1365-2133.2008.08489.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
48. Карппелин М., Сильяндер Т., Вуопио-Варкила Дж., Кере Дж., Хухтала Х., Вуэнто Р. и др. Факторы, предрасполагающие к острому и рецидивирующему бактериальному ненекротическому целлюлиту у госпитализированных пациентов: проспективное исследование случай-контроль. Clin Microbiol Infect. (2010) 16: 729–34. DOI: 10.1111 / j.1469-0691.2009.02906.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
49. Мэллон Э., Пауэлл С., Мортимер П., Райан Т.Дж.. Доказательства изменения клеточного иммунитета при лимфатическом отеке после мастэктомии. Br J Dermatol. (1997) 137: 928–33. DOI: 10.1111 / j.1365-2133.1997.tb01553.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
51. Вакас Б., Райан Т.Дж. Лимфедема: патофизиология и лечение в условиях ограниченных ресурсов — актуальность для программ борьбы с лимфатическим филяриатозом. Филария Дж. (2003) 2: 4. DOI: 10.1186 / 1475-2883-2-4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
52. Бьорнсдоттир С., Готтфредссон М., Торисдоттир А.С., Гуннарссон Г.Б., Рикардсдоттир Х., Кристьянссон М. и др. Факторы риска острого целлюлита нижней конечности: проспективное исследование случай-контроль. Clin Infect Dis. (2005) 41: 1416–22. DOI: 10.1086 / 497127
PubMed Аннотация | CrossRef Полный текст | Google Scholar
54.де Годой Ж.М., де Годой М.Ф., Валенте А, Камачо Э.Л., Пайва Э.В. Лимфосцинтиграфическая оценка у пациентов после рожистого воспаления. Лимфология (2000) 33: 177–80.
PubMed Аннотация | Google Scholar
57. Baddour LM, Bisno AL. Рецидивирующий целлюлит после операции коронарного шунтирования. Связь с поверхностной грибковой инфекцией в подкожной венэктомии конечностей. JAMA (1984) 251: 1049–52. DOI: 10.1001 / jama.1984.03340320035023
PubMed Аннотация | CrossRef Полный текст | Google Scholar
58.Мокни М., Дупуи А., Денгезли М., Дхауи Р., Буассида С., Амри М. и др. Факторы риска рожистого воспаления ног в Тунисе: многоцентровое исследование методом случай-контроль. Дерматология (2006) 212: 108–12. DOI: 10.1159 / 0000
PubMed Аннотация | CrossRef Полный текст | Google Scholar
59. Roujeau JC, Sigurgeirsson B, Korting HC, Kerl H, Paul C. Хронические дерматомикозы стопы как факторы риска острого бактериального целлюлита ноги: исследование случай-контроль. Дерматология (2004) 209: 301–7.DOI: 10.1159 / 000080853
PubMed Аннотация | CrossRef Полный текст | Google Scholar
60. Куирк М., Аюб Ф., МакКейб А., Боланд Ф., Смит Б., О’Салливан Р. и др. Факторы риска негнойного целлюлита ног: систематический обзор и метаанализ. Br J Dermatol. (2017) 177: 382–94. DOI: 10.1111 / bjd.15186
PubMed Аннотация | CrossRef Полный текст | Google Scholar
61. Кремер М., Цукерман Р., Авраам З., Раз Р. Долгосрочная антимикробная терапия для профилактики рецидивирующих инфекций мягких тканей. J Заражение. (1991) 22: 37-40. DOI: 10.1016 / 0163-4453 (91)
-3
PubMed Аннотация | CrossRef Полный текст | Google Scholar
62. Экелунд К., Скинхой П., Мадсен Дж., Конрадсен Х.Б. Инвазивные стрептококковые инфекции группы A, B, C и G в Дании, 1999-2002 гг .: эпидемиологические и клинические аспекты. Clin Microb Infect. (2005) 11: 569–76. DOI: 10.1111 / j.1469-0691.2005.01169.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
63.Баддур Л.М., Бисно А.Л. Бета-гемолитический стрептококковый целлюлит не группы А. Связь с венозным и лимфатическим нарушением. Am J Med. (1985) 79: 155–9. DOI: 10.1016 / 0002-9343 (85)
-8PubMed Аннотация | CrossRef Полный текст | Google Scholar
64. Молинари Г., Талай С.Р., Валентин-Вейганд П., Роде М., Чхатвал Г.С. Фибронектин-связывающий белок Streptococcus pyogenes, SfbI, участвует в интернализации стрептококков группы А эпителиальными клетками. Infect Immun. (1997) 65: 1357–63.
PubMed Аннотация | Google Scholar
65. ЛаПента Д., Рубенс С., Чи Е., Клири П.П. Стрептококки группы А эффективно проникают в клетки респираторного эпителия человека. Proc. Natl. Акад. Sci. США. (1994) 91: 12115–9. DOI: 10.1073 / pnas.91.25.12115
PubMed Аннотация | CrossRef Полный текст | Google Scholar
66. Ниман Р., Келлер Н., Барзилай А., Коренман З., Села С. Распространенность гена, связанного с интернализацией, prtF1, среди сохраняющихся штаммов стрептококков группы А, выделенных от бессимптомных носителей. Lancet (1998) 352: 1974–7. DOI: 10.1016 / S0140-6736 (97) 12452-7
PubMed Аннотация | CrossRef Полный текст | Google Scholar
67. Остерлунд А., Энгстранд Л. Внутриклеточное проникновение и выживаемость Streptococcus pyogenes в клетках респираторного эпителия in vitro . Acta отоларингол. (1995) 115: 685–8. DOI: 10.3109 / 00016489509139387
PubMed Аннотация | CrossRef Полный текст | Google Scholar
68. Osterlund A, Engstrand L.Внутриклеточное убежище для Streptococcus pyogenes в эпителии миндалин человека — исследования бессимптомных носителей и культивированных биопсий in vitro. Acta отоларингол. (1997) 117: 883–888. DOI: 10.3109 / 0001648970
19
PubMed Аннотация | CrossRef Полный текст | Google Scholar
69. Остерлунд А., Попа Р., Никкила Т., Шейниус А., Энгстранд Л. Внутриклеточный резервуар Streptococcus pyogenes in vivo : возможное объяснение рецидивирующего фаринготонзиллита. Ларингоскоп (1997) 107: 640–7. DOI: 10.1097 / 00005537-199705000-00016
PubMed Аннотация | CrossRef Полный текст | Google Scholar
70. Молинари Г., Чхатвал Г.С. Инвазия и выживаемость пиогенов Streptococcus в эукариотических клетках коррелирует с источником клинических изолятов. J Infect Dis. (1998) 177: 1600–7. DOI: 10.1086 / 515310
PubMed Аннотация | CrossRef Полный текст | Google Scholar
71. Jadoun J, Ozeri V, Burstein E, Skutelsky E, Hanski E, Sela S.Белок F1 необходим для эффективного проникновения Streptococcus pyogenes в эпителиальные клетки. J Infect Dis. (1998) 178: 147–58. DOI: 10.1086 / 515589
PubMed Аннотация | CrossRef Полный текст | Google Scholar
72. Jadoun J, Burstein E, Hanski E, Sela S. Белки M6 и F1 необходимы для эффективной инвазии стрептококков группы A в культивируемые эпителиальные клетки. Adv Exp Med Biol. (1997) 418: 511–5. DOI: 10.1007 / 978-1-4899-1825-3_121
PubMed Аннотация | CrossRef Полный текст | Google Scholar
73.Dombek PE, Cue D, Sedgewick J, Lam H, Ruschkowski S, Finlay BB, et al. Высокочастотная внутриклеточная инвазия эпителиальных клеток стрептококками серотипа M1 группы A: инвазия, опосредованная белком M1, и перестройки цитоскелета. Mol Microbiol. (1999) 31: 859–70. DOI: 10.1046 / j.1365-2958.1999.01223.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
74. Беннетт-Вуд В.Р., Карапетис Дж. Р., Робинс-Браун Р.М. Способность клинических изолятов стрептококков группы А прикрепляться к эпителиальным клеткам HEp-2 и проникать в них. J Med Microbiol. (1998) 47: 899–906. DOI: 10.1099 / 00222615-47-10-899
PubMed Аннотация | CrossRef Полный текст | Google Scholar
75. Loof TG, Rohde M, Chhatwal GS, Jung S, Medina E. Вклад дендритных клеток в защиту хозяина от Streptococcus pyogenes. J Infect Dis. (2007) 196: 1794–803. DOI: 10.1086 / 523647
PubMed Аннотация | CrossRef Полный текст | Google Scholar
76. Хайдан А., Талай С.Р., Роде М., Срипракаш К.С., Карри Б.Дж., Чхатвал Г.С.Глоточное носительство стрептококков группы C и G и острая ревматическая лихорадка у аборигенов. Ланцет (2000) 356: 1167–9. DOI: 10.1016 / S0140-6736 (00) 02765-3
PubMed Аннотация | CrossRef Полный текст | Google Scholar
77. Роде М., Талай С.Р., Расмуссен М. Молекулярные механизмы Streptococcus dysgalactiae subsp equisimilis, обеспечивающие внутрисосудистую персистенцию. Microbes Infect. (2012) 14: 329–34. DOI: 10.1016 / j.micinf.2011.10.008
PubMed Аннотация | CrossRef Полный текст | Google Scholar
78. Озери В., Розеншин И., Мошер Д.Ф., Фасслер Р., Хански Э. Роль интегринов и фибронектина в проникновении пиогенов Streptococcus в клетки через белок F1. Mol Microbiol. (1998) 30: 625–37. DOI: 10.1046 / j.1365-2958.1998.01097.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
79. Schrager HM, Rheinwald JG, Wessels MR. Капсула гиалуроновой кислоты и роль проникновения стрептококков в кератиноциты при инвазивной кожной инфекции. J Clin Invest. (1996) 98: 1954–8. DOI: 10.1172 / JCI118998
PubMed Аннотация | CrossRef Полный текст | Google Scholar
80. Роде М., Клири П.П. Адгезия и инвазия Streptococcus pyogenes в клетки-хозяева и клиническое значение внутриклеточных стрептококков. В: Ферретти Дж. Дж., Стивенс Д. Л., Фишетти В. А., редакторы. Streptococcus pyogenes: от базовой биологии до клинических проявлений. Оклахома-Сити, Оклахома: Центр медицинских наук Университета Оклахомы (2016).п. 547–86.
Google Scholar
81. Молинари Г., Роде М., Гусман, Калифорния, Чхатвал Г.С. Два различных пути инвазии Streptococcus pyogenes в нефагоцитарные клетки. Cell Microbiol. (2000) 2: 145–54. DOI: 10.1046 / j.1462-5822.2000.00040.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
82. Роде М., Мюллер Э., Чхатвал Г.С., Талай С.Р. Кавеолы клетки-хозяина действуют как входной порт для стрептококков группы А. Cell Microbiol. (2003) 5: 323–42. DOI: 10.1046 / j.1462-5822.2003.00279.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
86. Роде М., Чхатвал Г.С. Прилипание и инвазия стрептококков к эукариотическим клеткам и их роль в патогенезе болезней. Curr. Темы Microbiol Immunol. (2013) 368: 83–110. DOI: 10.1007 / 82_2012_281
PubMed Аннотация | CrossRef Полный текст | Google Scholar
88. Роде М., Грэм Р.М., Браницки-Хайнеманн К., Борхерс П., Пройс С., Шлейхер И. и др.Различия в ароматическом домене гомологичных стрептококковых белков, связывающих фибронектин, запускают различные механизмы клеточной инвазии и выживаемость. Cell Microbiol. (2011) 13: 450–68. DOI: 10.1111 / j.1462-5822.2010.01547.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
89. Barnett TC, Liebl D, Seymour LM, Gillen CM, Lim JY, Larock CN, et al. Глобально распространенный клон M1T1 группы A Streptococcus уклоняется от аутофагии для внутриклеточной репликации. Клеточный микроб-хозяин (2013) 14: 675–82. DOI: 10.1016 / j.chom.2013.11.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
90. Кобаяши С.Д., Браутон К.Р., Уитни А.Р., Войич Дж. М., Шван Т. Г., Массер Дж. М. и др. Бактериальные патогены модулируют программу дифференцировки апоптоза нейтрофилов человека. Proc Natl Acad Sci USA. (2003) 100: 10948–53. DOI: 10.1073 / pnas.1833375100
PubMed Аннотация | CrossRef Полный текст | Google Scholar
91.Сименс Н., Патенж Н., Отто Дж., Фидлер Т., Крайкемейер Б. Streptococcus pyogenes Связывание плазминогена / плазмина M49 облегчает инвазию кератиноцитов через интегрин-интегрин-связанные киназные пути (ILK) и защищает от гибели макрофагов. J. Biol Chem. (2011) 286: 21612–22. DOI: 10.1074 / jbc.M110.202671
PubMed Аннотация | CrossRef Полный текст | Google Scholar
92. Тулин П., Йоханссон Л., Лоу ДЭ, Ган Б.С., Котб М., МакГир А. и др. Жизнеспособные стрептококки группы А в макрофагах при острой инфекции мягких тканей. PLoS Med. (2006) 3: e53. DOI: 10.1371 / journal.pmed.0030053
PubMed Аннотация | CrossRef Полный текст | Google Scholar
93. Амелунг С., Нерлих А., Роде М., Спеллерберг Б., Коул Дж. Н., Низет В. и др. Фибронектин-связывающий белок FbaB-типа Streptococcus pyogenes способствует специфической инвазии в эндотелиальные клетки. Cell Microbiol. (2011) 13: 1200–11. DOI: 10.1111 / j.1462-5822.2011.01610.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
94.Денни Ф.В., Ваннамейкер Л.В., Бринк В.Р., Раммелкамп СН-младший Кастер EA. Профилактика ревматизма; лечение предшествующей стрептококковой инфекции. J Am Med Assoc. (1950) 143: 151–3. DOI: 10.1001 / jama.1950.02
0001001PubMed Аннотация | CrossRef Полный текст | Google Scholar
95. Бисно А. Л., Гербер М. А., Гвалтни Дж. М. Младший Каплан Е. Л., Американское общество инфекционных болезней Р. Х. Шварца. Практическое руководство по диагностике и лечению стрептококкового фарингита группы А.Общество инфекционных болезней Америки. Clin Infect Dis. (2002) 35: 113–25. DOI: 10.1086 / 340949
PubMed Аннотация | CrossRef Полный текст | Google Scholar
97. Чарни Э., Байнум Р., Элдредж Д., Фрэнк Д., Мак-Уинни Дж. Б., Макнабб Н. и др. Насколько хорошо пациенты принимают пенициллин перорально? Совместное исследование частной практики. Педиатрия (1967) 40: 188–95.
PubMed Аннотация | Google Scholar
98. Pichichero ME. Рост числа случаев неудачного лечения пенициллином при стрептококковом тонзиллофарингите группы А: новая роль цефалоспоринов? Pediatr Infect Dis J. (1991) 10: S50–5. DOI: 10.1097 / 00006454-1901-00011
PubMed Аннотация | CrossRef Полный текст | Google Scholar
99. Орефики Дж., Кардона Ф., Кокс С.Дж., Каннингем М.В. Детские аутоиммунные психоневрологические расстройства, связанные со стрептококковыми инфекциями (PANDAS). В: Ферретти Дж. Дж., Стивенс Д. Л., Фишетти В. А., редакторы. Streptococcus pyogenes: от фундаментальной биологии до клинических проявлений . Оклахома-Сити, Оклахома: Центр медицинских наук Университета Оклахомы (2016).п. 827–68.
Google Scholar
100. Brandt CM, Allerberger F, Spellerberg B, Holland R, Lutticken R, Haase G. Характеристика последовательных изолятов Streptococcus pyogenes от пациентов с фарингитом и неэффективным бактериологическим лечением: специальная ссылка на prtF1 и sic / drs. J Infect Dis. (2001) 183: 670–4. DOI: 10.1086 / 318542
PubMed Аннотация | CrossRef Полный текст | Google Scholar
101. Села С., Нееман Р., Келлер Н., Барзилай А.Связь между бессимптомным носительством Streptococcus pyogenes и способностью штаммов прилипать к культивируемым эпителиальным клеткам и усваиваться ими. J Med Microbiol. (2000) 49: 499–502. DOI: 10.1099 / 0022-1317-49-6-499
PubMed Аннотация | CrossRef Полный текст | Google Scholar
103. Каплан Е.Л., Чхатвал Г.С., Роде М. Снижение способности пенициллина уничтожать проглоченные стрептококки группы А из эпителиальных клеток: клинические и патогенетические последствия. Clin Infect Dis. (2006) 43: 1398–406. DOI: 10.1086 / 508773
PubMed Аннотация | CrossRef Полный текст | Google Scholar
104. Шварц Р.Х., Винцен Р.Л., младший Педрейра Ф., Фероли Е.Дж., Мелла Г.В., Гуандоло В.Л. Пенициллин V для лечения стрептококкового фаринготонзиллита. Рандомизированное испытание семи против десятидневной терапии. JAMA (1981) 246: 1790–5. DOI: 10.1001 / jama.1981.03320160022023
PubMed Аннотация | CrossRef Полный текст | Google Scholar
105.Килберн С.А., Фезерстоун П., Хиггинс Б., Бриндл Р. Вмешательства при целлюлите и рожистом воспалении. Кокрановская база данных Syst Rev. (2010). 6, 1–69. DOI: 10.1002 / 14651858.CD004299.pub2
CrossRef Полный текст | Google Scholar
106. Смит Э., Патель М., Томас К. Какие результаты сообщаются в исследованиях целлюлита? Результаты обзора результатов, включенных в исследования целлюлита и опроса по установлению приоритетов пациентов. Br J Дерматол . (2017) 178: 1028–34. DOI: 10.1111 / bjd.16235
PubMed Аннотация | CrossRef Полный текст | Google Scholar
107. Montravers P, Snauwaert A, Welsch C. Текущие руководящие принципы и рекомендации по лечению инфекций кожи и мягких тканей. Curr Opin Infect Dis. (2016) 29: 131–8. DOI: 10.1097 / QCO.0000000000000242
PubMed Аннотация | CrossRef Полный текст | Google Scholar
110. Винкен А.Г., Ли Дж.З., Балан Д.А., Риттенхаус Б.Е., Вилке Р.Дж., Гудман С. Сравнение линезолида с оксациллином или ванкомицином в эмпирическом лечении целлюлита в больницах США. Am. J. Ther. (2003) 10: 264–74. DOI: 10.1097 / 00045391-200307000-00006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
113. Орлинг А., Стьернквист-Десатник А., Шален С., Камме С. Клиндамицин при персистирующем стрептококковом фаринготонзиллите после лечения пенициллином. Scand J Infect Dis. (1994) 26: 535–41. DOI: 10.3109 / 0036554940
11
PubMed Аннотация | CrossRef Полный текст | Google Scholar
114. Танз Р. Р., Пончер Дж. Р., Коридон К. Э., Кабат К., Йогев Р., Шульман СТ.Лечение клиндамицином хронического глоточного носительства стрептококков группы А. J Pediatr. (1991) 119: 123–8. DOI: 10.1016 / S0022-3476 (05) 81052-2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
115. Каплан Э.Л., Джонсон ДР. Уничтожение стрептококков группы А из верхних дыхательных путей с помощью амоксициллина с клавуланатом после неэффективности перорального лечения пенициллином V. J Pediatr. (1988) 113: 400–3. DOI: 10.1016 / S0022-3476 (88) 80291-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
116.Ручей I, Гобер А.Е. Скорость эрадикации бета-гемолитических стрептококков группы А у детей с фаринго-тонзиллитом амоксициллином и цефдиниром. Int J Pediatr Otorhinolaryngol. (2009) 73: 757–9. DOI: 10.1016 / j.ijporl.2009.02.004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
117. Кейси-младший, Пичичеро, штат Мэн. Мета-анализ лечения цефалоспорином и пенициллином стрептококкового тонзиллофарингита группы А у детей. Педиатрия (2004) 113: 866–82.DOI: 10.1542 / педс.113.4.866
PubMed Аннотация | CrossRef Полный текст | Google Scholar
118. Брук I. Антибактериальная терапия острой группы стрептококкового фаринготонзиллита: короткий курс по сравнению с традиционными 10-дневными пероральными схемами. Детские лекарства (2002) 4: 747–54. DOI: 10.2165 / 00128072-200204110-00006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
119. Гербер М.А., Рэндольф М.Ф., Чанатри Дж., Райт Л.Л., Андерсон Л.Р., Каплан Е.Л. Один раз в день терапия стрептококкового фарингита цефадроксилом. J Pediatr. (1986) 109: 531–7. DOI: 10.1016 / S0022-3476 (86) 80139-1
PubMed Аннотация | CrossRef Полный текст | Google Scholar
120. Морита Дж. Я., Кан Э., Томпсон Т., Лаклер Л., Билл Б., Герарди Дж. И др. Влияние азитромицина на ротоглоточное носительство Streptococcus группы А и носоглоточное носительство устойчивых к макролидам Streptococcus pneumoniae . Pediatr Infect Dis J. (2000) 19: 41–6. DOI: 10.1097 / 00006454-200001000-00009
PubMed Аннотация | CrossRef Полный текст | Google Scholar
123.Desjardins M, Delgaty KL, Ramotar K, Seetaram C, Toye B. Распространенность и механизмы устойчивости к эритромицину в группе A и группе B Streptococcus : значение для сообщения результатов восприимчивости. J Clin Microbiol. (2004) 42: 5620–3. DOI: 10.1128 / JCM.42.12.5620-5623.2004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
124. Мартин Дж. М.. Состояние носителя Streptococcus pyogenes . В: Ферретти Дж. Дж., Стивенс Д. Л., Фишетти В. А., редакторы. Streptococcus pyogenes . Оклахома-Сити, Оклахома: Центр медицинских наук Университета Оклахомы (2016). п. 587–600.
Google Scholar
125. Чаудхари С., Билински С.А., Хеннесси Дж.Л., Солер С.М., Уоллес С.Е., Шахт С.М. и др. Пенициллин V и рифампицин для лечения стрептококкового фарингита группы А: рандомизированное испытание 10-дневного пенициллина против 10-дневного пенициллина с рифампицином в течение последних 4 дней терапии. J Pediatr. (1985) 106: 481–6. DOI: 10.1016 / S0022-3476 (85) 80687-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
126. Сильва-Коста С., Фриаес А., Рамирес М., Мело-Кристино Дж. Устойчивые к макролидам Streptococcus pyogenes: распространенность и стратегии лечения. Expert Rev Anti-Infect Ther. (2015) 13: 615–28. DOI: 10.1586 / 14787210.2015.1023292
PubMed Аннотация | CrossRef Полный текст | Google Scholar
127. Зимбельман Дж., Палмер А., Тодд Дж. Улучшение результатов лечения клиндамицином по сравнению с лечением бета-лактамными антибиотиками для инвазивной инфекции Streptococcus pyogenes. Pediatr Infect Dis. J. (1999) 18: 1096–100. DOI: 10.1097 / 00006454-1990-00014
PubMed Аннотация | CrossRef Полный текст | Google Scholar
128. Lancefield RC. Антигенный комплекс Streptococcus haemolyticus: I. демонстрация типоспецифического вещества в экстрактах Streptococcus haemolyticus. J Exp Med. (1928) 47: 91–103. DOI: 10.1084 / jem.47.1.91
CrossRef Полный текст | Google Scholar
129. Джонс К.Ф., Фишетти В.А.Важность местоположения связывания антител с белком M6 для опсонизации и фагоцитоза стрептококков M6 группы A. J Exp Med. (1988) 167: 1114–23. DOI: 10.1084 / jem.167.3.1114
PubMed Аннотация | CrossRef Полный текст | Google Scholar
130. Besgen P, Trommler P, Vollmer S, Prinz JC. Эзрин, маспин, пероксиредоксин 2 и белок теплового шока 27: потенциальные мишени аутоиммунного ответа, вызванного стрептококками, при псориазе. J Immunol. (2010) 184: 5392–402.DOI: 10.4049 / jimmunol.00
PubMed Аннотация | CrossRef Полный текст | Google Scholar
132. Дейл Дж. Б., Батцлофф М. Р., Клири П. П., Кортни Х. С., Гуд М. Ф., Гранди Дж. И др. Современные подходы к групповой разработке стрептококковой вакцины. В: Ферретти Дж. Дж., Стивенс Д. Л., Фишетти В. А., редакторы. Streptococcus pyogenes: от фундаментальной биологии до клинических проявлений . Оклахома-Сити, Оклахома: Центр медицинских наук Университета Оклахомы (2016). п. 993–1040.
Google Scholar
133.Спеллерберг Б., Брандт С. Лабораторная диагностика Streptococcus pyogenes (стрептококки группы А). В: Ферретти Дж. Дж., Стивенс Д. Л., Фишетти В. А., редакторы. Streptococcus pyogenes: от фундаментальной биологии до клинических проявлений . Оклахома-Сити, Оклахома: Центр медицинских наук Университета Оклахомы (2016). п. 931–46.
Google Scholar
134. Шет А, Каплан ЭЛ. Клиническое использование и интерпретация тестов на антитела к стрептококкам группы А: практический подход для педиатра или терапевта. Pediatr Infect Dis J. (2002) 21: 420–6. DOI: 10.1097 / 00006454-200205000-00014
CrossRef Полный текст | Google Scholar
Оценка лечения антибиотиками в зависимости от продолжительности госпитализации пациентов с рожей и бактериальным целлюлитом
Рожистое воспаление и целлюлит — это два кожных заболевания, которые представляют собой серьезную клиническую проблему и представляют интерес для врачей различных специальностей. Каждый год новые результаты исследований и новые предлагаемые руководства приводят к новым предложениям по оптимальному ведению обоих этих клинических состояний.Однако проблема выбора оптимального лечения остается актуальной, прежде всего потому, что чувствительность к антибиотикам наиболее распространенных патогенов, вызывающих эти кожные заболевания, локально различается и может меняться со временем. Несмотря на значительную заболеваемость, связанную с рожей и бактериальным целлюлитом, данные об эффективности антибиотиков, используемых в терапии этих заболеваний, ограничены [7]. Kilburn et al. [8] в Кокрановском метаанализе оценили 25 исследований бактериальной кожной инфекции, но не смогли четко определить окончательные выводы относительно оптимальной терапии противомикробного целлюлита.
На основании результатов, полученных в нашем исследовании, мы предполагаем, что лечение бактериальной инфекции кожи с помощью комбинированной терапии амоксициллин + клавулановая кислота должно приводить к наиболее быстрому клиническому улучшению, что сокращает продолжительность пребывания в больнице и, следовательно, снижает затраты. лечения больных рожей или бактериальным целлюлитом. Мы отметили, что быстрое улучшение в группе пациентов, получавших амоксициллин / клавулановую кислоту, редко было связано с необходимостью использования других антибактериальных средств, либо одновременно, либо последовательно, что может дополнительно поддерживать использование этих препаратов в качестве лечения первой линии.Однако к нашим наблюдениям следует относиться с осторожностью из-за ретроспективного характера анализа, на который, возможно, повлиял ряд мешающих факторов, которые не были должным образом рассмотрены в исследовании (например, личные предпочтения врачей при выборе конкретного варианта лечения, сопутствующие заболевания, тяжесть инфекции и др.).
В ретроспективном исследовании, проведенном Bishare et al. [9], пациенты, получавшие пенициллин, нуждались в более короткой госпитализации. В том же исследовании эти исследователи не обнаружили значительной пользы от использования антибиотиков, кроме пенициллина.В анализе Krasagakis et al. [10], наиболее часто используемым антибиотиком был пенициллин G, вводимый внутривенно. Эти авторы обнаружили, что группа, получавшая этот антибиотик этим путем, имела самую короткую среднюю продолжительность лихорадки после начала лечения, чем все другие группы пациентов. В свою очередь, исследование, проведенное Perelló-Alzamora et al. [11] показали, что у большинства пациентов наблюдалось улучшение или их вылечили с помощью амоксициллина в сочетании с клавулановой кислотой, без серьезных побочных эффектов этой терапии.Для пациентов, которые не могли переносить эту комбинацию антибиотиков, использовалась альтернативная форма лечения, а именно клиндамицин или хинолоны, с удовлетворительным эффектом.
В настоящее время нет однозначного консенсуса относительно эмпирической терапии рожи и бактериального целлюлита. Руководства Великобритании [12, 13] по-прежнему рекомендуют амоксициллин или флуклоксациллин в качестве лечения первой линии в большинстве случаев бактериального дерматита и инфекции подкожной ткани, вызванной β-гемолитическими стрептококками, S.aureus , или когда возбудитель не идентифицирован. В случае аллергии на пенициллин в качестве подходящей альтернативы рекомендуются макролидные антибиотики или клиндамицин.
Мы также обнаружили, что сопутствующая хроническая венозная недостаточность нижних конечностей является существенным фактором увеличения продолжительности госпитализации. Это заболевание вызывает не только застой в венозном кровотоке, но и в некоторых случаях может привести к лимфатическому отеку, который многими исследователями считается одним из основных факторов, предрасполагающих человека к развитию рожи и бактериального целлюлита. что касается его повторения.Dupuy et al. [14] в своем исследовании обнаружили, что лимфедема играет наиболее важную роль в патомеханизме бактериальной инфекции кожи. Павлоцкий и др. [15] также пришли к аналогичному выводу, подчеркнув, что факторами, способствующими рецидиву заболевания, являются, в частности, венозная недостаточность, лимфатический отек, а также сосуществующий опоясывающий лишай стопы. Данные о сосуществовании анемии у пациентов, госпитализированных по поводу бактериального целлюлита, и ее влиянии на течение заболевания менее очевидны.У наших пациентов клинически значимая анемия, определяемая как концентрация гемоглобина <10 г / дл, оказалась фактором, значительно увеличившим продолжительность пребывания в палате. Одно из возможных объяснений этого состоит в том, что пациенты с анемией обычно находятся в более плохом общем состоянии по сравнению с другими субъектами. Кроме того, более низкий уровень гемоглобина обеспечивает меньшее поступление кислорода и, таким образом, может усилить ишемию, спровоцированную кожной инфекцией, что приведет к усилению повреждения тканей.
Следует подчеркнуть, что наши результаты имеют ряд ограничений, которые необходимо учитывать при интерпретации результатов.Во-первых, исследование проводилось на относительно небольшом количестве пациентов из одного центра; в идеале исследование следует повторить в других больницах. Еще одним важным ограничением является ретроспективный характер исследования, которое не может полностью прояснить причины выбора одного варианта терапии по сравнению с другим; в результате многие смешивающие факторы не могут быть исключены из исследования. Отсутствие рандомизированного распределения по конкретному варианту лечения могло дополнительно повлиять на результаты, поскольку анализируемые группы могут значительно различаться с точки зрения тяжести заболевания, а также тяжести сопутствующих заболеваний.Однако мы предполагаем, что полученные результаты могут иметь практическое значение, поскольку они могут помочь оптимизировать рекомендации по лечению рожи и бактериального целлюлита, явно указав комбинацию амоксициллин + клавулановую кислоту как более эффективную форму антибактериальной терапии. по сравнению с другими препаратами. Несомненно, наши наблюдения нуждаются в подтверждении в проспективном исследовании на большей группе пациентов, которое должно позволить проверить и возможное подтверждение выводов, сделанных в текущем исследовании.
Целлюлит: информация для врачей | CDC
Целлюлит — это инфекция, которая возникает в подкожных тканях. Это может быть вызвано несколькими бактериями, но эта страница будет посвящена целлюлиту, вызываемому Streptococcus pyogenes (также называемым Streptococcus группы A или стрептококком группы A).
Этиология
- S. pyogenes — один из наиболее частых возбудителей целлюлита.
- С.pyogenes — это грамположительные кокки, которые растут цепочками (см. рисунок 1). Они проявляют β -гемолиз (полный гемолиз) при выращивании на чашках с кровяным агаром. Они принадлежат к группе А в системе классификации β-гемолитического стрептококка Лэнсфилда и, таким образом, также называются стрептококками группы А.
Рис. 1. Streptococcus pyogenes (Streptococcus группы А) на окраске по Граму. Источник: Библиотека изображений общественного здравоохранения, CDC
.Клинические особенности
Целлюлит поражает структуры, расположенные глубже, чем участки, пораженные импетиго или рожей. 1 В результате пораженная кожа обычно имеет розоватый оттенок с менее выраженной границей по сравнению с рожей, которая проявляется с хорошо разграниченными границами и ярко-красным цветом. 1
Местные признаки воспаления (тепло, эритема и боль) присутствуют в большинстве случаев целлюлита. 2 Могут присутствовать систематические симптомы, такие как лихорадка, озноб и недомогание, которые могут сопровождаться лимфангитом и, реже, бактериемией. 1 Также может присутствовать повышенное количество лейкоцитов.
Трансмиссия
Прямая передача стрептококка группы A от человека к человеку может происходить при контакте с поражениями кожи или попадании в дыхательные пути. 3 У людей с активной инфекцией вероятность передачи стрептококка группы А выше, чем у бессимптомных носителей. Местная дерматофитная инфекция (например, стопа спортсмена) может служить порталом входа для стрептококка группы А. 1
Факторы риска
Нарушение кожного барьера, например наличие язв, ран или грибковых кожных инфекций (например,g., спортивная стопа), является фактором риска развития целлюлита. 1,4,5 В анамнезе был целлюлит; венозная недостаточность, наличие хронических отеков или нарушение лимфодренажа конечностей; ожирение; и употребление инъекционных наркотиков также были определены как факторы риска целлюлита. 1,4,6
Диагностика и тестирование
Диагноз целлюлита обычно ставится клинически.
В отношении целлюлита Американское общество инфекционных болезней (IDSA) не рекомендует рутинный сбор культур, включая кровь, кожные аспираты, биопсии или мазки. 7 Однако посев крови и микробиологическое исследование, а также посев кожных аспиратов, биопсий и мазков могут помочь при подозрении на атипичные патогены. IDSA рекомендует эти процедуры пациентам с ослабленным иммунитетом, иммерсионными травмами или укусами животных. 7 Ожидание результатов посева никогда не должно откладывать начало лечения; однако, если они доступны, результаты посева можно использовать для подбора антибактериальной терапии.
Лечение
Для типичных случаев негнойного целлюлита IDSA рекомендует лечение антибиотиком, активным против стрептококков. 7 Из-за сложности определения возбудителя, вызывающего большинство случаев целлюлита, врачи могут выбрать антибиотики, которые охватывают как Staphylococcus aureus , так и стрептококк группы А.
Стрептококк группы А остается чувствительным к бета-лактамным антибиотикам. Легкую форму целлюлита можно лечить пероральными антибиотиками, включая пенициллин, цефалоспорины (например, цефалексин), диклоксациллин или клиндамицин. Если присутствуют признаки системной инфекции, можно рассмотреть возможность внутривенного введения антибиотиков, таких как пенициллин, цефтриаксон, цефазолин или клиндамицин. 7
Рекомендуемая продолжительность лечения антибиотиками для большинства случаев целлюлита составляет 5 дней. 7 Случаи, в которых не было улучшения в течение этого периода времени, могут потребовать более продолжительного лечения. 7
Кроме того, для снижения риска рецидива инфекции рекомендуется возвышение пораженного участка и лечение предрасполагающих факторов (например, отек, основные кожные заболевания). 7
Прогноз и осложнения
Иногда целлюлит может приводить к бактериемии и редко к инфекциям глубоких тканей, таким как септический тромбофлебит, гнойный артрит, остеомиелит и инфекционный эндокардит.Пациенты с нарушением лимфодренажа конечностей или те, кому было выполнено удаление подкожной вены для аортокоронарного шунтирования, подвергаются повышенному риску рецидива инфекции. 1
Профилактика
Распространение всех типов стрептококковой инфекции группы А можно уменьшить, соблюдая правила гигиены рук, особенно после кашля и чихания, и соблюдая правила дыхания (например, прикрываясь кашлем или чиханием). Раннее выявление и лечение поверхностных повреждений кожи также является ключом к профилактике целлюлита.Пациентов с рецидивирующим целлюлитом нижних конечностей следует обследовать на предмет наличия дерматофитии стопы и лечить при ее наличии. Травматические или укушенные раны следует очищать и лечить соответствующим образом (например, антибиотикопрофилактика, хирургическая обработка раны по показаниям) для предотвращения вторичных инфекций. 7
Эпидемиология
Среди примерно 23 650 случаев (7,26 на 100 000 населения) инвазивной стрептококковой инфекции группы А в США, которые произошли в 2017 году, почти 45% пациентов страдали целлюлитом, согласно данным наблюдения за активными бактериальными ядрами (ABC).Однако лишь небольшая часть целлюлита приводит к инвазивным заболеваниям. CDC не отслеживает заболеваемость неинвазивной стрептококковой инфекцией группы А. Следовательно, частота общего целлюлита, вызванного стрептококком группы А, вероятно, будет намного выше.
Список литературы
- Стивенс Д.Л., Брайант А.Е. Импетиго, рожа и целлюлит — внешний значок. В Ferretti JJ, Стивенс Д.Л., Фишетти В.А., редакторы. Streptococcus pyogenes : От базовой биологии до клинических проявлений. Оклахома-Сити (Оклахома-Сити): Центр медицинских наук Университета Оклахомы; 2016 г.
- Bisno AL, Stevens DL. Стрептококковые инфекции кожи и мягких тканей внешний значок. N Engl J Med. 1996; 334 (4): 240–5.
- Efstratiou A, Lamagni T. Эпидемиология Streptococcus pyogenesexternal icon. В Ferretti JJ, Стивенс Д.Л., Фишетти В.А., редакторы. Streptococcus pyogenes : От базовой биологии до клинических проявлений. Оклахома-Сити (Оклахома-Сити): Центр медицинских наук Университета Оклахомы; 2016.
- Бьорнсдоттир С., Готтфредссон М., Торисдоттир А.С. и др.Факторы риска острого целлюлита нижней конечности: проспективное исследование случай-контроль, внешний значок. Clin Infect Dis. 2005; 41 (10): 1416–22.
