Осложнения терапии НПВП | Еженедельник АПТЕКА
|
.gif) Спектр показаний к их применению достаточно широк: ревматические заболевания, неревматические заболевания опорно-двигательного аппарата, неврологические заболевания воспалительного генеза, болевой синдром и лихорадка различной этиологии, дисменорея, профилактика артериальных тромбозов. Побочные эффекты НПВП, в том числе серьезные, довольно часто отмечаются вследствие широкого, а нередко и бесконтрольного их применения при различных патологических состояниях.
Спектр показаний к их применению достаточно широк: ревматические заболевания, неревматические заболевания опорно-двигательного аппарата, неврологические заболевания воспалительного генеза, болевой синдром и лихорадка различной этиологии, дисменорея, профилактика артериальных тромбозов. Побочные эффекты НПВП, в том числе серьезные, довольно часто отмечаются вследствие широкого, а нередко и бесконтрольного их применения при различных патологических состояниях.
ПР любых ЛС могут быть обусловлены абсолютной и относительной передозировкой, фармакологическими свойствами самих ЛС, нарушениями иммунобиологических свойств организма, аллергическими реакциями, идиосинкразией, синдромом отмены [1]. Большинство ПР вызваны непосредственно фармакологическим воздействием НПВП. Все известные НПВП близки по фармакологическим свойствам и механизмам действия. Ведущий механизм, определяющий эффективность и токсичность НПВП, связан с подавлением активности циклооксигеназы (ЦОГ) — ключевого фермента метаболизма арахидоновой кислоты.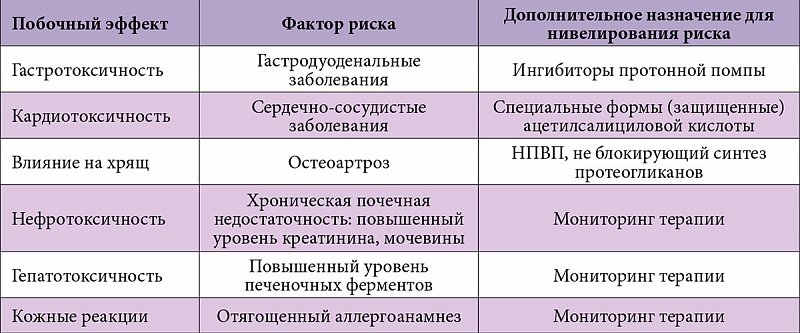
ЦОГ-2 играет важную роль в синтезе ПГ, вызывающих и поддерживающих местные и общие воспалительные реакции (повышение температуры тела, формирование отека, генерация боли, нарушение функции и др.) [7].
Таким образом, ингибиция ЦОГ-2 с последующим снижением синтеза провоспалительных ПГ рассматривается как один из важных механизмов противовоспалительной и анальгетической активности НПВП, а ЦОГ-1 — развития побочных реакций [4]. Поэтому селективность НПВП в отношении ЦОГ имеет большое значение и положена в основу их классификации (Frolich J.
ПР НПВП разнообразны и включают осложнения со стороны ПТ, центральной нервной системы (ЦНС), нефротоксичность, гепатотоксичность, ототоксичность, реакции гиперчувствительности и кожные аллергические реакции, а также другие редко возникающие побочные эффекты.
Наиболее частое осложнение при приеме НПВП — так называемая НПВП-гастропатия. Понятие «НПВП-гастропатия» включает гастритоподобные изменения, эрозии и язвы, объединенные общим патогенезом. Основной патогенный механизм действия НПВП для слизистой оболочки желудка заключается в блокаде ЦОГ-1, которая способствует выработке ПГ (прежде всего ПГE Под влиянием НПВП нарушается баланс между факторами защиты и агрессии в пользу последних. Таким образом, «НПВП-гастропатия» — не местная, а системная реакция организма, возникающая в ответ на подавление синтеза гастропротекторных ПГ, поэтому снижение дозы, переход на парентеральный или ректальный путь введения, использование кишечно-растворимых форм НПВП не могут устранить проблему риска развития НПВП-гастропатии. Примерно у 15–40% пациентов, принимающих НПВП, регистрируются эрозии или язвы желудка [6]. Чаще всего НПВП-гастропатию вызывают кеторолак и пироксикам [8]. Субъективная симптоматика ПР со стороны ПТ включает тошноту, рвоту, диспепсию, диарею, запор, изжогу, боль в эпигастральной области и отмечается у трети больных, чаще всего при длительном приеме НПВП [4].
Под влиянием НПВП нарушается баланс между факторами защиты и агрессии в пользу последних. Таким образом, «НПВП-гастропатия» — не местная, а системная реакция организма, возникающая в ответ на подавление синтеза гастропротекторных ПГ, поэтому снижение дозы, переход на парентеральный или ректальный путь введения, использование кишечно-растворимых форм НПВП не могут устранить проблему риска развития НПВП-гастропатии. Примерно у 15–40% пациентов, принимающих НПВП, регистрируются эрозии или язвы желудка [6]. Чаще всего НПВП-гастропатию вызывают кеторолак и пироксикам [8]. Субъективная симптоматика ПР со стороны ПТ включает тошноту, рвоту, диспепсию, диарею, запор, изжогу, боль в эпигастральной области и отмечается у трети больных, чаще всего при длительном приеме НПВП [4].
Однако развитие субъективной симптоматики плохо коррелирует с истинной тяжестью поражения ПТ. Около 50% пациентов, у которых возникают большие пептические язвы, а также у госпитализированных по поводу желудочных кровотечений, вызванных приемом НПВП, жалоб, свидетельствующих о поражении пищеварительного тракта, не предъявляют [2, 4].

Поскольку НПВП — липофильные вещества и проникают через гематоэнцефалический барьер, большинство из них способно вызвать побочные эффекты со стороны ЦНС, которые по частоте занимают второе место после гастропатии. Отмечаются головная боль, головокружение, лабильность настроения, депрессия, бессонница, деперсонализация, тремор, психозы (при лечении индометацином, толметином), сонливость, нарушения зрения, поражение периферической нервной системы (при лечении мелоксикамом), возможны снижение слуха и шум в ушах (при приеме салицилатов), описаны редкие случаи асептического менингита (при приеме ибупрофена, индометацина, сулиндака, толметина преимущественно у больных системной красной волчанкой).
Осложнения со стороны сердечно-сосудистой системы чаще всего развиваются у людей пожилого возраста. У данной категории пациентов существенно повышается риск декомпенсации кровообращения, что обусловлено задержкой натрия и увеличением объема циркулирующей крови. Риск обострения застойной сердечной недостаточности у лиц, принимавших НПВП, в 10 раз выше, чем у не принимавших эти препараты [5]. У больных с артериальной гипертензией лечение НПВП ассоциируется с повышением диастолического АД. При применении НПВП снижается эффективность ингибиторов АПФ, диуретиков, повышается АД, отмечается негативное влияние на общую выживаемость пациентов с застойной сердечной недостаточностью.
Метаболизм НПВП происходит преимущественно в печени с образованием неактивных метаболитов, экскретируемых с мочой. Данным препаратам свойственна гепатотоксичность, чаще всего проявляющаяся в виде повышения уровня печеночных ферментов, особенно аминотрансфераз (АсАТ и АлАТ). Отмечались также случаи холестаза, тяжелого идиосинкразического гепатита при применении индометацина, диклофенака, сулиндака и фенилбутазона. Описано фатальное гепатотоксическое действие индометацина у детей, поэтому препарат не рекомендуется использовать для лечения артритов у детей в возрасте младше 11 лет.
При лечении НПВП возможно поражение почек: обратимая почечная недостаточность с повышением уровня креатинина, канальцевый некроз, острый интерстициальный нефрит, нефротический синдром. К факторам риска индуцированного поражения почек относятся пожилой возраст, сопутствующие заболевания почек, сердечная недостаточность, прием диуретиков.
Отмечаются также реакции гиперчувствительности к НПВП. Наиболее высокий риск их возникновения у пациентов с тяжелой бронхиальной астмой и полипами носа — почти у 78% из них развиваются ПР на ацетилсалициловую кислоту [2]. У пациентов с носовыми полипами, бронхиальной астмой или хронической крапивницей также повышен риск гиперреакции на другие НПВП, обычно в виде бронхоспазма и одышки. Важно отметить, что это именно реакции гиперчувствительности, а не аллергии, поскольку они не опосредованы иммуноглобулином E.
К редко возникающим побочным эффектам НПВП относятся: лихорадка, волчаночный синдром, васкулит, перикардит, миокардит, апластическая анемия, изолированная эритроцитарная аплазия, тромбоцитопения, нейтропения, гемолитическая анемия, стоматит, кожные реакции (фоточувствительность, полиморфная эритема, крапивница, токсический эпидермальный некролиз).
Учитывая то, что у многих пациентов отмечается несколько хронических заболеваний и они вынуждены принимать одновременно препараты различных групп, необходимо обратить внимание на особенности взаимодействия НПВП с другими широко применяемыми ЛС. Так, совместное применение с непрямыми антикоагулянтами (в частности, варфарином) повышает риск кровотечения за счет ингибирования тромбоцитарных функций и повреждения слизистой оболочки желудка. Сочетанное использование с блокаторами b-адренорецепторов вызывает снижение выраженности их гипотензивного эффекта, а с ингибиторами АПФ, гидралазином и празозином — его нейтрализацию. Комбинированное применение НПВП с диуретиками приводит к нейтрализации их натрийуретического (фуросемид, спиронолактон) и гипотензивного эффекта (фуросемид, тиазидные диуретики). С другой стороны, концентрация некоторых препаратов (литий, дигоксин, аминогликозиды, метотрексат) в плазме при сочетанном применении с НПВП может значительно повышаться, что неизбежно влечет проявление их токсического действия.
Комбинированное применение НПВП с диуретиками приводит к нейтрализации их натрийуретического (фуросемид, спиронолактон) и гипотензивного эффекта (фуросемид, тиазидные диуретики). С другой стороны, концентрация некоторых препаратов (литий, дигоксин, аминогликозиды, метотрексат) в плазме при сочетанном применении с НПВП может значительно повышаться, что неизбежно влечет проявление их токсического действия.
Итак, на выбор оптимального НПВП для конкретного пациента влияет целый комплекс факторов: эффективность, безопасность, селективность по отношению к ЦОГ-2, наличие токсического действия на хрящ (что особенно важно при остеоартрозе), фармакодинамические свойства, удобство дозировки, форма выпуска, совместимость с другими ЛС, стоимость, индивидуальная чувствительность пациента, его возраст, наличие основного заболевания, сопутствующей патологии. Таким образом, НПВП, с одной стороны, — незаменимые препараты для лечения многих заболеваний, с другой, — имеют значительное количество различных нежелательных эффектов, связанных как с самими лекарствами, так и со взаимодействием их с другими активными химическими соединениями.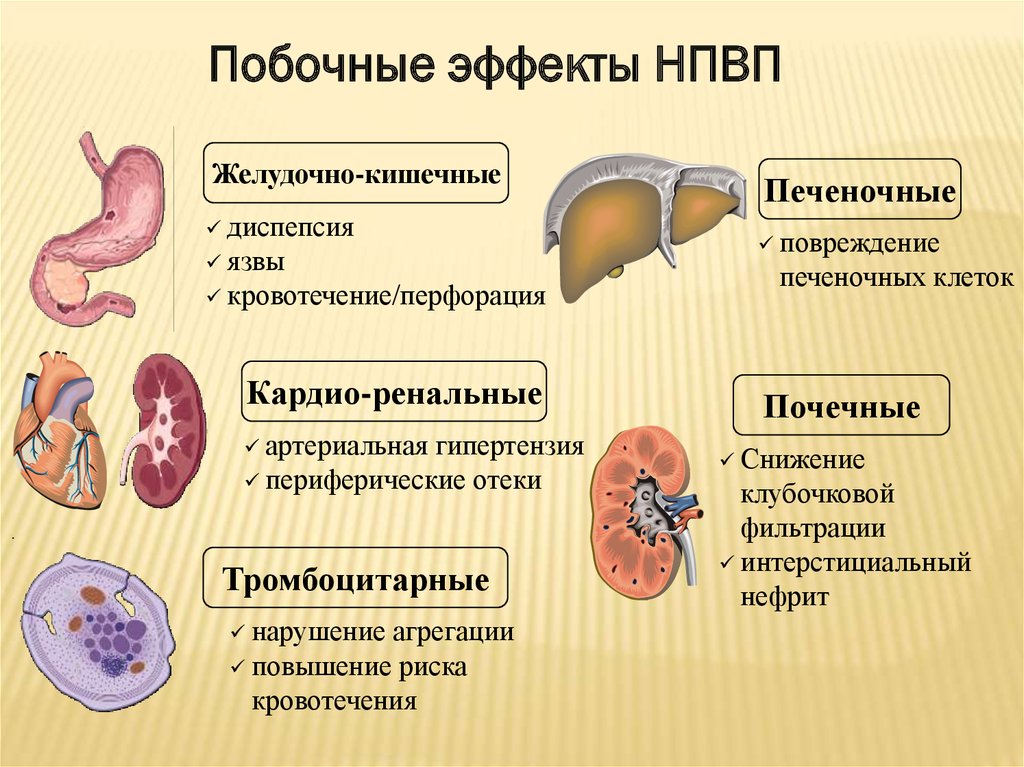
Елена Барсукова
|
ЛИТЕРАТУРА |
|
|
Против боли и воспаления: что важно знать о НПВС
Статті03/02/2015
История нестероидных противовоспалительных препаратов (НПВС) началась во второй половине XIX в., когда впервые при остром ревматизме был применен салицилат натрия, а в 1899 г. в практику была введена ацетилсалициловая кислота. Сегодня лечение боли и воспаления невозможно представить без НПВС. Ежедневно их принимают более 30 миллионов человек во всем мире.
Спектр лекарственных средств этой группы постоянно расширяется становясь «бесперебойным генератором» вопросов, ответы на которые сообща ищут фармакологи и врачи
Как действуют НПВС?
Нестероидные противовоспалительные препараты оказывают противовоспалительное, обезболивающее и жаропонижающее действие. Основными показаниями к назначению НПВС являются боль различного происхождения (костно-мышечная, головная боль, дисменорея и др.), воспалительные заболевания опорно-двигательного аппарата, ревматические заболевания, лихорадочные состояния.
Основными показаниями к назначению НПВС являются боль различного происхождения (костно-мышечная, головная боль, дисменорея и др.), воспалительные заболевания опорно-двигательного аппарата, ревматические заболевания, лихорадочные состояния.
Противовоспалительное действие НПВС реализуется за счет подавления активности фермента циклооксигеназы (ЦОГ) и биосинтеза медиаторов боли и воспаления — простагландинов. Известно, что физиологическая роль ЦОГ заключается в регуляции внутриглазного давления, заживлении язв верхних отделов желудочно-кишечного тракта, овуляции, образовании простациклина (PGI2) клетками сосудистого эндотелия и др.
В 90-х годах прошлого века были выделены две изоформы ЦОГ. Первая (ЦОГ-1) постоянно присутствует в тканях и относится к ферментам, регулирующим физиологические эффекты простагландинов. Вторая изоформа (ЦОГ-2) в норме обнаруживается в незначительных количествах. При воспалении уровень ЦОГ значительно повышается. Так, содержание ЦОГ-1 увеличивается в 2–4 раза, ЦОГ-2 — более чем в 20 раз.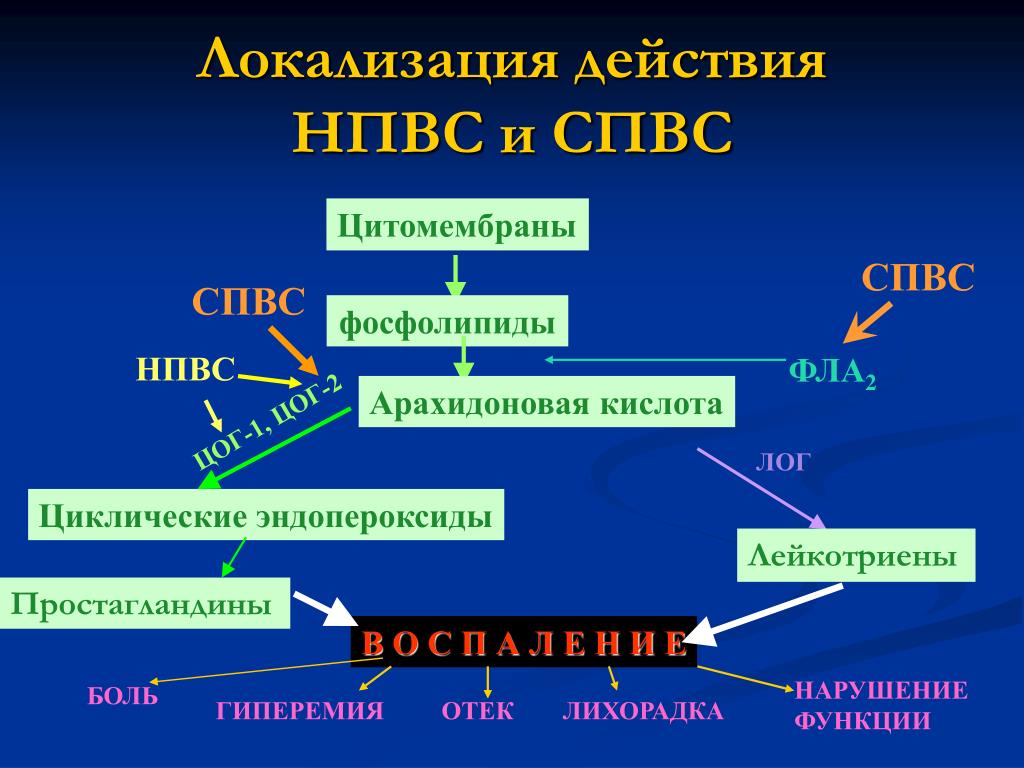 При повышенном содержании ЦОГ, особенно второй изоформы, синтез простагландинов увеличивается и проявляется их негативное воздействие на организм.
При повышенном содержании ЦОГ, особенно второй изоформы, синтез простагландинов увеличивается и проявляется их негативное воздействие на организм.
Выше уже упоминалось о том, что НПВС тормозят активность циклооксигеназ и таким образом влияют на выработку простагландинов, а значит, разрывают цепь воспалительной реакции. Противовоспалительный эффект НПВС обусловлен их способностью ингибировать провоспалительный изофермент ЦОГ-2.
По способности взаимодействовать с циклооксигеназой НПВС подразделяют на:
– селективные ингибиторы ЦОГ-1;
– неселективные ингибиторы ЦОГ-1 и ЦОГ-2;
– преимущественные ингибиторы ЦОГ-2;
– специфические ингибиторы ЦОГ-2.
Применение НПВС связано с развитием побочных эффектов?
Терапевтическое действие НПВС обусловлено блокадой провоспалительного фермента ЦОГ-2 и снижением синтеза простагландинов, тогда как побочные эффекты — блокадой ЦОГ- 1, конститутивного фермента, обеспечивающего клеточный метаболизм и защиту клеток от повреждения (в том числе в слизистой оболочке желудка). Действительно, практически все НПВП, которые использовали до 90-х годов прошлого века, в равной степени подавляли активность ЦОГ-1 и ЦОГ-2, что и приводило к развитию побочных действий, таких как гастропатия, нефротоксичность и коагулопатия.
Действительно, практически все НПВП, которые использовали до 90-х годов прошлого века, в равной степени подавляли активность ЦОГ-1 и ЦОГ-2, что и приводило к развитию побочных действий, таких как гастропатия, нефротоксичность и коагулопатия.
Поражение желудочно-кишечного тракта — основное побочное действие НПВС. При применении НПВС прежде всего страдает слизистая оболочка желудка вследствие нарушения синтеза простагландинов и простациклина. Так, простагландин Е2 (ПГ-Е2) — один из медиаторов, улучшающих сосудистую циркуляцию в желудке, способствует активации местной перфузии и повышению уровня секреции бокаловидными клетками.
При воспалении ПГ-Е2, ПГ-D2 и простациклин расширяют микрососуды, увеличивают их проницаемость, угнетают секрецию желудочного сока, уменьшают содержание в нем соляной кислоты и пепсина, нарушают процессы образования защитных мукополисахаридов, что приводит к усилению отторжения эпителия слизистой желудка. Подавление образования простациклина ведет к нарушению микроциркуляции и обменных процессов в бокаловидных клетках, снижению выработки бикарбонатов и слизи.
Нефротоксичность — второе по значимости побочное действие НПВС. Блокада синтеза ПГ-Е2 и простациклина в почках вызывает сужение сосудов и замедление почечного кровотока, в результате чего развивается ишемия почек, снижаются скорость клубочковой фильтрации и объем диуреза с возможным органическим поражением почек.
Лекарства и алкоголь — весьма опасный коктейль! Читайте на сайте “Фармацевт Практик”: Алкоголь и лекарства: сочетая несочетаемое
Наконец, коагулопатия при применении НПВС связана с нарушением соотношения тромбоксана А2 и простациклина в крови. НПВС угнетают выработку как тромбоксана А2, находящегося в тромбоцитах, так и простациклина, производимого эндотелием сосудов. После отмены препарата эндотелий способен намного быстрее восстанавливать синтез простациклина, тогда как тромбоксан А2 в тромбоцитах не восстанавливается.
Существуют факторы риска развития побочных эффектов при применении НПВП?
К факторам риска развития НПВС-индуцированной гастропатии относят возраст старше 60 лет, наличие заболеваний пищеварительного тракта в анамнезе, терапию антикоагулянтами и глюкокортикостероидами, одновременное применение двух и более НПВС, а также длительный (более 3 месяцев) прием НПВС. Группу повышенного риска развития осложнений со стороны сердечно-сосудистой системы составляют пациенты с ишемической болезнью сердца (стенокардией или перенесшие инфаркт миокарда) и цереброваскулярными заболеваниями (перенесшие инсульт или эпизоды транзиторных ишемических атак). Побочные эффекты возможны у лиц, подвергшихся операциям ангиопластики или стентирования коронарных сосудов. С осторожностью НПВС назначают пациентам с артериальной гипертензией, гиперлипидемией, сахарным диабетом, облитерирующими заболеваниями периферических артерий. Лицам с повышенным кардиоваскулярным риском показан прием ацетилсалициловой кислоты в кардиопротекторных дозах независимо от селективности НПВП.
Группу повышенного риска развития осложнений со стороны сердечно-сосудистой системы составляют пациенты с ишемической болезнью сердца (стенокардией или перенесшие инфаркт миокарда) и цереброваскулярными заболеваниями (перенесшие инсульт или эпизоды транзиторных ишемических атак). Побочные эффекты возможны у лиц, подвергшихся операциям ангиопластики или стентирования коронарных сосудов. С осторожностью НПВС назначают пациентам с артериальной гипертензией, гиперлипидемией, сахарным диабетом, облитерирующими заболеваниями периферических артерий. Лицам с повышенным кардиоваскулярным риском показан прием ацетилсалициловой кислоты в кардиопротекторных дозах независимо от селективности НПВП.
Есть противопоказания к применению НПВС?
Противопоказаниями к назначению НПВС являются:
– язвенная болезнь желудка или двенадцатиперстной кишки;
– анемия;
– склонность к кровотечениям;
– повышенное артериальное давление;
– патология сердечно-сосудистой системы;
– заболевания печени;
– заболевания почек.
Можно принимать НПВС в период беременности?
НПВС не рекомендуется принимать во время беременности, особенно в ІІІ триместре. Несмотря на то, что к настоящему времени прямого воздействия НПВС на плод не выявлено, принято считать, что эти препараты могут вызвать преждевременное закрытие артериального протока, а также осложнения со стороны почек у плода. Кроме того, имеются сведения о преждевременных родах у женщин, принимавших НПВС.
Как снизить риск нежелательных осложнений?
Наиболее приемлемым решением является применение препаратов с преимущественным ингибированием ЦОГ-2, которые обладают высоким профилем гастроинтестинальной безопасности. В то же время их применение может вызывать осложнения со стороны сердечно-сосудистой системы.
При лечении боли и воспаления следует применять НПВС очень короткими курсами тогда их влияние на сердечно-сосудистые события будет незначительным.
Рациональное комбинирование базисной терапии с НПВС может существенно ограничить длительность их применения. При этом использование специфических ингибиторов ЦОГ-2, которые по сравнению с «классическими» неселективными НПВС реже вызывают побочные эффекты со стороны пищеварительного тракта, печени и почек, особенно желательно на начальном этапе терапии.
При этом использование специфических ингибиторов ЦОГ-2, которые по сравнению с «классическими» неселективными НПВС реже вызывают побочные эффекты со стороны пищеварительного тракта, печени и почек, особенно желательно на начальном этапе терапии.
Немаловажное значение имеет лекарственная форма НПВС. Ректальные суппозитории в ряде случаев более предпочтительны по сравнению с пероральными формами. Использование НПВС в форме суппозиториев позволяет снизить риск побочных действий со стороны пищеварительного тракта и гарантировать поступление полной дозы лекарственного средства независимо от приема пищи и сопутствующей терапии (например, антацидами). Введенные в прямую кишку НПВС действуют быстрее и эффективнее благодаря особым условиям всасывания. Дистальный отрезок пищеварительного тракта имеет ряд анатомофизиологических особенностей (богатая венозная сеть) и представляет собой уникальную область организма, где процессы всасывания достигают особой напряженности и отличаются отсутствием или незначительным участием пищеварительных ферментов.
Как правило, поступление адсорбированных в прямой кишке веществ осуществляется одновременно через кровеносную и лимфатическую системы. Первая обеспечивает быструю доставку действующих веществ в большой круг кровообращения, а вторая — пролонгированность их действия. При этом лишь весьма незначительная часть адсорбированных препаратов поступает в воротную вену, несущую кровь от внутренних органов к печени. Более того, для ряда лекарственных средств биодоступность из слизистой оболочки прямой кишки приравнивается к таковой после их внутривенного введения.
В последнее время широкое применение нашли комбинированные НПВС. Их использование в анестезиологической практике позволяет снизить дозы наркотических анальгетиков.
Можно создать идеальный НПВС?
Противовоспалительный эффект различных НПВС может отличаться и зависит от режима дозирования. В большинстве сравнительных исследований используют фиксированные дозы препаратов, что не позволяет сделать достоверные выводы о характере ответа на тот или иной препарат. Очень важно избегать недооценки зависимости «доза-эффект», особенно при сравнении различных препаратов одной группы.
Очень важно избегать недооценки зависимости «доза-эффект», особенно при сравнении различных препаратов одной группы.
На популяционном уровне все НПВС в эквивалентных дозах обладают сходной эффективностью и токсичностью, однако клинический опыт свидетельствует о том, что у некоторых пациентов один НПВС более эффективно подавляет боль и воспаление или, напротив, чаще вызывает токсические реакции, чем другой. Причины этого до конца не изучены.
Индивидуальные различия в ответе на прием НПВС можно объяснить следующим образом. Во-первых, несмотря на общие физико-химические характеристики, каждый НПВС обладает уникальными свойствами, что может иметь клинические последствия. Во-вторых, ответ на прием НПВС может зависеть от режима дозирования, что связано прежде всего с фармакокинетикой конкретного препарата. В-третьих, фармакодинамические особенности, физико-химические свойства и механизм действия НПВС могут не совпадать с механизмами развития заболевания у конкретного больного. Следовательно, следует развенчать миф об образцово-показательном НПВС и подбирать препарат индивидуально, оценивая ожидаемый терапевтический эффект и возможный риск для пациента..gif)
Подготовила Александра Демецкая
“Фармацевт Практик” #03′ 2010
Поділіться цим з друзями!
Вам також буде цікаво це:
Страница не найдена |
Страница не найдена |404. Страница не найдена
Архив за месяц
ПнВтСрЧтПтСбВс
6789101112
13141516171819
20212223242526
2728293031
12
12
1
3031
12
15161718192021
25262728293031
123
45678910
12
17181920212223
31
2728293031
1
1234
567891011
12
891011121314
11121314151617
28293031
1234
12
12345
6789101112
567891011
12131415161718
19202122232425
3456789
17181920212223
24252627282930
12345
13141516171819
20212223242526
2728293031
15161718192021
22232425262728
2930
Архивы
Метки
Настройки
для слабовидящих
NovoSeven RT, дозирование Sevenfact (фактор VIIa, рекомбинантный), показания, взаимодействия, побочные эффекты и др.

ФАКТОР VIIA, РЕКОМБИНАНТНЫЙ — ВПРЫСК
(коэффициент VIIA, ree-KOM-bin-unt)
ОБЩЕЕ НАИМЕНОВАНИЕ БРЕНДА: Novoseven
ПРЕДУПРЕЖДЕНИЕ: Это лекарство вызвало очень серьезные тромбы (такие как сердечный приступ, инсульт, легочная эмболия-ТЭЛА, тромбоз глубоких вен-ТГВ). Вы можете подвергаться повышенному риску образования тромбов, если в анамнезе были сгустки крови, заболевания сердца / кровеносных сосудов, заболевания печени или если вы неподвижны (например, прикованы к постели после операции).Поговорите со своим врачом о рисках и преимуществах этого лекарства. Немедленно обратитесь за медицинской помощью, если у вас появятся симптомы сгустка крови, такие как боль / отек / покраснение / слабость в руках или ногах, боль в икроножных мышцах / теплый на ощупь отек, одышка, кашель с кровью, грудная клетка / Боль в челюсти / левой руке, внезапные изменения зрения, слабость на одной стороне тела, проблемы с речью или спутанность сознания.
ИСПОЛЬЗОВАНИЕ: Этот препарат используется для лечения и предотвращения кровотечений у людей с определенными заболеваниями (такими как гемофилия типа A или B, низкий уровень фактора VII, тромбастения Гланцмана). Люди с этими состояниями подвержены риску длительного кровотечения после травмы / операции и кровотечения внутри тела (особенно в суставах и мышцах). Этот продукт содержит искусственную форму фактора VIIa, который представляет собой белок (фактор свертывания крови) в крови, который работает с другими факторами свертывания, чтобы помочь свертыванию крови и остановить кровотечение.
Люди с этими состояниями подвержены риску длительного кровотечения после травмы / операции и кровотечения внутри тела (особенно в суставах и мышцах). Этот продукт содержит искусственную форму фактора VIIa, который представляет собой белок (фактор свертывания крови) в крови, который работает с другими факторами свертывания, чтобы помочь свертыванию крови и остановить кровотечение.
КАК ИСПОЛЬЗОВАТЬ: Прочтите информационный буклет для пациента, если он есть у вашего фармацевта, перед тем, как начать использовать это лекарство, и каждый раз, когда вы будете получать его повторно.Если у вас есть какие-либо вопросы, спросите своего врача или фармацевта. Это лекарство вводится путем инъекции в вену, как правило, в течение нескольких минут. Доза обычно повторяется каждые 2-6 часов или по указанию врача. Дозировка зависит от вашего состояния здоровья, веса и реакции на лечение. Не вводите раствор для смешивания непосредственно в порошок лекарства, потому что это может привести к тому, что лекарство станет неэффективным. Направьте шприц так, чтобы вода мягко стекала по стенке флакона.Не встряхивайте флакон. Аккуратно перемешайте смесь, пока весь порошок не растворится. Не смешивайте это лекарство с другими лекарствами. Если вы принимаете это лекарство дома, изучите все инструкции по приготовлению и применению у своего лечащего врача. Перед использованием проверьте продукт визуально на предмет наличия частиц или обесцвечивания. Если они присутствуют, не используйте жидкость. Узнайте, как безопасно хранить и выбрасывать медицинские принадлежности. Сообщите врачу, если ваше состояние не улучшится или ухудшится.
Направьте шприц так, чтобы вода мягко стекала по стенке флакона.Не встряхивайте флакон. Аккуратно перемешайте смесь, пока весь порошок не растворится. Не смешивайте это лекарство с другими лекарствами. Если вы принимаете это лекарство дома, изучите все инструкции по приготовлению и применению у своего лечащего врача. Перед использованием проверьте продукт визуально на предмет наличия частиц или обесцвечивания. Если они присутствуют, не используйте жидкость. Узнайте, как безопасно хранить и выбрасывать медицинские принадлежности. Сообщите врачу, если ваше состояние не улучшится или ухудшится.
ПОБОЧНЫЕ ДЕЙСТВИЯ: См. Также раздел «Предупреждение». Могут возникнуть лихорадка, головная боль, боль / покраснение / раздражение в месте инъекции, головокружение, тошнота или рвота. Если какой-либо из этих эффектов сохраняется или ухудшается, немедленно сообщите об этом своему врачу или фармацевту. Помните, что это лекарство было прописано, потому что ваш врач посчитал, что польза для вас больше, чем риск побочных эффектов. Многие люди, принимающие это лекарство, не имеют серьезных побочных эффектов. Немедленно сообщите своему врачу, если у вас есть какие-либо серьезные побочные эффекты, в том числе: отек лодыжек / стоп, новое или усиливающееся кровотечение / синяк, новая или усиливающаяся боль в суставах / отек, быстро / медленно сердцебиение, признаки проблем с почками (например, изменение количества мочи).Очень серьезная аллергическая реакция на этот препарат встречается редко. Однако немедленно обратитесь за медицинской помощью, если вы заметили какие-либо симптомы серьезной аллергической реакции, в том числе: сыпь, зуд / отек (особенно лица / языка / горла), сильное головокружение, затрудненное дыхание. Это не полный список возможных причин. побочные эффекты. Если вы заметили другие эффекты, не перечисленные выше, обратитесь к врачу или фармацевту. В США — обратитесь к врачу за медицинской консультацией по поводу побочных эффектов. Вы можете сообщить о побочных эффектах в FDA по телефону 1-800-FDA-1088 или на сайте www.
Многие люди, принимающие это лекарство, не имеют серьезных побочных эффектов. Немедленно сообщите своему врачу, если у вас есть какие-либо серьезные побочные эффекты, в том числе: отек лодыжек / стоп, новое или усиливающееся кровотечение / синяк, новая или усиливающаяся боль в суставах / отек, быстро / медленно сердцебиение, признаки проблем с почками (например, изменение количества мочи).Очень серьезная аллергическая реакция на этот препарат встречается редко. Однако немедленно обратитесь за медицинской помощью, если вы заметили какие-либо симптомы серьезной аллергической реакции, в том числе: сыпь, зуд / отек (особенно лица / языка / горла), сильное головокружение, затрудненное дыхание. Это не полный список возможных причин. побочные эффекты. Если вы заметили другие эффекты, не перечисленные выше, обратитесь к врачу или фармацевту. В США — обратитесь к врачу за медицинской консультацией по поводу побочных эффектов. Вы можете сообщить о побочных эффектах в FDA по телефону 1-800-FDA-1088 или на сайте www. fda.gov/medwatch. В Канаде — Обратитесь к врачу за медицинской консультацией о побочных эффектах. Вы можете сообщить о побочных эффектах в Министерство здравоохранения Канады по телефону 1-866-234-2345.
fda.gov/medwatch. В Канаде — Обратитесь к врачу за медицинской консультацией о побочных эффектах. Вы можете сообщить о побочных эффектах в Министерство здравоохранения Канады по телефону 1-866-234-2345.
МЕРЫ ПРЕДОСТОРОЖНОСТИ: Перед использованием фактора VIIa сообщите своему врачу или фармацевту, если у вас аллергия на него; или если у вас есть другие аллергии. Этот продукт может содержать неактивные ингредиенты, которые могут вызвать аллергические реакции или другие проблемы. Поговорите со своим фармацевтом для получения более подробной информации. Перед использованием этого лекарства расскажите своему врачу или фармацевту о своей истории болезни, особенно о: других проблемах с кровотечением / свертыванием (например.д., диссеминированное внутрисосудистое свертывание (ДВС-синдром), проблемы с кровеносными сосудами (например, атеросклероз), недавняя серьезная инфекция в крови, недавняя серьезная травма. Новорожденные могут подвергаться большему риску образования тромбов при использовании этого препарата..gif) риск образования тромбов при использовании этого препарата. Во время беременности этот препарат следует использовать только тогда, когда это явно необходимо. Обсудите риски и преимущества со своим врачом. Неизвестно, проникает ли этот препарат в грудное молоко. Из-за возможного риска для младенца проконсультируйтесь с врачом перед кормлением грудью.
риск образования тромбов при использовании этого препарата. Во время беременности этот препарат следует использовать только тогда, когда это явно необходимо. Обсудите риски и преимущества со своим врачом. Неизвестно, проникает ли этот препарат в грудное молоко. Из-за возможного риска для младенца проконсультируйтесь с врачом перед кормлением грудью.
ВЗАИМОДЕЙСТВИЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ: Взаимодействие с лекарствами может изменить то, как действуют ваши лекарства, или повысить риск серьезных побочных эффектов. Этот документ не содержит всех возможных лекарственных взаимодействий. Составьте список всех продуктов, которые вы используете (включая рецептурные / безрецептурные препараты и растительные продукты), и поделитесь им со своим врачом и фармацевтом. Не начинайте, не останавливайте и не изменяйте дозировку каких-либо лекарств без одобрения врача. Этот продукт не следует принимать одновременно с некоторыми другими продуктами с факторами свертывания крови (активированными и неактивированными концентратами протромбинового комплекса).
ПЕРЕДОЗИРОВКА: Если у кого-то произошла передозировка и наблюдаются серьезные симптомы, такие как обморок или затрудненное дыхание, позвоните по телефону 911. В противном случае немедленно позвоните в токсикологический центр. Жители США могут позвонить в местный токсикологический центр по телефону 1-800-222-1222. Жители Канады могут позвонить в провинциальный токсикологический центр.
ПРИМЕЧАНИЯ: Не сообщайте это лекарство другим. Лабораторные и / или медицинские тесты (например, тесты времени свертывания, активность фактора VII) должны выполняться периодически, чтобы отслеживать ваш прогресс или проверять наличие побочных эффектов.Обратитесь к врачу для получения более подробной информации.
ПРОПУЩЕННАЯ ДОЗА: Важно получать каждую дозу этого лекарства в соответствии с графиком. Если вы пропустите прием, немедленно обратитесь к врачу или фармацевту за новым графиком приема. Не удваивайте дозу, чтобы наверстать упущенное.
ХРАНЕНИЕ: Подробности по хранению см. В инструкции к продукту и у фармацевта. Храните все лекарства в недоступном для детей и домашних животных. Не смывайте лекарства в унитаз и не выливайте их в канализацию, если это не предписано. Правильно утилизируйте этот продукт, когда срок его годности истек или он больше не нужен.Проконсультируйтесь с фармацевтом или в местной компании по утилизации отходов.
В инструкции к продукту и у фармацевта. Храните все лекарства в недоступном для детей и домашних животных. Не смывайте лекарства в унитаз и не выливайте их в канализацию, если это не предписано. Правильно утилизируйте этот продукт, когда срок его годности истек или он больше не нужен.Проконсультируйтесь с фармацевтом или в местной компании по утилизации отходов.
МЕДИЦИНСКОЕ ПРЕДУПРЕЖДЕНИЕ: Ваше состояние может вызвать осложнения в случае неотложной медицинской помощи. Для получения информации о регистрации в MedicAlert звоните по телефону 1-888-633-4298 (США) или 1-800-668-1507 (Канада).
Последний раз информация обновлялась в августе 2021 г. Copyright (c) 2021 First Databank, Inc.
ВАЖНАЯ ИНФОРМАЦИЯ: КАК ИСПОЛЬЗОВАТЬ ДАННУЮ ИНФОРМАЦИЮ: Это краткое изложение и НЕ содержит всей возможной информации об этом продукте. Эта информация не гарантирует, что этот продукт безопасен, эффективен или подходит для вас.Эта информация не является индивидуальным медицинским советом и не заменяет совет вашего лечащего врача. Всегда спрашивайте у своего лечащего врача полную информацию об этом продукте и ваших конкретных медицинских потребностях.
Всегда спрашивайте у своего лечащего врача полную информацию об этом продукте и ваших конкретных медицинских потребностях.
Повидон — обзор | Темы ScienceDirect
9.4 Достоинства поли (винилпирролидонов)
PVP — это универсальный ингредиент, используемый в фармацевтической и косметической промышленности. Его получают путем многоступенчатого синтеза, который завершается полимеризацией винилпирролидона в водном растворе в присутствии перекиси водорода [1].Широкий ассортимент молекулярных масс, от нескольких тысяч до нескольких миллионов дальтон, может быть достигнут путем определения степени полимеризации. ПВП широко используется в биомедицине в качестве заменителя плазмы, связующих веществ в фармацевтических таблетках, гидрогелей для перевязок ран и дезинфицирующих средств. Его гигроскопичность, пленкообразование и адгезия к различным материалам сделали PVP широко используемым в фармацевтике, косметике и промышленном производстве. Взаимодействия между карбонильными группами ПВП и гидроксильной группой полифенолов хорошо известны. Из-за этих взаимодействий ПВП используется для разделения полифенолов и в качестве коллоидного стабилизатора в пиве путем тщательного удаления таноидных полифенолов [22,23]. Составы ПВП использовались для получения раствора с предпочтительной вязкостью, позволяющей наносить покрытие из фоторезиста однородной толщины при производстве экранов для дисплеев с высоким разрешением [24]. Далее описаны различные достоинства PVP.
Из-за этих взаимодействий ПВП используется для разделения полифенолов и в качестве коллоидного стабилизатора в пиве путем тщательного удаления таноидных полифенолов [22,23]. Составы ПВП использовались для получения раствора с предпочтительной вязкостью, позволяющей наносить покрытие из фоторезиста однородной толщины при производстве экранов для дисплеев с высоким разрешением [24]. Далее описаны различные достоинства PVP.
9.4.1 Нетоксичен
Поскольку ПВП широко используется в фармацевтической и пищевой промышленности, необходимо знать, достаточно ли он безопасен для здоровья человека.PVP обычно используется для улучшения характеристик хранения пива. В 1961 году было проведено исследование для определения всасывания ПВП в желудочно-кишечном тракте. В этом исследовании было замечено, что у объекта, потребляющего пиво, PVP с низкой средней молекулярной массой перфузировался в кровоток и в основном выводился с мочой в течение 24 часов. Кроме того, не было никаких признаков разложения ПВП в организме при инъекции. Чтобы гарантировать абсорбцию ПВП, испытуемым женщинам давали однократную пероральную дозу смеси пива (150 мл) с 2 г ПВП.Образцы мочи собирали в течение 4 дней и анализировали с 24-часовым интервалом. В образцах мочи ПВП не обнаружен [25]. Никаких доказательств раздражения глаз, сенсибилизации кожи или раздражения кожи раствором ПВП-йода не наблюдалось у экспериментальных животных при концентрации ПВП 10%. Считалось, что эти результаты подтверждают безопасность PVP для использования человеком. Неразбавленный PVP K-30 был признан безопасным для кожного нанесения в ходе клинических испытаний. В некоторых исследованиях наблюдалась генотоксичность ПВП. Однако в большинстве исследований он показал отрицательные результаты [26].По этой причине он широко используется в фармацевтической, косметической и пищевой промышленности без каких-либо заменителей.
Чтобы гарантировать абсорбцию ПВП, испытуемым женщинам давали однократную пероральную дозу смеси пива (150 мл) с 2 г ПВП.Образцы мочи собирали в течение 4 дней и анализировали с 24-часовым интервалом. В образцах мочи ПВП не обнаружен [25]. Никаких доказательств раздражения глаз, сенсибилизации кожи или раздражения кожи раствором ПВП-йода не наблюдалось у экспериментальных животных при концентрации ПВП 10%. Считалось, что эти результаты подтверждают безопасность PVP для использования человеком. Неразбавленный PVP K-30 был признан безопасным для кожного нанесения в ходе клинических испытаний. В некоторых исследованиях наблюдалась генотоксичность ПВП. Однако в большинстве исследований он показал отрицательные результаты [26].По этой причине он широко используется в фармацевтической, косметической и пищевой промышленности без каких-либо заменителей.
9.4.2 Повышение растворимости
В целом, чем ниже растворимость, тем ниже биодоступность. На это влияет несколько дополнительных факторов. Растворимость считается важным параметром при разработке рецептуры. Исследователи регулярно ищут новые способы улучшить биодоступность за счет увеличения растворимости. ПВП использовался для увеличения растворимости лекарств методом твердых дисперсий [27,28].В исследовании Mahapatra et al. сообщили о ПВП как о лучшем средстве для повышения растворимости валсартана, чем β-циклодекстрин и гидроксипропил β-циклодекстрин [29]. Koh et al. приготовили твердые дисперсии для повышения скорости растворения эфавиренца. Составы, содержащие только поливинилпирролидон, показали лучший профиль растворения [30]. Сообщалось, что ПВП увеличивает растворимость куркумина в 880 раз в твердой дисперсии, полученной совместным испарением куркумина и этанола ПВП К-30 [31]. Сообщалось об улучшении растворимости флавоноидов при использовании ПВП из-за присутствия карбонильных групп ПВП и гидроксильных групп агликонов флаванона (нарингина и гесперидина).Эти взаимодействия предотвращают кристаллизацию обоих агликонов флаванона в матрице ПВП [32].
Растворимость считается важным параметром при разработке рецептуры. Исследователи регулярно ищут новые способы улучшить биодоступность за счет увеличения растворимости. ПВП использовался для увеличения растворимости лекарств методом твердых дисперсий [27,28].В исследовании Mahapatra et al. сообщили о ПВП как о лучшем средстве для повышения растворимости валсартана, чем β-циклодекстрин и гидроксипропил β-циклодекстрин [29]. Koh et al. приготовили твердые дисперсии для повышения скорости растворения эфавиренца. Составы, содержащие только поливинилпирролидон, показали лучший профиль растворения [30]. Сообщалось, что ПВП увеличивает растворимость куркумина в 880 раз в твердой дисперсии, полученной совместным испарением куркумина и этанола ПВП К-30 [31]. Сообщалось об улучшении растворимости флавоноидов при использовании ПВП из-за присутствия карбонильных групп ПВП и гидроксильных групп агликонов флаванона (нарингина и гесперидина).Эти взаимодействия предотвращают кристаллизацию обоих агликонов флаванона в матрице ПВП [32].
9.4.3 Стабилизатор
Суспензии представляют собой двухфазную лекарственную форму, и до настоящего времени не было составлено ни одной идеальной суспензии, лишенной проблемы стабильности. Каждый состав суспензии страдает проблемами стабильности из-за седиментации и образования корки. Доступен широкий спектр суспендирующих агентов, которые используются в фармацевтической промышленности, где PVP имеет свое собственное положение.В литературе приводится ряд исследований, о которых сообщают ученые, чтобы показать влияние ПВП на стабильность суспензии. Один из таких видов исследований был проведен Huertas et al. где они изучали влияние адсорбции ПВП на стабильность суспензии кремнезема. Исследовали влияние содержания кремнезема, добавления полимера и разбавления суспензии водой. Метод турбидиметрии применялся для изучения стабильности исследуемых систем в зависимости от времени. Было показано, что суспензия без полимера характеризовалась наименьшей стабильностью, тогда как системы, содержащие ПВП (до и после разбавления), последовательно стабильны. Специфическая конформация цепей ПВП на твердой поверхности отвечает за стабилизационно-флокуляционные свойства ПВП в коллоидной суспензии [33].
Специфическая конформация цепей ПВП на твердой поверхности отвечает за стабилизационно-флокуляционные свойства ПВП в коллоидной суспензии [33].
9.4.4 Интрацитоплазматическая инъекция сперматозоидов
Техника интрацитоплазматической инъекции сперматозоидов (ИКСИ) становится более популярной, чем экстракорпоральное оплодотворение (ЭКО). Благодаря отличительным особенностям ПВП, он успешно использовался для ИКСИ, чтобы повысить вязкость раствора сперматозоидов, тем самым способствуя управлению и иммобилизации отдельных сперматозоидов как у домашних животных, так и у людей [34].
9.4.5 Пригодность для офтальмологии
В офтальмологических растворах ПВП используется в качестве смягчающего или увлажняющего средства и обычно присутствует в концентрации приблизительно 1% в водной матрице, которая также включает дополнительные вспомогательные вещества и активные фармацевтические компоненты. Было показано, что в сочетании с полиэтиленгликолем 400 и декстраном 70 он эффективен для кратковременного облегчения незначительных раздражений, для защиты глаз от дальнейшего раздражения от ветра или солнца и уменьшения сухости глаз [35].
9.4.6 Формовочный агент
PVP в качестве поверхностно-активного вещества использовался для получения и формы контролируемых наночастиц благородных металлов. Он может избежать агрегации частиц и поддерживать идентичную коллоидную дисперсию в качестве стабилизирующего агента. Кроме того, ПВП используется в качестве средства контроля формы или «модификатора габитуса кристаллов», поддерживая рост на точных гранях кристаллов, предотвращая при этом рост на других. Следовательно, добавление различных количеств ПВП может привести к широкому диапазону размеров и форм получаемых частиц, полезных при разработке различных микро- или наноносителей для доставки лекарств [36].
9.4.7 Применение в косметике
PVP — это универсальный ингредиент, используемый в косметической и косметической промышленности в качестве связующего вещества, пленкообразователя, стабилизатора эмульсии, суспендирующего агента и фиксатора волос, и в основном используется в таких продуктах, как тушь, подводка для глаз. , кондиционеры для волос, лаки для волос, шампуни и другие средства по уходу за волосами. PVP также обладает способностью высыхать и образовывать тонкое покрытие на коже, ногтях или волосах, а когда он рассматривается как ингредиент в продуктах для волос, он используется для фиксации прически, предотвращая способность волос впитывать влагу.Он также используется в растворах для контактных линз и в качестве загустителя в отбеливающих зубных пастах и гелях для отбеливания зубов.
, кондиционеры для волос, лаки для волос, шампуни и другие средства по уходу за волосами. PVP также обладает способностью высыхать и образовывать тонкое покрытие на коже, ногтях или волосах, а когда он рассматривается как ингредиент в продуктах для волос, он используется для фиксации прически, предотвращая способность волос впитывать влагу.Он также используется в растворах для контактных линз и в качестве загустителя в отбеливающих зубных пастах и гелях для отбеливания зубов.
9.4.8 Связующее
ПВП также используется в качестве связующего в процессе изготовления таблеток и нанесения покрытия [37]. В целом, физико-химические характеристики лекарственных средств, связующих и других вспомогательных веществ могут иметь большое влияние на эффективность связывания. Кроме того, раствор связующего имеет более высокое поверхностное натяжение, что дает более плотные гранулы с большим средним размером частиц [38].
Ново-фенирам — использование, побочные эффекты, взаимодействия
Как действует это лекарство? Что я буду из этого иметь?
Хлорфенирамин относится к группе препаратов, известных как антигистаминные препараты первого поколения . Для взрослых и детей в возрасте от 6 лет он используется для лечения симптомов, вызванных аллергией, , включая зуд и слезотечение, чихание, насморк, кожную сыпь и раздражение. Он также используется для лечения кожного зуда, вызванного укусами насекомых и других заболеваний, таких как ветряная оспа или корь.Хлорфенирамин действует, блокируя действие гистамина — вещества, выделяемого клетками организма, вызывающими симптомы аллергии.
Для взрослых и детей в возрасте от 6 лет он используется для лечения симптомов, вызванных аллергией, , включая зуд и слезотечение, чихание, насморк, кожную сыпь и раздражение. Он также используется для лечения кожного зуда, вызванного укусами насекомых и других заболеваний, таких как ветряная оспа или корь.Хлорфенирамин действует, блокируя действие гистамина — вещества, выделяемого клетками организма, вызывающими симптомы аллергии.
Ваш врач мог порекомендовать это лекарство при состояниях, отличных от перечисленных в этих статьях с информацией о лекарствах. Кроме того, некоторые формы этого лекарства не могут использоваться для всех состояний, обсуждаемых здесь. Если вы не обсуждали это со своим врачом или не знаете, почему вы принимаете это лекарство, поговорите со своим врачом. Не прекращайте прием этого лекарства, не посоветовавшись с врачом.
Не давайте это лекарство кому-либо еще, даже если у него такие же симптомы, как и у вас. Людям может быть вредно принимать это лекарство, если их не прописал врач.
В какой форме (формах) входит это лекарство?
Каждая круглая желтая таблетка с отметками «novo» над «4» на одной стороне содержит 4 мг хлорфенирамина малеата. Немедицинские ингредиенты: альгиновая кислота, кукурузный крахмал, D&C Yellow No. 10, двухосновный фосфат кальция, FD&C Yellow No. 6, стеарат магния и микрокристаллическая целлюлоза.
Как мне использовать это лекарство?
При аллергическом рините обычная доза для взрослых и детей от 12 лет и старше составляет 4 мг каждые 4-6 часов. Для таблеток с расширенным высвобождением обычная доза для взрослых и детей от 12 лет и старше составляет 12 мг каждые 12 часов.Максимальная рекомендуемая доза составляет 24 мг в течение 24 часов.
Для профилактики сезонного аллергического ринита рекомендуемая начальная доза составляет 4 мг перед сном, которую можно увеличить до 8 мг 3 раза в день по мере необходимости в течение 2-недельного периода.
Для детей от 6 до 11 лет обычная рекомендуемая доза составляет 2 мг каждые 4-6 часов. Максимальная рекомендуемая доза составляет 12 мг в течение 24 часов. Этот препарат не рекомендуется детям младше 6 лет, если он не рекомендован врачом.
Пожилым людям могут потребоваться более низкие дозы этого лекарства.
На дозу лекарства, которая нужна человеку, могут влиять многие факторы, например масса тела, другие заболевания и другие лекарства. Если ваш врач рекомендовал дозу, отличную от перечисленных здесь, не изменяйте способ приема лекарства без консультации с врачом.
Важно принимать это лекарство точно в соответствии с рекомендациями врача или фармацевта.Если вы пропустите прием, примите его как можно скорее и продолжайте придерживаться своего обычного графика. Если пришло время для следующей дозы, пропустите пропущенную дозу и продолжите свой обычный график дозирования. Не принимайте двойную дозу, чтобы восполнить пропущенную. Если вы не знаете, что делать после пропуска дозы, обратитесь за советом к своему врачу или фармацевту.
Если вы не знаете, что делать после пропуска дозы, обратитесь за советом к своему врачу или фармацевту.
Храните это лекарство при комнатной температуре, защищайте от света и влаги и храните в недоступном для детей месте.
Не выбрасывайте лекарства в сточные воды (например, в раковину или в унитаз) или вместе с бытовым мусором. Спросите своего фармацевта, как утилизировать лекарства, которые больше не нужны или срок годности которых истек.
Кому НЕ следует принимать это лекарство?
Не принимайте это лекарство, если вы:
- имеют аллергию на хлорфенирамин или какие-либо ингредиенты этого лекарства
- принимают ингибитор МАО (например,g., фенелзин, транилципромин, моклобемид)
Не давайте это лекарство новорожденным или недоношенным детям.
Какие побочные эффекты возможны при приеме этого лекарства?
Многие лекарства могут вызывать побочные эффекты. Побочный эффект — это нежелательная реакция на лекарство, когда оно принимается в обычных дозах. Побочные эффекты могут быть легкими или тяжелыми, временными или постоянными.
Побочный эффект — это нежелательная реакция на лекарство, когда оно принимается в обычных дозах. Побочные эффекты могут быть легкими или тяжелыми, временными или постоянными.
Побочные эффекты, перечисленные ниже, испытывают не все, кто принимает это лекарство. Если вас беспокоят побочные эффекты, обсудите риски и преимущества этого лекарства со своим врачом.
По крайней мере, 1% людей, принимающих это лекарство, сообщили о следующих побочных эффектах. Со многими из этих побочных эффектов можно справиться, а некоторые могут исчезнуть сами по себе со временем.
Обратитесь к врачу, если вы испытываете эти побочные эффекты, которые являются серьезными или надоедливыми. Ваш фармацевт может посоветовать вам, как бороться с побочными эффектами.
- боль в животе
- запор
- понос
- затрудненное мочеиспускание
- головокружение
- сонливость
- сухость во рту
- потеря аппетита
- тошнота
- сексуальные трудности
- усталость
- сухость влагалища
- рвота
Хотя большинство из перечисленных ниже побочных эффектов случаются не очень часто, они могут привести к серьезным проблемам, если вы не обратитесь за медицинской помощью.
При появлении любого из следующих побочных эффектов как можно скорее обратитесь к врачу:
- путаница
- трудности со сном
- возбуждение
- галлюцинации (видеть, слышать или чувствовать то, чего нет)
- несогласованность
- кошмаров
- болезненное мочеиспускание
- беспокойство или нервозность
- кожная сыпь или крапивница
- необычный синяк или кровотечение
- проблемы со зрением (e.г., нечеткость зрения)
Прекратите прием лекарства и немедленно обратитесь за медицинской помощью, если возникнут какие-либо из следующего:
Некоторые люди могут испытывать побочные эффекты, отличные от перечисленных. Проконсультируйтесь с врачом, если вы заметили какой-либо симптом, который вас беспокоит, пока вы принимаете это лекарство.
Существуют ли другие меры предосторожности или предупреждения для этого лекарства?
Перед тем, как начать прием лекарств, обязательно сообщите своему врачу о любых медицинских состояниях или аллергии, которые у вас могут быть, о любых принимаемых вами лекарствах, о том, беременны ли вы или кормите грудью, и о любых других важных фактах о вашем здоровье. Эти факторы могут повлиять на то, как вам следует принимать это лекарство.
Эти факторы могут повлиять на то, как вам следует принимать это лекарство.
Сонливость / снижение активности: Это лекарство может вызвать сонливость. Избегайте вождения или эксплуатации механизмов, пока вы не решите, что вы не чувствуете сонливость в течение дня или не испытываете ухудшение умственных или физических способностей при приеме этого лекарства.
Функция печени: Если у вас снижена функция печени, обсудите со своим врачом, как это лекарство может повлиять на ваше состояние здоровья, как ваше состояние может повлиять на дозировку и эффективность этого лекарства, и нужен ли какой-либо специальный мониторинг.
Медицинские условия: Если у вас есть какое-либо из следующих заболеваний, обсудите со своим врачом, как это лекарство может повлиять на ваше состояние здоровья, как ваше заболевание может повлиять на дозировку и эффективность этого лекарства, и требуется ли какой-либо специальный мониторинг. :
- закрытоугольная глаукома
- хронические заболевания легких, такие как астма, хронический бронхит или эмфизема
- увеличенная простата
- порок сердца
- Обструкция мочевого пузыря
- Непроходимость кишечника
- язвенная болезнь
- изъятий
Беременность: Это лекарство не следует использовать во время беременности, если польза не превышает риски.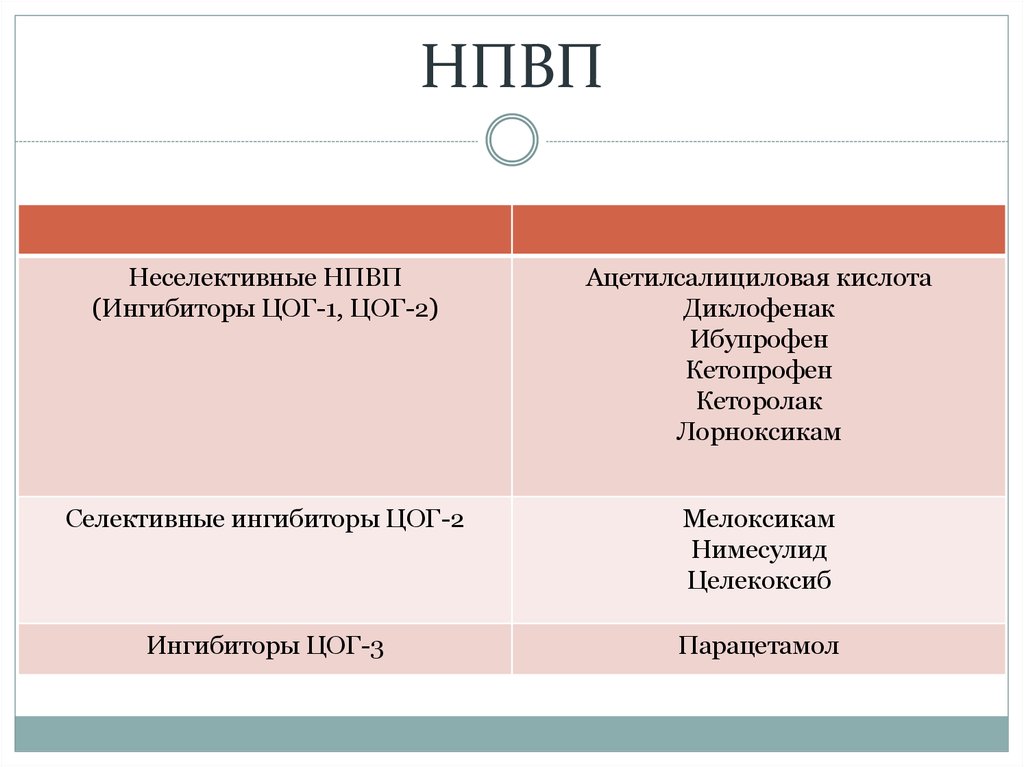 Если вы забеременели во время приема этого лекарства, немедленно обратитесь к врачу.
Если вы забеременели во время приема этого лекарства, немедленно обратитесь к врачу.
Кормление грудью: Это лекарство проникает в грудное молоко, но не оказывает серьезного или вредного воздействия на грудных детей. Поговорите со своим врачом о том, следует ли вам продолжать кормить грудью.
Дети: Безопасность и эффективность использования этого лекарства не установлены для детей младше 6 лет.
Пожилые люди: Пожилые люди могут испытывать больше побочных эффектов (например,g., сонливость, сухость во рту, затрудненное мочеиспускание) с этим лекарством. Это лекарство не следует использовать пожилым людям, если они не рекомендованы врачом, фармацевтом или другим медицинским работником.
Какие другие препараты могут взаимодействовать с этим лекарством?
Может быть взаимодействие между хлорфенирамином и любым из следующего:
- спирт
- барбитуратов (например, фенобарбитал, пентобарбитал)
- бензодиазепинов (например,g.
 , лоразепам, диазепам)
, лоразепам, диазепам) - кларитромицин
- эритромицин
- кетоконазол
- Ингибиторы МАО (например, фенелзин, транилципромин, моклобемид)
- лекарств с антихолинергическим действием (например, бензтропин, дифенгидрамин)
- наркотические анальгетики (например, кодеин, морфин, оксикодон)
- нейролептические препараты (например, галоперидол, рисперидон)
- фенитоин
- трициклические антидепрессанты (например,g., амитриптилин, нортриптилин, дезипрамин)
Если вы принимаете какие-либо из этих лекарств, поговорите со своим врачом или фармацевтом. В зависимости от ваших конкретных обстоятельств ваш врач может попросить вас:
- прекратить прием одного из препаратов,
- заменить одно лекарство на другое,
- изменить способ приема одного или обоих лекарств, или
- оставь все как есть.
Взаимодействие между двумя лекарствами не всегда означает, что вы должны прекратить прием одного из них. Поговорите со своим врачом о том, как контролируются или следует управлять любыми лекарственными взаимодействиями.
Лекарства, отличные от перечисленных выше, могут взаимодействовать с этим лекарством. Сообщите своему врачу или лицу, выписывающему рецепт, обо всех лекарствах, отпускаемых по рецепту, без рецепта (без рецепта) и лекарственных травах, которые вы принимаете. Также расскажите им о любых добавках, которые вы принимаете. Поскольку кофеин, алкоголь, никотин из сигарет или уличные наркотики могут влиять на действие многих лекарств, вы должны сообщить своему врачу, если вы их используете.
Авторские права на все материалы принадлежат MediResource Inc. 1996–2021 гг. Условия использования. Содержимое данного документа предназначено только для информационных целей. Всегда обращайтесь за советом к своему врачу или другому квалифицированному поставщику медицинских услуг по любым вопросам, которые могут у вас возникнуть относительно состояния здоровья. Источник: www.medbroadcast.com/drug/getdrug/Novo-Pheniram
Влияние молекулярной массы ПВП на поведение при растворении и физико-химические характеристики твердых дисперсий глицирретиновой кислоты
Было исследовано влияние поливинилпирролидона (ПВП) в качестве носителя твердых дисперсий глицирретиновой кислоты (ГА) с разной молекулярной массой на поведение при растворении и физико-химические свойства.PVP-GA-SD, полученные с PVP всех четырех молекулярных масс, показали хорошее повышение скорости растворения и равновесной растворимости по сравнению с чистым лекарственным средством и соответствующими физическими смесями. Результаты показали, что влияние увеличения молекулярной массы на скорость растворения и равновесную растворимость следует. Кроме того, скорость растворения и растворимость SD с соотношением носитель к лекарству 8: 1 были лучше, чем у образцов 4: 1. Картины DSC и XRD показали, что кристаллизация GA в SD, полученных с помощью PVP K30 и PVP K60 был значительно ингибирован, и оба они превратились в аморфные.На основе FTIR и рамановского детектирования образуется водородная связь между PVP и молекулами лекарства. Результаты SEM показали, что не было значительных различий во внешнем виде SD, приготовленных с четырьмя PVP, и не было обнаружено кристаллической морфологии GA. В заключение, результаты этого исследования продемонстрировали, что эффективность растворения PVP-GA-SD, полученных методом растворителя, связана с молекулярной массой PVP, и изменение молекулярной массы PVP не вызывает монотонного изменения в роспуск ГА.Образцы с PVP K30 в качестве носителя обладают наилучшими характеристиками растворения.
1. Введение
Глицирретиновая кислота (GA) является одним из основных активных ингредиентов, извлекаемых из корня или корневища солодки [1]. Это также продукт распада глицирретовой кислоты в организме, которая является основным активным компонентом солодки [2]. Молекулярная формула GA: C 30 H 46 O 4 , а молекулярная масса составляет 470,69. Структурная формула представлена на рисунке 1.Исследования показали, что глицирретовая кислота обладает противовоспалительным, противовирусным, противоопухолевым и другими фармакологическими эффектами [3–5]. В настоящее время его часто используют в клинической практике для лечения хронического гепатита и рака печени [6]. Однако из-за сильной гидрофобности глицирретовой кислоты ее растворимость и скорость растворения низкие. Это также ограничивает пероральную биодоступность глицирретовой кислоты [7]. В общем, растворимость гидрофобного лекарственного средства может быть улучшена путем добавления поверхностно-активного вещества, но большое количество солюбилизатора склонно к побочным эффектам, таким как гемолиз.Чтобы преодолеть плохую растворимость GA, в последние годы были проведены некоторые исследования новых систем доставки лекарств GA, включая липосомы GA [8], наноэмульсии GA [9], микрочастицы GA [10] и твердую дисперсию GA [ 11].
Метод твердых дисперсий (SDs) относится к однородной дисперсионной системе лекарственных средств в форме молекул, микрокристаллов, аморфных и других состояний в твердом носителе. Благодаря высокой дисперсности лекарства и высокой гидрофильности носителя смачиваемость лекарства улучшается.Таким образом, этот метод является эффективным методом улучшения растворения и пероральной биодоступности малорастворимых лекарств. В настоящее время существует несколько коммерческих продуктов на основе твердых дисперсий [12], таких как вемурафениб (Zelboraf®), регорафениб (Stivarga®) и эверолимус (Afinitor®). Твердые дисперсии часто получают четырьмя способами, включая метод смешивания, метод плавления, метод плавления растворителем и метод растворения. Метод с использованием растворителя также называется методом соосаждения, в этом методе твердая дисперсия может быть получена после испарения растворителя из раствора, содержащего носитель и лекарственное средство.Некоторые полимеры практически не используются в качестве носителей в способе плавления из-за их высокой температуры плавления или термического разложения. Поскольку метод с использованием растворителя может быть реализован без использования высокой температуры в процессе приготовления, этот метод подходит для термически нестабильных лекарств или носителей с высокой температурой плавления [13, 14]. В настоящее время наиболее часто используемым носителем в методе растворителей является поливинилпирролидон (ПВП) [15].
Поливинилпирролидон (ПВП) — аморфный высокомолекулярный полимер с высокой температурой плавления, устойчивый к нагреванию, легко растворимый в воде и многих органических растворителях.После перорального приема ПВП не всасывается в желудочно-кишечном тракте и не токсичен [16]. Обычно используемые спецификации PVP включают PVP K15, PVP K17, PVP K30, PVP K60 и PVP K90 (средняя молекулярная масса составляет около 8000, 10000, 50000, 400000 и 1000000). До настоящего времени сообщалось об исследованиях этих характеристик ПВП как твердых носителей дисперсии [17–19]. Вообще говоря, после того, как лекарство диспергировано в ПВП, легко образовать аморфную твердую дисперсию из-за сильного ингибирующего кристаллографического эффекта ПВП [20].Исследования показали, что профиль высвобождения лекарства из аморфных твердых дисперсий определяется свойствами полимера. Аморфные твердые дисперсии демонстрируют более высокую кажущуюся растворимость, чем кристаллическое лекарственное средство, из-за эффекта «пружины и парашюта», который включает два ключевых этапа, а именно создание метастабильного состояния перенасыщения и ингибирование осаждения [21]. Величина эффекта «пружины и парашюта» сильно зависит от типа и молекулярной массы полимера. Следовательно, важно изучить влияние молекулярной массы на свойства твердых дисперсий [22].
В Scopus найдено 59 статей по ключевым словам: «ПВП», «молекулярная масса» и «твердая дисперсия». В общей сложности 14 статей содержат исследования взаимосвязи между молекулярной массой ПВП и растворимостью или растворением лекарственного средства, и только в 6 исследованиях сравниваются экспериментально определенные скорости растворения твердых дисперсий, приготовленных с использованием более двух молекулярных масс ПВП в качестве носителей. Более того, все исследования были сосредоточены на синтетических препаратах с молекулярной массой менее 400, которые обычно используются в клинике с жаропонижающим, противовоспалительным и понижающим кровяное давление действием.
Большинство предыдущих исследований [23–26] показали, что скорость растворения лекарственного средства из SD уменьшается с увеличением молекулярной массы PVP. Несколько исследований показали, что ПВП немонотонно влияет на растворение лекарств в твердых дисперсиях [27]. Эти исследования показывают, что влияние молекулярной массы ПВП на скорость растворения лекарственного средства в твердых дисперсиях связано со структурными характеристиками лекарственного средства.
На сегодняшний день существует мало исследований твердых дисперсий глицирретиновой кислоты, и нет исследований влияния молекулярной массы ПВП на поведение растворения твердых дисперсий глицирретиновой кислоты или других структурно подобных пентациклических тритерпеноидов (олеаноловая кислота, глицирризиновая кислота. , урсоловая кислота и др.). По этой причине целью настоящего исследования было изучить влияние ПВП с различной молекулярной массой в качестве носителей на поведение растворения твердой дисперсии глицирретовой кислоты методом растворителя. Кроме того, различия в физических и химических свойствах, особенно в отношении ингибирования кристаллизации, были дополнительно исследованы путем изучения микроморфологии и структурных свойств с использованием SEM, FTIR, XRD и других методов идентификации.
2. Материалы и методы
2.1. Материалы
GA (чистота> 98%), эталонное соединение GA, PVP K15, PVP K17, PVP K30 и PVP K60 (аналитически чистый), было получено от Dalian Meilun Biology Technology Co., Ltd (Далянь, Китай. ). Этанол был приобретен у Sinopharm Chemical Reagent Co., Ltd. (Пекин, Китай). Чистую воду готовили с помощью системы очистки воды Milli-Q (Millipore, Бедфорд, Массачусетс, США).
2.2. Приготовление твердых дисперсий
PVP-GA-SD получали методом растворителя. Вкратце, GA и носитель взвешивали в соответствии с заданным количеством и помещали в чашку для выпаривания.Затем их совместно растворяли в 95% -ном () растворе этанол-вода и нагревали на водяной бане () при перемешивании. После удаления этанола смесь вынимали и помещали в вакуумную сушилку на несколько дней, а затем измельчали и просеивали через сита 80 меш для последующих экспериментов.
2.3. Приготовление физических смесей
Физические смеси (PM) готовили путем ручного смешивания GA и различных PVP, которые предварительно просеивали через 80 в ступке в течение 5 минут до получения гомогенной смеси.
2.4. Анализ для характеристики твердых дисперсий
2.4.1. Определение равновесной растворимости
Избыточный образец (чистый GA, PM или SD, эквивалентный 10,0 мг GA) добавляли в 10 мл чистой воды, PBS () и 0,1 N раствор HCl при перемешивании магнитной мешалкой (300 об / мин) при 25 °. C на водяной бане с регулируемой температурой до достижения равновесия (48 ч). Образцы фильтровали через тефлоновый мембранный фильтр 0,45 мкм, мкм, разбавляли подходящим образом метанолом и анализировали с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ), как описано ниже.Растворимость лекарственного средства определяли с использованием системы ВЭЖХ LabAlliance (модель серии III) (Lab Alliance, Тяньцзинь, Китай), снабженной четвертичным насосом, автосэмплером и отделением колонки, соединенным с УФ-детектором. Разделение проводили на колонке C18 (; 5 мкм м; Dikma Technologies, Пекин, Китай). Подвижная фаза включает метанол, воду и уксусную кислоту (89: 10: 1) при скорости потока 1,0 мл · мин -1 . Аналиты детектировали УФ-детектором при 250 нм. Для GA обнаружена хорошая линейность в диапазоне 0.5-50 мк г · мл -1 .
2.4.2. Тестирование растворения in vitro
Скорость растворения определяли с использованием прибора USP типа II (RCZ-8A, Tiandatianfa Tech., Ltd., Тяньцзинь, Китай). 900 мл чистой воды, 0,1 н. Раствор HCl и раствор фосфатного буфера () использовали в качестве среды растворения () для твердого образца (эквивалент 10,0 мг лекарственного средства) при скорости вращения лопастей 100 об / мин. Через заранее определенные интервалы времени отбирали аликвоты по 5 мл, фильтровали через фильтр 0.45, мкм, мкм, тефлоновый мембранный фильтр, и анализировали с помощью ВЭЖХ. Удаленный объем был заменен свежей средой для поддержания условий погружения. Растворение лекарства проводили в трех экземплярах.
2.4.3. Дифференциальная сканирующая калориметрия (DSC)
Измерения DSC проводили на сканирующем калориметре HSC-1 DSC (Hengjiu Instrument, Ltd., Пекин, Китай). Образцы точно взвешивали (10 мг) и запаивали в алюминиевый тигель. Образцы нагревали от 25 до 350 ° C со скоростью 10 ° C · мин -1 в атмосфере азота.
2.4.4. Рентгеновская дифракция (XRD)
Структурные свойства образцов получены на рентгеновском дифрактометре D8 Focus (Bruker, Германия) с излучением Cu-K α . Измерения проводились при напряжении 40 кВ и 40 мА. Образцы сканировали от 5 ° до 60 °, и скорость сканирования составляла 5 ° · мин -1 .
2.4.5. Инфракрасная спектроскопия с преобразованием Фурье (FTIR)
FTIR-спектры образцов получали на спектрофотометре Nicolet 6700 FT-IR (Thermo Scientific, Waltham, MA, USA).Каждый образец и бромид калия смешивали в агатовой ступке и прессовали в тонкий диск. Диапазон сканирования составлял 4000–400 см –1 , а разрешение — 4 см –1 .
2.4.6. Рамановская спектрометрия (RS)
FT-Рамановские спектры были получены с помощью Nicolet 6700 FTIR с модулем NXR FT-Raman (1064 нм) в диапазоне волновых чисел 3700–100 см -1 с накоплением 64 сканирований с 4 см -1 спектральное разрешение.
2.4.7. Сканирующая электронная микроскопия (SEM)
Образцы были прикреплены к штырю SEM с углеродным проводником и покрыты золотом с помощью распылителя SBC-12 (KYKY Tech., Ltd., Пекин, Китай). Затем морфологию поверхности образца наблюдали с помощью растрового электронного микроскопа S-4300 (Hitachi, Токио, Япония).
3. Результаты и обсуждение
3.1. Определение равновесной растворимости
Растворимость лекарства в твердой дисперсионной системе обычно выше, чем у чистого лекарства, и тип растворяющей среды также влияет на растворимость лекарства в твердой дисперсии. В этом исследовании была определена равновесная растворимость четырех видов PVP-GA-SD и четырех видов PVP-GA-PM в чистой воде, PBS и растворе соляной кислоты, как указано в разделе 2.4.1 соответственно. Результаты показаны в таблице 1.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 «-» означает, что концентрация ниже предела обнаружения. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Данные в таблице показали, что растворимость GA в чистой воде улучшалась за счет SD, полученных с PVP с различными молекулярными массами в качестве носителя. Среди них эффекты солюбилизации PVP K30-GA-SD и PVP K60-GA-SD были лучше, чем эффекты PVP K17-GA-SD и PVP K 15-GA-SD. PVPK30 с массовым соотношением носитель: лекарственное средство 8: 1 проявлял самую сильную солюбилизирующую способность, и его растворимость была такой же. В растворе соляной кислоты PVP K30-GA-SD и PVP K60-GA-SD сохраняли определенное улучшение солюбилизации, но растворимость других SD не могла быть обнаружена, а PVP K30-GA-SDs имеет значительно более высокую растворимость, чем PVP K60. -GA-SD.По сравнению с двумя вышеупомянутыми средами в PBS SD имели лучшую солюбилизацию. Точно так же эффекты солюбилизации PVP K30-GA-SD и PVP K60-GA-SD лучше, чем у PVP K15-GA-SD и PVP K17-GA-SD. Среди всех образцов твердых дисперсий PVP K30-GA-SD с массовым соотношением носитель-лекарственное средство 8: 1 имеет лучший солюбилизирующий эффект с растворимостью. С другой стороны, все физические смеси более растворимы в PBS, чем в чистой воде, и их растворимость в соляной кислоте не может быть обнаружена.
3.2. Определение скорости растворения in vitro
В общем, PBS и раствор соляной кислоты использовали в качестве моделирования кишечной и желудочной жидкости соответственно. Согласно приведенным выше результатам, равновесная растворимость каждой твердой дисперсии в PBS выше, чем в двух других средах растворения. Кроме того, использование среды с соляной кислотой не гарантирует, что все твердые дисперсии будут проводить эксперименты по растворению в условиях поглощения. Чтобы удовлетворить условию поглощения, PBS был выбран в качестве среды растворения при определении растворения.Скорости растворения чистого GA, четырех PM и четырех SD в PBS показаны на рисунке 2.
Результаты экспериментов показали, что молекулярная масса PVP оказывает значительное влияние на поведение растворения PVP-GA-SD. Однако нет линейной зависимости между скоростью растворения и молекулярной массой. Скорость растворения SD с соотношением носитель: лекарственное средство 8: 1 и 4: 1 имеют следующий порядок:, что также согласуется с соотношением между молекулярной массой PVP и равновесной растворимостью GA в PBS.С другой стороны, массовые отношения носитель-лекарственное средство имеют очевидное влияние на скорость растворения SD. До 120 мин скорость растворения SD с соотношением носитель-лекарственное средство 8: 1 () была выше, чем 4: 1 () при тех же условиях молекулярной массы PVP. Когда соотношение носитель-лекарственное средство составляло 4: 1, скорость растворения SD с PVP K30 и PVP K60 имела тенденцию к равновесию через 120 мин. Когда коэффициент загрузки лекарственного средства составлял 8: 1, скорость растворения каждого SD с PVP K30 и PVP K60 имела тенденцию к равновесию через 60 минут.В целом скорость растворения с PVP K30 в качестве носителя была самой высокой. Совокупный процент растворения PVP K30-GA-SD (8: 1) может достигаться на 10-й минуте.
Чистый GA и все PM были ниже, чем SD, и PM несколько отличаются от GA. Мы наблюдали, что максимальный процент растворения PM, приготовленных с PVP K15 и PVP K17, был немного выше, чем у образцов с двумя другими PVP.
3.3. Дифференциальная сканирующая калориметрия (DSC)
Методы термического анализа можно использовать для предположения об изменении кристалличности лекарственного средства или взаимодействиях лекарственного средства с носителем в твердых дисперсиях.Некоторые исследования показали, что эндотермические пики плавления лекарства могут наблюдаться в физических смесях определенных кристаллических лекарств и ПВП, и как только лекарство становится аморфным или лекарство взаимодействует с носителем, соответствующие пики температуры плавления исчезают или ослабевают [20, 28-30 ]. Поэтому в данном исследовании мы сравнили термические свойства твердых дисперсий, приготовленных из четырех ПВП с различной молекулярной массой.
На термограмме ДСК (рис. 3) GA показал пик поглощения при 299 ° C, который был пиком плавления GA.Не было обнаружено явных характеристических пиков для всех четырех ПВП с разной молекулярной массой из-за аморфной природы ПВП. Этот пик плавления ГА также не наблюдался в физических смесях ГА с ПВП. О таком же поведении сообщалось о физической смеси преднизолона с ПВП [31, 32]. Причиной этого может быть низкое содержание GA по сравнению с PVP, что приводит к низкой теплотворной способности, которая не может отображаться в спектрах PM. Кроме того, SD показали аналогичное поведение из-за отсутствия пика плавления GA, из которого можно сделать вывод, что кристаллическая структура лекарственного средства в этих образцах исчезла.Однако эта информация о том, изменилась ли кристалличность GA, недоступна, может быть подтверждена только с помощью других методов, таких как дифракция рентгеновских лучей.
3.4. Рентгеноструктурный анализ (XRD)
Многие исследования показали, что твердые дисперсии лекарственного средства ПВП, полученные методами растворителя, имеют тенденцию образовывать стеклообразное состояние. Поскольку носитель стеклообразного твердого раствора имеет высокую вязкость и легко взаимодействует с лекарством, кристаллизация лекарства подавляется [33–35]. Чтобы оценить, было ли это кристаллическим изменением GA в SD с различной молекулярной массой PVP, для обнаружения был проведен XRD-анализ.Как показано на фиг. 4 (a) и 4 (d), GA демонстрирует несколько отчетливых и острых дифракционных пиков кристаллической формы от 3 ° до 60 °, что указывает на то, что GA существует в высококристаллической форме.
Четыре ПВП с разной молекулярной массой не показали характерных дифракционных пиков в диапазоне сканирования, что указывает на то, что все они существуют в аморфной форме. Пики дифракции кристаллов GA наблюдались в соответствующих положениях всех PM, полученных с помощью четырех PVP с разной молекулярной массой, что позволяет предположить, что лекарство существует в кристаллической форме во всех PM.
Среди XRD-спектра SD характерные дифракционные пики GA SD, полученных с помощью PVP K30 и PVP K60, в основном исчезли, что указывает на то, что GA существует в аморфной форме. Характерные дифракционные пики ГА для SD, полученных с ПВП К15 и ПВП К17, все еще могут быть ясно видны, что указывает на то, что ГА существует в кристаллической форме. Следовательно, можно предположить, что кристаллизация ГК SD, полученных с ПВП К30 и ПВП К60, может быть значительно ингибирована. Этот результат имеет положительную корреляцию с более высокой растворимостью ПВП K30-SD и ПВП K60-SD по сравнению с двумя другими твердыми дисперсиями.
Согласно модели высвобождения лекарственного средства SD с водорастворимым полимером в качестве носителя, предложенной Крейгом, высвобождение лекарственного средства из SD связано не только с полимером, но и с лекарством [36]. Что касается PVP-GA-SD, приготовленных в этом исследовании, мы предполагаем, что, когда PVP K15, PVP K17 и PVP K30 используются в качестве носителей, GA в основном высвобождается в виде твердых частиц, а на скорость растворения в основном влияют размер и кристалличность. препарата. Из спектра XRD видно, что кристалличность PVP K30-GA-SD значительно ниже, чем у PVP K15-GA-SD и PVP K17-GA-SD, что приводит к более высокому химическому потенциалу и перенасыщению лекарственных средств в PVP K30-GA-SDs и, следовательно, имеет более высокую скорость растворения.С другой стороны, согласно модели высвобождения лекарства, молекулы лекарства должны сначала пройти через богатый полимером диффузионный слой, а затем высвободиться в объемную фазу. Согласно уравнению Стокса-Эйнштейна коэффициент диффузии обратно пропорционален вязкости. Хотя спектр XRD показывает, что GA в PVP K30-GA-SD и PVP K30-GA-SD оба преобразованы в аморфные, вязкость PVP K60 больше, чем PVP K30, поэтому, когда лекарство первоначально высвобождается из PVP K60, он блокируется диффузионным слоем полимера, поэтому скорость растворения PVP K60-GA-SD ниже, чем у PVP K30-GA-SD.
3.5. Инфракрасный (ИК) спектральный анализ
Многие исследования показали, что твердые дисперсии могут увеличивать растворимость лекарства, связанную с взаимодействиями лекарство-носитель, особенно с образованием водородных связей [37]. В этом исследовании FTIR использовался для обнаружения потенциальных эффектов межмолекулярного взаимодействия твердых дисперсных систем.
Как видно на рисунках 5 (a) и 5 (d), в ИК-спектрах GA пики GA при 1704 см -1 и 1664 см -1 приписываются C = O в карбоновой кислоте. и карбонильные части [38].Пик поглощения фенола-ОН в C3 находился при 3,440 см -1 , а пик поглощения при 2,940 см -1 обусловлен валентным колебанием гидроксила в карбоксильной группе (синяя пунктирная линия). Пики поглощения (красная пунктирная линия) C = O были обнаружены при примерно 1,662 см -1 в четырех ПВП с разной молекулярной массой [30, 39].
В ИК-спектрах различных PM, кроме PVP K15-GA-PM, все еще можно наблюдать два пика поглощения при 1704 см -1 и 1,664 см -1 GA, и они перекрываются с пиком поглощения карбонила. при 1662 см -1 ПВП, тогда как эти два пика поглощения в ИК-спектрах ПВП K15-GA-PM имели тенденцию образовывать один пик.Кроме того, пик абсорбции при 2940 см -1 можно ясно увидеть в физических смесях ПВП с четырьмя молекулярными массами и лекарственного средства. Однако в ИК-спектрах всех четырех SD пиков 2940 см -1 явно ослаблены, особенно для PVP K30-GA-SD и PVP K60-GA-SD. Кроме того, по сравнению с PM, два пика (1,704 см -1 и 1,664 см -1 ) GA превращаются в один пик, а интенсивность пика ослабляется и притупляется с разной степенью.Более отчетливо это видно в ИК-спектрах ПВП K30-GA-SD и ПВП K60-SD. Эти результаты предполагают, что гидроксил в карбоксильной группе в GA может образовывать водородную связь с C = O ПВП, что изменяет характеристики ИК-спектров; схематическая диаграмма межмолекулярной водородной связи между GA и PVP показана на рисунке 6. Этот результат также согласуется с результатами, обнаруженными с помощью XRD. Эффект водородной связи PVP K30-GA-SDs и PVP K60-GA-SDs более очевиден, и их характерная пиковая сила XRD также слабее, что указывает на то, что взаимодействие водородных связей между GA и PVP приводит к образованию аморфной структуры. глицирретовой кислоты.Кроме того, поскольку пик поглощения гидроксила ГА при 3440 см -1 перекрывается с характеристическим пиком поглощения ПВП при 3710-3020 см -1 , мы не можем наблюдать, соответствует ли пик поглощения гидроксила С3 ГА в ГА-СД имеет явную миграцию или пассивацию. Следовательно, с помощью инфракрасной спектроскопии мы не можем сделать вывод, образовала ли гидроксильная группа C3 водородная связь с карбонильной группой ПВП.
3.6. Рамановская спектроскопия
Рамановская спектроскопия и инфракрасная спектроскопия — это колебательные спектры молекул, и они дополняют друг друга.Вообще говоря, асимметричные колебания полярных групп больше подходят для обнаружения с помощью инфракрасного излучения. Колебания неполярных групп и молекулярные колебания полной симметрии больше подходят для обнаружения с помощью комбинационного рассеяния света. В некоторых исследованиях использовалась рамановская спектроскопия для изучения взаимодействия полимеров и лекарств в твердых дисперсиях [40, 41]. Поэтому, чтобы сравнить влияние носителей с разной молекулярной массой на структуру твердых дисперсий, для каждого образца был проведен анализ спектра комбинационного рассеяния.
Как показано на рисунках 7 (a) и 7 (d), чистый GA имел два острых характеристических пика при 1620 см -1 и 1670 см -1 , что приписывается валентным колебаниям карбонильной части и — COO- группа [11]. Четыре ПВП с разной молекулярной массой также показали значительный пик рассеяния карбонилов при 1670 см -1 [42], и форма пика нечеткая. Однако острый пик рассеяния в форме пика (красная прямоугольная рамка) может наблюдаться при 1670 см -1 в PM (синяя пунктирная линия) четырех ПВП и ГА с различной молекулярной массой, что указывает на то, что пик рассеяния PM при 1670 см -1 является результатом перекрытия двух пиков рассеяния без химической реакции.По сравнению с физическими смесями пики рассеяния GA-SD, полученных с использованием четырех ПВП с молекулярной массой, при 1670 см -1 , очевидно, шире и слабее (красная прямоугольная рамка). Это согласуется с результатами XRD. Более того, в спектрах PVP-GA-SD (4: 1), полученных из PVP с четырьмя молекулярными массами, все пики при 1670 см -1 все смещаются в сторону области с низким волновым числом (голубая пунктирная линия). Однако в спектре PVP-GA-SD (8: 1) пик рассеяния при 1670 см -1 не сдвинулся.Это может быть связано с низким содержанием ГА в образце, что привело к диспергированию и ослаблению водородных связей на площади поверхности и не привело к изменению пика рассеяния. Исходя из этого результата, можно предположить, что карбонильная группа ПВП образует водородную связь с гидроксильной группой молекулы глицирретовой кислоты.
3,7. Анализ с помощью сканирующего электронного микроскопа (СЭМ)
Рисунок 8 (а) представляет собой СЭМ-изображение ГА, показывающее, что ГА имеет стержнеобразную форму и четкую кристаллическую форму. Рисунки 8 (b) и 8 (e) представляют собой СЭМ-изображения PVP-GA-SD (8: 1), представляющие SD как неправильные массы с ненаблюдаемым стержнеобразным кристаллом GA.Это говорит о том, что глицирретовая кислота равномерно диспергирована в ПВП в аморфной или микрокристаллической форме. По сравнению с PVP K60-GA-SD поверхность твердых дисперсий, приготовленных из PVP K15, PVPK17 и PVP K30, более гладкая. Это может быть связано с большей молекулярной массой PVP K60, что приводит к большей когезии. Кроме того, средний размер частиц SD, полученных с PVP K60 в качестве носителя, был больше, чем размер образцов с другими тремя PVP с молекулярной массой. Однако исследования растворимости и растворения показали, что рабочие характеристики PVP K60-SD были лучше, чем PVP K15-SD и PVP K17-SD, что указывает на то, что размер частиц твердой дисперсии не оказывает значительного влияния на растворение.Согласно уравнению Нойеса-Уитни, скорость растворения лекарства связана с размером частиц лекарства [22]. Хотя размер частиц PVP K60-SD был больше, чем у образцов, приготовленных с использованием PVP K15 и PVP K17, эффективность диспергирования GA в PVP K60 может быть лучше, что приводит к лучшей растворимости и характеристикам растворения.
4. Выводы
Результаты подтвердили, что молекулярная масса носителя оказывает значительное влияние на скорость растворения лекарственного средства из твердых дисперсных систем.Для конкретных лекарств влияние молекулярной массы носителя на его свойства растворения уникально. Согласно нашим исследованиям, когда PVP используется в качестве носителя и метод растворителя используется для приготовления твердых дисперсий глицирретовой кислоты, влияние молекулярной массы PVP на растворимость и растворение лекарства не является монотонным. Среди всех ПВП эффект растворения твердой дисперсии глицирретовой кислоты был наилучшим, когда ПВП К30 использовался в качестве носителя. И влияние весового соотношения носитель-лекарственное средство на эффект растворения также очевидно.Скорость растворения при массовом соотношении носитель и лекарство 8: 1 выше, чем у образца 4: 1. Это может быть полезно для выбора подходящих материалов для приложений GA. Ожидается, что PVP K30-GA-SD могут быть использованы в качестве идеального материала для разработки пероральных продуктов на основе глицирретовой кислоты. С другой стороны, в этом исследовании мы использовали только метод растворителя и исследовали только влияние четырех носителей молекулярной массы (включая ПВП К15, ПВП К17, ПВП К30 и ПВП К60) на свойства твердых дисперсий.Возможно, другие методы подготовки (такие как электроспиннинг и экструзия из горячего расплава) или ПВП с другими молекулярными массами будут иметь лучшую скорость растворения, что требует дальнейших исследований.
Доступность данных
Данные, использованные для подтверждения результатов этого исследования, включены в статью.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Благодарности
Это исследование финансировалось Университетской программой медсестер для молодых ученых с творческими талантами в провинции Хэйлунцзян, Китай (UNPYSCT-2017168) и Фондом комитета по образованию в провинции Хэйлунцзян, Китай (2016-KYYWF-0856).
Роль укупорочных агентов в применении наночастиц в биомедицине и восстановлении окружающей среды: последние тенденции и перспективы на будущее | Журнал нанобиотехнологии
Салата О. Применение наночастиц в биологии и медицине. J Nanobiotechnol. 2004; 2: 3.
Артикул Google ученый
Ван С., Ян Х, Чжоу Л., Ли Дж., Чен Х. Двумерные наноструктуры за пределами графена: подготовка, биосовместимость и поведение при биодеградации.J Mater Chem B. 2020; 8: 2974.
CAS PubMed Статья PubMed Central Google ученый
Ван С., Чжоу Л., Чжэн И, Ли Л., Ву Ц, Ян Х, Хуанг М., Ан Х. Синтез и биосовместимость двумерных биоматериалов. Colloids Surf A. 2019; 583: 124004.
CAS Статья Google ученый
Гулати С., Сачдева М., Бхасин К.К. Укупорочные агенты в синтезе наночастиц: система поверхностно-активных веществ и растворителей.AIP Conf Proc. 2018; 1953: 030214.
Артикул CAS Google ученый
Айсида С.О., Батул А., Хан Ф.М., Рахман Л., Махмуд А., Ахмад И. и др. Композит с наностержнями PEG-Ni-ZnO, индуцированный кальцинированием, и его биомедицинские применения. Mater Chem Phys. 2020; 255: 123603.
CAS Статья Google ученый
Айсида С.О., Алнасир М.Х., Бота С., Башир АКХ, Бухер Р., Ахмад И. и др.Роль полиэтиленгликоля на микроструктурную, магнитную и удельную скорость поглощения в термоабляционных свойствах наночастиц феррита Mn-Zn по золь-гель протоколу. Eur Polymer J. 2020; 132: 109739.
CAS Статья Google ученый
Айсида С.О., Угвок Е., Увайс А., Ироэгбу С., Бота С., Ахмад И. и др. Инкубационный период индуцировал биогенный синтез ПЭГ, усилил нанокапсулы серебра Moringa oleifera и его антибактериальную активность.J Polym Res. 2019; 26: 225.
CAS Статья Google ученый
Раджендран К., Сен С. Влияние укупорочного агента на антимикробную активность наночастиц. Der Pharmacia Lettre. 2015; 7: 37–42.
CAS Google ученый
Джавед Р., Усман М., Табассум С., Зия М. Эффект укупорочных агентов: структурные, оптические и биологические свойства наночастиц ZnO.Appl Surf Sci. 2016; 386: 319–26.
CAS Статья Google ученый
Андерсон С.Д., Гвенин В.В., Гвенин Ц.Д. Магнитные функционализированные наночастицы для биомедицины, доставки лекарств и визуализации. Nanoscale Res Lett. 2019; 14: 188.
PubMed PubMed Central Статья CAS Google ученый
Рёмер И., Бриффа С.М., Дасильва Я.Р., Хапюк Д., Труйе В., Палмер Р.Э. и др.Влияние размера частиц, степени окисления и укупорочного агента различных наночастиц диоксида церия на фосфат-индуцированные превращения при различных pH и концентрациях. PLoS ONE. 2019; 14: 0217483.
Артикул CAS Google ученый
Парвин К., Банс В., Ледвани Л. Зеленый синтез наночастиц: их преимущества и недостатки. AIP Conf Proc. 2016; 1724: 020048.
Артикул CAS Google ученый
Niu Z, Li Y. Удаление и использование укупорочных агентов в нанокатализе. Chem Mater. 2014; 26: 72–83.
CAS Статья Google ученый
Гулати С., Сачдева М., Бхасин К.К. Укупорочные агенты в синтезе наночастиц: система поверхностно-активных веществ и растворителей. AIP Conf Proc. 2018; 1953: 030214.
Артикул CAS Google ученый
Радини И.А., Хасан Н., Малик М.А., Хан З.Биосинтез наночастиц железа с использованием экстракта семян Trigonella foenum-graecum для фотокаталитического разложения красителя метилового оранжевого и антибактериальных применений. J Photochem Photobiol B. 2018; 183: 154–63.
CAS PubMed Статья PubMed Central Google ученый
Шамели К., Ахмад М.Б., Заманян А., Сангпур П., Шабанзаде П., Абдоллахи Ю. и др. Зеленый биосинтез наночастиц серебра с использованием порошка клубней Curcuma longa.Int J Nanomed. 2012; 7: 5603–10.
CAS Статья Google ученый
Раджита Б., Малла Р.Р., Вадде Р., Каса П., Прасад ГЛВ, Фарран Б. и др. Горизонты применения нанотехнологий в лечении рака у женщин. Семинары по биологии рака. Академическая пресса; 2019.
Альберто Самора-Хусто Дж., Абрика-Гонсалес П., Рокаэль Васкес-Мартинес Дж., Муньос-Диосдадо А., Абрахам Бальдерас-Лопес Дж., Ибаньес-Эрнандес М. и др.Наночастицы золота, покрытые полиэтиленгликолем, как системы доставки ДНК и аторвастатина и оценка цитотоксичности. J Nanomateria. 2019; 2019: 5982047.
Google ученый
Пинзару И., Кориковак Д., Дехелеан С., Моакэ Е.А., Миок М., Бадерка Ф. и др. Стабильные наночастицы серебра, покрытые ПЭГ — подробный токсикологический профиль. Food Chem Toxicol. 2018; 111: 546–56.
CAS PubMed Статья PubMed Central Google ученый
Singletary M, Hagerty S, Muramoto S, Daniels Y, MacCrehan WA, Stan G и др. ПЭГилирование наночастиц цинка усиливает их способность усиливать обонятельные реакции на одорант. PLOS ONE. 2017; 12: 0189273.
Артикул CAS Google ученый
Теодореску М., Берсея М. Поли (винилпирролидон) — универсальный полимер для биомедицинских и других применений. Polym Plast Technol Eng. 2015; 54: 923–43.
CAS Статья Google ученый
Okoroh DO, Ozuomba JO, Aisida SO, Asogwa PU. Свойства наночастиц феррита цинка за счет посредничества ПВП и отжига при 500 ° C. Adv. Наночастицы. 2019; 8: 36–45.
CAS Статья Google ученый
Гударз Насери М., Сайон Э., Халил Заде Н. Удивительные эффекты и роль ПВП на кристалличность, фазовый состав и морфологию наночастиц феррита никеля, полученных методом термической обработки. Int Nano Lett.2013; 3: 1–8.
Артикул CAS Google ученый
Пандей Г., Сингх С., Хиткари Г. Синтез и характеристика наночастиц Fe3O4, покрытых поливинилпирролидоном (ПВП), методом химического соосаждения и удаления красителя Конго красного методом адсорбции. Int Nano Lett. 2018; 8: 111–21.
CAS Статья Google ученый
Альберг С., Антонопулос А., Дендорф Дж., Дринген Р., Эппле М., Флек Р. и др.Покрытые ПВП отрицательно заряженные наночастицы серебра: многоцентровое исследование их физико-химических характеристик, культивирование клеток и эксперименты in vivo. Beilstein J Nanotechnol. 2014; 5: 1944–65.
PubMed PubMed Central Статья CAS Google ученый
Джунаиди Дж., Трияна К., Сухариади Э., Сабарман Х., Ву Л. Роли поливинилового спирта (ПВС) в качестве укупорочного агента в полиольном методе синтеза серебряных нанопроволок.J Nano Res. 2017; 49: 174–80.
CAS Статья Google ученый
Айсида С.О., Ахмад И., Чжао Т.К., Мааза М., Эзема Ф.И. Влияние прокаливания на фотолюминесценцию, оптические, структурные и магнитные свойства наночастиц ZnFe2O4, допированных поливиниловым спиртом. Журнал Macromol Sci, Часть B. 2020; 59: 295–308.
CAS Статья Google ученый
Кириченко А, Пасько Д.А., Калугин О.Н.Поли (виниловый спирт) как водозащитный агент для наночастиц серебра: роль размера и структуры полимера. Phys Chem Chem Phys. 2017; 19: 8742–56.
CAS PubMed Статья PubMed Central Google ученый
Гааз Т.С., Сулонг А.Б., Ахтар М.Н., Кадхум А.А.Х., Мохамад А.Б., Аль-Амиери А.А. и др. Свойства и применение поливинилового спирта, нанотрубок галлуазита и их нанокомпозитов. Молекулы. 2015; 20: 22833–47.
CAS PubMed PubMed Central Статья Google ученый
Кунду Т.К., Карак Н., Барик П., Саха С. Оптические свойства наночастиц ZnO, полученных химическим методом с использованием поливинилового спирта (ПВС) в качестве покрывающего агента. МАКЭ. 2011; 1: 19–24.
Google ученый
Budi L, Rahayu H, Wulandari IO, Santjojo DH, Sabarudin A. Синтез и характеристика наночастиц Fe 3 O 4 с использованием поливинилового спирта (PVA) в качестве укупорочного агента и глутаральдегида (GA) в качестве сшивающего агента .IOP Conf Ser Mater Sci Eng. 2017; 299: 4–5.
Google ученый
Au L, Lim B, Colletti P, Jun YS, Xia Y. Синтез золотых микропланшетов с использованием бычьего сывороточного альбумина в качестве восстановителя и стабилизатора. Химия. 2010; 5: 123–9.
CAS Google ученый
Боланьос К., Коган М.Дж., Арайя Э. Покрытие наночастиц золота альбумином для улучшения их биомедицинских свойств.Int J Nanomed. 2019; 14: 6387–406.
Артикул Google ученый
ДжотиКумар А., Кайласнат М., Саймон Дж., Мэтью С. Стабилизированные BSA наночастицы золота: синтез и характеристика. Mater Today Proc. 2019; 9: 111–5.
CAS Статья Google ученый
Li H, Yang X. Квантовые точки CdS с блокировкой бычьего сывороточного альбумина в качестве датчика эффекта внутреннего фильтра для быстрого обнаружения и количественного определения протамина и гепарина.Анальные методы. 2015; 7: 8445–52.
CAS Статья Google ученый
Zhao S, Gao Y, Tan J, Zhu Y, Ying X, Zhang M и др. Простой синтез и антибактериальные применения иерархических нанокомпозитных частиц закиси меди / бычьего сывороточного альбумина. SN Appl Sci. 2019; 1 (8): 1–12.
Артикул CAS Google ученый
Resende JE, Gonçalves MA, Oliveira LCA, Da Cunha EFF, Ramalho TC.Использование этилендиаминтетрауксусной кислоты в качестве поглотителя хрома из кожаных отходов «мокрого синего»: термодинамические и кинетические параметры. J Chem. 2014; 2014: 754526.
Артикул CAS Google ученый
Harish GS, Reddy PS. Синтез и характеристика водорастворимых наночастиц ZnS: Ce, Cu, совместно легированных: влияние концентрации EDTA. Int Jo Sci Res. 2013; 4: 221–5.
Google ученый
Редди Д.А., Мурали Г., Виджаялакшми Р.П., Редди Б.К. Ферромагнетизм при комнатной температуре в наночастицах ZnS, легированных EDTA. Appl Phys A Mater Sci Process. 2011; 105: 119–24.
CAS Статья Google ученый
Rahal HT, Awad R, Abdel-Gaber AM, El-Said Bakeer D. Синтез, характеристика и магнитные свойства чистых наноразмерных частиц NiO с блокировкой EDTA. J Nanomater. 2017; 2017: 7460323.
Артикул CAS Google ученый
Yi Y, Zhang Y, Wang Y, Shen L, Jia M, Huang Y, et al. Этилендиаминтетрауксусная кислота в качестве блокирующих лигандов для частиц оксида железа с высокой степенью диспергирования в воде. Nanoscale Res Lett. 2014; 9: 27.
PubMed PubMed Central Статья CAS Google ученый
Эльгадир А., Уддин М., Фердош С., Адам С., Джалал А., Чоудхури А. Дж. К. и др. Влияние композитов хитозана и композитов наночастиц хитозана на различные системы доставки лекарств: обзор.J Food Drug Anal. 2014; 23: 619–29.
PubMed Статья CAS PubMed Central Google ученый
Mohan CO, Ravishankar CN, Lalitha KV, Srinivasa Gopal TK. Влияние съедобного покрытия хитозана на качество сардины из индийского масла с двойным филе (Sardinella longiceps) при хранении в охлажденном виде. Пищевые гидроколлоиды. 2012; 26: 167–74.
CAS Статья Google ученый
Пан И, Цинь А, Линь Икс, Ян Л, Ван Цюй, Ван Зи и др. Биоразлагаемый и биосовместимый высокоэластичный хитозановый каркас безопасен для клеток как in vitro, так и in vivo. Oncotarget. 2017; 8: 35583–91.
PubMed PubMed Central Статья Google ученый
Deng HH, Lin XL, Liu YH, Li KL, Zhuang QQ, Peng HP и др. Стабилизированные хитозаном наночастицы платины как эффективные имитаторы оксидазы для колориметрического определения кислой фосфатазы.Наноразмер. 2017; 9: 10292–300.
CAS PubMed Статья PubMed Central Google ученый
Франконетти А., Карнереро Дж. М., Прадо-Готор Р., Кабрера-Эскрибано Ф, Хайме К. Хитозан в качестве укупорочного агента: сведения о стабилизации наночастиц золота. Carbohyd Polym. 2019; 207: 806–14.
CAS Статья Google ученый
Cinteza LO, Scomoroscenco C, Voicu SN, Nistor CL, Nitu SG, Trica B, et al.Стабилизированные хитозаном Ag-наночастицы с превосходной биосовместимостью и их синергетическим антибактериальным действием в смесях с эфирными маслами. Наноматериалы. 2018; 8: 826.
PubMed Central Статья CAS Google ученый
Джаярамуду Т., Варапрасад К., Пьярасани Р.Д., Редди К.К., Кумар К.Д., Акбари-Фахрабади А. и др. Покрытые хитозаном наночастицы оксида меди / меди инкапсулировали устойчивые к микробам нанокомпозитные пленки.Int J Biol Macromol. 2019; 128: 499–508.
CAS PubMed Статья PubMed Central Google ученый
Mohan CO, Gunasekaran S, Ravishankar CN. Наночастицы золота, покрытые хитозаном, для индикации превышения температуры в замороженных хранимых продуктах. NPJ Sci Food. 2019; 3: 1–6.
Артикул Google ученый
Aisida SO, Ugwu K, Akpa PA, Nwanya AC, Ejikeme PM, Botha S, et al.Биогенный синтез и антибактериальная активность контролируемых наночастиц серебра с использованием экстракта Gongronema Latifolium. Mater Chem Phys. 2019; 237: 121859.
CAS Статья Google ученый
Айсида С.О., Мадубуону Н., Алнасир М.Х., Ахмад И., Бота С., Мааза М. и др. Биогенный синтез наностержней оксида железа с использованием экстракта листьев Moringa oleifera для антибактериальных применений. Appl Nanosci. 2020; 10: 305–15.
CAS Статья Google ученый
Aisida SO, Ugwu K, Akpa PA, Nwanya AC, Nwankwo U, Botha SS, et al. Биосинтез наночастиц серебра с использованием горького листа (Veronica amygdalina) для антибактериальной активности. Интерфейсы для серфинга. 2019; 17: 100359.
CAS Статья Google ученый
Дос Сантос Корреа А., Контрерас Л.А., Кейджок В.Дж., Барселуш Д.Х.Ф., Перейра А.Ч., Китагава Р.Р. и др. Золотые наночастицы, покрытые виролой масличной, проявляют активность по улавливанию радикалов и обладают низкой цитотоксичностью.Mater Sci Eng C Mater Biol Appl. 2018; 91: 853–8.
Артикул CAS Google ученый
Рашид С., Азим М., Хан С.А., Шах М.М., Ахмад Р. Характеристика и синергетический антибактериальный потенциал зеленых синтезированных наночастиц серебра с использованием водных экстрактов корней важных лекарственных растений Пакистана. Colloids Surf, B. 2019; 179: 317–25.
CAS Статья Google ученый
Ramanathan S, Gopinath SCB, Anbu P, Lakshmipriya T., Kasim FH, Lee C-G. Экологичный синтез наночастиц серебра, покрытых экстрактом Solanum trilobatum, совместим с хорошей антимикробной активностью. J Mol Struct. 2018; 1160: 80–91.
CAS Статья Google ученый
Мадубуону Н., Айсида С.О., Али А., Ахмад И., Чжао Т., Бота С. и др. Биосинтез наночастиц оксида железа с помощью композита Psidium guavaja-Moringa oleifera, их антибактериальное и фотокаталитическое исследование.Журнал J Photochem Photobiol, Б. 2019; 199: 111601.
CAS Статья Google ученый
Ezhilarasi AA, Vijaya JJ, Kennedy LJ, Kaviyarasu K. Green опосредованные наностержнями NiO с использованием экстракта Phoenix dactylifera (Dates) для биомедицинских и экологических применений. Mater Chem Phys. 2020; 241: 122419.
CAS Статья Google ученый
Рашид Т., Билал М., Икбал ХМН, Ли К.Зеленый биосинтез наночастиц серебра с использованием экстракта листьев Artemisia vulgaris и их потенциальные биомедицинские применения. Коллоиды Surf B Биоинтерфейсы. 2017; 158: 408–15.
CAS PubMed Статья PubMed Central Google ученый
Пандиян Н., Муругесан Б., Арумугам М., Сонамуту Дж., Самаянан С., Махалингам С. Ионная жидкость — более экологичный шаблонный агент с экстрактом растений Justicia adhatoda, способствующий зеленому синтезу морфологически улучшенной наноструктуры Ag-Au / ZnO. антибактериальное и противоопухолевое действие.Журнал J Photochem Photobiol, B. 2019; 198: 111559.
CAS Статья Google ученый
Сентилкумар Н., Нандхакумар Э., Прия П., Сони Д., Вималан М., Потехер IV. Синтез наночастиц ZnO с использованием экстракта листьев Tectona grandis (L.) и их антибактериальной, антиартритной, антиоксидантной и цитотоксической активности in vitro. New J Chem. 2017; 41: 10347–56.
CAS Статья Google ученый
Наз С., Ислам М., Табассум С., Фернандес Н. Ф., Каркаче де Бланко Э. Дж., Зия М. Грин синтез наночастиц гематита (α-Fe2O3) с использованием экстракта Rhus punjabensis и их биомедицинская перспектива при патогенных заболеваниях и раке. J Mol Struct. 2019; 1185: 1–7.
CAS Статья Google ученый
Satpathy S, Patra A, Ahirwar B, Hussain MD. Оптимизация процесса зеленого синтеза наночастиц золота с помощью экстракта Hygrophila spinosa T.Андерс и их биологические приложения. Phys E Low Dimension Syst Nanostruct. 2020; 121: 113830.
CAS Статья Google ученый
Ядав Р., Саини Х., Кумар Д., Паси С., Агравал В. Биоинженерия Piper longum L., опосредованные экстрактом наночастиц серебра, и их потенциальные биомедицинские применения. Mater Sci Eng C. 2019; 104: 109984.
CAS Статья Google ученый
Hola K, Markova Z, Zoppellaro G, Tucek J, Zboril R. Специальная функционализация наночастиц оксида железа для МРТ, доставки лекарств, магнитной сепарации и иммобилизации биологических веществ. Biotechnol Adv. 2015; 33: 1162–76.
CAS PubMed Статья PubMed Central Google ученый
Cao S-W, Zhu Y-J, Ma M-Y, Li L, Zhang L. Иерархически наноструктурированные магнитные полые сферы Fe3O4 и γ-Fe2O3: приготовление и возможное применение в доставке лекарств.J. Phys Chem C. 2008; 112: 1851–6.
CAS Статья Google ученый
Ян Х, Чен Л., Хан Б., Ян Х, Дуан Х. Приготовление полых полимерных микросфер двойного нацеливания на магнетит и опухоль с pH-чувствительностью для носителей противораковых лекарств. Полимер. 2010; 51: 2533–9.
CAS Статья Google ученый
Мирза А.У., Карим А., Нами САА, Хан М.С., Рехман С., Бхат С.А. и др.Биогенный синтез наночастиц оксида железа с использованием фитовидов Agrewia optiva и Prunus persica : характеристика, антибактериальная и антиоксидантная активность. J Photochem Photobiol, B. 2018; 185: 262–74.
CAS Статья Google ученый
Шалаби Т.И., Эль-Рефаи WM. Покрытые биоадгезивным хитозаном катионные нанолипосомы с улучшенной инкапсуляцией инсулина и пролонгированным пероральным гипогликемическим эффектом у мышей с диабетом.J Pharm Sci. 2018; 107: 2136–43.
CAS PubMed Статья PubMed Central Google ученый
Ravichandran V, Vasanthi S, Shalini S, Shah SAA, Tripathy M, Paliwal N. Green Синтез, характеристика, антибактериальная, антиоксидантная и фотокаталитическая активность экстракта листьев Parkia speciosa, опосредованная наночастицами серебра. Результаты Phys. 2019; 15: 102565.
Артикул Google ученый
Чандран С., Равичандран В., Чандран С., Чемманда Дж., Чандаршекар Б. Биосинтез наночастиц серебра, инкапсулированных ПВС. J Appl Res Technol. 2016; 14: 319–24.
Артикул Google ученый
Девананд Венкатасуббу G, Рамасами С., Рамакришнан В., Кумар Дж. Фолат нацелился на ПЭГилированные наночастицы диоксида титана в качестве наноносителя для направленной доставки лекарственного средства паклитаксела. Adv Powder Technol. 2013; 24: 947–54.
CAS Статья Google ученый
Джавед Р., Раис Ф, Фатима Х, ул Хак I, Калим М., Наз СС и др. Нанокомпозиты ZnO, инкапсулированные хитозаном: изготовление, характеристика и функционализация биодентальных подходов. Mater Sci Eng C. 2020; 116: 111184.
CAS Статья Google ученый
Прабха Г., Радж В. Приготовление и определение характеристик магнитных наночастиц с покрытием из полимерных нанокомпозитов для приложений доставки лекарств. J Magn Magn Mater. 2016; 408: 26–34.
CAS Статья Google ученый
Бхарати Д., Ранджиткумар Р., Васантхарадж С., Чандаршекар Б., Бхуванешвари В. Синтез и характеристика нанокомпозита хитозан / оксид железа для биомедицинских применений. Int J Biol Macromol. 2019; 132: 880–7.
CAS PubMed Статья PubMed Central Google ученый
Попов А.Л., Хан Б., Ермаков А.М., Савинцева И.В., Ермакова О.Н., Попова Н.Р. и др.PVP-стабилизированные наночастицы оксида вольфрама: чувствительная к pH противораковая платформа с высокой цитотоксичностью. Mater Sci Eng, C. 2020; 108: 110494.
CAS Статья Google ученый
Сельвам Р., Рамасами С., Мохиюддин С., Енох IVMV, Гопинатх П., Филимонов Д. Кожух из поливинилового спирта с добавлением молекулярного инкапсулятора на наночастицах феррита. Увеличенная лекарственная нагрузка на рак и противораковые свойства. Mater Sci Eng C. 2018; 93: 125–33.
CAS Статья Google ученый
Лабамбо А.Ф., Оно Л., Драго В., Маттосо Н., Варальда Дж., Сераковски М.-Р. и др. Регулировка дисперсии наночастиц Fe3O4 с помощью pH в мембранах ПВС / гуаровая камедь / электропрядение. Carbohydr Polym. 2015; 134: 775–83.
CAS PubMed Статья PubMed Central Google ученый
Ашфак М., Хан С., Верма Н. Синтез in situ биоматериала на основе PVA-CAP, диспергированного с наночастицами Cu и углеродными микронановолокнами, для приложений доставки антибиотиков.Биохим Энг Дж. 2014; 90: 79–89.
CAS Статья Google ученый
Ngernpimai S, Thomas C, Maensiri S, Siri S. Стабильность и цитотоксичность хорошо диспергированных наночастиц магнетита, полученных гидротермальным методом. Adv Mater Res. 2012; 506: 122–5.
CAS Статья Google ученый
Pinto RJB, Marques PAAP, Neto CP, Trindade T, Daina S, Sadocco P.Антибактериальная активность нанокомпозитов из серебра и бактериальных или растительных целлюлозных волокон. Acta Biomater. 2009; 5: 2279–89.
CAS PubMed Статья PubMed Central Google ученый
Трандафилович Л.В., Божанич Д.К., Димитриевич-Бранкович С., Лют А.С., Джокович В. Изготовление и антибактериальные свойства нанокомпозитов ZnO – альгинат. Carbohyd Polym. 2012; 88: 263–9.
Артикул CAS Google ученый
Erazo A, Mosquera SA, Rodríguez-Paéz JE. Синтез наночастиц ZnO различной морфологии: изучение их противогрибкового действия на штаммах Aspergillus niger и Botrytis cinerea . Mater Chem Phys. 2019; 234: 172–84.
CAS Статья Google ученый
Ferreira FV, Mariano M, Lepesqueur LSS, Pinheiro IF, Santos LG, Burga-Sánchez J, et al. Наночастицы серебра, покрытые додекантиолом, используются в качестве наполнителей нецитотоксической и противогрибковой поверхности PBAT на основе нанокомпозитов.Mater Sci Eng, C. 2019; 98: 800–7.
CAS Статья Google ученый
Наз С., Ахтар Дж., Чаудхари М.Ф., Зия М. Низкотемпературный синтез иерархических структур оксида меди и их превосходная биологическая активность. IET Nanobiotechnol. 2018; 12 (7): 968–72.
PubMed Статья PubMed Central Google ученый
Хаджипур М.Дж., Фромм К.М., Акбар Ашкарран А., Хименес де Аберастури Д., де Ларраменди И.Р., Рохо Т. и др.Антибактериальные свойства наночастиц. Trends Biotechnol. 2012; 30: 499–511.
CAS PubMed Статья PubMed Central Google ученый
Fresta M, Puglisi G, Giammona G, Cavallaro G, Micali N, Furneri PM. Наночастицы полиэтилцианоакрилата, нагруженные пефлоксацином, мезилатом и офлоксацином: характеристика коллоидного лекарственного носителя. J Pharm Sci. 1995; 84: 895–902.
CAS PubMed Статья PubMed Central Google ученый
Али Дж.С., Маннан А., Насруллах М., Иштиак Х., Наз С., Зия М. Антимикробные, антиоксидантные и цитотоксические свойства Monotheca buxifolia способствовали синтезированным наночастицам металлов и оксидов металлов. Inorganic Nano-Metal Chem. 2020; 50: 770–82.
CAS Статья Google ученый
Сонди И., Салопек-Сонди Б. Наночастицы серебра как противомикробный агент: тематическое исследование E. coli в качестве модели для грамотрицательных бактерий.J Colloid Interface Sci. 2004. 275: 177–82.
CAS PubMed Статья PubMed Central Google ученый
Nithya A, JeevaKumari HL, Rokesh K, Ruckmani K, Jeganathan K, Jothivenkatachalam K. Разностороннее действие нанокомпозита хитозан-серебро на поверхностную плазмонную фотокаталитическую и антибактериальную активность. J Photochem Photobiol, B. 2015; 153: 412–22.
CAS Статья Google ученый
Ramalingam B, Khan MdMR, Mondal B, Mandal AB, Das SK. Простой синтез наночастиц серебра, украшенных магнитно-хитозановыми микросферами, для эффективного удаления красителей и микробных загрязнений. ACS Sustain Chem Eng. 2015; 3: 2291–302.
CAS Статья Google ученый
Бряскова Р., Георгиева Н., Пенчева Д., Тодорова З., Лазарова Н., Кантарджиев Т. Синтез и характеристика гибридных материалов с внедренными наночастицами серебра и их применение в качестве антимикробных матриц для очистки сточных вод.Colloids Surf, A. 2014; 444: 114–9.
CAS Статья Google ученый
Gélvez APC, Farias LHS, Pereira VS, da Silva ICM, Costa AC, Dias CGBT, et al. Биосинтез, характеристика и лейшманицидная активность биокомпозита, содержащего AgNPs-PVP-glucantime. Наномедицина. 2018; 13: 373–90.
PubMed Статья CAS PubMed Central Google ученый
Kvítek L, Panáček A, Soukupová J, Kolář M, Večeřová R, Prucek R, et al. Влияние поверхностно-активных веществ и полимеров на стабильность и антибактериальную активность наночастиц (НЧ) серебра. J. Phys Chem C. 2008; 112: 5825–34.
Артикул CAS Google ученый
Jia Z, Sun H, Gu Q. Получение наночастиц Ag с триэтаноламином в качестве восстановителя и их антибактериальные свойства. Colloids Surf A. 2013; 419: 174–9.
CAS Статья Google ученый
Джавед Р., Ахмед М., Хак И.Ю., Ниса С., Зия М. Наночастицы CuO, допированные ПВП и ПЭГ, более биологически активны: с точки зрения антибактериальных, антиоксидантных, противодиабетических и цитотоксических свойств. Mater Sci Eng C Mater Biol Appl. 2017; 79: 108–15.
CAS PubMed Статья PubMed Central Google ученый
Аджита Б., Редди ЯК, Редди ПС, Чон Х. Дж, Ан CW. Роль укупорочных агентов в контроле размера наночастиц серебра, антибактериальной активности и потенциального применения в качестве оптического датчика перекиси водорода.RSC Adv. 2016; 6: 36171–9.
CAS Статья Google ученый
Мартинес-Кастаньон Г.А., Ниньо-Мартинес Н., Мартинес-Гутьеррес Ф., Мартинес-Мендоса Дж. Р., Руис Ф. Синтез и антибактериальная активность наночастиц серебра различного размера. J Nanopart Res. 2008; 10: 1343–8.
Артикул CAS Google ученый
Dhillon GS, Kaur S, Brar SK. Простое изготовление и характеристика наночастиц оксида цинка на основе хитозана, а также оценка их антимикробной и антибиотической активности.Int Nano Lett. 2014; 4: 107.
Артикул CAS Google ученый
Стефан М., Мелниг В., Прикоп Д., Неагу А., Михасан М., Тартау Л. и др. Ослабленное влияние наночастиц золота, покрытых хитозаном, на LPS-индуцированную токсичность у лабораторных крыс. Mater Sci Eng C Mater Biol Appl. 2013; 33: 550–6.
CAS PubMed Статья PubMed Central Google ученый
Ким Дж. С., Кук Э, Ю К. Н., Ким Дж. Х., Пак С. Дж., Ли Х. Дж. И др. Антимикробные эффекты наночастиц серебра. Nanomed Nanotechnol Biol Med. 2007; 3: 95–101.
CAS Статья Google ученый
Morones JR, Elechiguerra JL, Camacho A, Holt K, Kouri JB, Ramírez JT, et al. Бактерицидное действие наночастиц серебра. Нанотехнологии. 2005; 16: 2346–53.
CAS PubMed Статья PubMed Central Google ученый
Milanezi FG, Meireles LM, de Christo Scherer MM, de Oliveira JP, da Silva AR, de Araujo ML, Scherer R. Антиоксидантная, антимикробная и цитотоксическая активность наночастиц золота, покрытых кверцетином. Сауди Фарм Дж. 2019; 27: 968–74.
CAS PubMed PubMed Central Статья Google ученый
Zhai X, Zhang C, Zhao G, Stoll S, Ren F, Ленг X. Антиоксидантная способность наночастиц селена, стабилизированных хитозаном.J Nanobiotechnol. 2017; 15: 4.
Артикул CAS Google ученый
Матос А.И., Каррейра Б., Перес С., Моура ЛИФ, Конниот Дж., Фурниолс Т. и др. Нанотехнологии — важная стратегия комбинированной инновационной химио-иммунотерапии против колоректального рака. J Control Release. 2019; 307: 108–38.
CAS PubMed Статья PubMed Central Google ученый
Мухаммад З., Раза А., Гафур С., Наим А., Наз СС, Риаз С. и др. ПЭГ-блокированные наночастицы серебра метотрексата для эффективной противоопухолевой активности и биосовместимости. Eur J Pharm Sci. 2016; 91: 251–5.
CAS PubMed Статья PubMed Central Google ученый
Альфаро А., Леон А., Гуахардо-Корреа Е., Рекен П., Торрес Ф, Мери М. и др. Наночастицы MgO, покрытые полиэтиленгликолем в качестве носителя для противоопухолевого препарата 2-метоксиэстрадиол.PLOS ONE. 2019; 14: 0214900.
Артикул CAS Google ученый
Schleich N, Sibret P, Danhier P, Ucakar B, Laurent S, Muller RN, et al. Двойное противоопухолевое лекарство / суперпарамагнитные наночастицы на основе PLGA, нагруженные оксидом железа, для терапии рака и магнитно-резонансной томографии. Int J Pharm. 2013; 447: 94–101.
CAS PubMed Статья PubMed Central Google ученый
Agrawal AK, Urimi D, Harde H, Kushwah V, Jain S. Наночастицы хитозана с добавлением фолата повышают стабильность, биодоступность и эффективность инсулина у диабетических крыс после перорального введения. RSC Adv. 2015; 5: 105179–93.
CAS Статья Google ученый
Wu Z-H, Ping Q-N, Song Y-M, Lei X-M, Li J-Y, Cai P. Исследования липосом инсулина с двойным покрытием хитозаном и конъюгатами хитозан-ЭДТА. Acta Pharmaceutica Sinica.2004; 39: 933–8.
CAS PubMed PubMed Central Google ученый
Masciangioli T, Zhang W-X. Рецензирование: экологические технологии в наномасштабе. Environ Sci Technol. 2003; 37: 102A – 8A.
CAS PubMed Статья PubMed Central Google ученый
Boubel RW, Fox DL, Turner DB, Stern AC. История загрязнения воздуха.Fundam Air Pollut 1994: 3–18.
Сарадха Б., Матхур П.П. Влияние загрязнителей окружающей среды на мужскую репродуктивную функцию. Environ Toxicol Pharmacol. 2006; 21: 34–41.
CAS PubMed Статья PubMed Central Google ученый
Раджан CSR. Нанотехнологии в восстановлении подземных вод. IJESD. 2011: 182–7.
Lövestam G, Rauscher H, Roebben G, Klüttgen BS, Gibson N, Putaud JP, Stamm H.Соображения по поводу определения наноматериала для нормативных целей. Справочные отчеты Объединенного исследовательского центра (JRC). 2010; 80: 00–41.
Нурми Дж. Т., Тратнек П. Г., Сарати В., Баер Д. Р., Амонетт Дж. Э., Печер К. и др. Характеристика и свойства наночастиц металлического железа: спектроскопия, электрохимия и кинетика. Environ Sci Technol. 2005; 39: 1221–30.
CAS PubMed Статья PubMed Central Google ученый
Bhatt I, Tripathi BN. Взаимодействие созданных наночастиц с различными компонентами окружающей среды и возможные стратегии оценки их риска. Chemosphere. 2011; 82: 308–17.
CAS PubMed Статья PubMed Central Google ученый
Клейн SJ, Альварес PJJ, Batley GE, Fernandes TF, Handy RD, Lyon DY, et al. Наноматериалы в окружающей среде: поведение, судьба, биодоступность и эффекты. Environ Toxicol Chem.2008; 27: 1825–51.
CAS PubMed Статья PubMed Central Google ученый
Мояно Д.Ф., Ротелло В.М. Нано встречается с биологией: структура и функции на границе раздела наночастиц. Ленгмюра. 2011; 27: 10376–85.
CAS PubMed PubMed Central Статья Google ученый
Лю Дж., Легрос С., Ма Дж., Вейнот Дж. Г. К., фон дер Каммер Ф., Хофманн Т.Влияние функционализации поверхности и размера частиц на кинетику агрегации созданных наночастиц. Chemosphere. 2012; 87: 918–24.
CAS PubMed Статья PubMed Central Google ученый
Лу А-Х, Салабас Э.Л., Шют Ф. Магнитные наночастицы: синтез, защита, функционализация и применение. Angew Chem. 2007; 46: 1222–44.
CAS Статья Google ученый
Potara M, Focsan M, Craciun A.M, Botiz I., Astilean S. 15-Покрытые полимером плазмонные наночастицы для восстановления окружающей среды: синтез, функционализация и свойства. В: Хуссейн С.М., Мишра А.К., редакторы. Новые полимерные нанокомпозиты для восстановления окружающей среды; 2018, стр. 361–87.
Аашима, Мехта, СК. Глава 18 — Влияние функционализированных наноматериалов на восстановление окружающей среды: проблемы и будущие потребности. В: Мустансар Хуссейн С., редактор. Справочник функционализированных наноматериалов для промышленного применения; 2020, стр.505–24.
Khademalrasool M, Farbod M, Iraji zad A. Приготовление нанокомпозитов наночастиц ZnO / нанопроволок Ag в качестве плазмонных фотокатализаторов и исследование влияния концентрации и диаметра нанопроволок Ag на их фотокаталитические характеристики. J Сплавы Соединения. 2016; 664: 707–14.
CAS Статья Google ученый
Сайфуддин Н.М., Ниан К.Й., Чжан Л., Нин К. Композит с наночастицами хитозана и серебра в качестве системы фильтрации питьевой воды в месте использования для удаления пестицидов из воды.Азиатский J Biochem. 2011; 6: 142–59.
CAS Статья Google ученый
Йошизука К., Лу З., Иноуэ К. Комплексные с серебром микрочастицы хитозана для удаления пестицидов. React Funct Polym. 2000; 44: 47–54.
CAS Статья Google ученый
Двиведи К., Гупта А., Чаудхари А., Нанди СК. Гранулы композитного гидрогеля с наночастицами золота и хитозана демонстрируют эффективное удаление метилпаратиона из сточных вод.RSC Adv. 2014; 4: 39830–8.
CAS Статья Google ученый
Камарудин К.С., Мохамад М.Ф., Фатилах Н.Н., Мохамед М.С. Влияние концентрации ПВП на формирование размера и формы наночастиц золота (Au) для адсорбции ртути. J Appl Sci. 2010; 10: 3374–8.
CAS Статья Google ученый
Xu X, Wang Q, Choi HC, Kim YH. Инкапсуляция наночастиц железа с нановолоконными мембранами из ПВП для поддержания их каталитической активности.J Membr Sci. 2010; 348: 231–7.
CAS Статья Google ученый
Sugunan A, Thanachayanont C, Dutta J, Hilborn JG. Датчики ионов тяжелых металлов с использованием наночастиц золота, покрытых хитозаном. Sci Technol Adv Mater. 2005; 6: 335–40.
CAS Статья Google ученый
Морси Р.Э., Аль-Сабаг А.М., Мустафа Ю.М., ЭльХолы С.Г., Сайед М.С. Модифицированные политиофеном нанокомпозиты хитозан / магнетит для тяжелых металлов и селективного удаления ртути.Egypt J Petrol. 2018; 27: 1077–85.
Артикул Google ученый
Shambharkar BH, Chowdhury AP. Опосредованный этиленгликолем синтез наночастиц Ag8SnS6 и их использование в деградации эозинового желтого и бриллиантового зеленого. RSC Adv. 2016; 6: 10513–9.
CAS Статья Google ученый
Аруларасу М.В. Влияние органических укупорочных средств на оптическую и фотокаталитическую активность мезопористых наночастиц TiO2 золь-гель методом.SN Appl Sci. 2019; 1: 393.
Артикул CAS Google ученый
Молекулы | Бесплатный полнотекстовый | Оптимизация белковой терапии с помощью конъюгирования полимеров в качестве эффективного DDS
a) PVP-TNF-alpha Для создания конъюгированных белков с большей эффективностью и безопасностью, то есть для селективного повышения желаемой терапевтической активности биоактивных белков без увеличения их побочных эффектов, важно тщательно регулировать их поведенческие характеристики in vivo с учетом механизма их действия.Таким образом, требуется разработка полимерных модификаторов с полезными функциями DDS (система доставки лекарств), которые могут регулировать их поведенческие характеристики in vivo, такие как способность нацеливания и контролируемое высвобождение. Поэтому мы рассмотрели другие кандидаты в качестве полимерных модификаторов для введения этих новых функций. Как упоминалось выше, было обнаружено, что поливинилпирролидон (ПВП), в который полезные функциональные группы могут быть введены путем радикальной сополимеризации, удерживается в крови лучше, чем ПЭГ.. Кроме того, ПВП также обладает высокой биосовместимостью и широко используется в качестве расширителя плазмы. Имея это в виду и чтобы оценить полезность PVP в качестве полимерного модификатора для конъюгации белков, мы оценили терапевтическую эффективность PVP-TNF-α по сравнению с таковой конъюгата PEG (PEG-TNF-α) [21,22]. Конечный карбоксилсодержащий ПВП был получен радикальной полимеризацией ВП. Среднечисловую молекулярную массу (Mn) синтезированного ПВП контролировали путем варьирования количества агента переноса, добавляемого в реакцию.Ранее мы показали, что ПЭГ-ФНО-альфа и ПЭГ-ИЛ-6, конъюгированные с ПЭГ (5000 Mn), обладают выраженной противоопухолевой активностью или тромбопоэтической активностью, соответственно. Было обнаружено, что эти конъюгаты обладают более высокими терапевтическими эффектами in vivo, чем конъюгаты, полученные с PEG (2000 Mn) или PEG (12000 Mn). Поэтому в этом исследовании 6000 Mn PVP, очищенный гель-фильтрацией, использовали в качестве полимерного модификатора для первого выбора.
Природный человеческий TNF-альфа конъюгировали с активированным PVP (Mn; 6000, Mw / Mn = 1.14) через амидные связи между аминогруппами лизина TNF-альфа и N-гидроксискукцинимидными группами PVP на конце основной цепи. Полученный PVP-TNF-альфа очищали от нативного TNF-альфа и разделяли на пять фракций с различными молекулярными размерами с помощью GF-HPLC (стандарт белка). Активность PVP-TNF-альфа снижалась с увеличением молекулярной массы и степени модификации PVP (присоединение PVP к TNF-альфа). Этот результат также наблюдался, когда TNF-альфа был конъюгирован с PEG, и этот профиль изменений биоактивности PVP-TNF-alphas был подобен тому, который наблюдался при модификации TNF-alpha с помощью PEG (Mn; 5000, Mw / Mn = 1.32).
Противоопухолевые эффекты PVP-TNF-альфа на солидные опухоли S-180 сравнивали с эффектами нативных TNF-альфа и MPEG-TNF-альфа при однократном внутривенном введении. инъекция. Противоопухолевые эффекты оценивали по шкале геморрагического некроза через 24 часа после введения образца. Противоопухолевый эффект PVP-TNF-альфа фракции 3 (Mn; 101000), в которой 40% общих лизиновых аминогрупп TNF-альфа были связаны с PVP, был заметно выше, чем у нативного TNF-альфа в дозе 10000 JRU / мышь и индуцировал полную регрессию у двух из семи мышей (данные не показаны).
Рисунок 5. Противоопухолевый эффект PVP-TNF-α при плановом введении в дни выживания после инокуляции опухоли Meth-A. Мышам BALB / c, несущим Meth-A, давали образцы на 7, 10, 14 и 17 дни после инокуляции опухоли. Полная регрессия была определена, когда опухоль не росла повторно в течение> 100 дней. Статистическая значимость по сравнению с контролем с физиологическим раствором: * P <0,01.
Рисунок 5. Противоопухолевый эффект PVP-TNF-α при плановом введении в дни выживания после инокуляции опухоли Meth-A.Мышам BALB / c, несущим Meth-A, давали образцы на 7, 10, 14 и 17 дни после инокуляции опухоли. Полная регрессия была определена, когда опухоль не росла повторно в течение> 100 дней. Статистическая значимость по сравнению с контролем с физиологическим раствором: * P <0,01.
Чтобы исследовать полезность PVP в качестве полимерного модификатора и PVP-TNF-альфа фракции 3 в качестве системного противоопухолевого агента, мы сравнили противоопухолевую активность PVP-TNF-alpha фракции 3 с таковой нативных TNF-альфа и MPEG-TNF-альфа. с расписанием i.v. инъекции солидных опухолей Meth-A. Как показано на рисунке 5, PVP-TNF-альфа фракция 3 и MPEG-TNF-альфа в дозе 200 JRU показали максимальные противоопухолевые эффекты без каких-либо токсических побочных эффектов (таких как внезапная смерть и другие) и имели превосходящие противоопухолевые эффекты. нативного TNF-альфа в дозе 10 000 JRU. С другой стороны, требовалось только 50 JRU фракции 3 PVP-TNF-альфа, чтобы продемонстрировать заметную противоопухолевую активность, и рост опухоли был полностью подавлен в течение периода наблюдения, как в случае с 10 000 JRU нативного TNF-альфа и 100 JRU MPEG-TNF. -альфа.Эти результаты показали, что фракция 3 PVP-TNF-альфа была приблизительно в 200 и 2 раза более мощным противоопухолевым агентом, чем нативный TNF-альфа и MPEG-TNF-альфа, соответственно. Период полувыведения из плазмы PVP-TNF-альфа фракции 3 (360 мин) был примерно в 80 и 3 раза больше, чем у нативного TNF-альфа (4,6 мин) и MPEG-TNF-альфа (122 мин), соответственно. Как описано выше, противоопухолевые эффекты TNF-альфа обусловлены не только прямой цитотоксичностью против опухолевых клеток, но также специфическим повреждением сосудов опухоли и эффективной активацией противоопухолевых иммунных клеток.TNF-альфа избирательно увеличивает проницаемость сосудов опухоли. Увеличение полупериода TNF-альфа может привести к уменьшению его распределения в печени и селезенке, которые являются основными участками побочных эффектов, и выборочно повысит его противоопухолевые эффекты. Следовательно, мы уверены, что повышенная противоопухолевая эффективность PVP-TNF-альфа Fr.3 по сравнению с нативным TNF-альфа и MPEG-TNF-альфа может быть отнесена к увеличению периода полужизни. Эти результаты предполагают, что PVP является полезным полимерным модификатором для конъюгации TNF-альфа с целью повышения его противоопухолевой активности, а многофункционально конъюгированный TNF-альфа может быть активированным противоопухолевым агентом для клинического использования.Влияние молекулярной массы поливинилпирролидона на потенциал раздражения кожи и свойства косметических средств для мытья тела в коацерватной форме
Ссылки
[1] M. J. Rosen. Поверхностно-активные вещества и межфазные явления , 3-е изд. John Wiley & Sons, Inc., Нью-Йорк (2006). Искать в Google Scholar
[2] Т. Ф. Тадрос. Прикладные ПАВ. Принципы и применение . Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim (2005). Поиск в Google Scholar
[3] A.Барел, М. Пай, Х. Майбах. Справочник по косметической науке и технологиям , 4-е изд. Taylor & Francis Group, Бока-Ратон (2014 г.). Поиск в Google Scholar
[4] М. Абэ, Дж. Ф. Скамхорн. Системы смешанных поверхностно-активных веществ , 2-е изд. Марсель Деккер, Нью-Йорк (2005). Искать в Google Scholar
[5] Р. Дж. Фарн. Химия и технология ПАВ . Blackwell Publishing, New Jersey (2006). Искать в Google Scholar
[6] L. Rhein, M. Schlossman, A.О’Леник, П. Сомасундаран. Поверхностно-активные вещества в средствах личной гигиены и декоративной косметике , 3-е изд. CRC Press Taylor & Francis Group, Boca Raton (2006). Искать в Google Scholar
[7] Т. Буяк, Т. Василевски, З. Низиол-Лукашевска. Colloids Surf. B 135 , 497 (2015). Искать в Google Scholar
[8] Т. Василевски. J. Surf. Deterg. 13 , 513 (2010). Искать в Google Scholar
[9] Т. Василевски, Т. Буяк. Ind. Eng. Chem. Res. 53 , 13356 (2014). Искать в Google Scholar
[10] А. Северин, Т. Василевски, Т. Буяк. Ind. Eng. Chem. Res. 55 , 1134 (2016). Искать в Google Scholar
[11] Т. Василевски, Дж. Аркт, К. Пытковска, А. Бочо-Янишевска, М. Краевский, Т. Буяк. Przem. Chem. 94 , 111 (2015). Искать в Google Scholar
[12] А. Сейн, Дж. Энгбертс. Ленгмюра 11 , 455 (1995).Искать в Google Scholar
[13] А. Сейн, Дж. Энгбертс, Э. ван дер Линден, Дж. К. ван де Пас. Langmuir 9 , 1714 (1993). Искать в Google Scholar
[14] D. Lasic. Biochem. J. 256 , 1 (1988). Искать в Google Scholar
[15] Ф. Менгер, Б. Сайкс. Langmuir 14 , 4131 (1988). Искать в Google Scholar
[16] H. B. Bohidar. J. Surf. Sci. Technol. 24 , 105 (2008). Искать в Google Scholar
[17] R.Ван, Ю. Ван. Мягкое вещество. 10 , 1705 (2014). Искать в Google Scholar
[18] S. Benite. Микроинкапсуляция. Методы и промышленное применение . Taylor & Francis Group, Boca Raton (2006). Искать в Google Scholar
[19] Т. Калантар, К. Такер, А. Залуски, Т. Бумгаард, Б. Уилсон, М. Ладика, М. Джордан, С. Ли, XJ Чжан. J. Cosmet. Sci. 58 , 375 (2007). Искать в Google Scholar
[20] T. Agner, J.Серуп. J. Invest. Дерматол. 95 , 543 (1990). Искать в Google Scholar
[21] С. К. Дасилва, Р. П. Саху, Р. Л. Конгер, С. М. Перкинс, М. Х. Каплан, Дж. Б. Трэверс. Arch. Дерматол. Res. 304 , 65 (2012). Искать в Google Scholar
[22] Г. Д. Нильсен, Дж. Б. Нильсен, К. Э. Андерсен, П. Гранджин. Внутр. J. Occup. Environ. Здоровье 6 , 138 (2000). Искать в Google Scholar
[23] Р. М. Уолтерс, М. Дж. Февола, Дж.Дж. Либрицци, К. Мартин. Космет. Туалет . 123 , 53 (2008). Искать в Google Scholar
[24] A. Faucher, E. D. Goddard. J. Soc. Космет. Chem. 29 , 323 (1978). Искать в Google Scholar
[25] Т. Дж. Холл-Мэннинг, Г. Х. Холланд, Г. Ренни, П. Ревелл, Дж. Хайнс, М. Д. Баррат, Д. А. Баскеттер. Еда. Chem. Toxicol. 36 , 233 (1998). Искать в Google Scholar
[26] Т. Ивасаки, М. Огава, К. Эсуми, К. Мэгуро. Langmuir 7 , 30 (1990). Искать в Google Scholar
[27] П. Н. Мур, С. Пувада, Д. Бланкштейн. J. Cosmet. Sci. 54 , 29 (2003). Искать в Google Scholar
[28] Д. Т. Даунинг, В. Абрахам, Б. К. Вегнер, К. В. Уиллман, Дж. Л. Маршалл. Arch. Дерматол. Res. 285 , 151 (1993). Искать в Google Scholar
[29] Х. Лоффер, Р. Хэппл. Контактный дерматит 48 , 26 (2003). Искать в Google Scholar
[30] V.Шармонье, Б. М. Моррисон, М. Пай, Г. И. Майбах. Еда. Chem. Toxicol. 39 , 279 (2001). Искать в Google Scholar
[31] Т. Полефка. «Взаимодействие поверхностно-активных веществ с кожей», в Справочнике по детергентам . Часть A: Свойства. Surfactant Science Series , G. Broze (Eds.), Стр. 82. Публикации Марселя Деккера, Нью-Йорк (1999). Поиск в Google Scholar
[32] Дж. Г. Домингес, Ф. Балагер, Дж. Л. Парра, К. М. Пелехеро. Внутр. J. Cosmet. Sci. 3 , 57 (1981).Искать в Google Scholar
[33] А. Теглиа, Г. Секки. Космет. Туалет. 111 , 61 (1996). Искать в Google Scholar
[34] М. Пай, К. Блок, Н. Хамайда, Г. Э. Хюттман, С. Кирквуд, К. Лалли, PH Ллойд, П. Макела, Х. Разенберг, Р. Янг. Tenside Surfact. Deterg. 4 , 290 (2006). Искать в Google Scholar
[35] Дж. П. Макфадден, Д. Б. Холлоуэй, Э. Г. Уиттл, Д. А. Баскеттер. Контактный дерматит. 43 , 264 (2000).Искать в Google Scholar
[36] А. Теглиа, Г. Маццола, Г. Секки. Космет. Туалет. 108 , 56 (1993). Искать в Google Scholar
[37] I. Effendy, H. Maibach. Clin. Дерматол. 14 , 15 (1996). Искать в Google Scholar
[38] Т. Буяк, З. Низиол-Лукашевска, К. Гавел-Бембен, А. Северин, М. Кучарек, К. Ткачик, М. Матысяк . Green Chem. Lett. 8 , 78 (2015). Искать в Google Scholar
[39] K.Гавел-Бембен, Т. Буяк, З. Низиол-Лукашевская, Б. Антосевич, А. Якубчик, М. Карась, К. Рыбчинская. Molecules 20 , 5468 (2015). Искать в Google Scholar
[40] Т. Василевски, А. Северин, Т. Буяк. Green Chem. Lett. 9 , 114 (2016). Искать в Google Scholar
[41] З. Низиол-Лукашевска, П. Осика, Т. Василевский, Т. Буяк. Molecules 22 , 320 (2017). Искать в Google Scholar
[42] Z. Nizioł-ukaszewska, T.Василевский, Т. Буяк, П. Осика. Pol. J. Chem. Technol. 19 , 122 (2017). Искать в Google Scholar
[43] Т. Буяк, З. Низиол-Лукашевская, Т. Василевски. Tenside Surf. Дет. 55 , 96 (2018). Искать в Google Scholar
[44] I. Pezron, L. Galet, D. Clausse. J. Colloid Interface Sci. 180 , 285 (1996). Искать в Google Scholar
[45] A. Otzen. Biochem. Биофиз. Acta 1814 , 562 (2011).Искать в Google Scholar
[46] К. Холмберг, Б. Йонссон, Б. Кронберг, Б. Линдман. Поверхностно-активные вещества и полимеры в водном растворе , John Wiley & Sons, West Sussex (2003). Искать в Google Scholar
[47] Э. Д. Годдард. J. Colloid Interface Sci. 256 , 228 (2002). Искать в Google Scholar
[48] А. Буассье, Дж. Э. Лофрот, М. Ниден. Colloids Surf. A 301 , 444 (2007). Искать в Google Scholar
[49] D.П. Норвуд, Э. Минатти, У. Ф. Рид. Макромолекулы 31 , 2957 (1998). Искать в Google Scholar
[50] А. М. Тедески, Э. Бузи, Р. Басози, Л. Падуано, Г. Д’Эррико. J. Solution Chem. 35 , 951 (1998). Искать в Google Scholar
[51] A. Zanette, CF Lima, AA Ruzza, A. Belarmino, S. de F. Santos, V. Frescura, D. Marconi, SJ Froehner . Colloids Surf. A 147 , 89 (1999). Искать в Google Scholar
[52] R.Петкова, С.Чолакова, Н.Д. Денков. Colloids Surf. A 438 , 174 (2013). Искать в Google Scholar
[53] Б. М. Фолмер, Б. Кронберг. Langmuir 16 , 5987 (2000). Искать в Google Scholar
[54] Х. Мальдонадо-Вальдеррама, А. Мартин-Молина, А. Мартин-Родригес, М. А. Кабреризо-Вилчес, М. Дж. Гальвес-Руис, Д. Ланжевен. J. Phys. Chem. C 111 , 2715 (2007). Искать в Google Scholar
[55] G. Imokawa, K.Сумура, М.

 — М.: Анко, 2000. — 143 с.
— М.: Анко, 2000. — 143 с.