Нодулярный фасциит — Мезенхимные опухоли — Ошибки и трудности гистологической диагностики опухолей
Нодулярный фасциит ошибочно принимают за фибросаркому, по данным D. Mackenzie, более чем в 1/3 случаев. Проанализировав наиболее крупные серии наблюдений, этот автор приводит следующие сведения. Нодулярный фасциит может развиться в любом возрасте, но преимущественно между 20 и 40 годами. Мужчины и женщины заболевают приблизительно с одинаковой частотой. Рост обычно быстрый, в течение месяца, но известны отдельные случаи 10-летней и более давности.
Узел может быть как болезненным, так и безболезненным. Очень редко поражение оказывается множественным. Оно находится в непосредственной связи с поверхностными или глубокими фасциями, но не с кожей. Локализуется наичаще на конечностях, реже на туловище, голове или шее, очень редко в других местах, например во влагалище, трахее. Исключительно редко рецидивирует и никогда не метастазирует.
Образование не инкапсулировано, варьирует по величине от 1 до 5 см, в среднем — около 2 см. Внешний вид различен в зависимости от степени выраженности коллагенизации, ослизнения, количества вовлеченного в процесс жира.
Цвет обычно коричневато-беловатый с желтыми пятнами. Пальцеобразные выросты в окружающую клетчатку могут создавать ложное впечатление инвазии. Гистологическое строение довольно пестрое.
P. Allen (1972), например, описал около дюжины морфологических вариантов. Наиболее существен фибробластический компонент. Фибробласты имеют очень различную форму и величину и, в общем, крупнее, чем нормальные. Ядра их овальные, бледные, с хорошо различимым ядрышком. Часто они имеют звездчатые очертания.
Типичные митозы нередки. Встречаются многоядерные клетки, природа которых неясна. Не исключено, что они происходят не из фибробластов или гистиоцитов, а из поперечнополосатых мышечных волокон. Фибробласты расположены, в общем, довольно рыхло и хаотично. Они напоминают скорее фибробласты, растущие в условиях культуры тканей или воспаления, чем клетки фибросаркомы.
Среди фибробластов располагаются зрелые жировые клетки, макрофаги, лимфоциты и плазматические клетки. Много пролиферирующих капилляров различной степени зрелости, от эндотелиальных почек, не имеющих просвета, до зрелых сосудов. Скопления пролиферирующих капилляров местами напоминает грануляционную ткань.
Фибробласты и капилляры погружены в миксоидную или коллагеновую строму, в которой могут встречаться фокусы хрящевой и остеоидной ткани. При дифференциальном диагнозе с фибросаркомой D. Mackenzie рекомендует учитывать следующие признаки. Величина узла более 5 см уже сама по себе делает диагноз нодулярного фасциита маловероятным.
В высокодифференцированной фибросаркоме клетки более или менее одинаковы по величине, форме и часто образуют узоры, напоминающие вышивку «елочкой»; клетки нодулярного фасциита, как уже отмечалось, полиморфны и располагаются беспорядочно. Анапластическая фибросаркома отличается многочисленными атипическими митозами, гиперхромными ядрами и явно опухолевым разнообразием.
«Ошибки и трудности гистологической
www.medchitalka.ru
Нодулярный фасциит — медицинский справочник
Такаясу болезнь 241 Тендинит • дегенеративный 158 • кальцифицирующий 159 Тендовагинит 29,241 Теносиновит • виллонодулярный пигментный 131 • де Кервена 242 • нодулярный локальный 131 Тиманна болезнь 56 Титце синдром 24,243 Триамцинолон 114 Трикуспидальные пороки см. Пороки сердца Туберкулез позвоночника 22 У Узелки Ослера см. Эндокардит инфекционный Уровская болезнь см. Кашина—Бека болезнь Ф Фактор(ы) • некроза опухоли 250, 252 • ревматоидный 6, 15, 27, 31, 35, 47,51 Фасцит эозинофильный 263 Фелти синдром 31, 33 Фиброзит 243 Фиброматоз 133 Флинта шум 185 Форестье гиперостоз 237,244 Фосфолипиды 8 X Хаглунда — Шинца болезнь 56 Хаммена — Рича синдром 245 Хинолиновые препараты 8, 12, 35, 45, 46, 89, 94, 246, 263 Хлорбутин 103 Хондрокальциноз 35,248 Хондроматоз синовиальный 131 Хортона синдром 11 Ц Целлюлит см. Панникулит Циклофосфамид 103 Цитокины 249 Ш Шегрена синдром 31, 35, 252 Шойермана—Мау болезнь 56,58 Штейнерта болезнь см. Миопатии (Миотонии) Э Эбштейна аномалия 181 Элерса—Данлоса синдром 144,255 Эндокардит • бактериальный острый 259 • бородавчатый 68 • грибковый 261 • инфекционный 63,170,257 • париетальный с эозинофилией см. Эозинофильный коллагеноз • ревматический 195 Энтесопатия 261 Эозинофильный • коллагеноз 261 • гранулематоз 261 • фасцит 263 Эрба—Гольдфлама болезнь см. Миопатии (Миастения) Эритема узловатая 264 Этамид 166…
Доброкачественные солитарные фиброзные опухоли Фиброма Ф и б р о м ы к о с т н о — м ы ш е ч н о й с и с т е м ы развиваются преимущественно из сухожильных в л а г а л и щ пальцев, в о с н о в н о м б о л ь ш о г о пальца. Ф и б р о м а встречается преимущественно у молодых или среднего возраста мужчин. Пока н е и з в е с т н о , я в л я е т с я л и э т о т п р о ц е с с нео п л а с т и ч е с к и м или р е а к т и в н ы м . П р и УЗИ фибр о м а выглядит в виде г и п о э х о г е н н о г о о б р а з о вания с четким к о н т у р о м , близко р а с п о л о ж е н н о г о к с у х о ж и л и ю ( р и с . 11.13). Д и ф ф е р е н ц и ровать ф и б р о м у о т г и г а н т о к л е т о ч н о й опухоли по д а н н ы м УЗИ н е в о з м о ж н о . П р и МРТ и н т е н сивность сигнала в Т2-взвешенном изображен и и о д и н а к о в о н и з к а от ф и б р о з н о й т к а н и в ф и бромах и гемосидерина, определяемого в гигантоклеточных опухолях. Нодулярный фасциит Это о т н о с и т е л ь н о ч а с т о е з а б о л е в а н и е р е активного генеза неизвестной этиологии, встречающееся преимущественно у молодых людей. У пациента определяется быстро растущий солитарный узел, немного болезненн ы й п р и п а л ь п а ц и и . О б ы ч н о узел р а с п о л а г а е т с я в п о д к о ж н о й клетчатке, но м о ж е т л о к а лизоваться межмышечно или внутримышечно. Образование примерно в половине случаев в ы я в л я е т с я н а в е р х н е й к о н е ч н о с т и . Хотя о б р а з о в а н и е н е о б л а д а е т и н в а з и в н ы м…
Помимо мягких тканей, фиброма может формироваться в костях (десмопластическая фиброма кости, одонтогенная фиброма). Помимо фибром к доброкачественным фиброзным пролиферативным поражениям относятся гипертрофический рубец, келоид, нодулярный фасциит, пролиферативный фасциит, пролиферативный миозит и воспалительная миофибробластическая опухоль. Чрезмерно увеличенный рубец носит название гипертрофического рубца [hypertrophic scar]. Рубец хрящевидной плотности вследствие гиалиноза образующей его волокнистой ткани называется келоидом [keloid]. Нодулярный фасциит [nodular fasciitis] представляет собой быстро увеличивающийся в размерах узелок (примерно на 1 см в неделю), расположенный в подкожной клетчатке, скелетных мышцах или связанный с их фасциями; очаг поражения при этом редко превышает 3 см в диаметре и обычно имеет чёткие границы. После удаления рецидивирует редко. Пролиферативным фасциитом [proliferative fasciitis] называется аналогичное поражение, в ткани которого выявляются крупные фибробласты, напоминающие нейроны. Такой же процесс в скелетных мышцах носит название пролиферативный миозит [proliferative myositis]. Воспалительная миофибробластическая опухоль – выраженная пролиферация фибробластов и миофибробластов с наличием воспалительной инфильтрации очага поражения. Процесс локализуется обычно в мягких тканях и внутренних органах у детей и лиц молодого возраста. Опухоль, как правило, доброкачественная, но может рецидивировать после удаления, изредка трансформируется в саркому. Глубокие фиброматозы. Десмоидные опухоли (десмоиды) – глубокие фиброматозы, характеризующиеся выраженной пролиферацией активных фибробластов. Различают абдоминальный (в толще передней брюшной стенки), интраабдоминальный (в органах брюшной полости, прежде всего в брыжейке тонкой кишки) и экстра-абдоминальный (при локализации процесса за пределами брюшной стенки и органов брюшной полости) варианты десмоидных опухолей. Множественные поражения внутренних органов при фиброматозе детей раннего возраста часто завершаются смертью ребёнка. Фибросаркома [fibrosarcoma] – одна из наиболее редко встречающихся злокачественных опухолей человека. Выделяют два клинико-морфологических варианта фибросаркомы: фибросаркома детей раннего возраста (врождённая и до 5 лет жизни) и фибросаркома взрослых. Фибросаркома детей раннего возраста протекает относительно благоприятно, показатель 5-летней выживаемости при ней достигает 85%. II. ФИБРОГИСТИОЦИТАРНЫЕ ОПУХОЛИ Фиброгистиоцитарными опухолями называются опухоли фиброзной ткани с большим количеством макрофагов (гистиоцитов). Выделяют три группы фиброгистиоцитарных новообразований – доброкачественные, пограничные и злокачественные. К пограничным опухолям относятся часто рецидивирующие поражения с местно-деструирующим ростом, но редко метастазирующие, т.е. не обладающие всеми признаками злокачественных новообразований. Злокачественные фиброгистиоцитарные новообразования обозначаются общим термином 92… [стр. 92 ⇒]
Опухоли скелетных мышц, как правило, положительны по HHF-35, включая все типы рабдомиосарком. Поспешная идея о том, что HHF-35 является более чувствительным, чем десмин, основывалась, возможно, на исторических трудностях в обнаружении десмина в фиксированных формалином тканях. Гладкомышечные опухоли, лейомиомы, лейомиосаркомы и гломусные опухоли являются устойчиво позитивными, а гемангиоперицитома, как правило, негативна по HHF-35,представляя клинически полезный контрастный образец. Лейомиосаркомы могут показать более высокое число HHF-35 положительных клеток, чем наблюдаемые при иммунной окраске на десмин. Некоторые миофибробластные поражения, такие как узловатый фасциит и фиброма сухожильного влагалища, сильно HHF-35 положительны, находка, которая не должна приводить к ошибочному диагнозу лейомиосаркомы. Другие миофибробластные опухоли, например, десмоиды, имеют только разбросанные HHF-35-положительные клетки. Миофибробласты в десмопластической строме карцином более часто положительные для HHF-35, чем десмин. Злокачественные опухоли фибробластов (например, фибросаркомы, злокачественные фиброзные гистиоцитомы) могут содержать HHF35-положительные клетки, отражающие опухолевый или реактивный миофибробластный компонент. Альфа-актин гладких мышц (SMA) Антитела, специфичные к этому подмножеству актина (например, широко используемого 1A4) имеют реакционную способность в нормальных тканях, аналогичную HHF-35, за исключением того, что они не вступают в реакцию с клетками скелетных мышц. В опухолевых гладкомышечных и миофибробластных тканях они относительно похожи на HHF-35. Так, например, лейомиомы, лейомиосаркомы и гломусные опухоли являются положительными, а гемангиоперицитомы отрицательным для SMA. Антитела SMA обычно не окрашивают рабдомиосаркомы, хотя некоторые опухоли очагами положительны. Лучше всего подтвержденные SMA (и MSA) позитивные карциномы являются, возможно, миоэпителиальными карциномами, которые показали позитивность в 50% и 31% этих маркеров. Еще недостаточно ясно, представляют ли SMA позитивные клетки в других веретеноклеточных карциномах истинную миоидную дифференцировку, или миофибробластный интерстициальный компонент, если они отражают мультипотенциальную мезенхимальную дифференцировку или метаплазию. Саркомерный актин Антитела к саркомерному актину ожидаемо реагируют со скелетными мышцами и рабдомиосаркомами. Хотя хорошо дифференцированные рабдомиосаркомы постоянно показывают экспрессию, плохо дифференцированные позитивны вариабельно, и некоторые лейомиосаркомы также позитивны. Опыт автора и коллег был разочаровывающим в специфичности коммерчески доступных антител к саркомерному актину. Гладкомышечный миозин Образцы иммунореактивности напоминают таковые для гладкомышечного актина. Позитивными являются как гладкомышечные, так и некоторые миофибробластные опухоли, такие как нодулярный фасциит. [стр. 9 ⇒]
Границей между верхней и средней частями глотки является мысленно продленная кзади плоскость твердого неба. Средняя часть глотки — ротоглотка (mesopharynx) участвует в проведении как воздуха, так и пищи; здесь перекрещиваются дыхательный и пищеварительный пути. Спереди ротоглотка имеет отверстие — зев, ведущее в полость рта (рис. 2.3), задняя стенка ее граничит с С ш . Зев ограничен краем мягкого неба, передними и задними небными дужками и корнем языка. В средней части мягкого неба имеется удлинение в виде отростка, который называется язычком (uvula). В боковых отделах мягкое небо расщепляется и переходит в переднюю и заднюю небные дужки, в которых заложены мышцы; при сокращении этих мышц противоположные дужки сближаются, действуя в момент глотания как сфинктер. В самом мягком небе заложена мышца, которая поднимает его и прижимает к задней стенке глотки (m.levator veli palatini), при сокращении этой мышцы расширяется просвет слуховой трубы. Вторая мышца мягкого неба напрягает и растягивает его в стороны, расширяет устье слуховой трубы, но суживает ее просвет в остальной части (m.tensor veli palatini). Между небными дужками в треугольных нишах располагаются небные миндалины (первая и вторая). Гистологическое строение лимфаденоидной ткани глотки однотипно; между соединительнотканными волокнами (трабекулами) находится масса лимфоцитов, часть которых — в виде шаровидных скоплений, называемых фолликулами (рис. 2.4). Однако строение небных миндалин имеет важные с точки зрения клиники особенности. Свободная, или зевная, поверхность небных миндалин обращена в полость глотки и покрыта многослойным плоским эпителием. В отличие от других миндалин глотки каждая небная миндалина имеет 16—18 глубоких щелей, называемых лакунами, или криптами. Наружная поверхность миндалин соединена с боковой стенкой глотки посредством плотной фиброзной оболочки (пересечение шейных и щечных фасций), которую в клинике называют капсулой миндалины. Между капсулой миндалины и глоточной фасцией, покрывающей мышцы, имеется рыхлая паратонзиллярная клетчатка, что облегчает удаление миндалины при тонзиллэктомии. От капсулы в паренхиму миндалины проходит множество соединительнотканных волокон, которые соединяются между собой перекладинами (трабекулами), образуя густопетлистую сеть. Ячейки этой сети заполнены массой лимфоцитов (лимфоидная ткань), которые местами сформированы в фолликулы (лимфатическая, или нодулярная, ткань), образуя в целом лимфаденоид41… [стр. 41 ⇒]
Ф Фагоцитоз, 57, 156, 521 Фактор Виллебранда, 115, 414, 449 выживаемости, 87 некроза опухоли, 37, 53, 69 подвижности клеток, 250 рассеивания, 88, 250 расслабления эндотелиальный, 70 ревматоидный, 182, 183 роста, 18, 76, 87, 251 роста гепатоцитов, 88, 89 роста кератиноцитов, 88, 98 роста колониестимулирующий, 80, 90 роста трансформирующий, 87, 88, 95, 233 роста тромбоцитов, 88, 99 роста фибробластов, 89, 97 роста эндотелиальный сосудистый, 89, 96 роста эпидермальный, 88, 89 свертывания, 569 тканевой, 114 транскрипционный ядерный, 235 тромбоцит-активирующий, 68 Хагемана, 72, 73, 119 Фарингит, 643 Фармакогеномика, 29 Фасциит нодулярный, 983 Фенестрация, 877 Фенилкетонурия, 280, 287, 312, 335 Феномен Артюса, 159, 161 Ауспица, 993 Кебнера, 993 луковой шелухи, 431 мимикрии воспалительного ответа, 439 мимикрии молекулярной, 173 Рейно, 184, 188, 446, 521, 549 Фенотип мутаторный, 231 Феохромоцитома, 942 Ферменты лизосомальные, 70 Фетопротеин, 266, 272 Фибриллы, 206, 280, 403 Фибрилляция желудочков, 481 предсердий, 461 Фибриноген, 79, 117, 121 Фибриноид, 27 Фибринолиз, 63, 120, 564 Фиброаденома, 217, 879 Фиброз, 50, 62, 83, 755 кистозный, 325, 326, 408 легочный, 594 лимфатический паховый, 110 лимфоузловой, 110 массивный прогрессирующий, 596 молочной железы, 876 печеночный, 112 эндомиокардиальный, 499 Фиброма, 216, 222, 859 неоссифицированная, 963 Фиброматоз, 981, 983 Фибронектин, 93 Фиброплазия ретролентальная, 316… [стр. 22 ⇒]
Таблица 21.4. Мягкотканные опухоли Опухоли жировой ткани • Липома • Липосаркома Фиброзные опухоли и опухолеподобные образования • Нодулярный фасциит • Фиброматозы ◊ Поверхностный фиброматоз ◊ Глубокий фиброматоз ◊ Фибросаркома Фиброгистиоцитарные опухоли • Фиброзная гистиоцитома • Выбухающая дерматофиброма • Злокачественная фиброзная гистиоцитома Опухоли скелетных мышц • Рабдомиома • Рабдомиосаркома Опухоли гладких мышц • Лейомиома • Гладкомышечные опухоли с неясным злокачественным потенциалом ◊ Лейомиосаркома Сосудистые опухоли • Гемангиома • Лимфангиома • Гемангиоэндотелиома • Гемангиоперицитома • Ангиосаркома Опухоли периферических нервов • Нейрофиброма • Шваннома Злокачественная опухоль оболочек периферических нервов Опухоли с неопределенным гистогенезом • Синовиальная саркома • Альвеолярная мягкотканная саркома • Эпителиоидная саркома • Зернисто-клеточная опухоль… [стр. 1002 ⇒]
ФИБРОЗНЫЕ ОПУХОЛИ И ОПУХОЛЕПОДОБНЫЕ ОБРАЗОВАНИЯ Фиброзные новообразования — гетерогенная группа пролиферативных процессов. На одном полюсе находится нодулярный фасциит (по природе ближе к реактивной самоограничивающейся пролиферации), на другом — фибросаркомы (агрессивные злокачественные опухоли, для которых характерны локальные рецидивы и гематогенное метастазирование). Промежуточное положение занимают фиброматозы — доброкачественные опухоли, которые отличаются прогрессирующим ростом и склонностью к рецидивированию после резекции. Дифференциальная диагностика между различными типами этих опухолей требует высокой квалификации и опыта от патоморфолога. [стр. 1003 ⇒]
Нодулярный фасциит Нодулярный фасциит — самоограничивающаяся реактивная пролиферация фибробластов, обычно развивающаяся у взрослых лиц (в 10–15% случаев после травмы) на передней поверхности предплечья, грудной клетке и пояснице. Характерны жалобы на быстро растущее в течение нескольких недель одиночное, иногда болезненное, образование. После резекции нодулярный фасциит рецидивирует редко. Образование имеет узловатую структуру и слабо различимые границы, размер, как правило, не превышает нескольких сантиметров. Гистологически в миксоидной строме обнаруживаются хаотически расположенные скопления из «незрелых» фибробластов (рис. 21.28). Клетки полиморфны (веретеновидные и звездчатые), содержат хорошо различимые ядрышки; обнаруживаются многочисленные митозы. [стр. 1003 ⇒]
СКК обычно первично-хроническое заболевание, хотя в течение 6–12 мес нередко возникает спонтанное разрешение симптомов. В лечении используются НПВП, локальная инъекционная стероидная терапия, лечение физическими факторами. При их неэффективности применяется хирургическое лечение, которое обычно состоит в рассечении связки карпального канала, что приводит к ремиссии, но нередко дает рецидивы. Ладонный (пальмарный) фасциит (ПаФ) – относительно редкое заболевание, характеризующееся болезненным уплотнением ладонного апоневроза с формированием сгибательных контрактур пальцев. В отличие от контрактуры Дюпюитрена ПаФ характеризуется болевым синдромом. Также заболевание характеризуется сгибательной контрактурой всех пальцев кисти. При осмотре выявляется умеренное относительно равномерное уплотнение и болезненность ладонного апоневроза. Примерно в половине случаев ПаФ является проявлением паранеопластического синдрома при опухолях женской половой сферы и желудочно-кишечного тракта. В связи с этим все впервые обратившиеся пациенты с ПаФ должны быть обследованы по онкологической программе [21]. Ладонный фасциальный фиброматоз – контрактура Дюпюитрена (КД) – заболевание, характеризующееся стойким неболевым нарушением разгибания пальцев, прежде всего мизинца и безымянного. КД страдают преимущественно мужчины в соотношении к женщинам 5:1. Возраст в большей части после 40 лет, но встречается и в юношеском возрасте, причем, чем моложе больной, тем быстрее прогрессирует болезнь, а у больных до 30 лет стремительное развитие заболевания, характеризующееся быстрым прогрессом и неблагоприятным течением в послеоперационном периоде (келлоидные рубцы, рецидивы в виде стойких контрактур). Отмечен семейный характер КД в том числе у близнецов. Часто развитие КД у больных эпилепсией, злоупотребляющих алкоголем и курением, а также у больных сахарным диабетом 2-го типа, причем в сочетании с подошвенным фиброматозом. КД может быть врожденной, при этом иногда двусторонней. КД характеризуется прогрессирующим фиброзом ладонного апоневроза с формированием на ранней стадии характерных плотных подкожных узлов соответственно ходу лучей апоневроза, без ограничения функции пальцев. В последствие формируются распространенные безболезненные уплотнения, укорочение рубцовых тяжей апоневроза, формирование сгибательных контрактур пальцев, ограничение разгибания в пределах до 90°. В поздней стадии сгибательная контрактура пальцев и ограничение разгибания еще более усиливаются. Основным лечением КД является хирургическая реконструкция апоневроза. Нередко встречаются постоперационные рецидивы болезни. Нодулярный теносиновит сгибателей пальцев кисти или «защелкивающий палец» – характеризуется затруднениями движений пальца кисти и защелкиванием их в положении разгибания. Развивается обычно в пожилом возрасте, чаще у женщин. Возможно появление заболевания при хронической профессиональной или бытовой механической перегрузки и травматизации мягких тканей ладони и пальцев кисти. Клинические проявления характеризуются заклиниванием (затруднением при сгибании и разгибании пальца) и разгибанием со щелчком. Щелчок слышен на расстоянии, ощущается при пальпации… [стр. 15 ⇒]
Позднее была отмечена чувствительность этих опухолей к другим препаратам: цисплатину, этопозиду, ифосфамиду, высокодозному метотрексату и мелфалану. В последние годы наиболее широко используются комбинации двух, трех и четырех лекарственных препаратов. Теносиновиальная гигантоклеточная опухоль (доброкачественная и злокачественная). Теносиновиальная гигантоклеточная опухоль – это обычно локальный, моноартикулярный пролиферативный процесс, который может локализоваться в синовиальных оболочках суставов, бурс, сухожильных влагалищ, прилежащих фасциях и сухожилиях. В настоящее время пигментированный ворсинчатоузловатый синовит подразделяют на внутри- и внесуставные формы. Среди внутрисуставной формы выделяют диффузный и локализованный (полипоидный или нодулярный) синовиты. Внесуставная форма подразделяется на диффузный (внесуставной пигментированный ворсинчато-узловатый синовит или диффузная форма гигантоклеточной опухоли сухожильного и нодулярный (гигантоклеточная опухоль влагалища) сухожильного влагалища) синовиты. Заболевания редко полиартикулярны, не метастазируют, могут вызывать эрозию кости. Встречаются с равной частотой у мужчин и женщин. Локализованная теносиновиальная гигантоклеточная опухоль (син.: гигантоклеточная опухоль сухожильного влагалища, нодулярный теносиновит) поражает лиц, как правило, в возрасте 30-50 лет. Нодулярный теносиновит (доброкачественная гиганто0клеточная синовиома, по G. Geiler) впервые был описан Chossignac (1852). На протяжении всех последующих лет сущность этого процесса была предметом дискуссии. Высказывались соображения о его метаболической, гранулематозной и бластоматозной природе, что выразилось в большом количестве синонимов ксантома сухожилия, ксантоматозная гигантома, миелоксантома сухожилия, гигантоклеточная саркома, гигантома сухожилия, гнгантоклеточная опухоль сухожильного влагалища, фиброэндотелиома сустава, синовиэндотелиома, вариант ~ 97 ~… [стр. 97 ⇒]
medlib.xyz
Некоторые клинические синдромы и заболевания мышц, фасций и сухожилий. Пороки развития мышц
Пороки развития мышц — нередкая патология. Чаще всего встречается порок развития грудино-ключично-сосцевидной мышцы с недостаточной ее длиной, что приводит к неправильному положению головы — кривошее. Голова больного с кривошеей наклонена вперед, повернута в противоположную сторону, надплечье со стороны наклона несколько приподнято, имеется асимметрия лица, черепа. Однако надо учитывать, что кривошея может быть и приобретенной в виде спастической кривошеи, возникающей после энцефалита, инсульта, черепно-мозговой травмы, при торсионной дистопии, заболеваниях позвоночника, нарушении функции вестибулярного аппарата.Другими пороками развития мышц могут быть недоразвитие диафрагмы, приводящее к возникновению диафрагмальной грыжи, отсутствие или недоразвитие мышц плечевого пояса, что существенно сказывается на его функции и создает косметические неудобства.
Ревматическая полимиачгия — системное воспалительное заболевание, возникающее у лиц старше 50 лет. Болезнь начинается острыми болями в мышцах шеи, плечевого и тазового пояса, боль постоянная, усиливается в покос, имеет диффузный характер, появляется скованность, особенно по утрам, как при ревматоидном артрите, ее продолжительность — до 30 минут. Боль может усиливаться при движении, успокаиваться при принятии удобного положения.
При осмотре и пальпации обращает на себя внимание несоответствие между болевым синдромом и объективными данными, определяется лишь небольшая болезненность при исследовании мышц и сухожилий, особенно в области большого бугорка плечевой кости, ключично-акромиального и грудино-ключичного сочленения. Признаков уплотнения, отека, атрофии мышц не обнаруживается. Движения в плечевом поясе, в тазобедренных суставах, в шее ограничены, неохотны.
Больным трудно одеваться, причесываться, умываться, присесть на корточки, встать с низкого стула, подниматься и опускаться по лестнице, походка становится семенящей. Пассивные движения ограничены в меньшем объеме, чем активные. Ревматическая полимиалгия часто сочетается с артритом плечевого сустава, грудино-ключичного сочленения, лучезапястного, коленного сустава, артриты нестойкие. У больных отмечается повышение температуры тела, слабость, похудание, депрессия, височный артериит, что указывает на системность процесса.
Заболевание может возникнуть после вирусной инфекции, респираторных заболеваний, стрессовых ситуаций, переохлаждения.
Фасции — плотные соединительнотканные образования, покрывающие мышцы и их сухожилия, некоторые органы и сосудисто-нервные пучки. Они выполняют опорную и трофическую функцию. Фасции обычно поражаются одновременно с покрывающими их мышцами, пороки развития фасций сочетаются с пороками развития мышц. Встречаются недоразвитие фасций, их гипертрофия. Врожденный дефект фасций способствует образованию мышечной грыжи, дефект может быть и приобретенным. Слабость почечных фасций ведет к нарушению фиксации почек, слабость и повреждение фасции тазового дна проявляется выпадением прямой кишки и матки.
Травматические повреждения фасций бывают открытые и закрытые. Закрытое повреждение возможно при ударе тупым предметом или в результате резкого сокращения мышцы, а также при переломах костей, вывихах. Травматическое повреждение фасций может быть обусловлено особенностями профессии (носильщики, столяры), когда фасция постоянно подвергается давлению, ушибам. Чаще страдает наружная поверхность бедра, боль при этом может быть постоянной или при сгибании и отведении бедра. При пальпации фасции можно выявить болезненность и участки уплотнения.
Воспалительные поражения фасций — фасциит, наблюдаются одновременно с миозитом и имеют тот же генез. При фасциите появляется серозно-фибринозный выпот, в последующем развивается фибропластический пролиферативный процесс с образованием узелков, завершается фасциит фиброзно-рубцовыми изменениями, иногда со стойкими контрактурами.
Фасциит может быть очаговым и диффузным. Возможен узловатый фасциит с неизвестной этиологией, он проявляется опухолевидными узловатыми образованиями в подкожной клетчатке чаще верхних конечностей, которые представляют собой очаговое реактивное воспаление с быстрым инфильтрирующим ростом.
Пальпаторное исследование при фасциите выявляет ограниченную или распространенную болезненность, поверхность мышцы теряет равномерность, она уплотняется, тонус мышцы несколько повышается, имеется ограничение ее функции, возможны контрактура и амиотрофия.
В отдельных случаях при сгибании и разгибании конечности можно услышать щелкающий звук. При фасциите поясничной фасции можно пропальпировать болезненные узловатые образования в поясничной области, такой фасциит часто сопровождается люмбаго.
Диффузный эозинофилъный фасциит — наиболее тяжелый вариант патологии фасций, он представляет собой системное заболевание соединительной ткани с преимущественным поражением глубоких фасций, подкожной клетчатки, подлежащих мышц, кожи. Фасциит сопровождается эозинофилией и гипергаммаглобулинемией. Болезнь возникает после провоцирующих факторов — охлаждение, физическое перенапряжение, травма, острая инфекция, аллергическая реакция.
Развивается склеродермоподобный отек мягких тканей, в фасциях происходит фибриноидное изменение коллагена вплоть до некроза с последующим развитием фиброза и формированием сгибательных контрактур в различных суставах.
У больных появляется чувство стягивания кожи верхних и нижних конечностей, ощущение набухания и плотности мягких тканей, реже — зуд кожи. Движения в руках ограничены, появляется слабость в ногах при подъеме по лестнице. Кожа напоминает апельсиновую корку, плохо берется в складку из-за ее отека и отека подкожной клетчатки, боли нет. Возможны полимиалгии и мышечная слабость.
Опухоли фасций наблюдаются редко, они бывают доброкачественные (фиброма) и злокачественные (фибросаркома). Их величина от нескольких миллиметров до 5 см и более, располагаются они обычно глубоко, связаны с фаспиальными структурами и мышцами, чаще на бедрах. Встречается особое соединительнотканное образование с инфильтрирующим ростом — десмоид (десмоидная фиброма), — это плотные, одиночные узлы чаще, в брюшной стенке.
Опухоль растет из сухожильных и фасциально-апоневротических структур. Она прорастает в окружающие ткани, в первую очередь в мышцы. По мере роста в процесс вовлекаются кости и другие близлежащие органы. Такая клиническая картина сближает десмоид со злокачественными опухолями, однако метастазов он не даст.
Фиброзит (фибромиалгия, миофасциальная боль, фибралгия) — это ревматическое заболевание мягких тканей вне суставов («ревматизм мягких тканей»). По существу фиброзит1 представляет собой клинический синдром.
Возникновению фиброзита способствуют механические перегрузки, микротрав матизация, дистрофия мягких тканей. Он нередко наблюдается при таких ревматических заболеваниях, как ревматоидный артрит, системная красная волчанка, а также при инфекционных процессах, метаболических расстройствах, опухолях.
Основные клинические проявления фиброзита — боль в мягких тканях туловища и конечностей, скованность по утрам, усталость. Боль постоянная, тупая, распирающая, усиливающаяся в утренние и вечерние часы, после физических и психических нагрузок, при перемене погоды, охлаждении. Боль стихает под влиянием тепла, отдыха, массажа. На фойе распространенных болей методом пальпации можно выявить участки повышенной болезненности, отличающиеся особым постоянством, — это специфические болевые точки, надавливание пальцем на которые вызывает сильную, порой нестерпимую боль. Иногда над этими точками отмечается гиперемия, гиперестезия кожи, уплотнение мягких тканей.
Атрофии мышц, ограничения пассивных движений не отмечается. Смайтом (1972, 1981) предложены следующие критерии диагностики фиброзита:
• наличие генерализованных мышечных болей с продолжительностью не менее 3 месяцев;
• болезненность при пальпации не менее чем в 12 специфических точках;
• болезненность при взятии кожи в складку над верхней частью лопатки;
• нарушение сна;
• скованность и усталость по утрам.
В 1990 г. Американской коллегией ревматологов были предложены следующие критерии диагностики фибромиалгии.
1. Анамнез генерализованной боли. Определение: диффузная боль в левой и/или правой половине тела, выше или ниже талии, кроме того, возможна аксиальная боль (боль в шее, в области переднего отдела грудной клетки или спине).
Длительность боли в течение более чем 3 последних месяцев. Наличие другой клинической патологии не исключает диагноз фибромиалгии.
2. Боль при пальпации в 11 из 18 точек следующей локализации:
• билатерально в области затылка в месте прикрепления субокципитальной мышцы;
• билатерально в области шеи возле С5-С7 позвонков;
• билатерально посередине верхней границы трапециевидной мышцы;
• билатерально над лопаткой около медиальной границы т. supraspi-natus;
• билатерально у второго костно-хондрального реберного сочленения;
• билатерально на 2 см дистальнее латерального надмыщелка плечевой кости;
• билатерально в верхнем наружном квадранте ягодиц;
• билатерально кзади от трахеи;
• билатерально в области коленей, несколько проксимальнее сустава, в середине жирового тела Гоффы.
Пальцевое давление должно соответствовать 4 кг, положительным ответом считается только возникновение боли, а не нарушение чувствительности.
Больные фиброзитом отмечают повышенную утомляемость, нарушение сна, мнительность, обидчивость, ранимость, придирчивость. Наиболее часто фиброзит встречается у женщин в возрасте 25-35 лет.
И.А. Реуцкий, В.Ф. Маринин, А.В. Глотов
Опубликовал Константин Моканов
medbe.ru
| ВОКБ№1
ДЕПАРТАМЕНТ ЗДРАВООХРАНЕНИЯ ВОРОНЕЖСКОЙ ОБЛАСТИ
БУЗ ВО «ВОРОНЕЖСКАЯ ОБЛАСТНАЯ КЛИНИЧЕСКАЯ БОЛЬНИЦА № 1»
Нодулярный теносиновит
пальцев кисти
Методические рекомендации для хирургов,
ортопедов-травматологов и слушателей ИДПО
Составители:
Заведующий отделением микрохирургии БУЗ ВО ВОКБ № 1
д.м.н. Ходорковский М.А.
Врач отделения микрохирургии БУЗ ВО ВОКБ № 1
к.м.н. Скорынин О.С.
Воронеж – 2015
Введение
Нодулярный теносиновит – это доброкачественная местно-инвазивная опухоль мягких тканей, чаще всего поражающая синовиальные оболочки и сухожильные влагалища пальцев кисти. Нодулярный теносиновит — второе по частоте встречаемости (после сухожильного ганглия) новообразование мягких тканей кисти. Заболевание впервые описал в 1852 году французский хирург Эдуард Шассеньяк (Édouard-Pierre-Marie Chassaignac), назвав его «раком сухожильного влагалища».
|
Рис. 1. Эдуард Шассеньяк (1804 – 1879) |
В дальнейшем это новообразование получило множество названий: ворсинчатый артрит, гигантоклеточная фиброгемангиома, гистиоцитарная ксантоматозная гранулема, доброкачественная гигантоклеточная синовиома, доброкачественная синовиома, ксантогранулема, ксантома, ксантосаркома, миелоидная эндотелиома, миелоксантома, миелома сухожильного влагалища, миелоплаксическая опухоль, плазмоцитарный синовит, склерозирующая гемангиома, фиброгемосидерическая опухоль, фиброзная ксантома, фиброма сухожилия, эндотелиома. В современной отечественной литературе данная нозология именуется «нодулярный теносиновит», в зарубежной – «гигантоклеточная опухоль сухожильных влагалищ (giant cell tumor of the tendon sheath — GCTTS)» или «пигментированный ворсинчато-узловатый синовит (pigmented villonodular synovitis — PVNS)».
Заболевание обычно возникает у пациентов в возрасте от 30 до 50 лет, несколько чаще у женщин (64%). Частота встречаемости в популяции: 1 случай на 50 000. Несмотря на доброкачественный характер новообразования, частота местных рецидивов после хирургического лечения достигает 47%.
Этиология и патогенез
Такое количество наименований у одного заболевания свидетельствует об отсутствии единого взгляда на его этиопатогенез. Предполагалось, что эта патология возникает вследствие метаболических нарушений или воспалительного процесса. В дальнейшем, анализ ДНК и иммуногистохимические исследования показали наличие в очагах нодулярного теносиновита клеточных популяций, имеющих некоторые опухолевые характеристики. Однако принадлежность нодулярного теносиновита к доброкачественным или злокачественным новообразованиям соединительной ткани долгое время была предметом дискуссий. В настоящее время доказано, что, несмотря на высокую частоту местных рецидивов, нодулярный теносиновит не является злокачественным новообразованием и не метастазирует. Большинство специалистов считают, что причиной возникновения нодулярного теносиновита является реактивная или регенеративная гиперплазия, связанная с воспалительным процессом. Вместе с тем, фактор воспаления, запускающий этот механизм, до настоящего времени не идентифицирован ни клинически, ни экспериментально.
Клиника
Нодулярный теносиновит клинически проявляется как медленно растущее опухолевидное образование, располагающееся под кожей пальцев и кисти, вблизи сухожилий или суставов. Опухолевые узлы могут быть одиночными и множественными (рис. 2). Типичная локализация опухолей при нодулярном теносиновите – проксимальные фаланги II, III и IV пальцев кисти (рис. 3). Тыльная поверхность фаланг поражается в 57%, волярная – в 37%, обе поверхности – в 6% случаев. Размер опухоли в среднем составляет 1,6±0,6 см, и, как правило, не превышает 4 см. Большие опухоли могут охватывать фалангу циркулярно. Взаимосвязи между размером опухоли, ее локализацией, полом и возрастом пациентов не обнаружено. В 15% — 28% случаев растущая опухоль может вызвать деструкцию костной ткани фаланги без признаков инфильтративного роста. Болевой синдром при нодулярном теносиновите не характерен. Обычно пациенты обращаются с жалобами на деформацию пальца.
 |
 |
|
Рис. 2. Нодулярный теносиновит дистальной фаланги II пальца. |
Рис. 3. Частота поражения различных отделов кисти при нодулярном теносиновите. |
Патологическая анатомия
Макроскопически нодулярный теносиновит выглядит как один или несколько опухолевых узлов белого или серого цвета с желтыми участками в местах скопления ксантомных клеток и гемосидерина. Опухоль часто имеет дольчатое строение в виде узла с сателлитами, покрыта более или менее выраженной псевдокапсулой (рис. 4, 5).
 |
 |
|
Рис. 4. Опухолевый узел в псевдокапсуле |
Рис. 5. Опухолевый узел на разрезе |
Микроскопически при нодулярном теносиновите обнаруживаются перемычки из плотной фиброзной ткани, придающие опухоли узловатый вид. Характерно наличие нескольких типов клеток:
— маленькие круглые или продолговатые, часто с почковидными или расщепленными ядрами, иногда с заметными ядрышками;
— продолговатые, часто веретенообразной формы;
— гигантские клетки, имеющие 8-10 однотипных ядер и ксантомные клетки с редкими митозами (рис. 6).
Митотическая активность — низкая (3-5 митозов на 10 полей зрения). Изредка наблюдаются зоны некроза.
|
|
|
Рис. 6. Микроскопическая картина нодулярного теносиновита — в поле зрения видны гигантские клетки и макрофаги, содержащие гемосидерин. |
Классификация нодулярного теносиновита пальцев кисти
Многие авторы выделяют два типа нодулярного теносиновита – ограниченный и диффузный (встречается редко). В настоящее время общепринятой является классификация, предложенная в 2001 году пластическим хирургом из Саудовской Аравии Mohammad M. Al-Qattan. (таб. 1).
Таблица 1.
Классификация нодулярного теносиновита кисти (M.M. Al—Qattan, 2001)
|
Тип I (вся опухоль окружена одной псевдокапсулой) |
I a |
Одиночный узел в толстой белесоватой капсуле |
 |
|
I b |
Одиночный узел в тонкой капсуле |
 |
|
|
I c |
Несколько узлов в общей псевдокапсуле |
 |
Таблица 1(продолжение).
|
Тип II (вся опухоль не окружена одной псевдокапсулой) |
II a |
Один главный узел (с псевдокапсулой) и несколько сателлитных узлов в пределах одной анатомической зоны |
 |
|
II b |
Диффузный тип в виде множества гранулоподобных образований без псевдокапсулы |
||
|
II c |
Мультицентрический тип в виде нескольких отдельных самостоятельных узлов в пределах одного пальца |
Частота встречаемости различных типов нодулярного теносиновита представлена на диаграмме (рис. 7).
Рис. 7. Частота встречаемости различных типов нодулярного теносиновита кисти
Диагностика нодулярного теносиновита
Учитывая поверхностное расположение новообразований при нодулярном теносиновите, начинать диагностику следует с ультразвукового исследования (УЗИ) мягких тканей. Для этого используют ультразвуковые сканеры высокого разрешения с высокочастотным линейным датчиком (7,5 – 13 МГц) и функцией цветового допплеровского картирования (ЦДК). С помощью УЗИ можно визуализировать опухолевые узлы и их положение по отношению к сухожильным влагалищам и суставам, уточнить размеры, эхогенность, наличие зон костной деструкции (рис. 9). Степень васкуляризации опухоли оценивают с помощью ЦДК. Как правило, нодулярный теносиновит при УЗИ выглядит как гипоэхогенное новообразование, имеющее гомогенную структуру и всегда контактирующее с сухожильным влагалищем или суставной капсулой (рис. 8). При ЦДК в половине случаев выявляется периферический тип кровоснабжения опухоли, в остальных наблюдениях – сочетание периферического и центрального типов. Менее чем в половине наблюдений отмечается гиперваскуляризация опухоли (рис. 10).
|
Рис. 8. Продольная сонограмма ладонной поверхности IV пальца. На уровне пястно-фалангового сустава имеется солидное, гомогенное, гипоэхогенное новообразование (отмечено крестиками), непосредственно контактирующее с сухожилием сгибателя (обозначено буквой Т).
|
|
|
Рис. 9. Продольная сонограмма ладонной поверхности I пальца. На уровне проксимальной фаланги имеется солидное, гомогенное, гипоэхогенное новообразование (отмечено крестиками), непосредственно контактирующее с сухожилием сгибателя (обозначено буквой Т). Стрелками отмечена зона костной деструкции.
|
|
|
А |
Б |
|
Рис. 10. Поперечная сонограмма II пальца. А — На уровне проксимальной фаланги имеется солидное, гомогенное, гипоэхогенное новообразование (отмечено крестиками), циркулярно охватывающеес сухожилие сгибателя (обозначено буквой Т). Б – при ЦДК обнаружен центральный и периферический кровоток. |
|
Стандартная рентгенография кисти малоинформативна для диагностики нодулярного теносиновита, но позволяет выявить очаги костной деструкции. Основные причины возникновения костной патологии при нодулярном теносиновите представлены на схеме (рис. 11). На рис. 12 представлена рентгенографическая картина типичных вариантов костной деструкции при нодулярном теносиновите.
Рис. 11. Причины возникновения костной деструкции при нодулярном теносиновите.
|
А |
Б |
В |
Г |
|
Рис. 12. Рентгенограммы пальцев кисти при нодулярном теносиновите: А – мягкотканная опухоль в области дистального межфалангового сустава; Б – деструкция дистального межфалангового сустава; В – компрессионная атрофия кортикального слоя средней фаланги; Г – деструкция кости в месте вхождения питающих сосудов. |
|||
Методом выбора в диагностике нодулярного теносиновита является магнитно-резонансная томография (МРТ). Типичный для этой патологии результат МРТ – наличие четко отграниченного узлового образования, дающего изоинтенсивный к мышечной ткани сигнал в режиме Т1-взвешенных изображений. В режиме Т2-взвешенных изображений сигнал слабый или умеренный (рис. 13 — 15). Может наблюдаться градиентный отраженный сигнал при наличии отложений гемосидерина и повышение интенсивности при контрастировании (рис. 16).
|
Рис. 13. Осевая магнитно-резонансная томограмма пальцев кисти в режиме Т1-взвешенных изображений |
|
|
Рис. 14. Осевая магнитно-резонансная томограмма пальцев кисти в режиме Т2-взвешенных изображений |
|
|
Рис. 15. Сагиттальная магнитно-резонансная томограмма пальца в режиме Т1-взвешенных изображений |
|
|
Рис. 16. Осевая магнитно-резонансная томограмма кисти в режиме Т1-взвешенных изображений с контрастным усилением |
Тонкоигольная аспирационная биопсия опухоли с цитологическим исследованием материала может оказаться полезной для дифференциальной диагностики нодулярного теносиновита с другими новообразованиями мягких тканей пальцев кисти (рис. 17).
|
Рис. 17. Цитологическая картина материала, полученного с помощью тонкоигольной аспирационной биопсии при нодулярном теносиновите. Обнаруживаются разрозненные скопления макрофагов, единичные гигантские клетки (отмечены стрелкой). |
Дифференциальный диагноз
Перечень новообразований мягких тканей пальцев кисти, с которыми необходимо дифференцировать нодулярный теносиновит, представлен в таблице 2. Вышеперечисленные методы инструментальной диагностики позволяют успешно решить эту задачу.
Таблица 2.
Новообразования, с которыми необходимо дифференцировать нодулярный теносиновит
|
НОВООБРАЗОВАНИЯ |
||||
|
Сосудистые |
Костные |
Периферических нервов |
Кожи |
Мягких тканей |
|
||||
Лечение нодулярного теносиновита пальцев кисти
Общепринятым методом лечения нодулярного теносиновита является хирургическое удаление опухолевых узлов с капсулой. Рекомендуется использовать для этого деликатные инструменты и средства оптического увеличения. Вместе с опухолью следует удалять скомпрометированные участки сухожильного влагалища, суставной капсулы, надкостницы, связочного аппарата и даже сухожилия. Операция может быть выполнена под проводниковой анестезией по Лукашевичу-Оберсту или по Брауну-Усольцевой. Необходимо использовать местные анестетики длительного действия, так как после радикального удаления опухоли может потребоваться пластика сухожилий, связок и даже артропластика. При локализации опухоли на уровне пястно-фаланговых суставов или проксимальнее, показана проводниковая блокада плечевого сплетения. При небольших одиночных узлах разрез кожи производят в косом или поперечном по отношению к оси пальца направлении.
При больших и множественных новообразованиях разрезы должны быть Z-образными или зигзагообразными. Прямых продольных разрезов следует избегать. Определенные трудности возникают при распространенном процессе, захватывающем и волярную и тыльную поверхности пальца. В таких случаях, при планировании и осуществлении доступа следует сохранять сосудисто-нервные пучки пальца. Опухоли, имеющие выраженную капсулу, удаляются достаточно просто. Для отделения опухоли от окружающих тканей рекомендуется использовать периостальный элеватор-распатор типа Freer, применяемый в стоматологии и оториноларингологии (рис. 18).
|
Рис. 18. Периостальный элеватор-распатор типа Freer |
Рекомендуется следующий технический прием: опухоль пинцетом смещают «взад-вперед», одновременно отделяя опухолевый узел элеватором от окружающих тканей (рис. 19). Благодаря этому снижается риск того, что мелкие опухолевые сателлиты останутся неудаленными.
Рис. 19. Мобилизация опухолевого узла с помощью элеватора.
Тщательному удалению сателлитных узлов и отрогов следует уделить особое внимание, поскольку очень мелкие фрагменты опухоли плохо дифференцируются от окружающих тканей и могут стать причиной рецидива. При наличии очагов костной деструкции выполняют их кюретаж. В ряде случаев, вместе с опухолью удаляются фрагменты сухожилий или кольцевидных связок, что является показанием к их первичной реконструкции (рис. 20).
В послеоперационном периоде могут наблюдаться следующие осложнения: потеря чувствительности пальца (6%), ограничение подвижности в пястно-фаланговых и межфаланговых суставах (6%), формирование болезненного рубца (11%). Гнойно-некротические осложнения наблюдаются в 1% случаев.
|
А |
Б |
|
Рис. 20. А — нодулярный теносиновит, локализующийся в области кольцевидной связки А1. Б — Опухоль удалена вместе с кольцевидной связкой. Стрелкой отмечен участок диффузного поражения связки опухолью. |
|
Профилактика рецидивов нодулярного теносиновита
Характерной особенностью нодулярного теносиновита пальцев кисти является высокая частота местных рецидивов (до 47%). По мнению большинства специалистов, чаще всего рецидивируют опухоли II типа. К факторам риска возникновения рецидива нодулярного теносиновита относятся:
- Локализация в области дистального межфалангового сустава.
- Нерадикальная операция.
- Наличие костной деструкции.
- Высокая митотическая активность при гистологическом исследовании.
- Локализация опухоли вблизи сустава, пораженного артритом.
- Отсутствие в ДНК опухолевых клеток гена-супрессора nm 23.
- Опухоли II типа.
С целью профилактики рецидива нодулярного теносиновита рекомендуется послеоперационная лучевая терапия (ежедневная доза 1,5 – 2 Gy, суммарная очаговая доза 15 – 25 Gy). Показаниями к назначению лучевой терапии являются:
- Нерадикальное удаление опухоли.
- Высокая митотическая активность клеток.
- Костная деструкция.
По данным разных авторов, послеоперационная лучевая терапия снижает частоту рецидивов до 0% — 4%.
Рецидивирование нодулярного теносиновита является показанием к повторному оперативному вмешательству.
hospital-vrn.ru
Лечение диффузного фасциита
Общее описание
Диффузный фасциит – патология соединительной ткани с поражением кожи, подкожной клетчатки, мышц. Протекает на фоне эозинофилии (повышение числа эозинов в крови), гипергаммаглобулинемии (повышение в крови гамма-глобулина).
Болезнь названа по имени американского врача, исследователя ревматизма Шульмана, учёный в 1970-х годах выделил заболевание в отдельную форму. Редкость заболевания поразительна: отечественная наука сталкивалась лишь с несколькими случаями.
Болеют преимущественно мужчины в возрасте от 25 до 60 лет. У женщин болезнь Шульмана встречается приблизительно в два раза реже. Начинается заболевание с общих симптомов, многие пациенты не подозревают развитие диффузного фасциита. Специфические симптомы появляются постепенно. Многие терапевты склонны считать, что у пациента развивается системная склеродермия либо прочее аутоиммунное заболевание.
Классификация
Общепринятой является классификация опухолей мягких тканей и костей, разработанная экспертами ВОЗ. Первое её издание вышло в свет в 1969 г., второе — в 1994 г., третье — в 2002 г. В феврале 2013 г. ожидается четвёртое издание руководства ВОЗ.
Среди опухолей мягких тканей выделяют следующие группы:
- Опухоли из (мио)фибробластов
- «Фиброгистиоцитарные» опухоли
- Опухоли белой и бурой жировых тканей
- Опухоли гладкой и поперечно-полосатой мышечных тканей
- Сосудистые опухоли (эндотелиоцитарные и периваскулярные)
- Опухоли серозных и синовиальных оболочек
- Опухоли периферической нервной системы
- Хрящевые и костные опухоли мягких тканей
- Опухоли неясного гистогенеза.
Степень злокачественности мягкотканных сарком
Степень злокачественности мягкотканных сарком в настоящее время оценивается с учётом трёх показателей [система FNCLCC]: (1) степень дифференцировки опухоли, (2) пролиферативная активность опухолевых клеток, (3) наличие и выраженность некрозов опухолевой ткани.
I. Дифференцировка опухоли
- 1 балл — саркомы, ткань которых напоминает нормальный аналог мягких тканей взрослого человека
- 2 балла — саркомы с признаками слабого сходства с нормальными аналогами мягких тканей взрослого организма
- 3 балла — эмбриональные, недифференцированные саркомы и саркомы неясного типа.
II. Митотическая активность (число фигур митозов в 10 полях зрения при увеличении микроскопа 400)
- 1 балл — 0—9 фигур
- 2 балла — 10—19 фигур
- 3 балла — 20 и более фигур.
III. Некроз опухолевой ткани
- 0 баллов — отсутствие некрозов
- 1 балл — некроз опухоли занимает менее 50% её площади
- 2 балла — некроз опухоли занимает более 50% её площади.
Сумма баллов трёх микроморфологических признаков определяет три степени злокачественности мягкотканных сарком: I степень — 2—3 балла, II степень — 4—5 баллов, III степень — 6—8 баллов [M. Miettinen (Институт патологии Вооружённых сил США), 2003].
Признаки диффузного фасциита
Картина симптомов болезни характерна наличием уплотнения мягких тканей рук и ног. Нарушается их двигательная активность.
Развиваются сгибательные контрактуры в суставах пальцев. Сгибательная контрактура приобретает вид нарушения разгибания сустава в отличие от разгибательной контрактуры, когда сустав сложно сгибать.
Диффузный фасциит прогрессирует остро — через несколько дней после действия провоцирующих факторов.
Сначала больного беспокоит общее недомогание, повышенная температура, боль в суставах и мышцах. На неблагоприятном фоне развивается болезненный отёк дистального отдела конечностей. Поражаются стопы, голени, бёдра, туловище. Редко отёк распространяется на пальцы, шею, туловище. Одновременно появляется ощущение стягивания кожи, зуд.
Особенности диагностики болезни
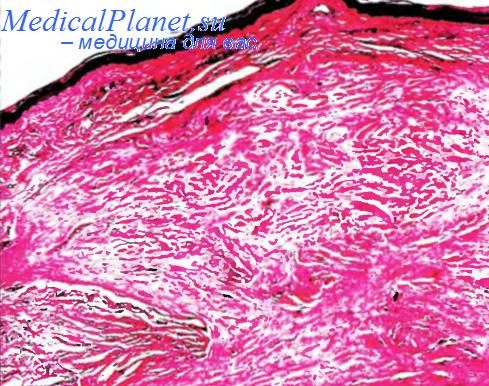

Своевременное распознавание заболевания затруднено ввиду редкости болезни. Однако больные с подозрением на эозинофильный фасциит направляются к ревматологу для углубленного анализа. Иногда требуется осмотр дерматолога для исключения заболеваний кожи.
Большое значение имеет наличие апельсиновой корки на коже, ограничение двигательной активности. Диагностическое значение показывает биохимический анализ кожи с верификацией данных гамма-глобулина, СОЭ, фибриногена. Положительный ревматоидный фактор заставляет думать о наличии болезни Шульмана.
Иногда пациенту ошибочно ставится диагноз «системная склеродермия», «тендовагинит» или «ревматоидный артрит». Это связано с недостаточной квалификацией врача и недостаточной изученностью заболевания. Поэтому важна дифференциальная диагностика: болезнь требуется отличать от системной склеродермии, подобных синдромов. Главные отличительные черты болезни Шульмана:
- Отсутствие синдрома Рейно;
- Отсутствие плотного отёка пальцев рук и кистей;
- При системной склеродермии у больного поражаются лёгкие и пищевод;
- При склеродермии Бушке развивается плотный отёк верхней части туловища. Характерное для эозинофильного фасциита поражение фасций отсутствует;
- При тендовагините поражение сустава несимметричное, в отличие от эозинофильного фасциита.
Решающее значение для диагностики имеет биопсия кожи, мышц, мышечных фасций.
Особенности лечения
Диффузный фасциит лечится особенно эффективно на ранних стадиях. Важно своевременно обнаружить болезнь. Запоздалое лечение менее эффективно. Однако возможно добиться стойкого эффекта благодаря длительному, комплексному лечению.
В терапии диффузного фасциита ведущее место имеет применение глюкокортикостероидов. В первую очередь, Преднизолон.
В редких случаях назначаются большие (60 мг и больше) дозы препарата. Назначение Преднизолона – длительное, до снижения активности патологического процесса.
Препарат полагается принимать до снижения объективных и субъективных признаков болезни. Известны случаи приёма Преднизолона длительно – до восьми лет.
Применение нестероидных противовоспалительных препаратов не даёт необходимой эффективности, в большинстве случаев не назначаются. Иногда препараты назначают в комбинации с Преднизолоном.

Наиболее эффективный препарат группы – Циметидин. Дополнительно назначаются цитостатики (Азатиоприн).
При выраженном фиброзе назначают D-пеницилламин. Дозировка цитостатиков – до 150 миллиграммов в сутки, а Д-пенициллин назначается до 600 мг в сутки.
При корректном назначении терапевтических мер, правильном выполнении больным рекомендаций врача патологические симптомы пропадают. Пациенты чувствуют облегчение состояния и заметное улучшение активных движений в суставах.
Показана местная противовоспалительная и противофиброзирующая терапия. Используют аппликации диметилсульфоксида, фонофорез Трилона Б. При условии, что активность патологического процесса снижена, применяют лечебную физкультуру и массаж. Лечебные теплые ванны способствуют улучшению состояния пациентов.
sustaw.top
Параартикулярные ткани: варианты поражения и их лечение (продолжение) | Хитров Н.А.
Статья посвящена вариантам поражения и лечению параартикулярных тканей
 Главная проблема людей современного общества – это способность вести «независимую жизнь». Заболевания опорно-двигательного аппарата причиняют механические, физические, психологические и эстетические страдания. Сохранность органов движения является медицинской и социальной задачей. Большую долю заболеваний локомоторного аппарата составляют периартриты – поражения параартикулярных тканей (ППАТ) суставов.
Главная проблема людей современного общества – это способность вести «независимую жизнь». Заболевания опорно-двигательного аппарата причиняют механические, физические, психологические и эстетические страдания. Сохранность органов движения является медицинской и социальной задачей. Большую долю заболеваний локомоторного аппарата составляют периартриты – поражения параартикулярных тканей (ППАТ) суставов.Параартикулярные ткани представляют совокупность околосуставных структур и отдаленных от суставов тканей. Околосуставные ткани включают: сухожилия мышц и их влагалища, сумки, связки, фасции, апоневрозы. Отдаленные от суставов структуры составляют: мышцы, нервно-сосудистые образования, подкожно-жировая клетчатка [1].
Среди ППАТ выделяют:
• теносиновит – воспаление сухожильного влагалища;
• тендинит – воспаление сухожилия;
• бурсит – воспаление синовиальной сумки;
• энтезопатию (энтезит) – воспаление энтезиса – места прикрепления сухожилия или связки к кости или суставной капсуле;
• капсулит – поражение капсулы сустава;
• фасциит, апоневрозит – поражение фасций и апоневрозов;
• миофасциальный болевой синдром – изменения в скелетной мышце и прилегающей фасции.
Neipel в 1966 г. впервые использовал термин «энтезопатия», J. Ball в 1971 г. сообщил о высокой частоте энтезопатий при анкилозирующем спондилите. В 1991 г. признано, что энтезопатии являются отличительной патогенетически значимой характеристикой спондилоартропатий. Особенно это касается энтезопатий пяточных областей (энтезиты ахиллова сухожилия, подошвенного апоневроза, ахиллотендинит, бурситы и др.), которые обычно сочетаются с периферическим суставным синдромом, но в ряде случаев являются единственным или доминирующим по тяжести поражением опорно-двигательного аппарата при спондилоартритах.
В энтезисах волокна сухожилия или связки перед тем, как перейти в костную структуру, становятся более компактными, затем хрящевыми, и, наконец, кальцифицированными. Питание энтеза происходит посредством анастомозов через оболочки сухожилий – перитенон, перихондрий или периост. Энтезы являются метаболически активными и имеют хорошо развитую иннервацию.
Именно область энтезиса становится «слабым звеном» в аппарате околосуставных тканей, где при чрезмерной нагрузке возникают микро- и макроскопические повреждения, приводящие в последующем к локальному воспалению [2, 3].
Воспаление приобретает важную роль как при энтезопатиях, так и при других ППАТ, лежит в основе обострения ППАТ, усиливает дегенерацию тканей. Воспаление в энтезисе не ограничивается соединительной тканью (например, тендинит или фиброзит). Отмечается также вовлечение в патологический процесс хряща и кости, что приводит первоначально к возникновению периостита, а в дальнейшем к появлению эрозий кости.
За рубежом ревматические поражения мягких тканей объединяются термином «внесуставной ревматизм» (non-articular rheumatism) или «ревматизм мягких тканей» (soft tissue rheumatism).
Ранее в РМЖ была опубликована статья, в которой подробно рассмотрены ППАТ верхних конечностей и спины [4]. В данной публикации остановимся подробно на поражениях параартикулярных тканей нижних конечностей.
Бедро
ППАТ в бедренной области носят разнообразный характер и представлены в основном теномиозитами мышц бедра, которые нередко протекают в безболевой форме и характеризуются щелчками при движении, слышимыми на расстоянии. Болевой синдром присутствует при энтезопатиях большого вертела бедренной кости, воспалительных явлениях в синовиальных сумках пояса нижних конечностей.Больные разного возраста жалуются на щелчки в области тазобедренного сустава (боль при этом обычно отсутствует). Больной сам показывает движения, при которых возникают щелчки. Данная клиника обусловлена: трением подвздошно-большеберцового тракта о большой вертел, трением сухожилия подвздошно-поясничной мышцы о подвздошно-лобковое возвышение, трением большой ягодичной мышцы о большой вертел, а также нестабильностью тазобедренного сустава. Данный симптом встречается при аномалиях развития, дисплазиях соединительной ткани структур бедра, дегенеративно-дистрофических процессах, травмах и др.
Визуализационные методы исследования (рентген, УЗИ, МРТ), помимо обнаружения дисплазий и других изменений в тазобедренном суставе, редко способствуют постановке диагноза. Уточнению данного вида ППАТ способствуют хорошо собранный анамнез, оценка объема и характера движений в тазобедренном суставе и в поясничной области, тщательная пальпация. Основное лечение состоит в том, чтобы успокоить больного, разъяснить суть заболевания, назначить упражнения для разработки мягкотканных структур, заинтересованных в формировании щелчков, под контролем методиста ЛФК. Возможно физиолечение, использование мягких ортезов на пояснично-бедренную область.
В области бедра встречаются болевые синдромы, вызванные поражением сухожильно-связочных и мышечных структур.
Тендинит подвздошно-поясничной мышцы – характеризуется болью в верхней части бедра, затрудняющей ходьбу. При этом встречается ограничение разгибания из-за боли в паху и спине. Отмечаются болезненность при сгибании бедра, болезненные щелчки во время полного разгибания тазобедренного сустава. Возможна боль в брюшной полости. Часто боль локализуется ниже паха, что соответствует месту прикрепления мышцы к малому вертелу бедра. Пальпаторно через переднюю брюшную стенку могут обнаруживаться болезненно уплотненные мышцы. При данном ППАТ возможно ущемление кожного бедренного нерва – невралгия Бернгардта–Рота, сопряженная с онемением и парестезией по наружной поверхности бедра.
Синдром мышцы, натягивающей широкую фасцию бедра – характеризуется появлением боли и дискомфорта при перекидывании пораженной ноги на здоровую. Спонтанная боль возникает редко (может быть ощущение «вбитого гвоздя» в области крыла подвздошной кости).
При положении пациента на боку, при слегка согнутой в тазобедренном и коленном суставах ноги, находящейся сверху, хорошо пальпируется выступающая сверху область большого вертела бедренной кости. Возникающий болевой синдром при этом расценивается как трохантерит. Варианты трохантеритов обычно включают в себя: энтезит большого вертела и более редко встречающийся бурсит вертельной сумки. Причинами трохантерита являются врожденные или приобретенные нарушения строения таза или ног, большие механические нагрузки, травмы, переохлаждение, излишек веса тела, особенно возникший за короткий срок. Часто причину установить не удается.
Энтезит большого вертела – частая причина болей в области бедра. Это заболевание осложняет течение остеоартроза у женщин 40–60 лет, но может протекать и без коксартроза. Проявляется болями, иррадиирующими по наружной поверхности бедра. Типичная жалоба больного – невозможность лежать, особенно спать на боку поражения. Имеет место отчетливая локальная болезненность области большого вертела, сохранность объема пассивной ротации в тазобедренном суставе и боль при сопротивлении активному отведению бедра. Если боль при этом усиливается при движении, ходьбе, то мы имеем дело с энтезопатией отводящих мышц. Постоянная боль указывает на вертельный бурсит.
В отличие от коксартроза трохантерит имеет характерные болевые точки при пальпации. При трохантерите нет ограничения движений в тазобедренном суставе, как пассивных, так и активных. Данные рентгеновского исследования позволяют дифференцировать признаки коксартроза с проявлениями энтезитов в области большого вертела бедренной кости.
Бурситы бедренной области встречаются реже патологии энтезисов, сухожилий и связок данной области. Чаще всего воспаляются следующие сумки тазовой области: вертельная сумка (вursa trochanterica), подвздошно-гребешковая сумка (вursa iliopectinea) и седалищная сумка (вursa ischiadica) [5].
Вертельный бурсит – развивается чаще, чем другие виды бурситов бедра. Вертельная сумка находится возле большого вертела бедренной кости. Вертельный бурсит развивается чаще у профессиональных спортсменов. Чаще заболевают женщины. Предрасположенность женщин к заболеванию вертельным бурситом объясняют особенностями строения женского таза. Женский таз шире, и большой вертел отстоит дальше от средней линии тела, что способствует более сильному трению мышц об него [6].
Основным симптомом являются боли в области большого вертела (по боковой поверхности бедра). Ходьба, различные движения и лежание на боку поражения усиливают боль. Начало вертельного бурсита может быть внезапным, но чаще носит медленно прогрессирующий характер. Беспокоят боли при сгибании бедра, при вставании со стула и при подъеме по лестнице. Особенно сильно беспокоят ночные боли – когда пациенты переворачиваются или лежат на больной стороне, эти боли будят их.
Если попросить показать участок наибольшей болезненности, больной точно указывает на область большого вертела. Если бы действительно была боль в суставе, больной указывал бы на паховую область.
Наилучшим способом диагностики вертельного бурсита служит пальпация области большого вертела для выявления локальной болезненности. Осмотр проводят в положении больного лежа на здоровом боку, со слегка согнутой в тазобедренном суставе и колене ногой. Надавливание на большой вертел вызывает резкую боль, нередко иррадиирующую по наружной стороне бедра в поясницу.
Подвздошно-гребешковый бурсит – второе по частоте развития заболевание среди воспалений сумок бедра. Подвздошно-гребешковая сумка располагается спереди от пояснично-подвздошной мышцы. При накоплении в ней значительного количества экссудата она может определяться в паху в виде опухолевидного образования. В связи с тем что подвздошно-гребешковая сумка находится очень близко к суставу, картина ее воспаления очень напоминает воспаление самого тазобедренного сустава. Основным симптомом этого вида бурсита является болезненность и отечность передневнутренней части бедра ниже уровня паховой связки, боль усиливается при разгибании бедра. Сдавление растянутой сумкой бедренного нерва может приводить к появлению болей и парестезий в бедре.
Седалищный бурсит (синдром «сидящего портного») – развивается при сидении на твердой поверхности, особенно у худых людей. Седалищная сумка располагается в непосредственной близости к седалищному бугру. Возможна энтезопатия этой области, которая встречается как в рамках какого-либо спондилоартрита (реактивный артрит, болезнь Бехтерева), так и самостоятельно. Седалищный бугор испытывает нагрузку в положении человека сидя, особенно на жестком основании. Типична жалоба больного на боль именно в этом положении, в меньшей степени при ходьбе. Боль при седалищном бурсите, в отличие от подвздошно-гребешкового, усиливается при сгибании бедра.
Колено
В области коленного сустава ППАТ представлены наиболее часто бурситами, энтезопатиями и теносиновитами.Препателлярный бурсит – бурсит преднадколенниковой сумки («колено паркетчика»). Воспаленная преднадколенниковая сумка расположена поверх надколенника и не связана с полостью коленного сустава. Воспаление ее встречается нечасто, вызывается повторной травмой или нагрузкой при длительном нахождении на коленях. Характеризуется флуктуирующей припухлостью, отеком, невыраженным болевым синдромом, возможным местным повышением температуры, гиперемией кожи. Может инфицироваться, особенно при повреждении кожи.
Рецидивов бурсита можно избежать, исключив этиологический фактор (защита коленного сустава при хронической травме с помощью ортеза). При инфицировании препателлярной сумки, что является следствием острой травмы и нарушения целостности кожных покровов в передней части коленного сустава, отмечается припухлость, резкая, дергающая боль в преднадколенниковой области, усиливающаяся при пальпации. Визуально там же отмечается гиперемия, гипертермия кожных покровов. В этом случае содержимое бурсы включает гной и больной должен лечиться как пациент с гнойным процессом.
Киста Бейкера (КБ) – растянутая жидкостью синовиальная сумка подколенной ямки, расположенная в ее медиальном отделе между внутренней головкой икроножной и полуперепончатой мышц и сообщающаяся с коленным суставом посредством соустья.
Наиболее признан клапанный механизм проникновения суставной жидкости через соустье из полости коленного сустава в КБ, когда обратный ток жидкости из КБ в суставную полость затруднен [7]. В 1877 г. W.M. Baker отметил тесную взаимосвязь наличия внутрисуставных повреждений и заболеваний коленного сустава с развитием подколенных кист.
КБ в большинстве случаев возникает как вторичное заболевание. Причинами ее возникновения являются синовиты сустава (остеоартроз, ревматоидный артрит и др.), посттравматические состояния коленного сустава. КБ при малых размерах обычно протекает безболезненно, она не видна невооруженным глазом, пальпация ее затруднительна. На фоне симптомов поражения коленного сустава клиника КБ отсутствует.
При больших размерах КБ видна визуально и легко пальпируется как плотноэластическое опухолевидное образование продолговато-яйцевидной формы, локализующееся в мягких тканях подколенной области, преимущественно в медиальных отделах подколенной ямки (рис. 1). При значительных размерах КБ может частично препятствовать сгибанию в коленном суставе. Пациенты с крупной КБ ощущают тяжесть по задней поверхности сустава при физических нагрузках, чувство дискомфорта, наличие опухолевидного образования в подколенной ямке. Симптомокомплекс может включать боль в икроножных мышцах или нарушение чувствительности по задней поверхности голени, особенно после длительной ходьбы или во время подъема и спуска по лестнице. Все эти симптомы могут быть изолированными, но чаще сочетаются с клиникой внутрисуставной патологии коленного сустава, присутствующей при этом [8–10].

Возможна резорбция жидкости из КБ с обратным развитием ее до полного исчезновения. Такой доброкачественный исход характерен для кист, образовавшихся недавно, обычно после чрезмерных механических перегрузок коленных суставов в процессе строительных работ, спортивных состязаний, интенсивного труда на дачных участках и т. д. В случае стойкого синовита коленного сустава КБ приобретает хроническое течение. При хроническом течении КБ жидкость подвергается частичной резорбции, что приводит к ее сгущению и затрудняет ее аспирацию из полости кисты. При длительном течении в КБ скапливается фибрин, образуются перемычки, септы, дочерние кисты (рис. 2).
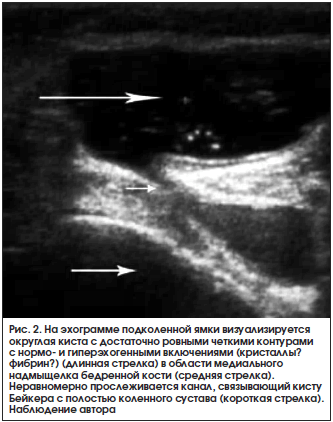
Обычно КБ протекает доброкачественно, лишь психологически пугая больных. Однако при быстром накоплении выпота в подколенной сумке возможен разрыв КБ с распространением суставной жидкости по задним межфасциальным пространствам голени. Клиника острого разрыва КБ напоминает картину тромбоза вен голени (отек голени, распирающие боли). После прорыва выпот из коленного сустава и самой КБ исчезает.
Возможно нагноение КБ, которое клинически напоминает тромбофлебит поверхностных вен голени и характеризуется возникновением на фоне суставного анамнеза выпотом и болью в подколенной ямке, гиперемией, гипертермией данной области, а также ознобм, лихорадкой, изменением формулы крови.
Использование УЗИ и МРТ позволяет установить наличие КБ, ее топографическое расположение в подколенной ямке, визуализировать контуры и содержимое кисты, проследить ее границы и протяженность, определить связь кисты с полостью сустава, выявить признаки разрыва и воспаления стенки, повреждения внутрисуставных структур, остеоартроза, артрита коленного сустава. УЗИ подколенной области необходимо не только для диагностики КБ, но и для выявления часто встречаемых патологических состояний: тромбоза (тромбофлебита) глубоких вен, аневризмы бедренной и подколенной артерии, абсцесса, опухоли, разрыва мышц и др.
Нередко страдает связка надколенника, которая несет большую функциональную нагрузку, являясь связующим звеном между квадрицепсом и голенью, принимая участие в разгибании коленного сустава. Надколенник при этом рассматривается как сесамовидная кость. Повреждение связки надколенника возникает при механических нагрузках и травмах обычно в местах соединения связки (в виде энтезопатии) с нижним краем надколенника («колено прыгуна») и большеберцовой костью («колено футболиста»).
«Колено прыгуна» – «верхний» лигаментит связки надколенника. Причиной заболевания служит механическая перегрузка коленного сустава, которая может быть как внезапной, так и хронической. Наиболее часто лигаментит надколенника развивается в результате неадекватного напряжения квадрицепса. «Колено прыгуна» чаще всего наблюдается у теннисистов, легкоатлетов, футболистов, баскетболистов, волейболистов. Предрасполагающим фактором обычно являются длительные прыжки на твердом покрытии.
Клиническая картина складывается из боли, припухлости и болевого ограничения подвижности. Боль, локализующаяся ниже надколенника, усиливается при пальпации и в положении сидя. Визуально в данном месте определяется небольшая припухлость. Отмечается ограничение подвижности в коленном суставе и ощущение утраты его силы.
Болезнь Осгуда–Шлаттера (Osgood–Schlatter’s disease) – можно рассматривать в узком смысле как «нижний» лигаментит связки надколенника, представляющий из себя энтезопатию. Обычно и традиционно болезнь Осгуда–Шлаттера рассматривается как хондропатия – периостит и воспаление бугристости большеберцовой кости. Причинами «колена футболиста» могут быть периодические незначительные травмы этого участка, часто возникающие у мальчиков в подростковом возрасте при физической активности.
Клиника болезни Осгуда–Шлаттера типична: наиболее часто она начинается с нерезких болей в области бугристости большеберцовой кости, которые появляются только при значительной физической нагрузке. С прогрессированием заболевания боли возникают уже при меньших нагрузках. В редких случаях боль появляется и в покое. Отличительным признаком болей при болезни Осгуда–Шлаттера является их усиление в области бугристости большеберцовой кости при напряжении четырехглавой мышцы бедра и при стоянии больного на коленях. Патогномоничным симптомом выступает локальная болезненность, от незначительной до сильной, при пальпации и/или перкуссии области бугристости большеберцовой кости. Пальпация других прилегающих областей, как правило, безболезненна. Амплитуда движений в коленном суставе не изменяется. Рентгенологически при хроническом течении болезни Осгуда–Шлаттера отмечается костная перестройка с кистовидной перестройкой и фрагментацией бугристости большеберцовой кости. При недолгом (остром) течении процесса в виде энтезопатии рентгенологически патологию можно не выявить [11].
Энтезопатия и теномиозит «гусиной лапки» – нередкий вариант ППАТ области коленного сустава. «Гусиная лапка» (pes anserinus) представляет собой место прикрепления к большеберцовой кости сухожилий портняжной (m. sartorius), тонкой (m. gracilis) и полусухожильной (m. semitendinosus) мышц. Анатомически находится на 3–4 см ниже проекции щели коленного сустава по медиальной его поверхности. Данное ППАТ часто осложняет течение гонартроза, в иных случаях наблюдается при здоровом коленном суставе. Заболевание развивается часто у людей, которые много времени проводят на ногах, например у спортсменов-бегунов.
Типичны жалобы больного на боль при ходьбе. Больной указывает пальцем болезненную точку. Отмечается усиление боли при сгибании и разгибании коленного сустава. При осмотре определяется резкая пальпаторная болезненность площадью 3–4 кв. см. Часто симптомы энтезопатии беспокоят пациента значительно больше, чем проявления собственно гонартроза.
Анзериновый бурсит – встречается реже теномиозита «гусиной лапки», наблюдается у женщин старше 55—60 лет, страдающих гонартрозом. У большинства из них отмечаются избыточная масса тела, деформация коленных суставов. Как правило, у этих больных, помимо жалоб, характерных для гонартроза (боли в суставах, усиливающиеся при нагрузке и к концу дня), присутствуют также жалобы на боли, возникающие ночью при давлении одного колена на другое и вынуждающие менять положение ног. У всех этих больных имеется выраженная локальная болезненность в анзериновой области при пальпации. Возможна визуально заметная деформация – припухлость данной области. При УЗИ бурсит «гусиной лапки» легко диагностируется в виде анэхогенного скопления жидкости.
Стопа
Сложное строение стопы и голеностопного сустава обеспечивает удержание тела человека в вертикальном положении. Имея сводчатое строение, стопа выполняет опорную и рессорную функции. Свод стопы фиксируется продольными и поперечными стяжками, а также подошвенным апоневрозом. Многочисленные мышцы стопы относятся к активным стяжкам, которые прикрепляются на разных уровнях стопы. Сухожилия служат «мостиками» между костями и мышцами стопы, которые плотно к ним крепятся. В тех случаях, когда мышечно-скелетная система ног подвергается значительным нагрузкам, связки стопы травмируются.Среди причин, которые могут вызвать развитие тендинитов стопы, выделяют: чрезмерные физические нагрузки на стопу, механическое повреждение и травму, патологию строения скелета, плоскостопие, неправильную осанку, систематическое ношение обуви с высоким каблуком, привычный подвывих стопы, возрастные отклонения, дегенеративно-дистрофические нарушения в тканях стопы, заболевания суставов (ревматоидный артрит, подагра и др.), нарушение обмена веществ. По причине высокой частоты встречаемости тендинитов и энтезитов стопу называют «энтезитным органом».
Ахиллодиния, или тендинит ахиллова сухожилия – состояние, часто встречающееся при спондилоартритах. Грубое поражение ахиллова сухожилия можно увидеть у больных с синдромом гипермобильности суставов с выраженным плоскостопием, как правило, в возрасте старше 30 лет. При ахиллодинии возникают отечность и боли при нагрузке в области дистальной части сухожилия и/или в месте прикрепления сухожилия к пяточной кости. В последнем случае боли могут быть связаны с бурситом заднетаранной сумки, которая здесь располагается. Боли наиболее выражены при ходьбе и длительном стоянии.
Сгибание и разгибание стопы усиливает боль. Область наибольшей болезненности находится в месте соединения сухожилия с пяточной костью и на 2–3 см проксимальнее. Сухожилие в указанной области отечно и утолщено. Может случиться спонтанный разрыв сухожилия, который характеризуется внезапным возникновением сильной боли по задней поверхности стопы, особенно во время дорсального сгибания.
Тендинит задней большеберцовой мышцы – воспаление сухожилия задней большеберцовой мышцы и его влагалища. Место наибольшей болезненности при этом располагается на медиальной поверхности голеностопного сустава. Боль и отек отмечаются по ходу сухожилия. Боль усиливается при подворачивании стопы внутрь, при пальпации и перкуссии области медиальной лодыжки. Данное ППАТ часто сочетается с туннельным синдромом большеберцового нерва, расцениваемым, как синдром тарзального канала. Под медиальной лодыжкой вместе с сухожилиями задней большеберцовой мышцы и мышц-сгибателей пальцев проходит большеберцовый нерв. Теносиновит указанных мышц с сопутствующим расширением сухожилий приводит к механическим симптомам сдавления и ишемии большеберцового нерва, что проявляется болями, парестезиями и онемением, распространяющимися по медиальной части стопы. При диагностике используют симптом Тинеля и манжеточный тест [12].
Тендинит малоберцовых мышц – под латеральной лодыжкой наблюдается (как изолированно, так и при сопутствующих воспалительных артропатиях) утолщение колбасовидной формы по ходу сухожильного влагалища перонеальных мышц. При ходьбе и пальпации этой области возникает боль.
Подошвенный (плантарный) фасциит (ПлФ) – заболевание, обусловленное воспалительно-дегенеративными изменениями подошвенной фасции. Клиническим признаком ПлФ является боль в подошве, и особенно в пятке. Боли в пяточной области обычно возникают и/или усиливаются при нагрузке. Болевые ощущения более выражены в утренние часы. При выраженном процессе боли распространяются по всей подошвенной поверхности стопы, усиливаются при давлении на низ стопы (при ходьбе, беге, пальпации). Боль ощущается сильнее при первых шагах, после вставания с постели. Постоянная микротравматизация фасции может послужить причиной хронического асептического воспаления с болевым синдромом. Диагностике ПлФ способствуют анализ жалоб пациента, физикальный осмотр, рентгенография, УЗИ, МРТ.
На фоне ПлФ, в качестве компенсаторной реакции, возможно образование краевых костных разрастаний (остеофитов), получивших название «пяточных шпор» (ПШ). ПШ представляют собой депозиты кальция на нижней части пяточной кости. ПШ нередко ассоциированы с ПлФ. ПШ на задней части пяточного бугра нередко ассоциированы с воспалением ахиллова сухожилия (тендинитом) и могут быть причиной болезненности и болей в задней части пятки, усиливающихся при сгибании стопы.
ПШ анатомически располагаются в месте энтезиса – по ходу прикрепления подошвенной фасции или ахиллова сухожилия к пяточной кости.
Важно отметить, что ПШ могут не вызывать никаких симптомов вообще и случайно обнаруживаются во время рентгенологического обследования. ПШ преимущественно страдают люди старше 40 лет, причем больше к этому заболеванию предрасположены женщины. ПШ часто наблюдаются у пожилых людей, т. к. инволюционные изменения в тканях приводят к снижению эластичности подошвенной фасции. Другие факторы развития ПШ: избыточный вес, ожирение, длительное нахождение на ногах, плоскостопие или, наоборот, высокий свод стопы, плохо подобранная или изношенная обувь, метаболические нарушения.
В большинстве случаев пациенты жалуются на интенсивную, очень резкую боль в пятке во время ходьбы. Характерным симптомом ПШ являются так называемые «стартовые» боли – возникающие в утренние часы или после длительного сидения. Причиной боли служит травмирование мягких тканей шпорой.
Рентгенологически выявляется наличие костного выроста по подошвенной или задней поверхности пяточной кости. Этот вырост имеет вид шипа и может сопровождаться периоститом, эрозиями пяточной кости. На ранних стадиях возможно рентгенологическое отсутствие костного шипа. В этом случае причиной болей выступают воспалительные изменения (плантарный фасциит или подпяточный бурсит). Рентгенологическое обнаружение и размер ПШ не всегда коррелируют с выраженностью болевого синдрома. Крупные ПШ могут существовать безболезненно ввиду адаптации перифокальных тканей к болевым раздражителям.
Отсутствие пяточной шпоры в совокупности с пяточной болью требует дифференциального диагноза, в первую очередь с системными воспалительными заболеваниями (ревматоидный артрит, синдром Рейтера и др.), которые также могут дебютировать пяточной болью.
Подошвенный фасциальный фиброматоз, или синдром Леддерхозе (СЛ) – фиброматоз невоспалительного характера. СЛ аналогичен и нередко сочетается с контрактурой Дюпюитрена. Данное ППАТ проявляется локальными утолщениями подошвенной фасции. Вначале заболевание не доставляет страданий, однако в конечных стадиях подошвенная фасция утолщается, стягивается, приводя к сгибательной контрактуре пальцев. Ходьба при этом становится болезненной. У части пациентов симптомы возникают на обеих стопах.
Пальпаторно плотные, безболезненные, округлые и в виде жгутов узлы при СЛ наиболее часто присутствуют около самой высокой точки поперечного свода стопы. Узелки обычно безболезненны, и боль возникает лишь при трении их об обувь или пол. При УЗИ и МРТ выявляется инфильтрирующая масса в апоневрозе рядом с подошвенными мышцами, позволяющая выявить степень повреждения.
Относительно факторов риска СЛ следует отметить, что заболевание нередко носит семейный характер, чаще встречается у мужчин, сочетается с ладонным фиброматозом, болезнью Пейрони, эпилепсией, сахарным диабетом. Обсуждается связь с алкоголизмом, курением, заболеваниями печени, щитовидной железы, напряженной работой с нагрузкой на ноги.
На ранних стадиях лечения рекомендуется избегать прямого давления на узелки, применять мягкие стельки, супинаторы в обуви. На поздних стадиях СЛ используются хирургические методы лечения со сложным прогнозом, т. к. очень близко расположены сухожилия, нервы и мышцы. Так же как и при контрактуре Дюпюитрена, часто развиваются рецидивы болезни. Стопа испытывает нагрузку всего тела, что приводит к нередким постоперационным осложнениям.
Лечение
В лечении ППАТ главенствующим условием является исключение провоцирующих факторов, прежде всего механических перегрузок. Необходимо ограничение механической нагрузки на структуры, которые вовлечены в конкретное поражение. При выраженном воспалении их показан полный покой с использованием ортезов, лангет в острый период заболевания. Двигательный режим, лечебная физкультура, массаж, мануальная терапия должны носить механически щадящий характер и осуществляться в безболевой зоне.Локальная инъекционная терапия, прежде всего глюкокортикоидами (ГК) с учетом анатомо-морфологических особенностей ППАТ, показаний, противопоказаний, правильно выбранной дозы ГК, числа и кратности введения, позволяет добиться хороших клинических результатов в лечении ППАТ.
Также используются анальгетики, слабые опиоиды, миорелаксанты, седативные препараты. При стихании острого процесса используются физические методы: тепло и криотерапия, магнито-, лазеротерапия, электро- и фонофорез, грязевые аппликации, бальнеолечение. Применяются ударно-волновая терапия и методы психической релаксации. В случае возникновения ППАТ на фоне ревматических болезней необходимо лечение основного заболевания.
ППАТ как частный вид скелетно-мышечных болезней независимо от этиологии во многом обусловлены едиными патогенетическими закономерностями, определяющими появление и переход заболевания в хроническое состояние. Эффективное купирование болевого синдрома – первоочередная задача фармакотерапии ППАТ, т. к. боль представляет наиболее тягостное ощущение, определяющее тяжесть страданий и снижение качества жизни пациента [13].
Противовоспалительные средства являются непременным условием терапии ППАТ, включая прежде всего нестероидные противовоспалительные препараты (НПВП) локального (накожного) и системного (перорального, ректального и внутримышечного) применения. Лечебная эффективность и переносимость различных НПВП у каждого пациента индивидуальны, и при назначении НПВП необходим строго персональный подход с оценкой эффективности и побочных действий применяемого препарата [14, 15].
Для противовоспалительного и обезболивающего действия желательно использовать Амелотекс (международное непатентованное название – мелоксикам) – НПВП, относящийся к классу оксикамов, производных энолиевой кислоты, обладающий анальгетическим, противовоспалительным и жаропонижающим действием. Мелоксикам преимущественно ингибирует ферментативную активность ЦОГ-2, подавляет синтез простагландинов в области воспаления в большей степени, чем в слизистой оболочке желудка или почках, реже вызывает эрозивно-язвенные поражения ЖКТ по сравнению с другими НПВП. Мелоксикам имеет ряд иных фармакологических свойств, позволяющих прогнозировать его высокую эффективность при лечении боли и воспаления: влияние на синтез важнейших провоспалительных цитокинов (интерлейкин–6, фактор некроза опухоли α), блокада синтеза металлопротеиназ, антигистаминное действие, снижение активности агрессивных клеток (макрофагов и нейтрофилов) в очагах воспаления и др. [16–18].
Амелотекс выпускается в виде раствора для внутримышечного введения, свечей, таблеток и геля. Одна ампула (1,5 мл) содержит в качестве активного вещества 15 мг мелоксикама.
Для купирования болевого и воспалительного синдрома при ППАТ желательно использовать внутримышечный способ введения лекарственного препарата ввиду быстрого лечебного эффекта и минимального побочного воздействия на ЖКТ. При невозможности внутримышечных инъекций, во избежание отрицательного воздействия на ЖКТ возможно альтернативное назначение НПВП в виде ректальных свечей (при этом снижается риск развития гастропатий).
В начале лечения, в острый период, желательно проведение курса внутримышечных инъекций Амелотекса по 1,5 мл 1 р./сут 10–15 дней или ректальное использование Амелотекса по 1 свече 1 р./сут на протяжении 1–2-х недель. Далее при сохранении клиники возможен переход на пероральное применение – 15 мг/сут. На период лечения ППАТ Амелотексом желательно использовать гелевую форму препарата: наносить на область поражения параартикулярных тканей 3–6 р./сут в течение 10–14 дней.
Таким образом, к лечению ППАТ необходим дифференцированный подход, т. к. данные заболевания носят собирательный характер и включают патологию энтезисов, связок, сухожилий мышц, параартикулярных сумок и т. п. В патогенезе развития ППАТ лежат различные травматические, воспалительные и дегенеративно-дистрофические механизмы. Лечение ППАТ должно проводиться комплексно, с исключением травмирующих факторов, упорядоченным двигательным режимом, с физическими методами, локальной инъекционной стероидной терапией, а также НПВП, включая различные формы Амелотекса. Амелотекс является препаратом выбора при наличии относительных противопоказаний к приему НПВП, а также при неэффективности других методов лечения.
www.rmj.ru
Диффузный эозинофильный фасциит (болезнь Шульмана)
Диффузный эозинофильный фасциит (ДЭФ) — относительно редкое системное заболевание соединительной ткани с преимущественным поражением глубокой фасции (воспаление с исходом в фиброз), подкожной клетчатки и подлежащих мышц и дермы, сопровождающееся эозинофилией и гипергаммаглобулинемией.Как самостоятельная нозологическая форма заболевание выделено в 1974 г. L. Е. Shulman из склеродермической группы болезней. ДЭФ развивается преимущественно в возрасте 25-60 лет, хотя возможно возникновение заболевания в детском и пожилом возрасте. Мужчины болеют в 2 раза чаще, чем женщины.
Этиология и патогенез
Этиология и патогенез заболевания изучены недостаточно. Среди провоцирующих факторов, способствующих развитию ДЭФ, отмечают чрезмерную или необычную для больного физическую нагрузку (физическое перенапряжение), в частности поднятие тяжестей, спортивные перетренировки. Из других предшествующих факторов следует отметить переохлаждение, травмы, операции, нервно-психическое перенапряжение и стрессы. Предполагается также роль генетической предрасположенности. В патогенезе ДЭФ центральное место занимают иммунные нарушения, что подтверждается наличием гипергаммаглобулинемии, повышением содержания иммуноглобулинов, особенно иммуноглобулина G, циркулирующих иммунных комплексов и развитием иммунного воспаления в глубокой фасции и близлежащих тканях.
Клиника
Заболевание обычно начинается остро с возникновения характерных изменений в течение первого месяца (и даже недели), хотя возможно и постепенное начало с медленным прогрессированием заболевания. Начало болезни может совпадать с физическим перенапряжением.
В клинической картине преобладает уплотнение мягких тканей верхних и нижних конечностей, главным образом в области предплечий и голеней. Кисти и стопы при этом, как правило, не поражаются. Возможно распространение процесса на туловище, редко — на шею и лицо. Характерен симптом «апельсиновой корки» в виде мягких втяжений при максимальном натяжении кожи (при максимальном разгибании конечности). Могут также наблюдаться диффузная или очаговая гиперпигментация кожи в пораженных участках, кожный зуд, сухость и явления гиперкератоза.
Пораженные ткани отечны и напряжены. Несмотря на то, что кожные покровы над ними не вовлечены в процесс, кожа в этих участках выглядит сморщенной. При эозинофильном фасциите нередко развиваются сгибательные контрактуры локтевых и коленных суставов, редко — пальцев кистей. У части больных отмечаются полиартралгии.
Вовлечение внутренних органов не наблюдается. Специфические лабораторные изменения отсутствуют. Не присуща заболеванию и сосудистая патология, лишь изредка имеют место сосудистые нарушения в виде «стертого» синдрома Рейно. Тесты на ревматоидные факторы и антинуклеарные антитела обычно отрицательны. У некоторых больных выявляется значительная эозинофилия (до 50%). Увеличение числа эозинофилов обнаруживается и в участках воспаления.
Диагностика
Из лабораторных показателей диагностическим признаком болезни считается эозинофилия (до 50%). Периферическая и тканевая эозинофилия выявляется обычно в раннем периоде заболевания, а в дальнейшем может уменьшиться или полностью исчезнуть, особенно при назначении ГКС. Могут также наблюдаться: увеличение СОЭ, наличие СРБ, гиперα2— и γ-глобулинемия, повышение содержания в сыворотке крови серомукоида, фибриногена, церулоплазмина, иммуноглобулинов G и М, ЦИК, повышение титра антинуклеарных и ревматоидного факторов. Это отражает воспалительную и иммунологическую активность заболевания.
При морфологическом исследовании патологические изменения обнаруживаются преимущественно в фасциях и прилежащих тканях. В раннем периоде ДЭФ утолщенная и отечная фасция содержит набухшие коллагеновые волокна, инфильтрирована лимфоплазмоцитарными клетками, гистиоцитами и эозинофилами. Аналогичная инфильтрация выявляется в подкожной клетчатке, нижних слоях дермы и участках мышцы, прилегающих к фасции. В поздних стадиях наблюдается преобладание склероза и гиалиноза в фасции и прилегающих тканях, уменьшение или исчезновение клеточной инфильтрации и экссудативных процессов.
Диагноз ДЭФ основывается в первую очередь на сочетании характерных клинических (уплотнение тканей преимущественно в области предплечий и голеней с нарушением объема движений и развитием сгибательных контрактур) и лабораторных (эозинофилия, гипергаммаглобулинемии) признаков болезни. При постановке диагноза следует также учитывать связь с предшествующим физическим перенапряжением, преимущественное поражение мужчин и острое начало заболевания. Диагноз ДЭФ должен быть подтвержден морфологическим исследованием биоптатов фасции и прилежащих тканей.
Лечение
Лечение ДЭФ должно быть длительным и систематическим. Терапия более эффективна в раннем периоде болезни. Прежде всего назначаются кортикостероиды, главным образом преднизолон в начальной дозе 20-40 мг в сутки. После достижения клинического эффекта доза постепенно снижается до поддерживающей — 5-10 мг в сутки. В такой дозе преднизолон может применяться в течение многих месяцев и даже лет. Лечение стероидами может комбинироваться с НПВП (мелоксикам, диклофенак и др.) и аминохинолиновыми производными. При неэффективности гормонотерапии дополнительно назначаются иммуносупрессоры, преимущественно азатиоприн по 150 мг в сутки в течение нескольких месяцев.
Показано применение при ДЭФ антифиброзных средств, в частности тиоловых соединений и димексида.
Д-пеницилламин назначается по 450-600 мг в сутки, унитиол вводится внутримышечно ежедневно по 5-10 мл 5% раствора в течение 30-40 дней или методом суперэлектрофореза с димексидом (20-25 ежедневных сеансов на курс лечения). Используются также аппликации 50% раствора димексида.
Определенный клинический эффект оказывает используемая в последние годы карбогемосорбция. При невысокой активности патологического процесса проводится массаж и лечебная физкультура.
«Ревматология»
Т.Н. Бортная
medbe.ru


