причины, симптомы, диагностика и лечение — Клиника «Доктор рядом»
Нефрологический термин «киста почки» используют для обозначения патологического состояния, характеризующегося развитием в структурах органа новообразования доброкачественной природы. Сама по себе киста представляет собой полость с жидкостью, располагающую капсулой из соединительной ткани. Она является частым явлением в нефрологии: её диагностируют в 25% случаев, как правило — у пациентов старше сорока пяти лет. В группу риска попадают мужчины с избыточной массой тела, повышенным АД, болезнями МВС инфекционной природы.
Причины и лечение кисты почек взаимосвязаны, поскольку первые (наряду с целым рядом других параметров) определяют выбор методик коррекции состояния. Правильный выбор играет важную роль, поскольку обуславливает результаты лечебных мероприятий.
Если у вас совпадает больше 80% перечисленных симптомов, то настоятельно рекомендуем вам обратиться к врачу за консультацией.
Этиология кисты почек
Инициирующие факторы кисты левой/правой почки могут быть разными. Они обуславливают нарушения развития соединительной ткани и эпителия, которые формируют кисты. К ним относят:
| Инициирующий фактор | Чем проявлен? |
| Поражение почечных тканей вследствие заболеваний |
|
| Старение организма | После сорока пяти лет нагрузка на мочевыделительную систему возрастает. Помимо этого, срабатывает комплекс несущественных, но многочисленных нарушений в организме, которые усиливают воздействие друг друга. |
| Врождённый | Кисты обеих почек или одной из них могут быть результатом сбоев в период внутриутробного развития. |
Классификация кист почек
Систематизация новообразований осуществляется с учётом разных параметров: местонахождения, структуры, содержимого.
| Вид новообразования | Характерные особенности |
| Исходя из расположения |
|
| Синусные кисты почек | Локализуются в области почечных ворот или лоханок, бывают двух видов:
|
| Субкапсулярные | Располагаются под капсулой почки. |
| Интрапаренхиматозная киста почки | Обнаруживается в тканях почечной капсулы или в области синусов. |
| В соответствии со структурными особенностями |
|
| Солитарный | Полость с одной камерой, наполненная жидкостью, диаметром от нескольких миллиметров до десяти сантиметров. Очень распространена, выявляют почти в 80% случаев. |
| Поликистоз | Множественные кисты разной формы и диаметра, нередко — формирующиеся в тканях обеих почек. Инициирующий фактор нередко кроется во врождённых аномалиях МВС, поэтому обнаруживают новообразования уже в детском возрасте. |
| Мультилокулярный | Внутри полость располагает разделительными перегородками. Передаётся по наследству. |
Признаки кисты почки
Чаще всего заболевание протекает без клинических проявлений, поскольку развитие новообразования происходит медленно, за счёт чего почечные ткани успевают адаптироваться к нему, исключая существенную утрату функциональности.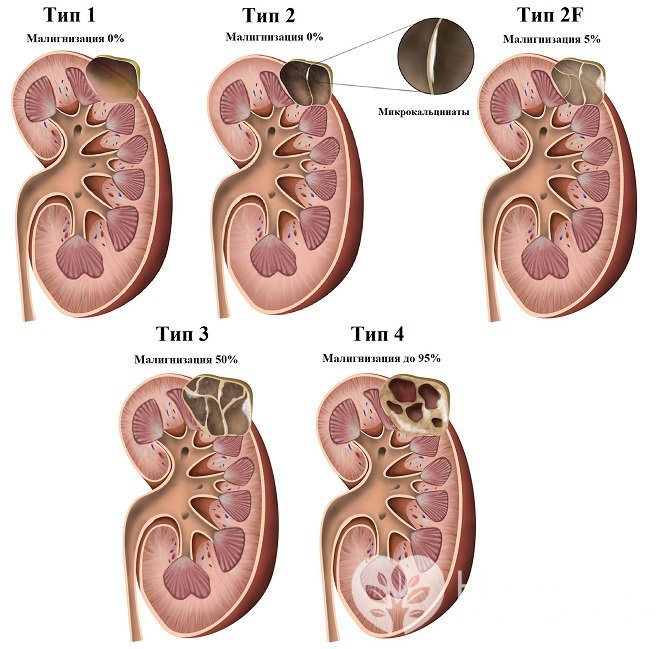
Однако, по мере роста новообразование обуславливает компрессионный эффект на сосуды и стимулирует такую структуру, как околоклубочковый комплекс, что приводит к повышению АД и его нестабильности. Пациент начинает жаловаться на головные боли и учащенное сердцебиение. Помимо этого, он страдает от болевой симптоматики, вызванной компрессионным эффектом и декомпенсацией почечной функции.
Кисты больших размеров провоцируют развитие следующих клинических проявлений:
- уменьшение объёма выделяемой урины;
- частые позывы к опорожнению МП;
- кровяная примесь в урине;
- болевая симптоматика, иррадиирущая в паховую область;
- интоксикация организма из-за задержки урины в нём;
- быстрая утомляемость и отёки.
Развитие почечной недостаточности проявляется запахом аммиака из ротовой полости больного (и характерно при поражении обеих почек) или в случае, если у него имеется лишь одна почка.
Диагностика кисты почки
Своевременное выявление новообразования серьёзно затруднено из-за отсутствия симптомов. Если его и диагностируют на ранних стадиях, то случайно, во время профилактических исследований или диагностики по другому поводу. Признаки, на которые обязан обратить внимание лечащий врач, заключаются в изменениях показателей урины и подъёме АД по неустановленным причинам. Диагностические исследования заключаются в следующем:
Если его и диагностируют на ранних стадиях, то случайно, во время профилактических исследований или диагностики по другому поводу. Признаки, на которые обязан обратить внимание лечащий врач, заключаются в изменениях показателей урины и подъёме АД по неустановленным причинам. Диагностические исследования заключаются в следующем:
- УЗ-сканирование, в том числе допплерография сосудов — позволяют визуализировать новообразование и определить, какое влияние оно оказывает на обеспечение кровью почек;
- Компьютерная томография — даёт возможность отличить кистозные формирования от новообразований злокачественной природы;
- Исследования функции почек — позволяют определить активность МВС, сбои в её работе и предусматривают проведение урографии и динамической сцинтиграфии;
- Лабораторные тесты — при больших формированиях выявляют уменьшение суточного объёма мочи, примесь в ней крови и белка.
Лечение кисты почки
Тактика лечения новообразований определяется лечащим врачом с учётом их размеров, клинических проявлений и индивидуальных показаний пациента. Солитарные или субкапсулярные кисты, диаметр которых не превышает 50-ти мм, не лечат. Пациенту нужно регулярно проходить профилактические осмотры для того, чтобы в случае прогрессирования заболевания и появления симптоматики своевременно начать лечение.
Солитарные или субкапсулярные кисты, диаметр которых не превышает 50-ти мм, не лечат. Пациенту нужно регулярно проходить профилактические осмотры для того, чтобы в случае прогрессирования заболевания и появления симптоматики своевременно начать лечение.
Мультилокулярные кисты склонны к малигнизации, поэтому их лечение просто необходимо. Удаление кисты почки может проводиться с применением разных методик.
| Методика удаления | Характерные особенности, показания |
| Пункционная аспирация | Однокамерные кисты диаметром до 60-ти мм удаляют путём введения иглы в их полость и аспирации содержимого. Такой подход позволяет минимизировать объём новообразования и добиться эффекта его склерозирования, но процент рецидивов в данном случае достаточно высок. |
| Лапароскопия кисты почки | Позволяет иссечь новообразование и провести его гистологию, а также сохраняет принцип малой инвазивности, поскольку проводится через минимальный разрез, не превышающий 5-ти мм. |
| Склеротерапия | Показана при однокамерных кистах диаметром не более 50-ти мм. Предусматривает пункцию в области поясницы, при которой введение иглы осуществляется под контролем КТ или УЗИ. Сначала удаляют содержимое кистозной полости, а потом вводят в неё склерозирующее средство. Таким образом существенно снижают количество рецидивов. |
| Хирургическая операция по удалению кисты почки | Радикальное иссечение проводится традиционным способом и предусматривает удаление опухоли и ушивание здоровой почечной ткани. Показаниями к применению являются крупные или многокамерные новообразования, их разрывы и тяжёлые нагноения. Может, также, проводиться с применением эндоскопического оборудования. |
| Нефрэктомия | Операция направлена на удаление поражённой почки в случае, если она серьёзно повреждена, а вторая почка функциональна и здорова. |
Киста почки — симптомы и лечение
Киста почки — довольно распространенное заболевание, а с широким введением в практику профилактического ультразвукового исследования число больных, у которых выявлена киста почки на ранних стадиях значительно выросло.
Это заболевание поражает почечную паренхиму чаще всего в возрасте 40-50 лет и старше, и представляет из себя шаровидную полость, заполненную жидкостью, являясь в большинстве случаев доброкачественной опухолью. Киста почки, как многие новообразования, выявленные на ранней стадии, успешно поддается лечению, без хирургического вмешательства. Появление кисты почки может происходить еще во внутриутробном периоде или стать следствием внешних факторов образа жизни человека. Так к причинам возникновения кисты почки можно отнести:
- Курение
- Алкоголь
- Инфекции
- Радиоактивное воздействие
- Травмы поясничной области
- Гормональные изменения
- Нарушенное кровообращение
Как проявляет себя киста почки
- Постоянная или периодическая боль в поясничной области заставляет человека обратиться к врачу.
 После проведения диагностических процедур у таких пациентов чаще всего выявляется киста почки.
После проведения диагностических процедур у таких пациентов чаще всего выявляется киста почки. - Артериальная гипертензия, то есть повышенное давление в полых органах или кровеносных сосудах, часто является предвестником появления кисты почки. Симптомами этого заболевания могут быть сильные головные боли в затылочной части головы, бессонница, сниженная работоспособность, нервозность и раздражительность, ухудшение зрения.
- Еще один признак, сопровождающий наличие кисты почки – кровь в моче, которая может быть видна как невооруженным взглядом, так и при проведении анализа крови, когда внешне цвет мочи не изменен, но выявляется повышенное содержание эритроцитов.
Диагностика кисты почек
Для постановки диагноза почечной кисты необходимо проведение таких анализов:
- Общий анализ крови (для определения кол-ва эритроцитов)
- Определение концентрацию глюкозы, креатина, мочевины и белка в крови
- Ультразвуковое исследование почек
- Компьютерная томография органов забрюшинного пространства с контрастированием
- Исследование функции почек
Не все исследования необходимы при первичном обнаружении кисты почек и на ранней стадии, но будут необходимы для исключения онкологии или при поступлении пациента в стационар для хирургического вмешательства: специалистам необходимо учесть и предусмотреть все риски до и после проведения операции.
Операции при почечной кисте
Необходимость хирургического вмешательства в клинике «Семейная» определяется специалистами высокого уровня. Чаще всего при кисте диаметром менее 5 см, не проявляющей себя клинически, то есть не вызывающей нарушений в кровообращении почки и оттока крови, не рекомендуют проведение операций. Такие кисты требуют наблюдения с применением УЗИ. Самым распространенным методом лечения в таких случаях считается пункция под контролем УЗИ. В стационаре клиники «Семейная» успешно проводят такие операции, но, к сожалению, не все виды почечных кист можно пунктировать, а кроме того после проведения этой операции остается вероятность рецидива заболевания.
Лапароскопические методы хирургии при кисте почек
В стационаре клиники «Семейная» операцию при кисте почек делают по высоким технологиям, успешно применяя лапароскопическую хирургию, гарантирующую успешное проведение операций при любых размерах и локализации новообразования. Это радикальная операция, предполагающая иссечение кисты с гистологическим исследованием, предполагает сохранение малоинвазивности, то есть на брюшной полости остается 3 размера по 5 мм. При проведении лапароскопической операции хирург видит на мониторе тонкие анатомические образования, что делает хирургическое вмешательство безопасным и деликатным. Кроме того, в клинике «Семейная» применяются современное хирургическое оборудование и методики, в том числе ультразвуковые хирургические ножницы, позволяющие проводить бескровные операции. Для профилактики рецидивов может применяться аргон-усиленная плазма (производства США), при близком расположении сосудов используются современные гемостатические средства передовых Европейских производителей. С целью профилактики спаечной болезни и тромбозов применяются синтетические рассасывающиеся шовные материалы, современные противоспаечные барьеры и также компрессионный трикотаж.
Это радикальная операция, предполагающая иссечение кисты с гистологическим исследованием, предполагает сохранение малоинвазивности, то есть на брюшной полости остается 3 размера по 5 мм. При проведении лапароскопической операции хирург видит на мониторе тонкие анатомические образования, что делает хирургическое вмешательство безопасным и деликатным. Кроме того, в клинике «Семейная» применяются современное хирургическое оборудование и методики, в том числе ультразвуковые хирургические ножницы, позволяющие проводить бескровные операции. Для профилактики рецидивов может применяться аргон-усиленная плазма (производства США), при близком расположении сосудов используются современные гемостатические средства передовых Европейских производителей. С целью профилактики спаечной болезни и тромбозов применяются синтетические рассасывающиеся шовные материалы, современные противоспаечные барьеры и также компрессионный трикотаж.
После проведения лапараскопических операций на почке пациенты в первый же день могут самостоятельно вставать с постели и пить, на второй день принимать пищу, а на 3-й день пациента могут выписать из стационара. К работе можно приступать через 10-14 дней. В дальнейшем необходимо регулярное наблюдение уролога и проведение УЗИ и КТ по назначению лечащего врача.
К работе можно приступать через 10-14 дней. В дальнейшем необходимо регулярное наблюдение уролога и проведение УЗИ и КТ по назначению лечащего врача.
Консультация хирурга-уролога при кисте почек
В клинике «Семейная» в Рязани по вопросам кисты почек прием ведут хирурги-урологи с большим опытом работы, которые помогут разобраться с каждым конкретным случаем. При назначении лечения важно знать все сопутствующие заболевания и состояние кисты почек в данный момент. Многим пациентам требуется правильно подобранное нехирургическое лечение, а кому-то срочно нужна операция. Решение о хирургическом вмешательстве принимается на консилиуме, включающем врачей всех смежных специализаций. Для детального изучения Вашего случая запишитесь на консультацию по тел. 8 (4912) 50-60-20. По вопросам возможности бесплатного хирургического лечения в рамках Программы оказания высоко-технологической помощи запишитесь на консультацию к главному врачу Кондрашову Владимиру Ивановичу.
MEDISON.RU — Диагностика и лечение жидкостных образований почек
Введение
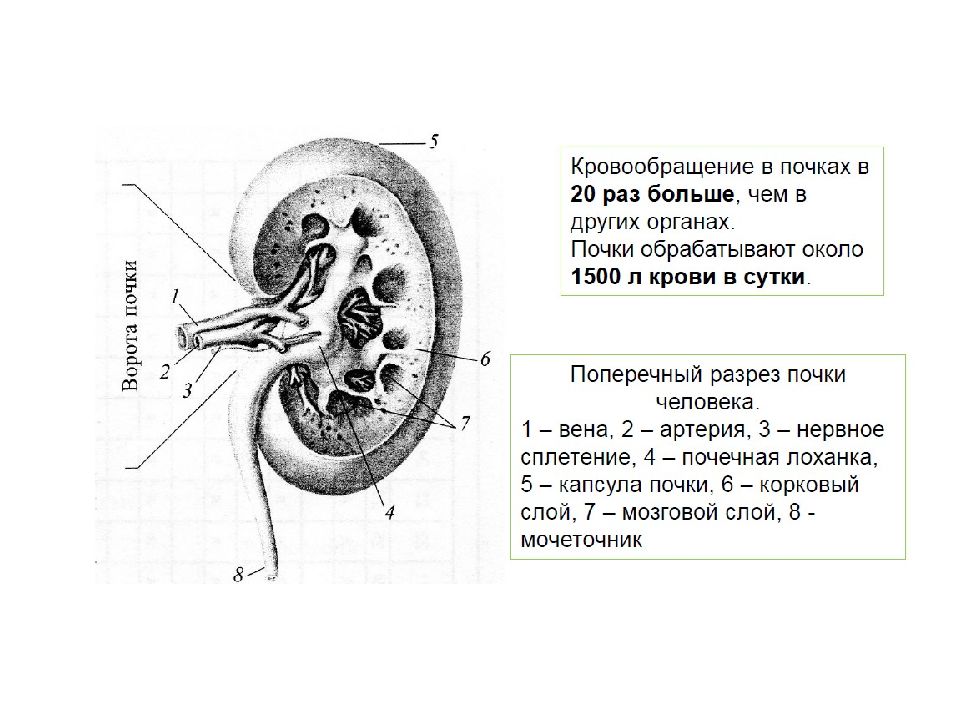
С внедрением в урологию и нефрологию ультразвукового метода исследования, значительно чаще стали выявлять жидкостные образования почек [1, 2, 5, 14, 16]. Использование компьютерной томографии (КТ) и магнитно-резонансной томографии (МРТ) позволило почти у 50 % пациентов диагностировать кисты почек. В настоящее время описаны характерные ультразвуковые и томографические признаки солитарной кисты почек — жидкостное образование с четкими, ровными контурами, анэхогенным содержимым, эффектом дистального усиления (рис. 1). Наличие в кистах плотных перегородок, накапливающих контрастные препараты, неровность стенок являются признаками злокачественной опухоли почки.
Рис. 1. Солитарная киста нижнего сегмента почки.
1. Солитарная киста нижнего сегмента почки.
Основным методом диагностики жидкостных образований почек на сегодняшний день является УЗИ. Большинство жидкостных образований почек представлены солитарными кистами, требующими активных методов лечения лишь при размерах более 5 см, нарушении уро- или гемодинамики органа. Другая большая группа жидкостных образований почек представлена множественными кистами почечного синуса и парапельвикальными кистами. Больные данными заболеваниями нуждаются только в динамическом УЗ наблюдении. В некоторых случаях дифференциальная диагностика кист почечного синуса с расширенной чашечно-лоханочной системой имеет определенные трудности [1, 4, 5] (рис. 2). Весьма информативным и надежным методом дифференциальной диагностики при данных состояниях является фармакоультразвуковое исследование с введением диуретиков. При этом кисты не изменяют своей формы и размеров на фоне расширения чашечно-лоханочной системы. С целью определения состояния кровотока почек применяется эходопплерография сосудов почек.
С целью определения состояния кровотока почек применяется эходопплерография сосудов почек.
Рис. 2. Киста почечного синуса.
Значительно больше сложностей возникает в обследовании пациентов с жидкостными образованиями, имеющими нетипичную УЗ картину, при подозрении на рак в кисте. Злокачественный процесс в кисте по данным различных авторов, составляет от 0,1 до 10 %. При обследовании данной группы пациентов необходимо прибегать к КТ или МРТ почек.
Лечение простых кист почек чаще всего сводится к их пункции с эвакуацией содержимого и склерозированием стенок [3, 8, 9, 11]. Открытые оперативные методы в настоящее время используются лишь при осложненных и злокачественных кистах. В последние годы активно разрабатываются и внедряются лапароскопические (ретроперитонеоскопические) методы лечения кист почек [12].
Материал и методы
В урологической клинике ММА им. И.М. Сеченова в течение 2001-2003 гг. обследовано 122 пациентов с жидкостными образованиями почек. У 56 — выявлены множественные кисты почечного синуса. Всем пациентам выполнено УЗИ органов мочевой системы. Больным с кистами почечного синуса и парапельвикальными кистами с целью дифференциальной диагностики с расширенной чашечно-лоханочной системой проводилось фармакоультразвуковое исследование почек (проба с лазиксом) [1]; 60 пациентам выполнена экскреторная урография.
В 75 наблюдениях применена спиральная компьютерная томография (СКТ) почек с контрастированием и последующей трехмерной реконструкцией полученных изображений.
Показаниями к выполнению компьютерной томографии явились подозрения на рак почки (14), дифференциальная диагностика расширенной чашечно-лоханочной системы, жидкостных образований забрюшинного пространства уриномы, кисты надпочечников (6), пороков развития почек и мочевых путей (15). У 12 пациентов кисты почек случайно выявлены при компьютерной томографии по поводу других заболеваний мочеполовой системы.
У 12 пациентов кисты почек случайно выявлены при компьютерной томографии по поводу других заболеваний мочеполовой системы.
20 пациентам выполнена магнитно-резонансная томография, из них — 6 в связи с подозрением на рак почки, 5 по причине непереносимости рентгеноконтрастных препаратов, в 3 наблюдениях — у беременных. У 6 больных использована модификация магнитно-резонансной томографии — магнитно-резонансная урография, что позволило с высокой степенью достоверности дифференцировать расширенную чашечно-лоханочную систему и кисты почек [14, 17, 18, 21].
Всем пациентам проведено эходопплерографическое исследование почек. Отмечено, что выраженные нарушения гемодинамики почки могут наблюдаться и при отсутствии клинической симптоматики и являются показаниями к оперативному лечению [13, 19].
Обсуждение результатов
УЗИ, являясь первым диагностическим методом обследования урологических больных, практически во всех наблюдениях позволяет получить существенную информацию о состоянии почек и мочевых путей, выявить жидкостное образование почки, определить его характеристики.
Экскреторные урограммы в основном были выполнены амбулаторно до консультации в клинике. В 28 (46,7 %) наблюдениях выявлены изменения: оттеснение чашечек, удлинение их шеек, девиация верхней трети мочеточника, расширение и деформация лоханки. В 32 (53,3 %) наблюдениях на экскреторных урограммах никаких изменений отмечено не было.
Применение компьютерной томографии позволяет получить полную информацию о состоянии паренхимы почки, верхних мочевых путей, расположении, форме кист, соотношении их с чашечно-лоханочной системой почки и магистральными сосудами. Вместе с тем результаты сравнительного анализа показали, что нативная фаза компьютерной томографии в обследовании кист почечного синуса практически не имеет преимуществ перед ультразвуковым исследованием, так как без контрастирования достаточно трудно отличить скопления жидкостных элементов без четких границ в проекции почечного синуса от чашечно-лоханочной системы. В связи с этим мы рекомендуем выполнение компьютерной томографии с контрастным усилением. Необходимо также отметить, что компьютерная томография не всегда позволяет выявить перегородки в полости кисты, определяемые при УЗИ. В нашем исследовании было 2 подобных наблюдения.
Необходимо также отметить, что компьютерная томография не всегда позволяет выявить перегородки в полости кисты, определяемые при УЗИ. В нашем исследовании было 2 подобных наблюдения.
Магнитно-резонансная томография может быть использована при неэффективности или противопоказаниях к выполнению рентгеноконтрастных исследований. На магнитно-резонансных томограммах без контрастирования можно получить послойное изображение почки, элементов чашечно-лоханочной системы, структур почечного синуса. Метод не связан с лучевой нагрузкой, что является его важным преимуществом для определенной категории больных. Магнитно-резонансная томография с контрастированием позволяет выявить участки повышенного накопления парамагнитных препаратов (магнивист, омнискан) в стенках и перегородках жидкостных образований, что является признаком повышенной, патологической васкуляризации — злокачественного процесса (рис. 3).
Рис.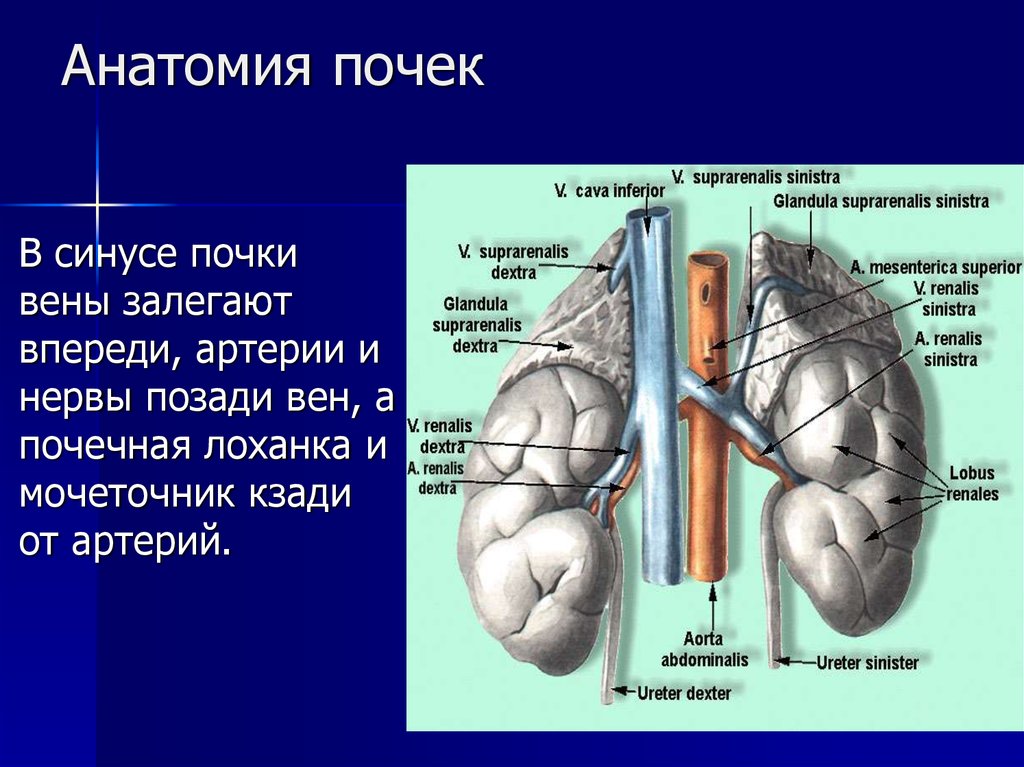 3. Жидкостное образование левой почки, интенсивно накапливающее парамагнитный препарат, предположительно опухоль.
3. Жидкостное образование левой почки, интенсивно накапливающее парамагнитный препарат, предположительно опухоль.
Магнитно-резонансная урография — ценный метод дифференциальной диагностики кист и расширенной чашечно-лоханочной системы, в определенных случаях может рассматриваться как альтернатива экскреторной урографии (рис. 4).
Рис. 4. Стеноз лоханочно-мочеточникового сегмента справа, гидронефроз.
В 5 наблюдениях компьютерная томография не позволила однозначно опровергнуть или подтвердить наличие рака в кисте, в 2 — вообще не были выявлены перегородки в полости кисты, видимые при УЗИ. Из них в 4 случаях магнитно-резонансная томография с контрастированием позволила выявить признаки повышенного накопления парамагнитного препарата в стенках и перегородках кисты, признаки патологического кровотока в стенках кисты, оценены магнетические свойства жидкости, заполняющей полость кисты, что позволило уточнить характер образования в почке и определить дальнейшую тактику лечения.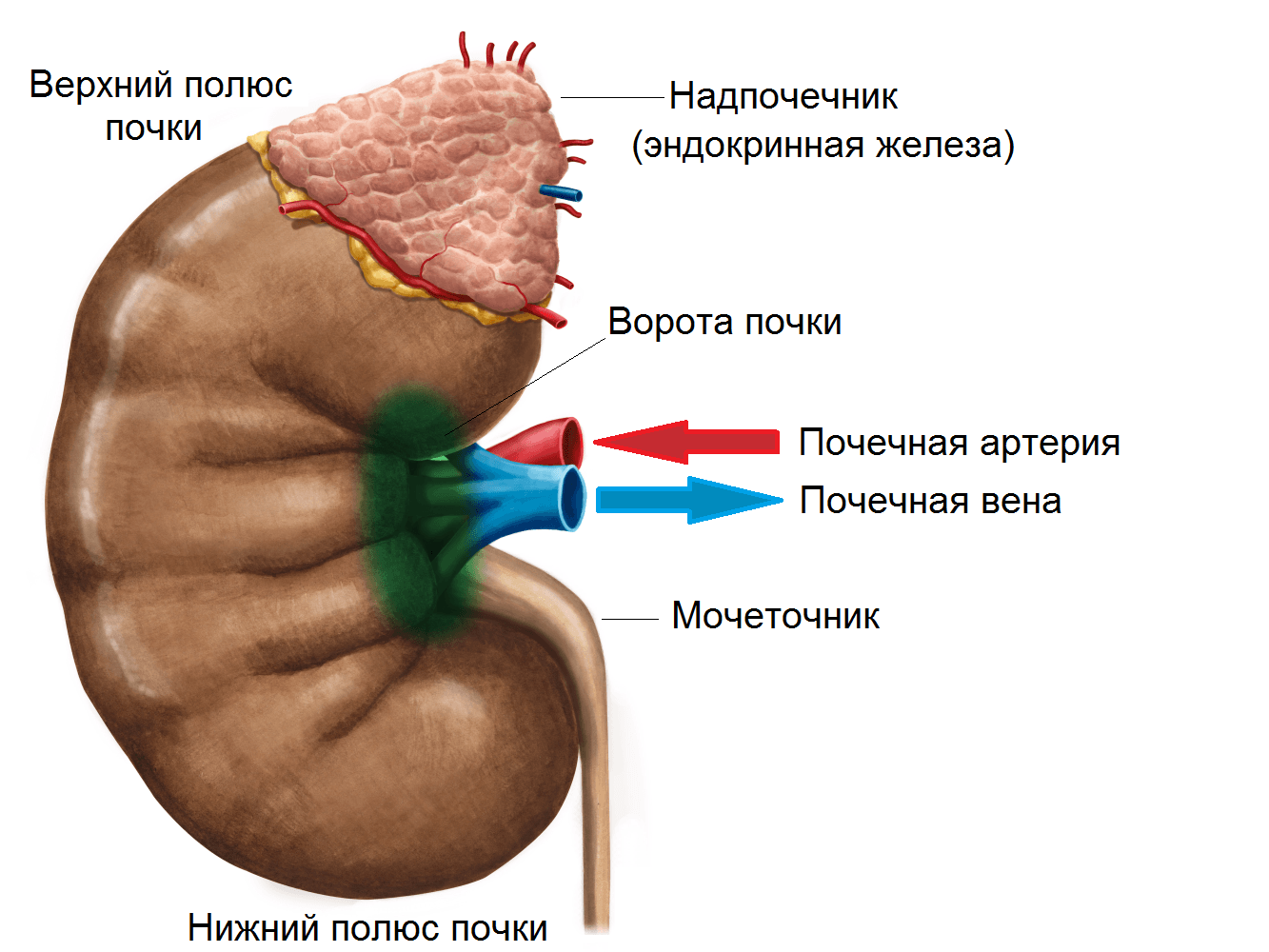
52 пациентам с клинической симптома тикой, нарушениями гемо- и уродинамики почки выполнена пункция кисты под УЗ контролем с последующим склерозированием стенок. Пациенты в удовлетворительном состоянии выписаны домой через 1-2 дня. Рецидив кист отмечен у 8 (15,4 %) в течение 6 месяцев после операции, из них у 5 обнаружены кисты менее 3 см бессимптомного течения и не требовавшие повторной пункции, в 3 наблюдениях манипуляция повторена. В одном случае возникло нагноение кисты, потребовавшее экстренной операции — резекции купола кисты, дренирования забрюшинного пространства. Послеоперационный период протекал гладко, без осложнений, пациент выписан на 10-е сутки.
В 15 (12,3 %) наблюдениях при УЗИ высказано предположение о наличии злокачественного процесса; 13 (86,7 %, n=15) пациентам этой группы выполнена спиральная компьютерная томография почек с контрастированием (рис. 5). В 6 (40 %, n=15) наблюдениях полученная при компьютерной томографии информация оказалась недостаточной, в связи с чем применена магнитно-резонанстная томография. На основании результатов комплексного обследования, с использованием УЗИ, СКТ, у 9 пациентов убедительных данных на наличие опухоли почки выявлено не было. Данная группа находится под динамическим наблюдением, УЗИ проводится каждые 6 месяцев, компьютерная томография — ежегодно.
На основании результатов комплексного обследования, с использованием УЗИ, СКТ, у 9 пациентов убедительных данных на наличие опухоли почки выявлено не было. Данная группа находится под динамическим наблюдением, УЗИ проводится каждые 6 месяцев, компьютерная томография — ежегодно.
Рис. 5. Образование жидкостной плотности в среднем сегменте почки с неровными конурами и перегородками, подозрение на опухоль.
В 2 (1,64 %) наблюдениях при УЗИ и компьютерной томографии в почках обнаружено множество жидкостных образований различного размера, с плотными перегородками, интенсивно накапливающими контрастные препараты, в связи с чем заподозрена кистозная форма почечноклеточного рака.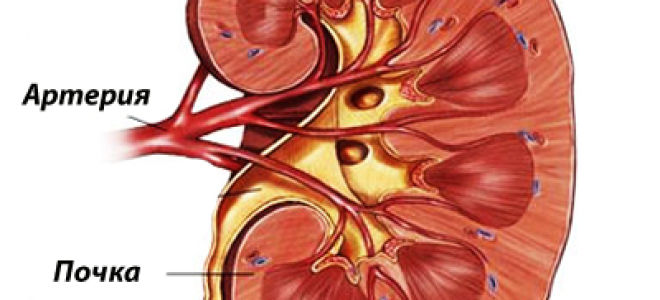 В 4 (3,28 %) наблюдениях выявлены кисты с перегородками, неровными стенками, накапливающими контрастные препараты — картина, подозрительная на рак в кисте. В одном наблюдении при УЗИ выявлено образование почки жидкостной плотности, с плотными стенками — заподозрена саркома почки. При СКТ образование интенсивно накапливало рентгеноконтрастный препарат. При последующей операции и гистологическом исследовании выявлена ангиолейомиолипома (0,82 %).
В 4 (3,28 %) наблюдениях выявлены кисты с перегородками, неровными стенками, накапливающими контрастные препараты — картина, подозрительная на рак в кисте. В одном наблюдении при УЗИ выявлено образование почки жидкостной плотности, с плотными стенками — заподозрена саркома почки. При СКТ образование интенсивно накапливало рентгеноконтрастный препарат. При последующей операции и гистологическом исследовании выявлена ангиолейомиолипома (0,82 %).
Из 15 пациентов 6 оперированы: 4 нефрэктомии, 1 резекция почки, 1 энуклеорезекция почки. При гистологическом исследовании полученного материала в 3 (2,46 %) наблюдениях выявлен рак в кисте, 1 (0,82 %) — кистозная форма рака почки. В одном при гистологическом исследовании картина соответствовала мультилокулярной кисте почки (0,82 %), в одном наблюдении выявлена ангиолейомиолипома (0,82 %). В 1 наблюдении наличие рака почки не вызывало сомнений, однако ввиду тяжелого интеркур рентного фона от выполнения операции было решено воздержаться, пациент направлен в онкологическое учреждение для симптоматического лечения.
Заключение
Проведенное исследование свидетельствует о том, что проблема жидкостных образований почек весьма актуальна, и, несмотря на существующий арсенал современных методов обследования, диагностика этих заболеваний в ряде случаев весьма затруднительна.
УЗИ является основным методом первичного обследования пациентов с жидкостными образованиями почек. В ситуациях, требующих уточнения полученной информации, целесообразно прибегать к СКТ и МРТ почек.
Ввиду низкой информативности экскреторной урографии мы не рекомендуем ее в обследовании больных кистами почек. Магнитно-резонансная томография с контрастированием является методом более информативным, чем УЗИ и КТ, особенно при выявлении признаков злокачественного роста.
Частота выявления рака в кисте, по нашим данным, составила 3,28 %. Признаки возможного злокачественного процесса в кисте при УЗИ являются показанием к уточняющей диагностике и нефрэктомии или резекции почки.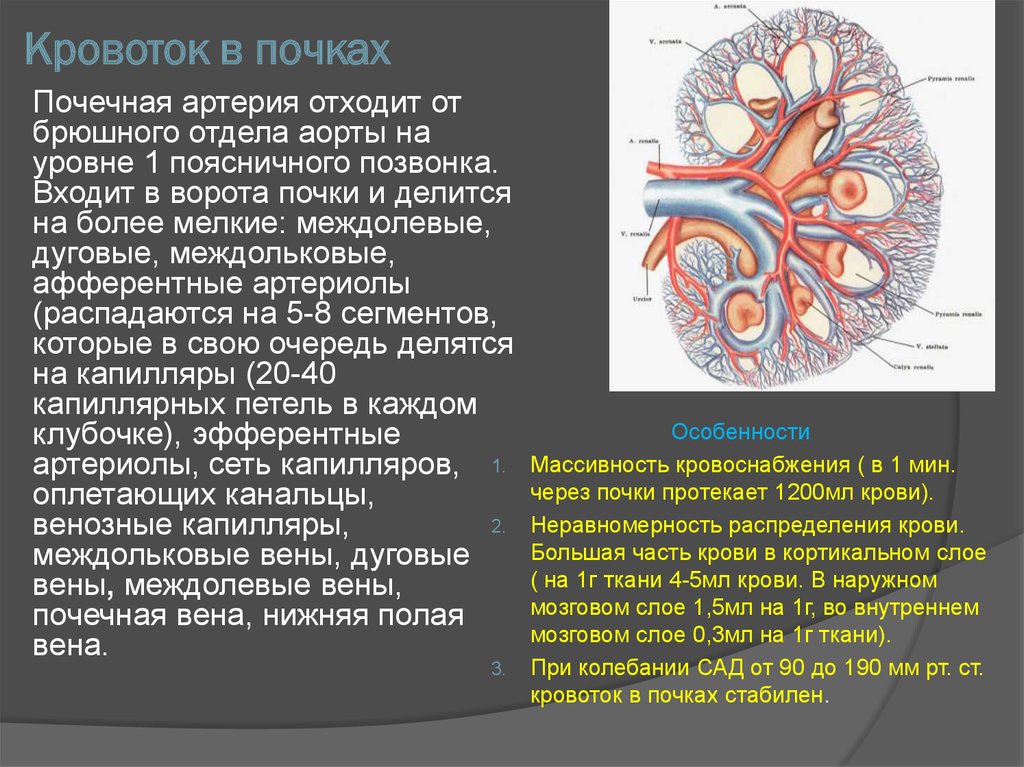
Большинство пациентов кистами почек не требуют лечения и могут длительно наблюдаться. Опыт нашей клиники и данные литературы показывают, что пункционный метод лечения остается основным и ведущим в лечении этой категории пациентов.
Литература
- Аляев Ю.Г, Амосов А.В., Газимиев М.А. Ультразвуковые методы функциональной диагностики в урологической практике. Москва: Изд. Р. Валент. 2001. С 192.
- Айвазян А.В., Войно-Ясенецкий A.M. Пороки развития почки и мочеточников/ М.: Наука. 1988.
- Ахметов Н.Р. Хирургическое лечение солитарных кист почек/Дис. …к.м.н. Уфа, 2000.
- Буйлов В.М., Турзин В.В. Соно- и урографическая диагностика кист почечных синусов. / Тезисы докладов 1-го съезда Ассоциации специалистов ультразвуковой диагностики в медицине. М. 1991, 121 с.
- Демидов В.Н., Амосов А.
 В. Ультразвуковая диагностика кист почек. /Клиническая медицина. 1981. N7. С. 68-70.
В. Ультразвуковая диагностика кист почек. /Клиническая медицина. 1981. N7. С. 68-70. - Аопаткин Н.А., Мазо Е.Б. Простая киста почек. М.: Медицина. 1982. 140 с.
- Аопаткин Н.А., Аюлько А.В. Аномалии мочеполовой системы. Киев: Здоровья. 1987. 416 с.
- Сафиуллина З.Х. Пункционные методы лечения паразитарных кист почек и печени под контролем ультразвуковой томографии. /Автореферат дис. …к.м.н., Уфа. 1996. 26 с.
- Brunken С, Pfeiffer D, TauberR. [Long term outcome after percutaneous sclerotherapy of renal cysts with polidocanol]. Urologe A 2002 May; 41(3): 263-6.
- Chung BH, Kim JH, Hong CH. Comparison of single and multiple sessions of percutaneous sclerotherapy for simple renal cyst. BJU Int 2000 Apr; 85(6): 626-7.
- Delakas D, Karyotis I, Loumbakis P. Long-term results after percutaneous minimally invasive procedure treatment of symptomatic simple renal cysts.
 /Int Urol Nephrol 2001; 32(3): 321-6.
/Int Urol Nephrol 2001; 32(3): 321-6. - Denis E, Nicolas F, Ben Rais N, Cloix P, Dawahra M, Marechal JM, Gelet A. [Laparoscopic surgical treatment of simple cysts of the kidney] Prog Urol 1998 Apr; 8(2): 195-200.
- Hashimoto Y, Kimura G, Tsuboi N. [Usefulness of power Doppler ultrasound in a patient with renal cell carcinoma in the wall of a simple renal cyst]. Hinyokika Kiyo 2001 May; 47(5): 325-7.
- Holmberg G. Diagnostic aspects, functional significance and therapy of simple renal cysts. Umea 1992.
- Stuart W. Evaluation and management of solid and cystic renal masses. The journal of urology 1998; 159: 1120-1133.
- Michele Scialpil, Arcangelo Di Maggio. Small Renal Masses./AJR 2000; 175: 751-757
- Nascimento AB, Mitchell DG, Zhang XM. Rapid MR imaging detection of renal cysts: age-based standards./Radiology 2001 Dec; 221(3):628-32.
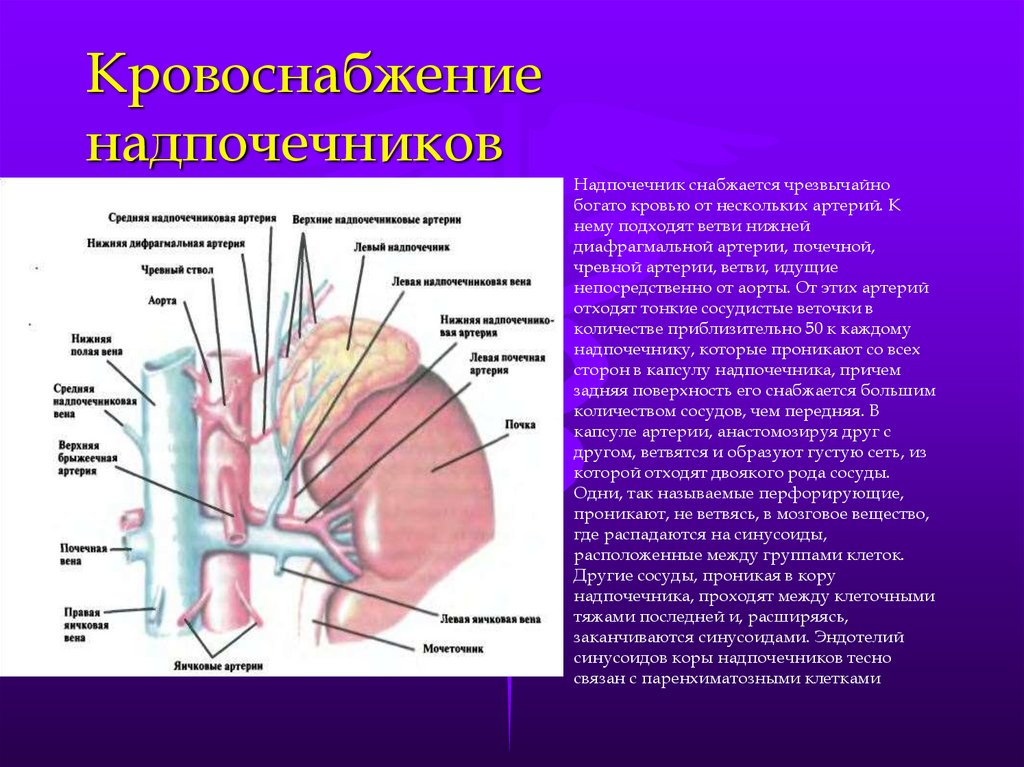
- Richard Tellol,2, Brian D. Davison MR. Imaging of Renal Masses Interpreted on CT to Be Suspicious. /AJR 2000; 174: 1017-1022.
- R de Bruyn, I Gordon / Imaging in cystic renal disease. /Arch Dis Child 2000; 83: 401-407
- Tread N, Ichioka K, Matsuta Y. The natural history of simple renal cysts, /J Urol 2002 Jan; 167(1): 21-3.
- Vincent B. Ho, MD, Scott F. Renal Masses: Quantitative Assessment of Enhancement with Dynamic MR Imaging. /Radiology 2002; 224: 695-700.
УЗИ сканер RS80
Эталон новых стандартов! Беспрецедентная четкость, разрешение, сверхбыстрая обработка данных, а также исчерпывающий набор современных ультразвуковых технологий для решения самых сложных задач диагностики.
Ультразвуковая диагностика пиелонефрита и рака почек
Пиелонефрит и рак почек – это патологии мочевыделительной системы, которые можно диагностировать при помощи ультразвукового метода исследования на ранних этапах развития.
Пиелонефрит и рак почек – это патологии мочевыделительной системы, которые можно диагностировать при помощи ультразвукового метода исследования на ранних этапах развития.
Пиелонефрит
Пиелонефрит – воспаление почек с вовлечением в воспалительный процесс почечной паренхимы, чашечек и лоханки. Возбудителями чаще всего становятся бактерии – кишечная палочка, энтерококки, протей, стафилококки и синегнойная палочка. Микробы могут проникать в почки восходящим путем из нижних отделов мочеполового тракта, а также попадать в них с кровью из отдаленных инфекционных очагов (например, из кариозных очагов, воспаленных миндалин).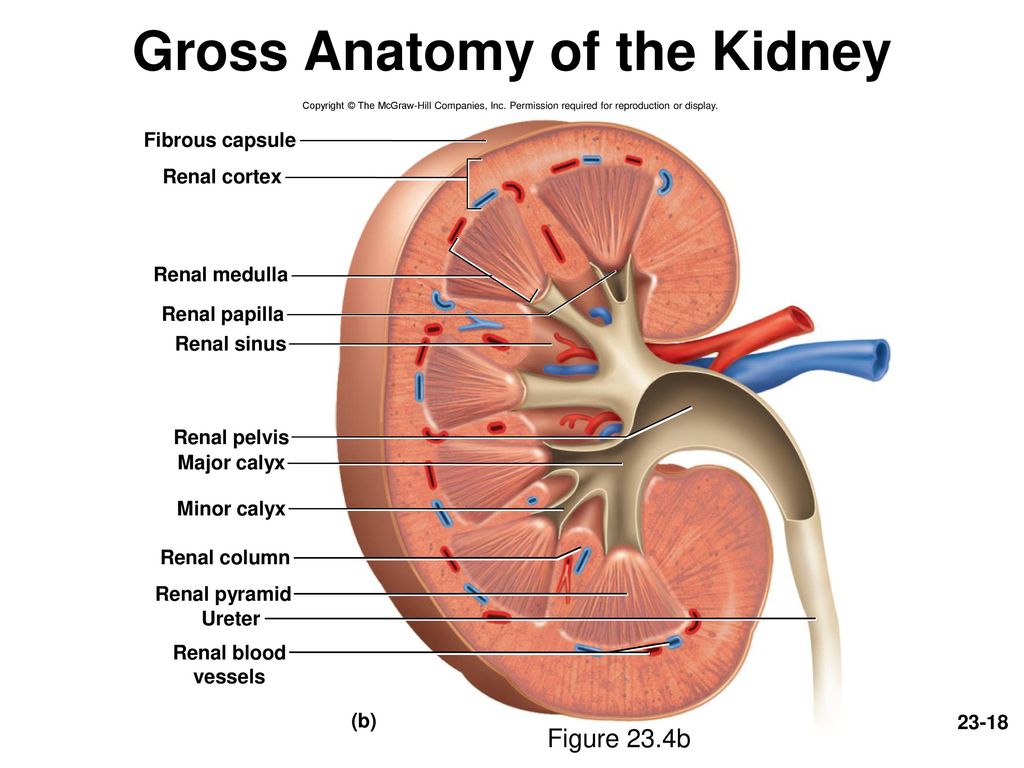
По течению различают две основные формы пиелонефрита – острую и хроническую. Для острого воспаления характерны признаки общей интоксикации и местные симптомы:
- слабость;
- головная боль;
- снижение работоспособности;
- повышение температуры;
- боль в пояснице обычно ноющего характера;
- учащение мочеиспускания;
- необычный цвет мочи, появление неприятного запаха.
Хронический пиелонефрит во время обострения проявляется практически теми же симптомами, что и острый пиелонефрит. Со временем присоединяются признаки хронической недостаточности почек – анемия, отечность, хроническая интоксикация, повышение артериального давления.
Рак почки
Заболеваемость раком почки за последнее время возросла. Часто эту патологию обнаруживают случайно при ультразвуковом или рентгенологическом исследовании по поводу другого заболевания. Рак почек может какое-то время протекать бессимптомно, а его начальные признаки порой напоминают пиело- или гломерулонефрит. К ним относятся:
К ним относятся:
- боли в пояснице;
- появление крови в моче;
- артериальная гипертензия;
- слабость;
- снижение веса;
- отеки;
- симптомы анемии;
- длительное незначительное повышение температуры без видимых причин;
- симптомы со стороны других органов вследствие метастазирования – переломы костей, кровохаркание, кашель, признаки сдавления спинного мозга и др.
УЗИ при пиелонефрите
УЗИ почек и надпочечников – один из основных методов диагностики пиелонефрита, который позволяет оценить структурные изменения почечной ткани.
Подготовка
Перед проведением процедуры примерно за 3 дня рекомендуется придерживаться диеты, направленной на снижение газообразования в кишечнике. Для этого исключают из пищи бобы, фасоль, горох и другие бобовые, зерновые крупы, черный и отрубной хлеб, фрукты и свежее молоко. При метеоризме на это время назначают препараты, снижающие газообразование (эспумизан, активированный уголь и др. ). В некоторых случаях требуется наполненный мочевой пузырь, с целью чего пациент должен выпить за час до исследования 1 литр жидкости. Обычно об этом специалист предупреждает заранее.
). В некоторых случаях требуется наполненный мочевой пузырь, с целью чего пациент должен выпить за час до исследования 1 литр жидкости. Обычно об этом специалист предупреждает заранее.
УЗ-признаки острого пиелонефрита:
- почки увеличены в размерах;
- подвижность почек ограничена во время дыхания;
- расширена чашечно-лоханочная система;
- наблюдается везикуло-уретральный рефлюкс (обратный ток мочи из мочевого пузыря в мочеточники).
Ультразвуковые признаки хронического пиелонефрита:
- размеры почек уменьшены;
- контур имеет неровности и деформации;
- неравномерность эхосигнала в области лоханок;
- истончение и повышенная эхогенность паренхиматозного слоя почек.
Ультразвуковая диагностика рака почек
УЗИ почек и надпочечников не только помогает диагностировать различные заболевания этих органов, но и дифференцировать их между собой. Как сказано выше, симптомы рака почки часто схожи с признаками пиелонефрита. Ультразвуковое исследование позволяет разграничить эти патологии без инвазивных вмешательств. Существует несколько форм почечного рака, ультразвуковые признаки которых отличаются.
Солидный рак
УЗ-признаком солидной формы рака является обнаружение в области почки однородного гипо- или изоэхогенного образования. Солидная опухоль обычно растет «наружу». Определяется неровный внешний контур, нередко имеются участки кальцификации (отложение солей кальция). С помощью допплеровского картирования (разновидность УЗИ) можно определить кровоток опухоли, который усилен в центре и ослаблен по периферии образования.
Инфильтративный рак
Инфильтрирующая опухоль прорастает внутрь почечных синусов. Она имеет однородную структуру и сниженную эхогенность. По мере роста приобретает неоднородную структуру вследствие появления очагов кровоизлияний. Чашечно-лоханочная система может быть расширенной. Вследствие инфильтративного роста такая форма рака почек раньше дает симптомы, поэтому диагностируется на более ранних стадиях, чем солидные опухоли.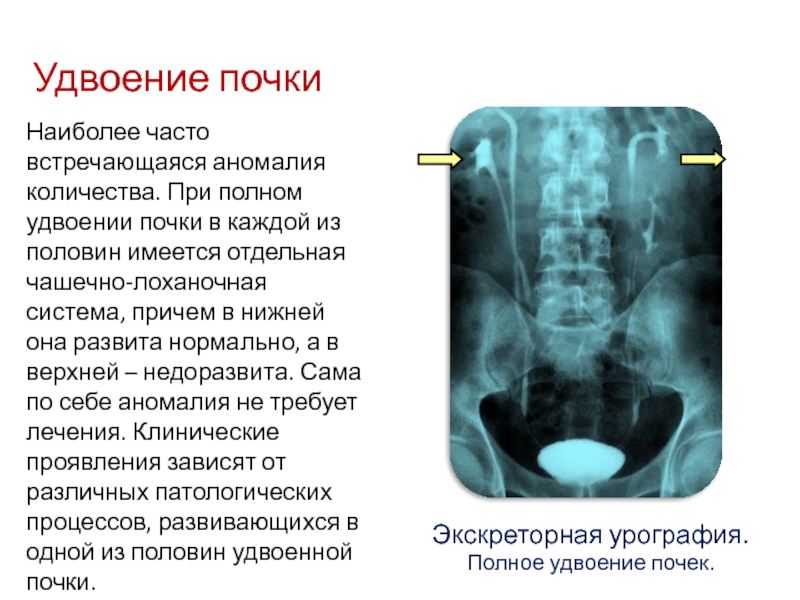
Мультикистозный рак
В почке обнаруживается анэхогенное (т.е. темное на картинке) образование, которое часто имеет внутренние перегородки. Может быть принято за многокамерную кисту.
Рак стенки кисты
На ранней стадии в почках при УЗИ обнаруживают кисту с плотными стенками. По мере роста раковой опухоли на стенке кисты начинает определяться гипоэхогенное образование, состоящее из нескольких кистозных полостей, заполненных гипоэхогенным содержимым (некротические массы). Необходима дифференциальная диагностика с гематомой надпочечников, полученной в результате травмы.
Карцинома лоханки
На ранней стадии в чашечно-лоханочной системе определяется образование с однородной структурой и сниженной эхогенностью. Постепенно структура теряет однородность, опухоль прорастает в ткани мочевого пузыря и уретры.
СТАДИИ РАКА ПОЧКИ
Дифференциальная диагностика пиелонефрита и рака почки
В отличие от пиелонефрита, рак почек чаще бывает односторонним. В большинстве случаев при УЗ-исследовании определяется отдельное образование, а при пиелонефрите изменения бывают более диффузные. Для уточнения диагноза используют дополнительные лабораторно-инструментальные методы диагностики. Рак почки – очень серьезное заболевание, которое можно вылечить на ранних стадиях. Пиелонефрит имеет более благоприятный прогноз, но при несвоевременном лечении может приводить к развитию хронической почечной недостаточности и другим осложнениям (гидронефроз, сепсис и т. др.).
В большинстве случаев при УЗ-исследовании определяется отдельное образование, а при пиелонефрите изменения бывают более диффузные. Для уточнения диагноза используют дополнительные лабораторно-инструментальные методы диагностики. Рак почки – очень серьезное заболевание, которое можно вылечить на ранних стадиях. Пиелонефрит имеет более благоприятный прогноз, но при несвоевременном лечении может приводить к развитию хронической почечной недостаточности и другим осложнениям (гидронефроз, сепсис и т. др.).
Поэтому при любых симптомах патологии почек необходимо как можно скорее пройти обследование, в частности,УЗ-исследование почек и надпочечников.
ОЖИРЕНИЕ И ЗАБОЛЕВАНИЯ ПОЧЕК: СКРЫТЫЕ ПОСЛЕДСТВИЯ ЭПИДЕМИИ | Ковесди
1. Forouzanfar MH, Alexander L, Anderson HR et al. Global, regional, and national comparative risk assessment of 79 behavioral, environmental and occupational, and metabolic risks or clusters of risks in 188 countries, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet 2015; 386:2287-2323
Lancet 2015; 386:2287-2323
2. Flegal KM, Kruszon-Moran D, Carroll MD et al. Trends in Obesity Among Adults in the United States, 2005 to 2014. JAMA 2016;315:2284-2291
3. Cattaneo A, Monasta L, Stamatakis E et al. Overweight and obesity in infants and pre-school children in the European Union: a review of existing data. Obes Rev 2010; 11:389-398
4. Olaya B, Moneta MV, Pez O et al. Country-level and individual correlates of overweight and obesity among primary school children: a cross-sectional study in seven European countries. BMC Public Health 2015; 15:475
5. Subramanian SV, Perkins JM, Ozaltin E, Davey SG: Weight of nations: a socioeconomic analysis of women in low- to middleincome countries. Am J Clin Nutr 2011; 93:413-421
Am J Clin Nutr 2011; 93:413-421
6. Tsujimoto T, Sairenchi T, Iso H et al. The dose-response relationship between body mass index and the risk of incident stage >/=3 chronic kidney disease in a general japanese population: the Ibaraki prefectural health study (IPHS). J Epidemiol 2014; 24:444-451
7. Elsayed EF, Sarnak MJ, Tighiouart H et al. Waist-to-hip ratio, body mass index, and subsequent kidney disease and death. Am J Kidney Dis 2008; 52:29-38
8. Pinto-Sietsma SJ, Navis G, Janssen WM et al. A central body fat distribution is related to renal function impairment, even in lean subjects. Am J Kidney Dis 2003; 41:733-741
9. Foster MC, Hwang SJ, Larson MG et al. Overweight, obesity, and the development of stage 3 CKD: the Framingham Heart Study. Am J Kidney Dis 2008; 52:39-48
Overweight, obesity, and the development of stage 3 CKD: the Framingham Heart Study. Am J Kidney Dis 2008; 52:39-48
10. Kramer H, Luke A, Bidani A et al. Obesity and prevalent and incident CKD: the Hypertension Detection and Follow-Up Program. Am J Kidney Dis 2005; 46:587-594
11. Chang A, Van HL, Jacobs DR et al. Lifestyle-related factors, obesity, and incident microalbuminuria: the CARDIA (Coronary Artery Risk Development in Young Adults) study. Am J Kidney Dis 2013; 62:267-275
12. Ejerblad E, Fored CM, Lindblad P et al. Obesity and risk for chronic renal failure. J Am Soc Nephrol 2006; 17:1695-1702
13. Gelber RP, Kurth T, Kausz AT et al. Association between body mass index and CKD in apparently healthy men. Am J Kidney Dis 2005; 46:871-880
Association between body mass index and CKD in apparently healthy men. Am J Kidney Dis 2005; 46:871-880
14. Lu JL, Molnar MZ, Naseer A et al. Association of age and BMI with kidney function and mortality: a cohort study. Lancet Diabetes Endocrinol 2015;3:704-714
15. Munkhaugen J, Lydersen S, Wideroe TE, Hallan S: Prehypertension, obesity, and risk of kidney disease: 20-year follow-up of the HUNT I study in Norway. Am J Kidney Dis 2009; 54:638-646
16. Iseki K, Ikemiya Y, Kinjo K et al. Body mass index and the risk of development of end-stage renal disease in a screened cohort. Kidney Int 2004; 65:1870-1876
17. Vivante A, Golan E, Tzur D et al.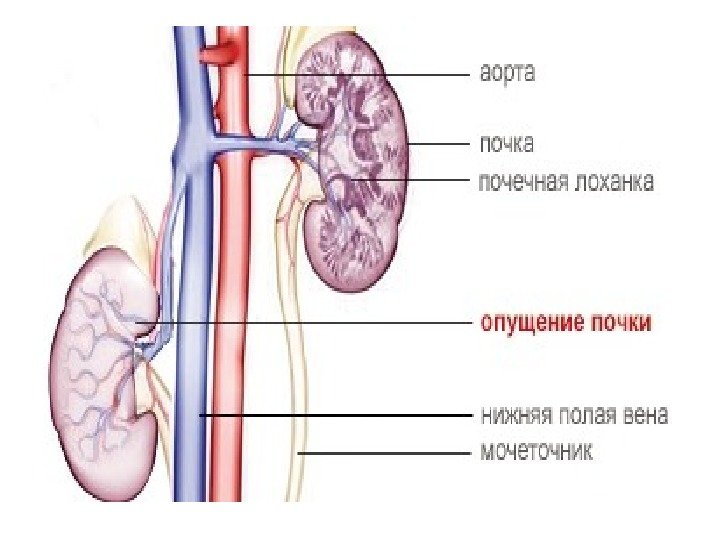 Body mass index in 1.2 million adolescents and risk for end-stage renal disease. Arch Intern Med 2012; 172:1644-1650
Body mass index in 1.2 million adolescents and risk for end-stage renal disease. Arch Intern Med 2012; 172:1644-1650
18. Hsu C, McCulloch C, Iribarren C et al. Body mass index and risk for end-stage renal disease. Ann Intern Med 2006; 144:21-28
19. Lu JL, Kalantar-Zadeh K, Ma JZ et al. Association of body mass index with outcomes in patients with CKD. J Am Soc Nephrol 2014; 25:2088-2096
20. Thoenes M, Reil JC, Khan BV et al. Abdominal obesity is associated with microalbuminuria and an elevated cardiovascular risk profile in patients with hypertension. Vasc Health Risk Manag 2009;5:577-585
21. Kramer H, Gutierrez OM, Judd SE et al. Waist Circumference, Body Mass Index, and ESRD in the REGARDS (Reasons for Geographic and Racial Differences in Stroke) Study. Am J Kidney Dis 2016; 67:62-69
Am J Kidney Dis 2016; 67:62-69
22. Foster MC, Hwang SJ, Massaro JM et al. Association of subcutaneous and visceral adiposity with albuminuria: the Framingham Heart Study. Obesity (Silver Spring) 2011; 19:1284-1289
23. Postorino M, Marino C, Tripepi G et al. Abdominal obesity and all-cause and cardiovascular mortality in end-stage renal disease. J Am Coll Cardiol 2009; 53:1265-1272
24. Kovesdy CP, Czira ME, Rudas A et al. Body mass index, waist circumference and mortality in kidney transplant recipients. Am J Transplant 2010; 10:2644-2651
25. Scales CD, Jr, Smith AC, Hanley JM et al. Prevalence of kidney stones in the United States. Eur Urol 2012; 62:160-165
26. Curhan GC, Willett WC, Rimm EB et al. Body size and risk of kidney stones. J Am Soc Nephrol 1998; 9: 1645-1652
Curhan GC, Willett WC, Rimm EB et al. Body size and risk of kidney stones. J Am Soc Nephrol 1998; 9: 1645-1652
27. Taylor EN, Stampfer MJ, Curhan GC: Obesity, weight gain, and the risk of kidney stones. JAMA 2005; 293:455-462
28. Bhaskaran K, Douglas I, Forbes H et al. Body-mass index and risk of 22 specific cancers: a population-based cohort study of 5.24 million UK adults. Lancet 2014; 384:755-765
29. Arnold M, Pandeya N, Byrnes G et al. Global burden of cancer attributable to high body-mass index in 2012: a populationbased study. Lancet Oncol 2015; 16:36-46
30. Renehan AG, Tyson M, Egger M et al. Body-mass index and incidence of cancer: a systematic review and meta-analysis of prospective observational studies. Lancet 2008; 371:569-578
Lancet 2008; 371:569-578
31. Bluher M: The distinction of metabolically ‘healthy’ from ‘unhealthy’ obese individuals. Curr Opin Lipidol 2010; 21:38-43
32. Sharma K: The link between obesity and albuminuria: adiponectin and podocyte dysfunction. Kidney Int 2009; 76:145-148
33. Wolf G, Ziyadeh FN: Leptin and renal fibrosis. Contrib Nephrol 2006; 151:175-183
34. Ellington AA, Malik AR, Klee GG et al. Association of plasma resistin with glomerular filtration rate and albuminuria in hypertensive adults. Hypertension 2007; 50:708-714
35. Bastard JP, Maachi M, Lagathu C et al.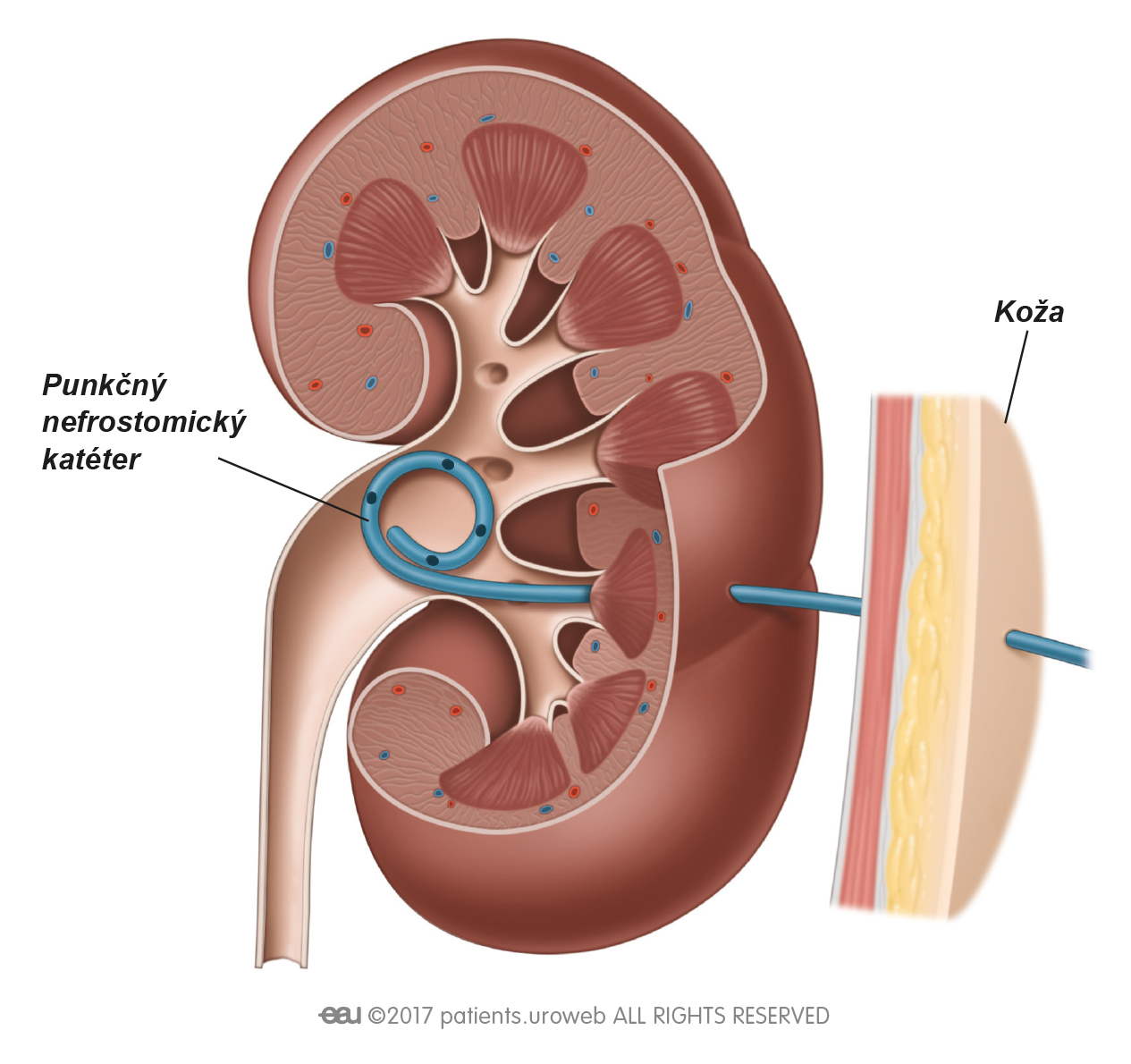 Recent advances in the relationship between obesity, inflammation, and insulin resistance. Eur Cytokine Netw 2006; 17:4-12
Recent advances in the relationship between obesity, inflammation, and insulin resistance. Eur Cytokine Netw 2006; 17:4-12
36. Furukawa S, Fujita T, Shimabukuro M et al. Increased oxidative stress in obesity and its impact on metabolic syndrome. J Clin Invest 2004; 114:1752-1761
37. Ruan XZ, Varghese Z, Moorhead JF: An update on the lipid nephrotoxicity hypothesis. Nat Rev Nephrol 2009; 5:713-721
38. Ruster C, Wolf G: The role of the renin-angiotensin-aldosterone system in obesity-related renal diseases. Semin Nephrol 2013; 33:44-53
39. Oterdoom LH, de Vries AP, Gansevoort RT et al. Fasting insulin modifies the relation between age and renal function. Nephrol Dial Transplant 2007; 22:1587-1592
40. Reaven GM: Banting lecture 1988. Role of insulin resistance in human disease. Diabetes 1988; 37:1595-1607
41. Kambham N, Markowitz GS, Valeri AM et al. Obesityrelated glomerulopathy: an emerging epidemic. Kidney Int 2001; 59:1498-1509
42. de Vries AP, Ruggenenti P, Ruan XZ et al. Fatty kidney: emerging role of ectopic lipid in obesity-related renal disease. Lancet Diabetes Endocrinol 2014; 2:417-426
43. Foster MC, Hwang SJ, Porter SA et al. Fatty kidney, hypertension, and chronic kidney disease: the Framingham Heart Study. Hypertension 2011;58:784-790
44. Henegar JR, Bigler SA, Henegar LK et al. Functional and structural changes in the kidney in the early stages of obesity. J Am Soc Nephrol 2001; 12:1211-1217
45. Knight SF, Quigley JE, Yuan J et al. Endothelial dysfunction and the development of renal injury in spontaneously hypertensive rats fed a high-fat diet. Hypertension 2008; 51:352-359
46. Tsuboi N, Utsunomiya Y, Kanzaki G et al. Low glomerular density with glomerulomegaly in obesity-related glomerulopathy. Clin J Am Soc Nephrol 2012; 7:735-741
47. Ribstein J, du CG, Mimran A: Combined renal effects of overweight and hypertension. Hypertension 1995; 26:610-615
48. Maalouf NM, Sakhaee K, Parks JH et al. Association of urinary pH with body weight in nephrolithiasis. Kidney Int 2004; 65:1422-1425
49. Lemann J, Jr., Pleuss JA, Worcester EM et al. Urinary oxalate excretion increases with body size and decreases with increasing dietary calcium intake among healthy adults. Kidney Int 1996; 49:200-208
50. Siener R, Glatz S, Nicolay C, Hesse A: The role of overweight and obesity in calcium oxalate stone formation. Obes Res 2004; 12:106-113
51. Taylor EN, Stampfer MJ, Curhan GC: Diabetes mellitus and the risk of nephrolithiasis. Kidney Int 2005; 68:1230-1235
52. Klisic J, Hu MC, Nief V et al. Insulin activates Na(+)/H(+)exchanger 3: biphasic response and glucocorticoid dependence. Am J Physiol Renal Physiol 2002; 283:F532-F539
53. Chobanian MC, Hammerman MR: Insulin stimulates ammoniagenesis in canine renal proximal tubular segments. Am J Physiol 1987; 253:F1171-F1177
54. Daudon M, Lacour B, Jungers P: Influence of body size on urinary stone composition in men and women. Urol Res 2006; 34:193-199
55. Sinha MK, Collazo-Clavell ML, Rule A et al. Hyperoxaluric nephrolithiasis is a complication of Roux-en-Y gastric bypass surgery. Kidney Int 2007;72:100-107
56. Calle EE, Kaaks R. Overweight, obesity and cancer: epidemiological evidence and proposed mechanisms. Nat Rev Cancer 2004; 4:579-591
57. Dalamaga M, Diakopoulos KN, Mantzoros CS: The role of adiponectin in cancer: a review of current evidence. Endocr Rev 2012; 33:547-594
58. Lamas O, Marti A, Martinez JA. Obesity and immunocompetence. Eur J Clin Nutr 2002; 56 Suppl 3:S42-S45
59. Lim C, Savan R: The role of the IL-22/IL-22R1 axis in cancer. Cytokine Growth Factor Rev 2014; 25:257-271
60. Grivennikov SI, Greten FR, Karin M. Immunity, inflammation, and cancer. Cell 2010; 140:883-899
61. Kovesdy CP, Anderson JE, Kalantar-Zadeh K. Paradoxical association between body mass index and mortality in men with CKD not yet on dialysis. Am J Kidney Dis 2007; 49:581-591
62. Kalantar-Zadeh K, Kuwae N, Wu DY et al. Associations of body fat and its changes over time with quality of life and prospective mortality in hemodialysis patients. Am J Clin Nutr 2006; 83:202-210
63. Beddhu S, Pappas LM, Ramkumar N, Samore M. Effects of body size and body composition on survival in hemodialysis patients. J Am Soc Nephrol 2003; 14:2366-2372
64. Curtis JP, Selter JG, Wang Y et al. The obesity paradox: body mass index and outcomes in patients with heart failure. Arch Intern Med 2005; 165:55-61
65. Wilson DO, Rogers RM, Wright EC, Anthonisen NR: Body weight in chronic obstructive pulmonary disease. The National Institutes of Health Intermittent Positive-Pressure Breathing Trial. Am Rev Respir Dis 1989; 139:1435-1438
66. Escalante A, Haas RW, del R, I: Paradoxical effect of body mass index on survival in rheumatoid arthritis: role of comorbidity and systemic inflammation. Arch Intern Med 2005; 165:1624-1629
67. Kalantar-Zadeh K, Kilpatrick RD, Kuwae N, Wu DY: Reverse epidemiology: a spurious hypothesis or a hardcore reality? Blood Purif 2005; 23:57-63
68. Noori N, Kopple JD, Kovesdy CP et al. Mid-arm muscle circumference and quality of life and survival in maintenance hemodialysis patients. Clin J Am Soc Nephrol 2010; 5:2258-2268
69. Dekker FW, de MR, van Dijk PC et al. Survival analysis: time-dependent effects and time-varying risk factors. Kidney Int 2008; 74:994-997
70. Snyder JJ, Foley RN, Gilbertson DT et al. Body size and outcomes on peritoneal dialysis in the United States. Kidney Int 2003; 64:1838-1844
71. Lee PS, Sampath K, Karumanchi SA et al. Plasma gelsolin and circulating actin correlate with hemodialysis mortality. J Am Soc Nephrol 2009; 20:1140-1148
72. Horwich TB, Fonarow GC, Hamilton MA et al. The relationship between obesity and mortality in patients with heart failure. J Am Coll Cardiol 2001; 38:789-795
73. Stenvinkel P, Marchlewska A, Pecoits-Filho R et al. Adiponectin in renal disease: relationship to phenotype and genetic variation in the gene encoding adiponectin. Kidney Int 2004; 65:274-281
74. Mohamed-Ali V, Goodrick S, Bulmer K et al. Production of soluble tumor necrosis factor receptors by human subcutaneous adipose tissue in vivo. Am J Physiol 1999; 277:E971-E975
75. Rauchhaus M, Coats AJ, Anker SD: The endotoxinlipoprotein hypothesis. Lancet 2000; 356:930-933
76. Jandacek RJ, Anderson N, Liu M et al. Effects of yo-yo diet, caloric restriction, and olestra on tissue distribution of hexachlorobenzene. Am J Physiol Gastrointest Liver Physiol 2005; 288:G292-G299
77. Kramer HJ, Saranathan A, Luke A et al. Increasing body mass index and obesity in the incident ESRD population. J Am Soc Nephrol 2006; 17:1453-1459
78. Postorino M, Mancini E, D’Arrigo G, Marino C, Vilasi A, Tripepi G, Gallus S, Lugo A, Santoro A, Zoccali C: Body mass index trend in haemodialysis patients: the shift of nutritional disorders in two Italian regions. Nephrol Dial Transplant 2016; 31(10):1699-705
79. 2008-2013 Action Plan for the Global Strategy for the Prevention and Control of Noncommunicable Diseases. 2009. World Health Organization. Ref Type: Online Source
80. O’Donoghue DJ, Stevens PE. A decade after the KDOQI CKD/guidelines: a perspective from the United Kingdom. Am J Kidney Dis 2012; 60:740-742
81. Bolignano D, Zoccali C. Effects of weight loss on renal function in obese CKD patients: a systematic review. Nephrol Dial Transplant 2013; 28 Suppl 4:iv82-iv98
82. Chang Y, Ryu S, Choi Y et al. Metabolically Healthy Obesity and Development of Chronic Kidney Disease: A Cohort Study. Ann Intern Med 2016;164:305-312
83. Wing RR, Bolin P, Brancati FL et al. Cardiovascular effects of intensive lifestyle intervention in type 2 diabetes. N Engl J Med 2013; 369:145-154
84. Mallamaci F, Ruggenenti P, Perna A et al. ACE inhibition is renoprotective among obese patients with proteinuria. J Am Soc Nephrol 2011; 22:1122-1128
85. Friedman AN, Wolfe B. Is Bariatric Surgery an Effective Treatment for Type II Diabetic Kidney Disease? Clin J Am Soc Nephrol 2016; 11:528-535
86. Chang AR, Chen Y, Still C et al. Bariatric surgery is associated with improvement in kidney outcomes. Kidney Int 2016; 90:164-171
87. Jamal MH, Corcelles R, Daigle CR et al. Safety and effectiveness of bariatric surgery in dialysis patients and kidney transplantation candidates. Surg Obes Relat Dis 2015; 11:419-423
88. Ahmadi SF, Zahmatkesh G, Ahmadi E et al. Association of Body Mass Index with Clinical Outcomes in Non-DialysisDependent Chronic Kidney Disease: A Systematic Review and Meta-Analysis. Cardiorenal Med 2015; 6:37-49
УЗИ почек: показатели нормы, расшифровка результатов
Ультразвуковое исследование почек в большинстве случаев является полноценным и достаточно информативным методом диагностики с целью определения заболевания и назначения адекватного лечения, а так же исключения патологии при скрининговых обследованиях.
Что показывает УЗИ почек?
При ультразвуковом исследовании почек УЗИ-аппарат позволяет определить следующие основные параметры:
- количество, расположение, контуры и форму почек,
- размеры органа,
- состояние структуры почечной паренхимы,
- наличие доброкачественных или злокачественных новообразований,
- наличие конкрементов в полостях почки,
- признаки воспаления,
- состояние почечного кровотока.
Количество
В норме почки являются парным органом, но встречаются аномалии.
Возможно врожденное отсутствие почки – односторонняя аплазия (агенезия), либо утрата парности в результате хирургического удаления. Встречается врожденное удвоение почки, чаще одностороннее.
Аплазия левой почки
Удвоенная почка без признаков обструкции
Расположение
В норме почки расположены на разных уровнях относительно друг друга: правая (D) почка находится на уровне позвонков 12 грудного и 2 поясничного, левая (L) почка – на уровне позвонков 11 грудного и 1 поясничного.
На УЗИ можно выявить опущение почки (нефроптоз) или нетипичную локализацию органа (дистопия), вплоть до расположения в малом тазу.
В норме почка имеет бобовидную форму и ровный наружный контур с четкой визуализацией фиброзной капсулы в виде гиперэхогенной линии.
Размеры
Физиологической норме у взрослого человека соответствуют размеры почек:
- длина – 100-120 мм,
- ширина – 50-60 мм,
- толщина – 40-50 мм.
Толщина слоя паренхимы – еще один очень важный параметр, в норме составляет 18-25 мм. Этот показатель зависит от возраста пациента: у пожилых людей он может уменьшаться до 11 мм в результате склеротических изменений. Паренхима является функциональной частью почки, в ней расположены структурно-функциональные единицы – нефроны. Увеличение показателя может быть признаком отека или воспаления почки, уменьшение свидетельствует о дистрофии органа.
У детей размеры почек зависят от возраста и роста ребенка. При росте до 80 см измеряются только два параметра – длина и ширина органа. У детей ростом 100 см и выше измеряется и толщина паренхимы.
В норме должна четко выявляться граница почечных пирамидок в паренхиматозном слое: эхогенность пирамидок ниже, чем паренхимы. При гидронефрозе дифференциация между ними отсутствует.
Увеличение размеров почки характерно для острого пиело- или гломерулонефрита, а так же если почка утратила парность и испытывает повышенную функциональную нагрузку.
Эхогенность паренхимы
Этот показатель определяет состояние почечной паренхимы, ее структуру. В норме она однородна.
Эхогенность – это степень интенсивности отражения звуковой волны от тканей: чем плотнее ткань, тем интенсивнее отражение и светлее изображение на мониторе. Ткани с низкой плотностью имеют слабую эхогенность и визуализируются темными участками. Жидкости и воздух анэхогенны.
К примеру, полостную кисту, содержащую жидкость, специалист описывает как анэхогенное образование. Гиперэхогенность характерна для склеротических процессов в почке (гломерулонефрит, диабетическая нефропатия, опухоли, амилоидоз).
Состояние полостной системы почек
Полостная система почек или чашечно-лоханочная система (ЧСЛ) выполняет функцию сбора мочи. На УЗИ могут диагностироваться следующие изменения:
- воспалительные уплотнения слизистой лоханок (пиелонефрит),
- расширение ЧЛС: пиелоэктазия – расширение лоханок, каликоэктазия – расширение чашечек (гидронефроз, обструкция мочеточников камнем или опухолью),
- наличие конкрементов (камни, песок).
Ультразвуковое изображение расширения полостных систем обеих почек у плода
В норме ЧЛС анэхогенна и не визуализируется. Камни размером 4-5 мм и более в УЗИ-заключении описываются как эхотень, гиперэхогенное включение, эхогенное образование. Наличие песка обозначается как микрокалькулез почек.
Состояние почечного кровотока
Для визуализации почечных кровеносных сосудов используют дуплексное сканирование (или допплерографию), при котором УЗИ-сканер выдает информацию в виде цветного изображения или спектрального графика. Методика является неинвазивной и безболезненной.
Исследование позволяет определить состояние сосудистой стенки, наличие внутрисосудистых обструкций и стенозов, определить скорость кровотока. В норме скорость может колебаться от 50 до 150 см/сек.
На цветовой схеме нормальными считаются темные тона. Яркий цвет фиксирует ускоренный кровоток и свидетельствует о наличии стеноза, основным признаком которого считается усиление кровотока в почечной артерии больше 200 см/сек.
Определяется индекс сопротивления кровотока или индекс резистентности, который напрямую зависит от возраста пациента: чем старше, тем выше скорость кровотока и выше индекс. В норме индекс сопротивления для почечной артерии – 0,7, для междолевых артерий – 0,34-0,74.
Кто проводит расшифровку результатов?
Расшифровку ультразвукового исследования почек должен проводить врач-уролог. К словесному заключению обычно прилагается фото УЗИ или сонограмма, где стрелками отмечается место выявленных патологических изменений.
При обнаружении опухолей или сосудистых изменений неплохо, если будет прилагаться видео УЗИ.
Какие заболевания выявляет УЗИ почек?
Ультразвуковая диагностика наиболее информативна относительно следующих почечных заболеваний и синдромов:
- нефроптоз,
- сужение мочеточников,
- опухоли, кисты, абсцессы,
- камнеобразования,
- воспалительные процессы (пиелонефрит, гломерулонефрит),
- гидронефроз,
- дистрофия почек,
- амилоидоз,
- поражение почечных сосудов.
Если в заключении УЗИ почек значится «выраженный пневматоз кишечника», это означает неинформативность обследования по причине метеоризма и в этом случае УЗИ придется повторить после подготовки (употребление ветрогонных препаратов).
Видео:
УЗ анатомия почек
Порядок выполнения: ультразвуковое исследование почек
Подготовка к УЗИ почек
как обнаружить и что делать?
Нам не привыкать к простуде в холодное время. Но если недомогание, затруднённое дыхание и отёчность преследует круглый год, это повод задуматься, нет ли более серьёзных заболеваний носоглотки. Киста в пазухе носа — одна из частых причин подобного недомогания.
Что из себя представляет киста в пазухе носа?
Носоглотка покрыта изнутри слизистой оболочкой, которая защищает органы дыхания от пересыхания, пыли и переохлаждения. В ней находятся железы, продуцирующие слизь. Если она не может попасть в пазухи носа и скапливается внутри железы, образуется киста — пузырёк, наполненной жидкостью.
Сама киста, расположенная в пазухе носа, не представляет опасности. Она не может перейти в злокачественное образование и стать причиной для серьёзных заболеваний. Но со временем киста может перекрыть дыхание. А при очень большом размере — деформировать череп или способствовать постоянным бронхитам и пневмониям.
Чаще всего кисту можно обнаружить в лобных пазухах (область над переносицей и бровями). Реже — под крыльями носа, над верхней челюстью или под переносицей. Одновременно может образоваться несколько кист. Над верхней челюстью они образуются из-за проблем с зубами и дёснами. Из-за того, что пазухи носа и ротовая полость находятся рядом, инфекции и воспаления легко переходят между ними.
Такие новообразования всегда остаются доброкачественными, но не могут исчезнуть без серьёзного вмешательства.
Симптомы и признаки
Коварство кисты пазухи носа в том, что начало болезни похоже на обычное ОРЗ. Поэтому есть все шансы не успеть вовремя начать лечение. А это может быть чревато серьёзными последствиями: искривятся носовые хрящи и начнутся тяжёлые гнойные воспаления, особенно в случае разрыва кисты.
Тревогу должны вызвать следующие симптомы:
- невозможно снять заложенность носа обычными препаратами;
- долгая головная боль;
- боль у переносицы, крыльев носа или над глоткой, которая становится сильнее при наклонах и поворотах головы;
- ощущения инородного тела в носовых проходах;
- в месте, где развилась киста, даже лёгкое прикосновение вызывает боль.
Если болезнь запустить, часто начинает портиться зрение, появляется боль в глазах. А если при развитии кисты в заполняющую её жидкость попала инфекция (например, из больного зуба), то симптомы схожи с гайморитом: повышается температура, появляются гнойные выделения и отёки.
Каковы причины болезни?
К сожалению, решающий фактор в развитии кисты — наследственность. Если у ваших родителей или старших родственников была такая проблема, нужно быть внимательнее.
Кроме того, нужно быть осторожнее, если:
- вы часто страдаете простудами,
- постоянно контактируете с аллергенами,
- есть проблемы с зубами или дёснами,
- у вас изменённая форма костей лица из-за врождённой или приобретённой травмы.
Даже при хорошей наследственности совпадение остальных факторов существенно повышает риск образования кисты. Поэтому, при серьёзном недомогании, обязательно пройдите проверку и не ставьте диагнозы самостоятельно!
К кому обращаться, если есть подозрение на кисту?
Если вы подозреваете, что у вас киста в пазухе носа, незамедлительно обратитесь к отоларингологу или терапевту. После визуального осмотра вам предстоит пройти более точное обследование: рентген, МРТ, КТ или эндоскопию. Последняя, кроме внешнего осмотра, позволит сразу же взять ткани кисты на анализ.
Кроме того, иногда требуется консультация стоматолога. Если причиной болезни стал запущенный кариес и пародонтит, без лечения зубов остаётся риск образования новой кисты.
Лечение и профилактика
Если вы в группе риска, можно отсрочить наступление болезни совсем простыми способами:
- вовремя лечить все заболевания носоглотки: будь то простуда или боль в зубах;
- укреплять иммунитет — в этом помогут правильный образ жизни, свежий воздух, здоровый сон и полноценное питание;
- избегать вредных летучих веществ: табака, растворителей, бытовой химии и красок;
- если у вас есть аллергия, причин которой не удаётся избежать, придётся регулярно принимать антигистаминные препараты.
Решение о способе лечения должен принимать специалист. Обычно назначают препараты, которые помогает снять воспаления, отёки и победить инфекцию. Можно даже удалить кисту, если её наличие приносит боль и дискомфорт.
Ни в коем случае нельзя заниматься самолечением — оно может привести к увеличению кисты в размерах. И уж тем более не стоит обращаться к народной медицине.
После успешного лечения придётся пару раз в год посещать врача-отоларинголога — заболевание может дать рецидив. Впрочем, при правильном образе жизни и своевременном лечении ОРЗ и кариеса шанс повторного образования кисты очень мал.
Кисты почки (почечные кисты) — Диагностика, оценка и лечение
Кисты почек — это мешочки с жидкостью, которые образуются в почках. Их обычно называют «простыми» кистами, то есть они имеют тонкую стенку и содержат похожую на воду жидкость. Кисты почек становятся довольно распространенным явлением с возрастом и обычно не вызывают симптомов или вреда.
Поскольку они редко вызывают симптомы, почечные кисты чаще всего обнаруживаются при визуализирующих исследованиях, выполняемых по другим причинам.Некоторые кисты почек могут казаться более сложными и иметь более толстые стенки или содержать твердый материал вместо жидкости. Ваш врач, скорее всего, проведет дополнительные визуализационные тесты, чтобы контролировать сложные кисты почек и отличить доброкачественные кисты от рака. Эти тесты могут включать в себя УЗИ брюшной полости или таза, КТ брюшной полости и таза или МРТ тела. Почечные кисты обычно остаются в покое и не требуют лечения, если только они не вызывают симптомы или не нарушают функцию почек. Если требуется лечение, ваш врач может использовать склеротерапию или операцию для дренирования кисты и принять меры для предотвращения ее рецидива.
Что такое кисты почек?
Кисты почек — это мешочки с жидкостью, которые образуются в почках. В большинстве случаев это простые кисты почек, то есть у них тонкие стенки и внутри только жидкость, похожая на воду. Они довольно часто встречаются у пожилых людей и обычно не вызывают никаких симптомов или вреда.
В редких случаях кисты почек могут потребовать лечения из-за инфекции, кровотечения или увеличения. Когда возникают такие осложнения кисты почек, симптомы могут включать:
- Лихорадка
- Боль или болезненность между ребрами и тазом
- Боль в верхней части живота
- Изменения в мочеиспускании
- Кровь в моче ( Гематурия )
Причина возникновения кист почек неизвестна, хотя возраст является основным фактором риска.По оценкам, одна треть людей старше 70 лет имеет по крайней мере одну простую кисту почек. Наличие более одной простой кисты в каждой почке может быть нормальным явлением, особенно с возрастом.
Наличие нескольких простых кист почек отличается от наличия множества кист в почках из-за поликистозной болезни почек (PKD). PKD — это генетическое заболевание, характеризующееся скоплением кист, которое может нарушать функцию почек.
начало страницы
Как диагностируются и оцениваются кисты почек?
Поскольку они редко вызывают симптомы, почечные кисты чаще всего обнаруживаются при визуализирующих исследованиях, выполняемых по другим причинам.В таких случаях без каких-либо симптомов простые кисты почек обычно остаются в покое и не нуждаются в дополнительных исследованиях. Однако некоторые почечные кисты выглядят сложнее, чем обычная простая почечная киста. Эти сложные кисты почек могут иметь более толстую стенку или твердый материал внутри, а не просто жидкость. После обнаружения сложных кист почек могут быть выполнены дополнительные визуализирующие исследования, чтобы контролировать их и отличать доброкачественные кисты от рака.
Некоторые типы визуализационных тестов, которые может назначить ваш врач, включают:
УЗИ брюшной полости и УЗИ органов малого таза : Эти исследования выполняются для получения снимков почек и подтверждения наличия жидкости внутри почечных кист.Ваш врач может использовать ультразвуковое исследование, чтобы контролировать кисты почек на предмет любых изменений с течением времени.
Для получения дополнительной информации об УЗИ, проводимом у детей, посетите страницу Детское УЗИ брюшной полости.
Abdominal and Pelvic CT : Эта процедура, которую часто используют в качестве дополнения к ультразвуку при исследовании сложных кист почек, помогает отличить доброкачественные кисты от опухолей почек. КТ может включать инъекцию контрастного вещества. См. Страницу «Доза излучения» для получения дополнительной информации о процедурах КТ.
Для получения дополнительной информации о компьютерной томографии, выполняемой детям, посетите страницу «Детская компьютерная томография».
Магнитно-резонансная томография тела (МРТ) : В этом тесте визуализации используются магнитное поле и радиочастотные импульсы для получения подробных изображений почек. МРТ может включать инъекцию контрастного вещества. См. Страницу безопасности МРТ для получения дополнительной информации о процедурах МРТ.
начало страницы
Как лечат кисты почек?
Почечные кисты обычно не требуют лечения, если только они не вызывают симптомы или не нарушают функцию почек. Варианты лечения включают:
- Склеротерапия : Склеротерапия, также известная как чрескожная алкогольная абляция, включает введение длинной иглы через кожу в кисту под контролем ультразвука. Врач осушает кисту и заполняет ее раствором на спиртовой основе, который заставляет ткань затвердеть и сморщиться, уменьшая вероятность рецидива.Процедура обычно проводится в амбулаторных условиях под местной анестезией.
- Хирургия: При больших кистах хирург делает небольшой разрез и доступ к кисте осуществляется лапароскопом. Затем хирург дренирует кисту и сожжет или срежет ее внешний слой. Лапароскопическая операция требует общей анестезии.
начало страницы
Какой тест, процедура или лечение лучше всего мне подходят?
начало страницы
Эта страница была просмотрена 20 февраля 2019 г.
Гранулематоз с полиангиитом (GPA) — Американский почечный фонд (AKF)
Гранулематоз с полиангиитом (ГПА), ранее известный как гранулематоз Вегенера, представляет собой заболевание, вызывающее отек и раздражение кровеносных сосудов в почках, носу, носовых пазухах, горле и легких.Набухшие кровеносные сосуды затрудняют доступ крови к органам и тканям, которые в ней нуждаются, что может быть вредным. Болезнь также вызывает образование шишек, называемых гранулемами, которые повреждают область вокруг них. У некоторых людей GPA влияет только на легкие. ГПД, поражающий почки, может привести к хроническому заболеванию почек и почечной недостаточности.
Первые признаки GPA обычно проявляются в носу, носовых пазухах, горле или легких. Вы можете заметить насморк, инфекции носовых пазух или кровотечение из носа. Другие знаки могут включать:
- Кашель
- Проблемы с дыханием
- Свистящее дыхание
- Лихорадка
- Чувство слабости
- Онемение рук, ног, пальцев рук и ног
Вы можете не заметить никаких симптомов, если GPA влияет на ваши почки.Признаки проблем с почками могут обнаруживаться только в анализах крови и мочи, но если у вас есть симптомы, вы можете заметить кровь в моче. Средний балл может ухудшиться очень быстро. Если вы заметили неизлечимый насморк, кровь из носа или кашель с кровью, немедленно обратитесь к врачу. ГПД может быстро ухудшиться, и важно лечить его как можно раньше, чтобы предотвратить необратимое повреждение органов, например почечную недостаточность.
Если ваш врач считает, что у вас может быть средний балл, вам могут потребоваться анализы крови и мочи, рентген грудной клетки, компьютерная томография или магнитно-резонансная томография и биопсия.Если ваши тесты показывают, что у вас средний балл, ваш врач может посоветовать вам принимать лекарства, которые контролируют воспаление (отек и раздражение) и ослабляют вашу иммунную систему. Эти лекарства называются иммунодепрессантами. Другой вариант лечения, ослабляющий вашу иммунную систему, называется плазмаферез (plaz-muh-fuh-REE-sis). Другие методы лечения могут помочь справиться с побочными эффектами и предотвратить осложнения. Если GPA вызывает отказ почек, вам понадобится диализ или трансплантация почки.
Для получения дополнительной информации посетите:
Защитный эффект человеческого жира почечного синуса на гломерулярные клетки отменяется гепатокином фетуин-A
Характерные черты изолированных первичных периваскулярных жировых клеток и жировых клеток почечного синуса человека
RSFC можно выделить, охарактеризовать и субкультивировать из RSF четырех разных пациентов .Затем были исследованы функциональные свойства и эффекты этого уникального почечного периваскулярного жирового компартмента ex vivo . Культивированный RSFC показал форму веретена с цитоплазматическими выступами и формированием кластеров (рис. 1a, верхний уровень), аналогичную PVFC, выделенному из артерий руки 7 . При воздействии среды для дифференцировки цитоплазма почти каждого RSFC была плотно упакована липидами, и как RSFC, так и PVFC демонстрировали высокую способность дифференцироваться в зрелые адипоциты (> 90% клеток), что было обнаружено окрашиванием масляным красным (рис.1а, нижний уровень). Анализ FACS показал, что первичные культуры не были загрязнены другими типами клеток (дополнительный рисунок S1).
Рисунок 1( a ) Характер роста и характеристика RSFC и PVFC после выделения. Верхняя панель: характерный рост RSFC (слева) и PVFC (справа) в культуре. Нижняя панель: дифференцированные адипоциты, окрашенные масляным красным, демонстрируют типичные цитоплазматические липидные капли (увеличение × 4, как деталь на вставке × 40) ( b – f ) Сравнение зависимой от времени экспрессии мРНК различных (провоспалительных и регенеративных) факторы PVFC (серые столбцы) по сравнению с RSFC (черные столбцы), определенные с помощью ПЦР в реальном времени (световой цикл) через 6, 24, 48 и 72 часа культивирования.( b ) IL-6, ( c ) IL-8, ( d ) MCP-1, ( e ) VEGF и ( f ) HGF. Статистический анализ: линейные смешанные модели со случайным наклоном, в которых донор и время наблюдения являются случайными эффектами. Значения представляют собой среднее значение ± стандартная ошибка среднего из 4 независимых экспериментов (значения p показаны для базовой экспрессии мРНК по сравнению с геном домашнего хозяйства RPS13).
Сравнение уровней мРНК и продукции белков провоспалительных и регенеративных факторов в человеческих жировых клетках, полученных из RSF и других жировых компартментов человека
RSFC показало увеличение мРНК IL-6 (в 5 раз) и IL-8 (> в 10 раз) -выражение по сравнению с PVFC во все исследованные временные точки (рис.1b, c), тогда как уровни мРНК MCP-1 были лишь немного выше, чем у PVFC (рис. 1d). Экспрессия мРНК VEGF была сходной в обоих типах жировых клеток (фиг. 1e), тогда как HGF была несколько (но не значительно) выше, чем в RSFC (фиг. 1f).
Мы также сравнили базальную экспрессию этих факторов в висцеральных жировых клетках (VFC) и подкожных жировых клетках (SCFC) (дополнительный рисунок S2). Эти соответствующие результаты показывают, что паттерны экспрессии (про) воспалительных факторов одинаково повышены в VFC и RSFC по сравнению с PVFC или SCFC, тогда как регенеративный фактор VEGF существенно не отличался.Согласно нашим предыдущим исследованиям, 7 HGF обычно выше экспрессируется в PVFC по сравнению с SCFC или VFC, но этот уровень даже был превышен в RSFC через 72 часа (рис. 1f и дополнительный рис. S2e).
В RSFC была обнаружена чрезвычайно высокая продукция IL-6, IL-8, MCP-1, HGF и VEGF. Очень высокий уровень (про) воспалительных белков IL-6 (через 24 часа: 390 ± 175 пг / мл, через 48 часов: 585 ± 223 пг / мл и через 72 часа: 679 ± 301 пг / мл, n = 6), а также ИЛ-8 (через 24 часа: 243 ± 127 пг / мл, через 48 часов: 684 ± 379 пг / мл и через 72 часа: 905 ± 510 пг / мл, n = 6). супернатанты RSFC, которые были сопоставимы с VFC 7 .Уровни белка отражали данные экспрессии мРНК. Кроме того, RSFC секретировал более высокие уровни хемоаттрактанта MCP-1 (через 24 часа: 110 ± 59 пг / мл, через 48 часов: 214 ± 68 пг / мл и через 72 часа: 352 ± 82 пг / мл, n = 6 ), который превышал таковые для других типов жировых клеток, описанных ранее 7 , но в пределах сравнимого диапазона концентраций, обнаруженного в PVFC.
Уровни белка HGF в RSFC (через 24 часа: 1410 ± 513 пг / мл, через 48 часов: 2864 ± 1540 пг / мл и через 72 часа: 7242 ± 303 пг / мл, n = 6) в целом были сопоставимы с те, которые были обнаружены в PVFC, но были значительно выше, чем в VFC и SCFC, открытие, которое также наблюдалось ранее 7 .Белки VEGF увеличивались в зависимости от времени (через 24 часа: 179 ± 24 пг / мл, через 48 часов: 180 ± 56 пг / мл и через 72 часа: 365 ± 47 пг / мл, n = 6). Эти уровни также находились в сопоставимом диапазоне концентраций с уровнями PVFC. Вместе эти результаты показывают, что продукция белка соответствовала экспрессии соответствующей мРНК.Влияние RSFC на характер экспрессии мРНК ЭК и ПО человека в сокультуре
Выделение чистых ЭК было возможно в 80% препаратов сосудов. ЭК имел характерный узор из булыжников (рис.2а). Картина роста ПО показана на рис. 2б. Монокультурные ЭК и ПО показали замечательную экспрессию мРНК (про) воспалительных и регенеративных факторов в течение всего периода культивирования 72 часа (рис. 2c-f). Экспрессия мРНК соответствующей EC- и PO-монокультуры служила контролем. PO не экспрессировал релевантные уровни HGF (не показаны).
Рисунок 2Влияние RSFC на клубочковые клетки человека. Схема роста EC ( a ) и PO ( b ). Экспрессия мРНК (про) воспалительных ( c ) и регенеративных факторов ( e ) в EC и PO ( d, f ) соответственно.Следует отметить, что PO не экспрессировал HGF. Клетки совместно культивировали с RSFC в течение 24, 48 и 72 часов. Статистический анализ: представлены линейные смешанные модели со случайным наклоном, в которых донор и время наблюдения являются случайными эффектами, а культура — фиксированными эффектами (моно- или сокультивирование) для этих значений p . Значения представляют собой среднее значение ± стандартная ошибка среднего из шести независимых экспериментов.
При совместном культивировании ЭК с RSFC, экспрессия мРНК IL-6, IL-8 и MCP-1 значительно снижалась (рис.2c), тогда как HGF значительно повышается в период между 24–72 часами (рис. 2e). VEGF не изменился. ICAM-1 и преимущественно ALCAM подавлялись (дополнительный рис. S3a). По сравнению с ЕС, при ПО наблюдали сильное подавление IL-6, IL-8 и MCP-1 (фиг. 2d) и небольшое снижение экспрессии мРНК VEGF (фиг. 2f). ICAM-1 и ALCAM были значительно подавлены (дополнительный рис. S3b). Поскольку релевантная экспрессия мРНК регенеративного фактора HGF не была обнаружена в ПО, но его антагонист TGF-β, хорошо известный профибротический фактор в почках, этот фактор был дополнительно проанализирован в ПО.Экспрессия мРНК TGF-β также значительно снижалась во время совместного культивирования ПО с RSFC (фиг. 2f). Все эти эффекты сохранялись в течение всего периода культивирования от 24 до 72 часов.
Обратные эффекты ЭК на RSFC были аналогичны тем, которые ранее были описаны для сокультив PVFC 7 . В то время как в RSFC, совместно культивированном с EC или PO, индуцировалась экспрессия мРНК (про) воспалительных факторов (дополнительный рис. S4a и c), HGF и VEGF были только умеренно затронуты в RSFC, совместно культивированном с EC (дополнительный рис.S4b). Влияние кокультивированного ПО на (провоспалительные) (дополнительный рисунок S4c) и регенеративные факторы (дополнительный рисунок S4d) в RSFC было даже более выраженным.
Влияние фетуина-A на RSFC
Для имитации потенциального влияния жировой ткани печени на RSF и, следовательно, на клетки клубочков, гепатокин фетуин-A был добавлен в культуральную среду RSFC. Доза 600 мкг / мл фетуина-A является репрезентативной для уровней в плазме у лиц с ожирением 21, 22 . Экспрессия мРНК IL-6 и lL-8 в RSFC была слегка повышена под действием фетуина-A или пальмитата, но комбинация усиливала (до 50%) эффекты каждого отдельного стимулятора (рис.3а). Умеренная стимуляция LPS указывает на то, что эффекты не были вызваны соответствующими примесями в препаратах фетуина-A. Экспрессия мРНК MCP-1 также стимулировалась фетуином-A, но не индуцировалась дополнительно пальмитатом в той же степени, что и для (провоспалительных факторов). Стимуляция VEGF также немного усиливалась пальмитатом (рис. 3b). Напротив, HGF значительно подавлялся под влиянием фетуина-A с (5-кратным) или без (2-кратным) пальмитатом (рис. 3b).Ранее Pal et al . 23 продемонстрировал на мышах, что фетуин-A является эндогенным лигандом, который физически взаимодействует и обеспечивает перекрестные помехи между рецептором пальмитат-TLR4 и передачу сигналов, что приводит к продукции (провоспалительных цитокинов), открытие, которое мы ранее могли подтвердить с помощью жировых клеток человека. данные 14 . Ранее мы продемонстрировали в PVFC, что (про) воспалительные эффекты фетуина-A опосредуются путем NFκB и блокируются ингибированием TLR4 14 .Однако в этом исследовании с RSFC мы попытались ответить на вопрос, участвуют ли также NFκB-независимые протеинкиназы после активации TLR4. И ингибитор NFκB, и ингибитор JNK почти полностью аннулировали стимулирующие эффекты фетуина-A / пальмитата на IL-6 и IL-8 (рис. 3c). Эффекты на MCP-1 были немного отменены ингибитором NFκB. Ингибиторы MEK1 / 2 и p38MAPkinase не оказали значительного воздействия (данные не показаны). В отличие от этих TLR4-опосредованных стимулирующих эффектов на интерлейкины, экспрессия мРНК HGF сильно ингибировалась фетуин-A / пальмитатом, что не могло быть отменено ингибитором NFκB (рис.3d), но полностью аннулируется ингибитором JNK (рис. 3d). Наконец, стимулирующие эффекты на регенеративный фактор VEGF могут быть отменены любым ингибитором (рис. 3d). Данные показывают, что эффекты фетуина-A на (про) воспалительные факторы и HGF регулируются разными сигнальными путями.
Рисунок 3Влияние фетуина-А и / или пальмитата на RSFC. Влияние 600 мкг / мл фетуин-A ± 50 мкмоль / л пальмитата, пальмитата как такового и ЛПС (в качестве контроля эндотоксина) на экспрессию мРНК ( a ) (провоспалительных белков IL-6, IL -8 и MCP-1, и ( b ) регенеративные факторы HGF и VEGF через 24 часа после лечения RSFC.( c, d ) Обработка RSFC ингибитором NFkappaB или ингибитором JNK. Статистический анализ: ANOVA и апостериорный тест Тьюки. Значения представляют собой среднее значение ± стандартная ошибка среднего из трех независимых экспериментов (* p <0,05 и ** p <0,01 для клеток, обработанных фетуином-A и / или пальмитатом, по сравнению с контролями (con), определенными как 1, так и # p <0,05 и ## p <0,01 или † <0,05 и †† <0,01 для культур, обработанных фетуином-A / пальмитатом, по сравнению с идентичными культурами, предварительно обработанными соответствующими ингибиторами).Влияние RSFC, обработанного фетуином-A, на экспрессию мРНК (про) воспалительных и регенеративных факторов в совместно культивируемых EC и PO. Сокультуры RSFC с EC или PO обрабатывали фетуином-A (600 мкг / мл) в течение 24 часов. Показана экспрессия мРНК (про) воспалительных факторов ( e , g ) и регенеративных факторов ( f , h ) в EC и PO соответственно. Статистический анализ: парный t-критерий для анализа различий в парах измерений от одних и тех же доноров. Значения представляют собой среднее значение ± стандартная ошибка среднего из четырех независимых экспериментов (* p <0.05 и ** p <0,01 для сокультуры, обработанной фетуином-A, по сравнению с контролями (con), определенными как 1).
Влияние RSFC, обработанного фетуином-A, на EC и PO в сокультурах
Чтобы доказать, что RSFC, обработанный фетуином-A, может влиять на EC или PO клубочков, были изучены сокультуры с RSFC. Фетуин-A вызывал сильную повышающую регуляцию экспрессии мРНК Il-6 и, в частности, MCP-1 (до 7 раз) в EC, по сравнению с необработанными контрольными культурами (фиг. 3e). Экспрессия мРНК TGF-β увеличилась, тогда как HGF немного снизилась, но не статистически значимо (рис.3е). Поскольку известно, что TGF-β индуцирует экспрессию CTGF ( фактор роста соединительной ткани), например, В почечных мезангиальных клетках мы также изучали этот матрицеклеточный и профибротический белок в RSFC. CTGF заметно экспрессировался всеми тремя типами клеток, а фетуин-A вызывал небольшую повышающую регуляцию экспрессии мРНК CTGF в RSFC ( p = 0,06, контрольные культуры: 70,22 ± 30,57 по сравнению с культурами, обработанными фетуином-A, экспрессия 101,41 ± 51,74 мРНК связана с уборка RPS13, n = 4, дополнительный рис.S5).
Данные мРНК были подчеркнуты анализом белков: секреция белков IL-6, IL-8, MCP-1 и VEGF была повышена (дополнительный рисунок S6), HGF оставался неизменным. Экспрессия и секреция мРНК IL-6 и IL-8, которые подавлялись в PO при совместном культивировании с RSFC (см. Рис. 2d), не только отменялись, но даже значительно усиливались при воздействии RSFC, обработанного фетуином-A (рис. 3g). ). Секреция белков MCP-1 и VEGF увеличивалась в 1,5-2 раза (фиг. 3h и дополнительный S6b).
Поскольку повышенная экспрессия MCP-1, преимущественно в EC, указывает на повышенное привлечение мононуклеарных клеток, мы также изучили экспрессию молекул адгезии ICAM-1 и ALCAM в RSFC, EC и PO под влиянием фетуина-A.Мы обнаружили тенденцию к усилению регуляции ICAM-1 и ALCAM в PO и значительной стимуляции ALCAM в RSFC и EC (дополнительный рисунок S7).
Иммуногистохимическое обнаружение макрофагов и васкуляризация в RSF человека
Для подтверждения присутствия макрофагов в RSF человека, которые могли быть привлечены MCP-1 и связываться с ICAM-1 или ALCAM, окрашивание против CD68 (макрофаги M1 и M2 ) и CD206, лектин С-типа на макрофагах M2, были выполнены при резекции RSF человека.Значительное количество как активированных провоспалительных макрофагов M1, так и деактивированных / (против) воспалительных макрофагов M2 присутствует между большими, заполненными жиром адипоцитами (рис. 4a, b) и интенсивными микро- (рис. 4c) и макро- (рис. 4d) васкуляризация, которую выявляли при окрашивании ЭК на CD31.
Рисунок 4Иммуногистохимическое определение макрофагов и ЭК. RSF, полученный при резекции почек у человека: ( a ) CD 68, специфичный как для макрофагов M1, так и M2, и ( b ) CD 206, лектин C-типа на макрофагах, специфичный для макрофагов M2, расположенных внутри жира. ткани (тонкие стрелки), но также вдоль кровеносных сосудов (жирная стрелка).Микроваскуляризация обнаруживается по окрашиванию CD31 EC ( c ), расположенных между жировыми клетками, и ( d ) более крупных сосудов между жировой тканью. Клетки отмечены коричневым окрашиванием (стрелки). Масштабная линейка соответствует 100 мкм.
Как показано на рис. 5, мы предлагаем механизм баланса между (провоспалительным цитокином, высвобождаемым RSFC) и молекулами адгезии и факторами регенерации. Перекрестные помехи с ожирением печени меняют баланс до нездорового состояния, когда привлекаются моноциты / макрофаги.
Рисунок 5Предлагаемый механизм баланса между (про) воспалительными цитокинами, высвобождаемыми RSFC, и молекулами адгезии, а также регенеративным фактором HGF (VEGF и противодействующий TGF-β, существенно не изменяются и поэтому не показаны для ясность). Взаимодействие с ожирением печени через повышенный уровень гепатокина фетуин-A изменил баланс с ( a ) «здоровый» на ( b ) «нездоровый» ((провоспалительный и хемоаттрактивный) статус.
Жир почечных синусов у человека
Репрезентативный гистологический срез человека показывает непосредственную близость RSF человека к сосудистой стенке без какого-либо барьера для адвентиции артерий (рис. 6a). Площадь RSF была измерена у 449 участников. Антропометрические и клинические данные исследуемой когорты представлены в таблице 1. Процент площади поперечного сечения жировой ткани в почечном синусе по сравнению с площадью поперечного сечения почки отдельно оценивался с помощью МРТ с обеих сторон.Примеры двух участников показаны на рис. 6b – e. RSF_MI участника на рис. 6b, c составляет 0,23, тогда как RSF_MI участника на рис. 6d, e составляет только 0,07. Почки на левой стороне показали значительно больше жира в почечном синусе, чем почки на правой стороне (RSF_MI = 0,088 против 0,054, p <0,0001). Среднее значение RSF_MI было выше у мужчин, чем у женщин (0,091 против 0,055, p <0,0001), и положительно коррелировало с возрастом (R 2 = 0,21, бета = 0,17, p <0,0001) и ИМТ (R 2 = 0). .06, бета = 0,0023, p <0,0001).
Рисунок 6Жир почечных синусов человека. ( a ) Гистологический срез человека показывает непосредственную близость RSF к сосудистой стенке. ( b – e ) Поперечные T1-взвешенные срезы МРТ двух 61-летних участников мужского пола: ( b, d ) Обе почки показаны на уровне хили. Хотя у участников сопоставимый ИМТ, размеры отделений RSF разительно отличаются. ( c, e ) Те же срезы МРТ, что и слева, но с выделенными областями RSF желтым цветом и областями почек синим, чтобы проиллюстрировать расчет \ ({\ rm {RSF}} \ _ {\ rm {MI }} = \ frac {желтый \, область} {желтый \, область + синий \, область} \).RSF_MI участника на рис. 6b, c составляет 0,23, тогда как RSF_MI участника на рис. 6d, e составляет только 0,07. ( f, g ) Связь RSF_MI с отношением альбумина к креатинину в моче (uACR), стратифицированным по содержанию жира в печени (содержание жира в печени> 5,6% классифицировалось как ожирение печени, НАЖБП). RSF_MI отображается в логарифмической шкале. uACR был преобразован в приближенное нормальное распределение. На графике нанесены недиабетические остатки с поправкой на пол, возраст и ИМТ. Площадь RSF не коррелировала с uACR у субъектов без ожирения печени (n = 212), но положительные отношения были обнаружены у субъектов с ожирением печени (n = 105).
Таблица 1 Антропометрические и клинические данные межквартильного размаха исследуемой когорты.Для оценки релевантности результатов in vitro было определено влияние RSF на скорость экскреции альбумина с мочой у субъектов, не страдающих диабетом. Мы обнаружили тенденцию к ассоциации площади RSF с отношением альбумина к креатинину (uACR) (p = 0,07) после поправки на пол, возраст и ИМТ. Наша биологическая гипотеза предполагает, что пагубное влияние RSF на функцию почек может иметь место при сопутствующей НАЖБ.Мы обнаружили взаимодействие между RSF и содержанием жира в печени, рассчитанным на uACR (p = 0,03), показывая, что содержание жира в печени действительно может модулировать связь RSF с uACR. В стратифицированном анализе субъекты без НАЖБ (содержание жира в печени <5,6%, n = 212) RSF не ассоциировались с uACR (бета = 0,04, p = 0,94, рис. 6f). У субъектов с НАЖБ (содержание жира в печени> 5,6%, n = 105) была обнаружена значимая связь между RSF и uACR (бета = 0,40, p = 0,0005, рис. 6g). Концентрации фетуина-A в плазме были связаны с uACR у субъектов с ожирением печени (n = 41, бета = 0.3, p = 0,05), в то время как у субъектов без ожирения печени ассоциации не наблюдалось (n = 88, бета = -0,09, p = 0,41), что указывает на влияние ожирения печени на функцию почек. Чтобы решить проблему функции почек, мы проанализировали рСКФ, которая была обратно коррелирована с RSF (дополнительный рисунок S8), предполагая более низкую рСКФ для субъектов с более высоким RSF (r = 0,24, p <0,0001). Однако мы не обнаружили связи между уровнями фетуина-A и RSF (p = 0,76 после поправки на пол, возраст, ИМТ), но тенденцию к положительной связи между уровнями фетуина-A и ИМТ (оценка = 1.5, р = 0,06).
Почечный синус — обзор
2.17.11 Ультразвуковая анатомия
US отображает анатомию пациента в виде тонких срезов. Понимание нормальной и патологической анатомии и осмысление значения изображения становятся основополагающими для использования эхографии в диагностике (Kremkau, 2006). Какими бы сложными ни были нормальные и патологические признаки органа или ткани, их можно свести к относительно небольшому количеству основных типов изображений. В этом контексте переориентация мышления важна для клинициста, и мышление срезами для визуализации органа является первым действием.Например, если цилиндр (трубчатая конструкция как сосуд) разрезан по его короткой оси, полученное изображение будет кругом (Hedrick et al., 2005).
Исследование брюшной полости в США (Cohen and McGahan, 2007) выявило множество структур, которые выглядят как черные круглые формы (с жидким содержимым). К таким трубчатым структурам относятся аорта, нижняя полая вена, воротная вена, печеночные вены, желчные протоки и желчный пузырь (Bates, 2004; , рисунок 11, ). Поворот зонда с короткой оси на длинную или наоборот демонстрирует их реальную форму и их анатомическую природу.Когда структура остается круглой по обеим осям, она должна быть сферической, и врач должен заподозрить аномалию, потому что в брюшной полости обычно нет идеальной сферической структуры (кисты). Каждую идентифицированную анатомическую структуру можно охарактеризовать с помощью УЗИ с точки зрения размеров, эхогенности (гипер, изо- и гипо) и эхоструктуры (однородной и неоднородной).
US — идеальный метод для распознавания кист, определенных твердых образований и макрокальцификаций. Простые кисты являются безэховыми, имеют линейные тонкие стенки и характеризуются увеличением заднего отдела.Обычно это доброкачественные черты. Обнаружения, связанные со сложными кистами, включают неровные и толстые стенки, обломки внутри кисты и толстые сосудистые перегородки. Часто это признаки злокачественного новообразования (Becker and Schneider, 1975; Carter and Green, 2011).
Камни (внутри желчного пузыря, почки, мочеточника или мочевого пузыря; Bortoff et al., 2000) или кальцификаты обычно выглядят как эхогенные очаги с отчетливым затемнением сзади, связанным с сильным отражением звука от камня и отсутствием звука сзади к нему ( Рисунок 7 ).Двенадцатиперстная кишка, желудок и кишечник также могут быть связаны с своего рода затенением из-за наличия газа в просвете. У газа большая разница в акустическом импедансе по сравнению с тканями, он является отражающим и плохо проводит звук (Wilson et al., 1999).
Различные нормальные органы имеют обычную анатомическую форму и размеры, но имеют разную степень эхогенности. Например, поджелудочная железа (Martinez-Noguera and Onofrio, 2007) обычно более эхогенная, чем печень (Taylor et al., 1976), в то время как кора почек менее эхогенная, чем нормальная печень, особенно когда орган жирный (Lafortune et al., 1991; , рис. 12, ).
Рисунок 12. Анатомия и эхоструктура органов. (а) Печень, правая доля. (б) Селезенка. (c) Трансверсальное сканирование поджелудочной железы. (d) Почки.
Жир различается по своим акустическим свойствам: подкожный жир относительно гипоэхоген, тогда как жир почечных синусов, мезентериальный жир и ангиомиолипомы являются эхогенными. Воспалительный жир очень эхогенен.
Твердые узелки и образования внутри органов или в брюшной полости характеризуются внутренней эхотекстурой, демонстрируя широкий спектр проявлений в США (с точки зрения эхогенности, однородности и границ), и всегда являются патологическими образованиями (Kang and Chandarana, 2012 ). Когда внутри образования или узелка есть несколько областей разной эхогенности, их эхотекстура описывается как сплошная неоднородная (Tchelepi and Ralls, 2004). Границы могут быть гладкими и четко очерченными (признаки доброкачественности) или нерегулярными и плохо очерченными (признаки злокачественности).Неровные и плохо очерченные границы характеризуют инфильтративную эхотекстуру.
Солидные поражения внутри органа обычно представляют собой новообразование (доброкачественное или злокачественное) или гранулематозную ткань (Tchelepi and Ralls, 2004). Они могут быть гомогенными и гипоэхогенными, изоэхогенными или гиперэхогенными по сравнению с тканью, в которую они встроены. Минимальный градиент импеданса необходим для отличия гомогенного узелка от нормальной ткани (, рис. 13, ). По этой причине внутри однородного органа лучше всего различать негомогенные и смешанные (твердые и жидкие) поражения.Метастазы в печени, как правило, многоузловые и проявляют разносторонние проявления, от явных свидетельств до едва заметных проявлений инфильтрации. УЗИ с усилением контраста (Catalano et al., 2005; см. Ниже) может усилить контраст между нормальными и патологическими тканями из-за их различной микрососудистости.
Рис. 13. Метастаз в правой доле печени (стрелки). (Слева) КТ-изображение с усилением контрастности. (Справа) Ультразвуковое изображение. Карцинома поджелудочной железы.
Некоторые анатомические особенности печени, поджелудочной железы, селезенки и почек постоянны и легко представлены в УЗИ.
Печень выглядит как однородный орган серого цвета на УЗИ. Его гладкая паренхима прерывается сосудами и связками, а сама печень обеспечивает отличное акустическое окно для различных органов и крупных сосудов, расположенных в верхней части живота. Три печеночные вены соединяются с нижней полой веной при косом сканировании печени, а портальная вена разветвляется на правый и левый отделы ( Рис. 11 (c) и 11 (d) ). При продольном сканировании печени главная воротная вена видна позади печеночной артерии (медиальная) и общего желчного протока (латеральная).Интрапаренхиматозное портальное дерево исходит от ворот гепатита, где главная воротная вена входит в печень.
Общий желчный проток может быть легко продемонстрирован в его внутрипеченочной части чуть впереди и немного правее воротной вены. Внепеченочную часть протока увидеть труднее, поскольку она часто закрыта газом из двенадцатиперстной кишки. Общий желчный проток должен быть <4–7 мм в диаметре. Расширение всего желчного дерева или его части обычно является результатом непроходимости.Реже желчное дерево может быть расширено, но не закупорено. Наиболее частыми причинами обструкции являются камни в общем протоке или новообразование желчного протока или головки поджелудочной железы (Foley and Quiroz, 2007).
Нормальный желчный пузырь лучше всего визуализировать после голодания, так как он растянут. Это грушевидный орган с гиперэхогенной тонкой стенкой, содержащий анэхогенную желчь ( Рисунок 10 (c) ).
Поджелудочная железа ( Рисунок 12 (c) ) может быть трудно идентифицировать, особенно у пациентов с кишечной непроходимостью или у пациентов с ожирением.Нормальная паренхима поджелудочной железы однородна, иногда с хорошо визуализируемым тонким и линейным панкреатическим протоком. Панкреатит может привести к увеличению органа с гипоэхогенным эффектом, но это не всегда так.
Нормальная селезенка ( Рисунок 12 (b) ) имеет тонкую однородную текстуру с гладкими краями и заостренным нижним краем. Он имеет такую же эхогенность, что и печень, но у некоторых пациентов может быть слегка гипо- или гиперэхогенным. Контуры селезенки правильные, медиальная поверхность прямая или вогнутая.Происхождение селезеночной вены очерчено в гиларовой области.
Нормальная почка взрослого человека ( Рисунок 12 (d) ) представляет собой бобовидную структуру, окруженную четко выраженной гладкой эхогенной капсулой. Паренхима почки окружает центрально расположенный гиперэхогенный жировой почечный синус, который содержит почечную лоханку, чашечки, основные ветви почечной артерии и вены, а также лимфатические сосуды. Нерасширенные мочеточники, а также полости таза и чашечки не видны. Их сонографические свидетельства являются выражением дилатации и служат диагностикой непроходимости.Если непроходимость существует долго, кора почек может атрофироваться, истончаться. Таким образом, нормальная толщина коры головного мозга является хорошим прогностическим индикатором (Jeffrey and Federle, 1983; Noble and Brown, 2004).
Тазовые органы (матка, придатки, мочевой пузырь и простата) можно исследовать с помощью транспариетальных и, что еще лучше, внутриполостных зондов.
Существует несколько ограничений на выполнение полного и точного УЗИ брюшной полости. Тени от ребер и кишечные газы могут затруднить получение качественных изображений.Пациенты с ожирением и те, кому была проведена реанимация большим объемом жидкости, часто сталкиваются с такими же проблемами, как и пациенты с травмами. Наконец, визуализация более глубоких структур (например, аорты и поджелудочной железы) может быть очень сложной задачей.
Лечение рака почки (PDQ®) — версия для пациента
О PDQ
Запрос данных врача (PDQ) — это обширная база данных по раку Национального института рака (NCI). База данных PDQ содержит резюме последней опубликованной информации о профилактике, обнаружении, генетике, лечении, поддерживающей терапии, а также дополнительной и альтернативной медицине.Большинство резюме представлено в двух версиях. Версии для медицинских работников содержат подробную информацию на техническом языке. Версии для пациентов написаны на понятном нетехническом языке. Обе версии содержат точную и актуальную информацию о раке, и большинство версий также доступно на испанском языке.
PDQ — это услуга NCI. NCI является частью Национальных институтов здравоохранения (NIH). NIH — это центр биомедицинских исследований при федеральном правительстве. Обзоры PDQ основаны на независимом обзоре медицинской литературы.Это не политические заявления NCI или NIH.
Цель этого обзора
В этом обзоре информации о раке PDQ содержится текущая информация о лечении рака почек. Он предназначен для информирования и помощи пациентам, семьям и лицам, осуществляющим уход. Он не дает официальных руководящих принципов или рекомендаций для принятия решений в отношении здравоохранения.
Рецензенты и обновления
Редакционные коллегии составляют сводки информации о раке PDQ и поддерживают их в актуальном состоянии. Эти советы состоят из экспертов в области лечения рака и других специальностей, связанных с раком.Резюме регулярно пересматриваются, и в них вносятся изменения при появлении новой информации. Дата в каждой сводке («Обновлено») — это дата самого последнего изменения.
Информация в этом обзоре пациента была взята из версии для медицинских работников, которая регулярно пересматривается и обновляется по мере необходимости редакционной коллегией PDQ по лечению взрослых.
Информация о клиническом испытании
Клиническое испытание — это исследование, призванное ответить на научный вопрос, например, лучше ли одно лечение, чем другое.Испытания основаны на прошлых исследованиях и на том, что было изучено в лаборатории. Каждое испытание отвечает на определенные научные вопросы, чтобы найти новые и более эффективные способы помощи больным раком. Во время клинических испытаний лечения собирается информация об эффектах нового лечения и о том, насколько хорошо оно работает. Если клинические испытания покажут, что новое лечение лучше, чем то, что используется в настоящее время, новое лечение может стать «стандартным». Пациенты могут захотеть принять участие в клиническом исследовании.Некоторые клинические испытания открыты только для пациентов, которые еще не начали лечение.
Клинические испытания можно найти в Интернете на сайте NCI. Для получения дополнительной информации позвоните в Информационную службу рака (CIS), контактный центр NCI, по телефону 1-800-4-CANCER (1-800-422-6237).
Разрешение на использование данного обзора
PDQ является зарегистрированным товарным знаком. Содержимое документов PDQ можно свободно использовать как текст. Его нельзя идентифицировать как сводную информацию о раке NCI PDQ, если не отображается вся сводка и не обновляется регулярно.Тем не менее, пользователю будет разрешено написать предложение, например: «В сводке информации о раке PDQ NCI о профилактике рака груди указываются риски следующим образом: [включить выдержку из резюме]».
Лучший способ процитировать это резюме PDQ:
Редакционная коллегия PDQ® Adult Treatment. Лечение рака почки PDQ. Бетесда, Мэриленд: Национальный институт рака. Обновлено <ММ / ДД / ГГГГ>. Доступно по адресу: https://www.cancer.gov/types/kidney/patient/kidney-treatment-pdq. Дата обращения <ММ / ДД / ГГГГ>.[PMID: 26389448]
Изображения в этом обзоре используются с разрешения автора (ов), художника и / или издателя только для использования в обзорах PDQ. Если вы хотите использовать изображение из сводки PDQ и не используете все сводки, вы должны получить разрешение от владельца. Он не может быть предоставлен Национальным институтом рака. Информацию об использовании изображений в этом обзоре, а также многих других изображений, связанных с раком, можно найти в Visuals Online. Visuals Online — это коллекция из более чем 3000 научных изображений.
Заявление об ограничении ответственности
Информация в этом резюме не должна использоваться для принятия решений о страховом возмещении. Более подробную информацию о страховом покрытии можно найти на сайте Cancer.gov на странице «Управление онкологическими услугами».
Свяжитесь с нами
Более подробную информацию о том, как связаться с нами или получить помощь на веб-сайте Cancer.gov, можно найти на нашей странице «Свяжитесь с нами для получения помощи». Вопросы также можно отправить на Cancer.gov через электронную почту веб-сайта.
Три клинических случая с обзором литературы
Введение
Опухоли, возникающие из почечного синуса, встречаются редко.К насколько нам известно, только три случая опухолей, возникших в результате о почечных синусах до настоящего времени сообщалось в литературе (1–3). В 1999, Амин и др. (1) сообщили о первом известном случае опухоли почечного синуса с патология миелолипомы. Гемангиомы, липосаркомы и были обнаружены миелолипомы, происходящие из почечного синуса. Этот В отчете представлены три случая опухолей почечного синуса: ангиолейомиома, ангиомиолипома и липома соответственно. В настоящее время они трудно диагностировать только с помощью изображений, когда они происходят из это местоположение и биопсия не могут дать однозначного ответа.Варианты лечения включают как консервативные, так и хирургические методы лечения. подходы в зависимости от достоверности диагноза, прогрессирование симптомов пациента и признаки роста. Письменное информированное согласие было получено от всех пациентов.
Сообщения о случаях болезни
Корпус 1
33-летний мужчина представлен на месторождении Шэнли. Центральная больница (Дунъин, Китай) с болью в правом боку на 6 человек. месяцы. Ультрасонографическое наблюдение продемонстрировало измерение массы ~ 3,5 см в диаметре в правом почечном синусе.Компьютеризированная томография (КТ) брюшной полости показала отсутствие улучшения, однородная, гладкая и явная масса размером ~ 3,5 × 3,7 × 3,0 см размером (рис.1). На основе По результатам компьютерной томографии у пациента диагностирован тазовый опухоль. Внутривенная урография (ВВУ) показала, что правая почечная лоханка и почечная чашечка были сдавлены, но дефект наполнения был не наблюдается в почечной лоханке. Все эти изменения предполагали, что опухоль могла возникнуть из правой почечной лоханки. Проведено хирургическое исследование опухоли почечного синуса.An масса сущности, которая была хорошо описана и имела диаметр ~ 3,5 см, была расположен в почечном синусе и прикреплен к почечной капсуле и таз. Исследование замороженного среза ткани показало, что опухоль была доброкачественной и возникла из мезенхимальной ткани. Произведена радикальная резекция новообразования и нормальной почки. ткани остались. По результатам послеоперационной патологии выявлено, что опухоль была четко ограничена с хорошо дифференцированной гладкой мускулатурой клетки и толстостенные сосуды. Иммуногистохимический анализ показали положительное окрашивание на виментин, актин гладких мышц, актин, CD34 и отрицательное окрашивание на Des, S-100 и нейрон-специфическое энолаза.Пациенту был поставлен диагноз ангиолейомиома в связи с результаты патологии. Наблюдение за пациентом составляло 3 года. не продемонстрировал рецидивов или каких-либо других связанных с этим проблем с этим поражением.
Корпус 2
34-летнюю женщину направили на нефтяное месторождение Шэнли. Центральная больница из-за внезапного прострела правого фланга с макрогематурия в течение 3 дней 25 июля 2007 г. Правый верхний бок. наблюдалась болезненность и перкуторная боль в правой почке во время физического осмотра.Результаты ультразвукового исследования правая почка демонстрирует гиперэхогенное образование в правой почке. sinus размером ~ 8,4 × 5,5 × 8,5 см. Овал и масса с низким затуханием со значением CT −70 HU в правой почке пазуха была идентифицирована на КТ размером ~ 8 × 6 × 8 см. Увеличивающаяся неоднородная масса, расположенная в правой почке. (Рис.2), правая почечная капсула утолщение, низкая плотность и субкапсулярная масса наблюдались в КТ с контрастным усилением. Результаты IVU показали, что нижний коллектив система была сдавлена без дефектов заполнения правой почки таз (рис.3). Левая почечная функция была хорошей, хотя сопровождалась задержкой развития правой почки улучшение. У пациента диагностирована ангиомиолипома почек. выполнена резекция правой почки и опухоли правой почки. В опухоль, прикрепленная к окружающим тканям, имела диаметр ~ 8 см и была расположен в правом почечном синусе. Пациент прошел правую иссечение почки из-за неконтролируемого диффузного кровотечения и повреждения правую почечную лоханку восстановить не удалось. Послеоперационный отчеты о патологии подтвердили диагноз ангиомиолипома правая почка.Пациент имел хорошее физическое состояние и покинул больницу через 7 дней. Пациент находился под наблюдением в течение 10 месяцев, рецидивов и метастазов не было.
Корпус 3
Женщина 55 лет поступила во вторую больницу. Тяньцзиньского медицинского университета (Тяньцзинь, Китай) с люмбаго в левый фланг, который продержался 1 год. На физическом При осмотре болезненности в левом боку не было. B-режим Ультрасонография показала гиперэхогенные поражения в воротах левой почки.КТ брюшной полости с контрастным усилением показала отсутствие усиления, однородная и очевидная масса в левом почечном синусе, измеряющая Размером 8 × 5 × 5 см со значением CT от −50 HU до −35 HU (Рис.4). Результаты IVU показали Коллективная система левой почки была сдавлена. Магнитный резонансная томография (МРТ) показала высокий сигнал на изображении, взвешенном по Т1 (T1WI) и T2WI, но низкий сигнал при визуализации подавления жира (Рис. 5). Пациенту поставлен диагноз при липоме левого почечного синуса. Была выполнена леворадикальная нефрэктомия. выполнено.Все опухоли сформировали твердую, большую, гладкую и очевидную форму. масса. Поверхность среза опухоли была желтой. Послеоперационный патологические отчеты подтвердили диагноз липома левой почечный синус. Наблюдение за пациентом составляло 4 года. не выявлено рецидивов.
Обсуждение
Почечный синус — это полость внутри почки. содержащие таз и чашечки, жировую ткань, сосуды почек, нервы и лимфатические ткани, и является продолжением почечной хилум. Типы опухолевых тканей в почечном синусе обширны, включая жировую, лимфатическую, нервную и сосудистую ткани.Липомы и липосаркомы происходят из жировой ткани, болезни Кастлемана и лимфомы происходят из лимфатической ткани, опухолей ганглиозных клеток происходят из нервной ткани, а ангиолейомиома и гемангиоперицитомы происходят из сосудистой ткани (4,5).
Опухоли, возникающие из почечного синуса, встречаются редко и две трети таких опухолей доброкачественные (6). Самый распространенный тип возникающих опухолей из почечного синуса — липома (7,8). Предыдущие исследования показали, что исключительный дифференциал Диагностика поражений или поражений ворот почек включает: гемангиома, ангиомиолипома, лейомиома, миелоидная липома, Кастлмана болезнь и опухоли Массона (7,9–11).Злокачественные опухоли, такие как липосаркома, неходжкинская лимфома и Иногда сообщалось о злокачественных параганглиомах (12–14).
В силу ассоциации жировой ткани, методы визуализации, такие как КТ и МРТ, могут преувеличивать внутренние усиление или низкое затухание и, следовательно, может настоятельно рекомендовать диагностика опухолей почечных синусов. Одновременно диагностика почечной опухоли носовых пазух в основном зависят от результатов визуализации. Ультразвуковая эхография выявляет занимающие поражения или кровеносные сосуды.КТ или МРТ используется для оценки стадии развития и инвазивного диапазона новообразование. Мультидетекторный КТ обеспечивает более быстрый анализ благодаря более тонкий слой сканирования и более высокое пространственное разрешение (15). Кроме того, трехмерный реконструктивная компьютерная томография может более точно определить поражения в объем сложных поражений почечных пазух по сравнению с другими методы визуализации. КТ-признаки первичных опухолей почечного синуса: следующим образом: i) обычно располагается в почечном синусе, а почечная паренхима и лоханка могут быть поражены злокачественной опухолью; ii) очевидная граница между опухолями и почечным коллективом система, с часто сдавленным тазом и чашечками, и более легкий почечный сифон; iii) усиленное КТ-сканирование демонстрирует сдавленные сосуды, расположенные в воротах почек и iv) период экскреции усиленной КТ выявляет сжатие почек таз и чашечка без дефектов наполнения (16–18).МРТ имеет больше преимуществ, чем КТ в выявлении инвазии. почечной вены и нижней полой вены. Эта техника может быть используется у пациентов с почечной недостаточностью и у пациентов с аллергией с использованием контрастных веществ. IVU также может использоваться для оценки того, опухоль повлияла на собирательную систему почек и почки функция. Первичные новообразования почечных синусов часто сопровождаются сжатая система сбора (19–21). Отсутствие дефектов наполнения таза и чашечек может быть используется для выявления первичной опухоли почечной лоханки.Это было предположили, что злокачественные опухоли сопровождают почечную лоханку нарушение, когда система сбора почек нерегулярна (22,23). Один пациент в настоящем исследовании был диагностирована опухоль почечной лоханки, которая, как предполагалось, имела происходит из почечного синуса и без наполнения почечной лоханки дефект. Комбинированное применение ВВУ, КТ и МРТ может повысить частоту диагностики (15). Трудно получить качественный диагноз почечного синуса. опухоли, в то время как ангиолейомиомы и ангиомиолипомы заметно усиленный (11).В настоящее время в исследовании у двух пациентов была диагностирована ангиомиолипома почечного синуса. у одного была диагностирована липома по внешнему виду жировой ткани и значения CT (примерно -70 и -50 HU, соответственно).
Клинические проявления опухолей почечных синусов. неспецифичны; ряд пациентов с люмбаго и немного пациентов с гематурией и инфекциями мочевыводящих путей (24–26). Симптомы появляются, когда диаметр опухоль> 4 см. Гематурия наблюдалась, когда опухоль была больше и сопровождалась поражением почечной лоханки.К насколько нам известно, никаких симптомов доброкачественных опухолей не выявлено. наблюдается при диаметре опухоли <4 см; следовательно, до появления почечного сифона операция не требуется. Опухоли с явными симптомами и диаметром> 4 см должны быть резецированный. В настоящих трех случаях мы сохранили почку как насколько это возможно, во время операции из трех зарегистрированных случаев. Ранее сообщавшиеся новообразования требовали резекции почки, когда диаметр был> 7 см, особенно доброкачественные опухоли, которые занимали весь синус почки (27).в В настоящем исследовании два случая продемонстрировали одно и то же состояние; опухоль диаметр был> 7 см и занимал всю почечную пазуху, с вовлечением почечной лоханки или с серьезным спаечением. Следовательно, выполнена нефрэктомия. Опухоли почечного синуса останутся недиагностированный, если только возможность гемангиомы через чрескожный или интраоперационная биопсия исключена (2). В текущем исследовании один пациент был диагностирована доброкачественная опухоль на основании интраоперационной биопсии результаты и иссечение опухоли, одновременно сохранение почки.Поэтому рекомендуется хирургическое исследование. прежде чем исключить возможность опухоли почечного синуса, чтобы чтобы избежать ненужной нефрэктомии. Злокачественные опухоли почечного синуса, особенно тем, у кого нарушение паренхимы почек, следует пройти радикальную нефрэктомию с удалением почек одновременно с опухолевыми эмболами (3).
Таким образом, первичные опухоли почечного синуса являются редко и большинство из них доброкачественные, но часто ошибочно диагностируются как рак лоханки почек. Прогноз при опухолях почечного синуса: хорошо.КТ, МРТ и анализ ВВУ имеют большое значение для ориентации и качественная диагностика опухолей почечных синусов. Лечение подходы, однако, могут быть установлены путем сопоставления клинических симптомы, размер и характер опухоли. Сохранение почки во время хирургическое вмешательство, насколько это возможно, является ключом к лечению пациентов при опухолях почечных синусов.
Список литературы
|
1 |
Амин М.Б., Тикоо С.К. и Шульц Д. Миелолипома почечного синуса: необычное место для редкого экстра-надпочечниковое поражение.Arch Pathol Lab Med. 123: 631–634. 1999 г., PubMed / NCBI |
|
2 |
Гупта Н.П., Кумар П., Гоэль Р. и Динда А.К .: Гемангиома почечного синуса, имитирующая образование почек: диагностика вызов. Int Urol Nephrol. 36: 485–487. 2004. Просмотр статьи: Google Scholar |
|
3 |
Мацусита М, Ито А, Исидоя С, Эндох М, Мория Т. и Араи Y: Внутривенная расширенная липосаркома, возникающая из-за почечный синус.Int J Urol. 14: 769–770. 2007. Просмотр статьи: Google Scholar: PubMed / NCBI |
|
4 |
Аказа Х, Койсо К. и Нийдзима Т: Клинические оценка уротелиальных опухолей почечной лоханки и мочеточника на основе новой системы классификации. Рак. 59: 1369–1375. 1987 г. Просмотр статьи: Google Scholar: PubMed / NCBI |
|
5 |
Mazairac AH и Joles JA: Почечный синус ожирение и гипертония.Гипертония. 56: 814–815. 2010 г. Просмотр статьи: Google Scholar: PubMed / NCBI |
|
6 |
Лопес-Бельтран А, Скарпелли М, Монтирони Р и Kirkali Z: 2004 классификация ВОЗ почечных опухолей Взрослые. Eur Urol. 49: 798–805. 2006. Просмотр статьи: Google Scholar: PubMed / NCBI |
|
7 |
Metro MJ, Ramchandani P, Banner MP и др.: Ангиомиолипома почечного синуса: диагностика чрескожно биопсия.Урология. 55: 2862000. Просмотр статьи: Google Scholar |
|
8 |
Diamond A, Kodroff M и Ravitz G: Renal ангиомиолипома пазухи. Урология. 9: 221–223. 1977 г. Просмотреть статью: Google Scholar: PubMed / NCBI |
|
9 |
Каркамо Валор П., Мартинес-Пиньейро Х.А., Лопес-Тельо Дж., Пикасо Гарсия М. и Контрерас Рубио Ф .: Гемангиоперицитома почечного синуса: случай и обзор литературы.Arch Esp Urol. 49: 944–949. 1996. (на испанском языке). PubMed / NCBI |
|
10 |
Ёсида М., Иноуэ С., Янагисава Р., Киши Х. и Takahashi M: случай множественной лейомиомы почек, расположенной в почечный синус и ворот. Hinyokika Kiyo. 36: 937–940. 1990. (В Японский). PubMed / NCBI |
|
11 |
Джораку А., Миянага Н., Секидо Н. и др.: А. случай внутрисосудистой папиллярной гиперплазии эндотелия (Masson’s опухоль), возникающая из почечного синуса.Jpn J Clin Oncol. 27: 433–436. 1997. Просмотр статьи: Google Scholar |
|
12 |
Симадзуи Т., Нутахара К., Исии И. и Хорибе Y: Случай злокачественной параганглиомы в почечном синусе. Hinyokika Kiyo. 31: 2027–2033. 1985. (на японском языке). PubMed / NCBI |
|
13 |
Хонда Х, Лу СС, Франкен Е.А. младший, Бонсиб С.М., Yuh WT и Williams RD: Злокачественная лимфома почечного синуса: случай отчет.J Comput Tomogr. 12: 190–192. 1988. Просмотр статьи: Google Scholar: PubMed / NCBI |
|
14 |
Яман О, Сойгюр Т., Озер Дж., Арикан Н. и Яман Л.С.: Почечная липосаркома почечного синуса. Int Urol Nephrol. 28: 477–480. 1996. Просмотреть статью: Google Scholar: PubMed / NCBI |
|
15 |
Чаабуни М.Н. и Мхири М.Н.: Псевдотуморальные липоматоз почечного синуса. Анн Урол (Париж). 27: 93–96.1993. (на французском языке). |
|
16 |
Катабатина В.С., Викрам Р., Нагар А.М., Tamboli P, Menias CO и Prasad SR: Мезенхимальные новообразования почки у взрослых: спектр изображений с рентгенологически-патологическими корреляция. Рентгенография. 30: 1525–1540. 2010. Просмотр статьи: Google Scholar: PubMed / NCBI |
|
17 |
Древняк Т, Жепецки М, Ющак К, Moczulski Z, Reczyńska K и Jakubowska M: Методология и оценка почечной артериальной системы.Cent European J Urol. 66: 152–157. 2013. |
|
18 |
Шетти А. и Адият К.Т.: Сравнение между спиральная компьютерная томография, ангиография и интраоперационная Выводы. Urol Ann. 6: 192–197. 2014. Просмотреть статью: Google Scholar: PubMed / NCBI |
|
19 |
Карвалью Дж. К., Томас Д. Дж., МакХью Дж. Б., Шах РБ и Kunju LP: p63, CK7, PAX8 и INI-1: оптимальный иммуногистохимическая панель для распознавания слабодифференцированных уротелиально-клеточная карцинома из высокодифференцированных опухолей почек система сбора.Гистопатология. 60: 597–608. 2012. Просмотр статьи: Google Scholar: PubMed / NCBI |
|
20 |
Камат А., Розенкранц А.Б. и Босняк М.А.: Результаты МРТ ангиомиолипомы почечного синуса в 5 случаях. J Comput Assist Tomogr. 34: 915–920. 2010. Просмотр статьи: Google Scholar: PubMed / NCBI |
|
21 |
Мох Х., Артибани В., Делахант Б., Фикарра В., Knuechel R, Montorsi F, Patard JJ, Stief CG, Sulser T и Wild PJ: Переоценка текущей стадии UICC / AJCC TNM для почечных клеток карцинома.Eur Urol. 56: 636–643. 2009. Просмотр статьи: Google Scholar: PubMed / NCBI |
|
22 |
Кузака П., Пастевка К., Фарина Дж., Кузака Б., Pypno W и Wejman J: Вложенный вариант уротелиальной карциномы почечная лоханка — история болезни. Pol J Pathol. 65: 74–77. 2014 г. Просмотр статьи: Google Scholar: PubMed / NCBI |
|
23 |
Lin Z, Chng JK, Chong TT и Soo KC: почечная плоскоклеточный рак таза с нижней полой веной проникновение: отчет о болезни и обзор литературы.Int J Surg Case Rep. 5: 444–447. 2014. Просмотреть статью: Google Scholar: PubMed / NCBI |
|
24 |
He YF, Chen J, Xu WQ, Ji CS, Du JP, Luo HQ и Ху Б.: Отчет о болезни. Метастатический почечно-клеточный рак слева гайморовая пазуха. Genet Mol Res. 13: 7465–7469. 2014. Просмотреть статью: Google Scholar: PubMed / NCBI |
|
25 |
Амбросио М.Р., Рокка Б.Дж., Онорати М., Беллан C, Barbanti G, del Vecchio MT и Tripodi S: Почечный синус псевдолимфома у пациента с множественными карциномами: описание случая и краткий обзор литературы.Histol Histopathol. 27: 1327–1332. 2012.PubMed / NCBI |
|
26 |
Широтаке С., Ёсимура I, Косака Т. и Мацузаки С.: Случай ангиомиолипомы почечного синуса. Clin Exp Нефрол. 15: 953–956. 2011. Просмотр статьи: Google Scholar: PubMed / NCBI |
|
27 |
Чой Ю.Дж., Хван Т.К., Кан С.Дж., Ким Б.К. и Шим С.И.: Гемангиоперицитома почечного синуса, распространяющаяся на почки. hilum: необычное представление вызывает неправильное толкование как переходно-клеточная карцинома.J Korean Med Sci. 11: 351–355. 1996 г. Просмотр статьи: Google Scholar: PubMed / NCBI |
Гранулематоз с полиангиитом — Симптомы и причины
Обзор
Гранулематоз с полиангиитом — это необычное заболевание, которое вызывает воспаление кровеносных сосудов носа, пазух, горла, легких и почек.
Ранее называвшееся гранулематозом Вегенера, это состояние относится к группе заболеваний кровеносных сосудов, называемых васкулитом.Он замедляет приток крови к некоторым вашим органам. В пораженных тканях могут образовываться очаги воспаления, называемые гранулемами, которые могут повлиять на работу этих органов.
Ранняя диагностика и лечение гранулематоза с полиангиитом могут привести к полному выздоровлению. Без лечения состояние может быть фатальным.
Продукты и услуги
Показать больше товаров от Mayo ClinicСимптомы
Признаки и симптомы гранулематоза с полиангиитом могут развиваться внезапно или в течение нескольких месяцев.Первые тревожные признаки обычно связаны с пазухами, горлом или легкими. Состояние часто быстро ухудшается, поражая кровеносные сосуды и органы, которые они снабжают, например, почки.
Признаки и симптомы гранулематоза с полиангиитом могут включать:
- Гнойный дренаж с корками из носа, заложенностью, инфекциями носовых пазух и носовыми кровотечениями
- Кашель, иногда с кровавой мокротой
- Одышка или хрипы
- Лихорадка
- Усталость
- Боль в суставах
- Онемение конечностей, пальцев рук и ног
- Похудание
- Кровь в моче
- Кожные язвы, синяки или сыпь
- Покраснение, жжение или боль в глазах и проблемы со зрением
- Воспаление уха и проблемы со слухом
У некоторых людей болезнь поражает только легкие.При поражении почек проблема может быть обнаружена с помощью анализов крови и мочи. Без лечения может развиться почечная или легочная недостаточность.
Когда обращаться к врачу
Обратитесь к врачу, если у вас насморк, который не поддается лечению безрецептурными лекарствами от простуды, особенно если он сопровождается кровотечением из носа и гнойным материалом, кашлем с кровью или другими предупреждениями. признаки гранулематоза при полиангиите. Поскольку это заболевание может быстро ухудшиться, ранняя диагностика является ключом к эффективному лечению.
Причины
Причина гранулематоза с полиангиитом неизвестна. Это не заразно, и нет никаких доказательств того, что оно передается по наследству.
Состояние может привести к воспалению, сужению кровеносных сосудов и вредным воспалительным массам ткани (гранулемам). Гранулемы могут разрушать нормальные ткани, а суженные кровеносные сосуды уменьшают количество крови и кислорода, которые достигают тканей и органов вашего тела.

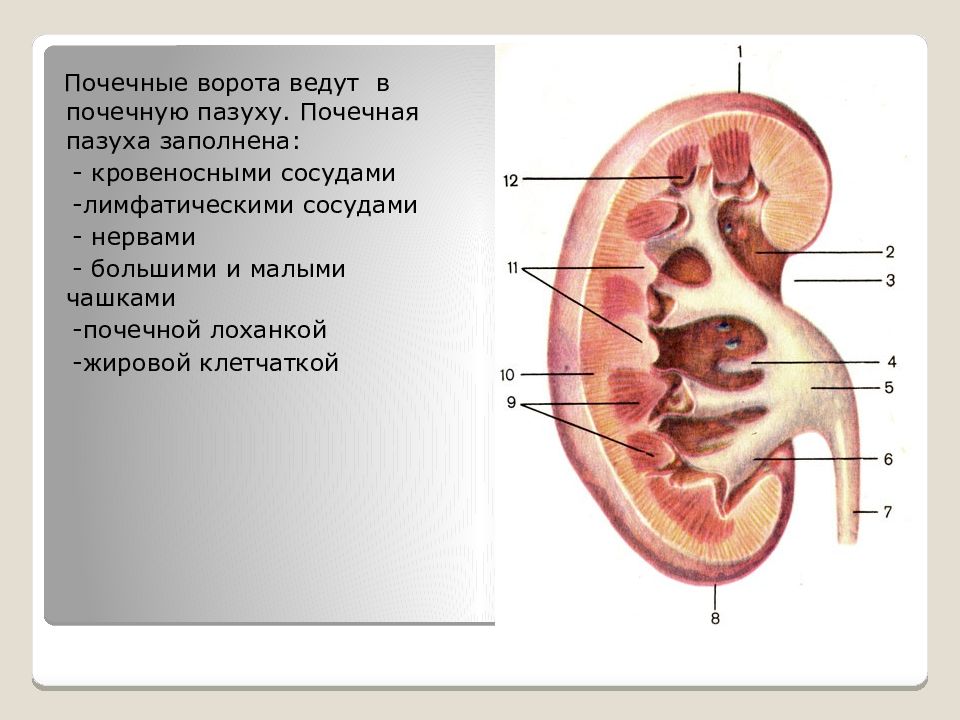 Они возникают во время развития зачатков почек из-за генных мутаций, а их диагностика происходит в детском возрасте.
Они возникают во время развития зачатков почек из-за генных мутаций, а их диагностика происходит в детском возрасте.