Перелом кости, остеосинтез, сращение перелома
Мы с детства знаем, что переломы заживают самостоятельно, стоит только зафиксировать поврежденную часть тела на некоторое время. Как же протекает процесс сращения перелома?
Воссоединение фрагментов кости заключается в трёх этапах:
1. Образование гематомы. Протекает до 2 недель.
В кости присутствуют сосуды, которые рвутся во время перелома. Кровь из них вытекает, сворачивается и образует гематому. Это и является ключевым фактором запуска процесса заживления.
На данном этапе важно зафиксировать фрагменты кости пострадашего. В «простых» случаях это делается с помощью внешнего ортеза – гипсовых, полимерных повязок и фиксаторов.
Если фрагменты кости невозможно закрепить в правильном положении без непосредственного доступа к месту перелома, то проводится операция остеосинтеза. Это «сборка» кости или сустава с помощью фиксирующих конструкций, устанавливаемых непосредственно на поврежденную кость и ее фрагменты.
2. Мягкая мозоль. Протекает до 6 недель.
Гематома создаёт подходящую среду для созревания мягкой костной мозоли. Она строится из нитей соединительной ткани и новых мельчайших сосудов.
3. Твердая мозоль и успешное восстановление кости. Протекает до 12 недель
Постепенно мягкая мозоль наполняется основными строительными клетками костной ткани – остеобластами. Плотность и твердость соединительной ткани увеличивается, ее нити сплетаются туже.
Когда перелом не срастается
К сожалению, бывают переломы, которые не срастаются без дополнительной медицинской помощи. По статистике количество таких травм достигает 10%.
В группу риска попадают люди старше 55 лет, страдающие сахарным диабетом, принимающие нестероидные противовоспалительные препараты. И, конечно, обладатели различных дегенеративных и дистрофических заболеваний костной системы (остеопороза, артритов, артроза и т.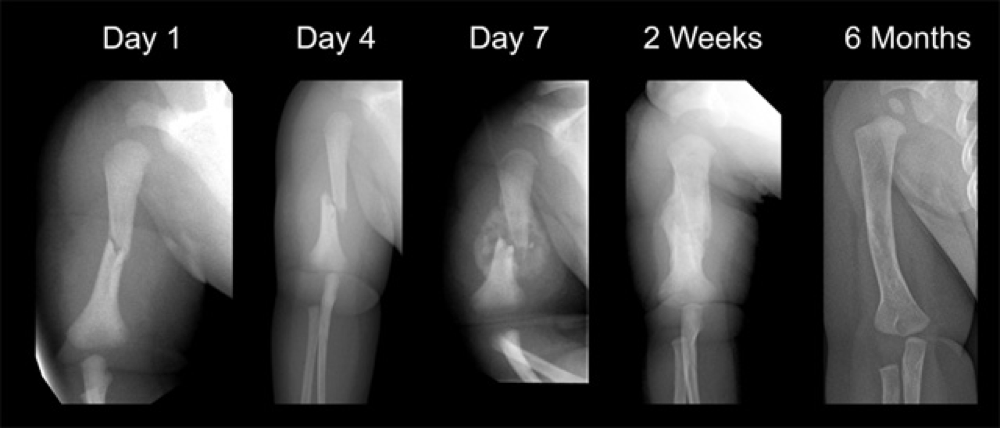
Прямыми причинами того, что кость не срастается, могут быть нарушения в процессе регенерации костной ткани – недостаточное образование отека и гематомы, слабый рост новых сосудов, не созревает соединительная ткань.
В зависимости от этих причин подбирается адекватное лечение. Однако, первым этапом становится остеосинтез. С помощью хирургического вмешательства задается правильное и более плотное расположение фрагментов, при необходимости дополнительная костная ткань берется из здоровой кости.
Клиника «Линия жизни» специализируется на лечении сложных переломов хирургическим способом.
Несращение кости реабилитация и восстановление| МЦ «Аватаж»
Несращение кости или правильнее говорить замедленная консолидация переломов – не такое уже и редкое заболевание в век урбанизации и научно-технического прогресса. Зачастую, являясь последствием перелома, несращение кости приводит к тому, что человек становиться инвалидом.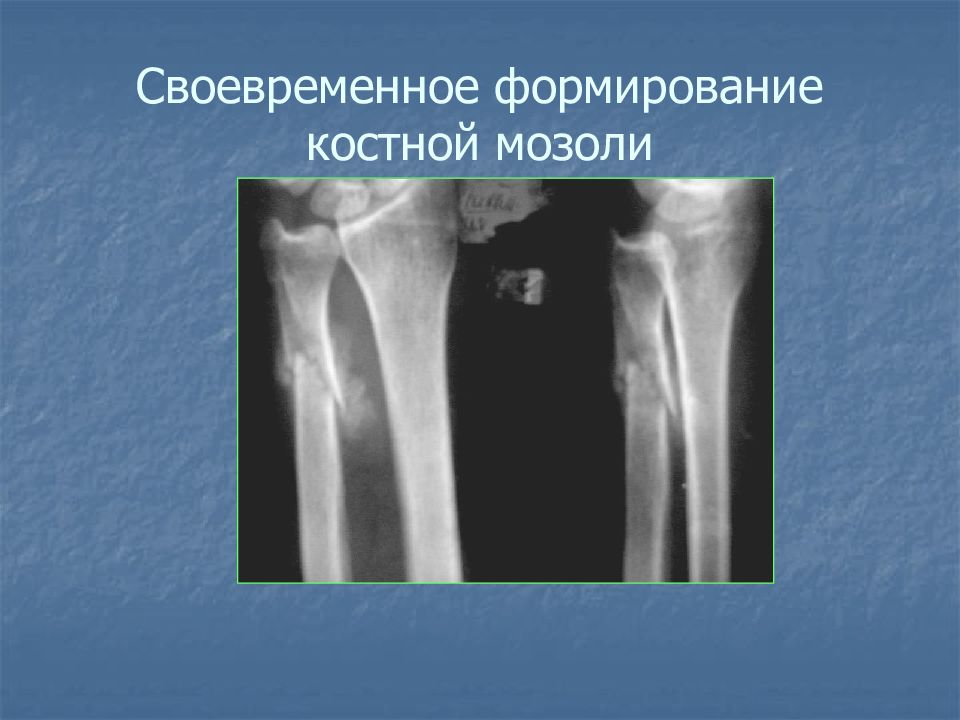 При этом радикально изменяется жизнь человека, а иногда, пострадавший рискует надолго быть прикованным к костылям и даже к постели.
При этом радикально изменяется жизнь человека, а иногда, пострадавший рискует надолго быть прикованным к костылям и даже к постели.
Замедленная консолидация перелома что это?
Что такое замедленная консолидация переломов (несращение кости). Большинство переломов костей срастается (консолидируется) через 3-6 месяцев. Если перелом к этому сроку не зажил, то врачи говорят о замедленной консолидации перелома или замедленном сращении перелома. Псевдоартроз (ложный сустав, несросшийся перелом) являются осложнением перелома кости, когда происходит прерывание процесса заживления перелома. Между основными фрагментами перелома образуется фиброзная или хрящевая ткань и поэтому даже через 6-8 месяцев не возникает образования костной мазоли и заживления перелома.
Причинами возникновения замедленной консолидации переломов и, соответственно, несращения перлома кости, и псевдоартроза являются:
- чрезмерная подвижность вследствие неадекватной иммобилизации при переломе костей,
- наличие щели между фрагментами поврежденной кости
- оскольчатые переломы,
- нарушение кровоснабжения участка перелома,
- инфекция в области перелома
- длительный прием стероидных гормонов,
- сопутствующие системные заболевания, такие как сахарный диабет, сосудистые заболевания конечностей.

Практически всегда требуется оперативное лечение при оскольчатых переломах, переломах со смещением, открытых переломах. Без этого не обойтись. Однако, после операций частым осложнением является замедленная консолидация перелома, а иногда происходит образование псевдоартроза. Для лечения этих состояний приходилось прибегать к повторным операциям, что не гарантировало сращения кости. Больные могли по несколько лет передвигаться на костылях и постоянно прибегать к посторонней помощи. Процент операций, осложненных замедленной консолидацией по данным некоторых авторов составляет до 25%.
Лечебные мероприятия при переломах костей следующие репозиции (правильное сопоставление отломков) и прочной фиксации отломков на весь период срастания. Без фиксации отломков сращение кости не произойдет.
нередким осложнением даже после операции.
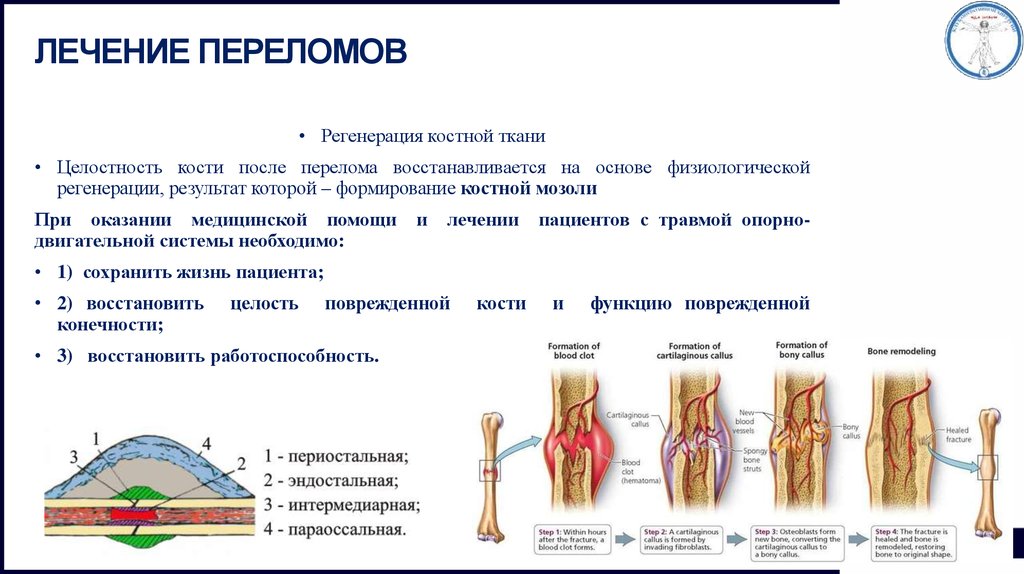 Даже надежная фиксация отломков кости при помощи внутренних и внешних металических конструкций не достигает цели и не происходит сращение кости. Травматологи в этих случаях предлагают повторные операции с пересадкой костного лоскута из подвздошной кости в место перелома. Но и в этом случае имеется высокая вероятность, что кость не сростеться. Несращение кости – и пациенты ходят на костылях или вообще лишены возможности передвижения. Исходя из чего необходимо совершенствовать и внедрять в практику новые методы лечения.
Даже надежная фиксация отломков кости при помощи внутренних и внешних металических конструкций не достигает цели и не происходит сращение кости. Травматологи в этих случаях предлагают повторные операции с пересадкой костного лоскута из подвздошной кости в место перелома. Но и в этом случае имеется высокая вероятность, что кость не сростеться. Несращение кости – и пациенты ходят на костылях или вообще лишены возможности передвижения. Исходя из чего необходимо совершенствовать и внедрять в практику новые методы лечения.Какой же выход? Что нового в лечении и реабилитации переломов?
Как оказывается он есть! В последнее время появилось эфективное решение этой проблемы – это ударно-волновая терапия, действительно уникальный метод лечения несросшихся переломов, псевдоартрозов. За 10 лет лечения ЗКП специалисты МЦ “Аватаж” разработали собственную методику лечения замедленной консолидации переломов и псевдоартрозов с использованием оборудования Storz Medical, которая былы запатентована. По нашим данным эффективность такого лечения составляет 100%. Все пациенты, обратившиеся к нам в центр были выписаны с выздоровлением – образованием костной мозоли.
По нашим данным эффективность такого лечения составляет 100%. Все пациенты, обратившиеся к нам в центр были выписаны с выздоровлением – образованием костной мозоли.
В чем уникальность ударно-волновой терапии при несращении кости?
Ударная волна воздействуя на ткани приводит к стимуляции ангиогенеза (единственный метод в медицине!). В область травмы увеличивается приток питательных веществ и кислорода. Происходит ускорение заживления ткани. При воздействии на кость происходит активация остеобластов, которые начинают синтез костной ткани. Как следствие воздействия ударно-волновой терапии на область перелома возникает образование костной мозоли и сращение кости.
 Все они получили сращение кости. 12 лет собственного опыта в лечении переломов и сотрудничество с ведущими кафедрами травматологии и ортопедии в Украине позволили создать свои методики лечения и профилактики замедленной консолидации переломов и псевдоартрозов.
Все они получили сращение кости. 12 лет собственного опыта в лечении переломов и сотрудничество с ведущими кафедрами травматологии и ортопедии в Украине позволили создать свои методики лечения и профилактики замедленной консолидации переломов и псевдоартрозов.Как проводиться процедура ударно-волновой терапии при лечении замедленной консолидации перелома?
При замедленной консолидации перелома (несращение кости) процедура проводиться с частотой 1 раз в 7-10 дней. В медицинском центре Аватаж врачи применяют специальные насадки, стимулирующие образование костной мозоли (стимулируют остеогенез). Воздействие производится в область перелома. Врачи медицинского центра “Аватаж” применяют собственные запатентованные методики лечения и профилактики замедленной консолидации перелома, базирующиеся на использовании оборудования Storz Medical.
Как говорил знаменитый ученый профессор Г. Илизаров: “Напряжение в растяжении является могучим фактором, активизирующим рост тканей. Согласно этой закономерности можно возбуждать образование новых структурных единиц фиброзной ткани, сосудов, кожи, костей”.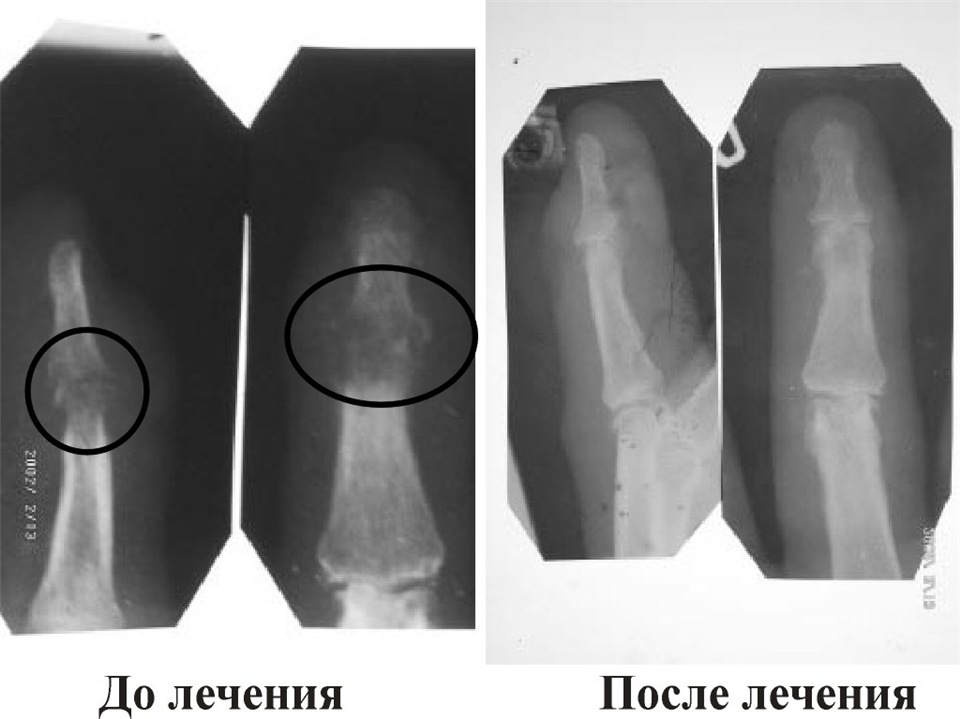
Примеры результатов лечения и реабилитации несросшегося перелома.
За последний несколько последних лет с диагнозом замедленная консолидация перелома и псевдоартроз пролечилось более 180 пациентов. У всех лечение завершилось образованием костной мозоли. Были и такие пациенты, у которых перелом не срастался несколько лет. У таких пациентов также наступило образование костной мозоли после проведения курса ударно-волновой терапии с использованием запатентованной методики Аватаж и современного оборудования Storz Medical.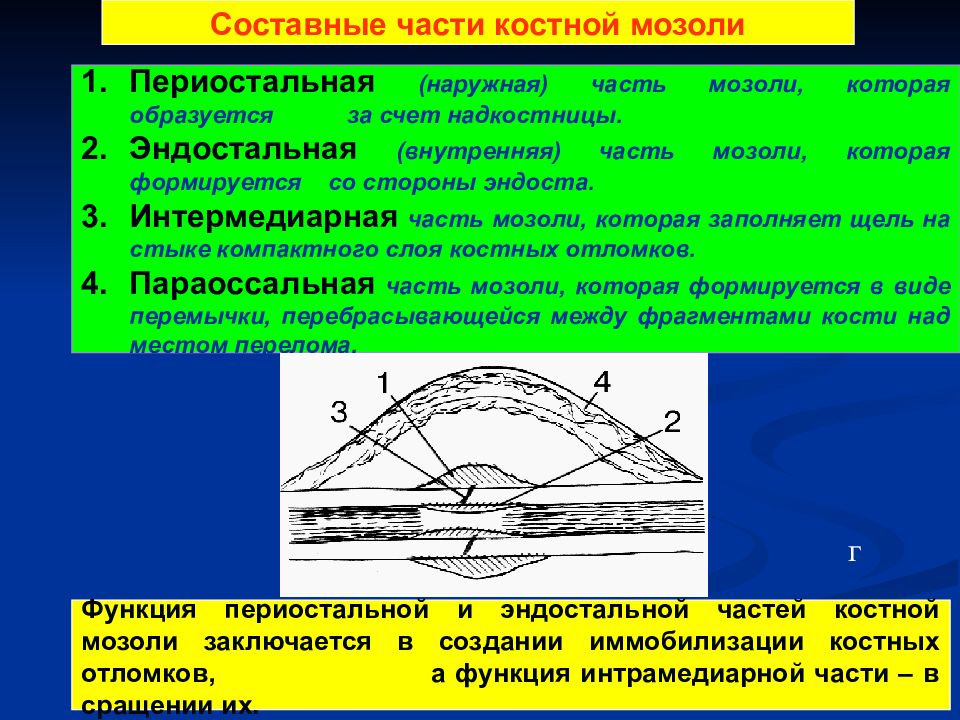
Пациент Р.
Осколчатый закрытый перелом левой плечевой кости с замедленной консолидацией перелома и контрактурой левого плечевого сустава. Пациент отказался от оперативного лечение и в течение 5 месяцев проходил амбулаторное лечение. Признаков сращения кости не наблюдалось. Пациент был направлен на реабилитацию в МЦ “Аватаж”. Было проведен курс реабилитации с использованием УВТ, биомеханической стимуляции мышц, кинезиотерапии, миостимуляции. Результат – полная консолидация перелома, уменьшение оли и восстановление объема движений в плече спустя 1,5 месяца после начала курса восстановления.
|
Перелом плечевой кости. Замедленная консолидация перелома. Видны отломки кости, которые смещены. Снимок – до лечения |
Сращение костных обломков у пациентов с оскольчатым переломом плечевой кости после прохождения курса лечения. |
Пациентка П.,
Сложный перелом обеих костей предплечья, была проведена операция фиксации отломков костей, с помощью пластин.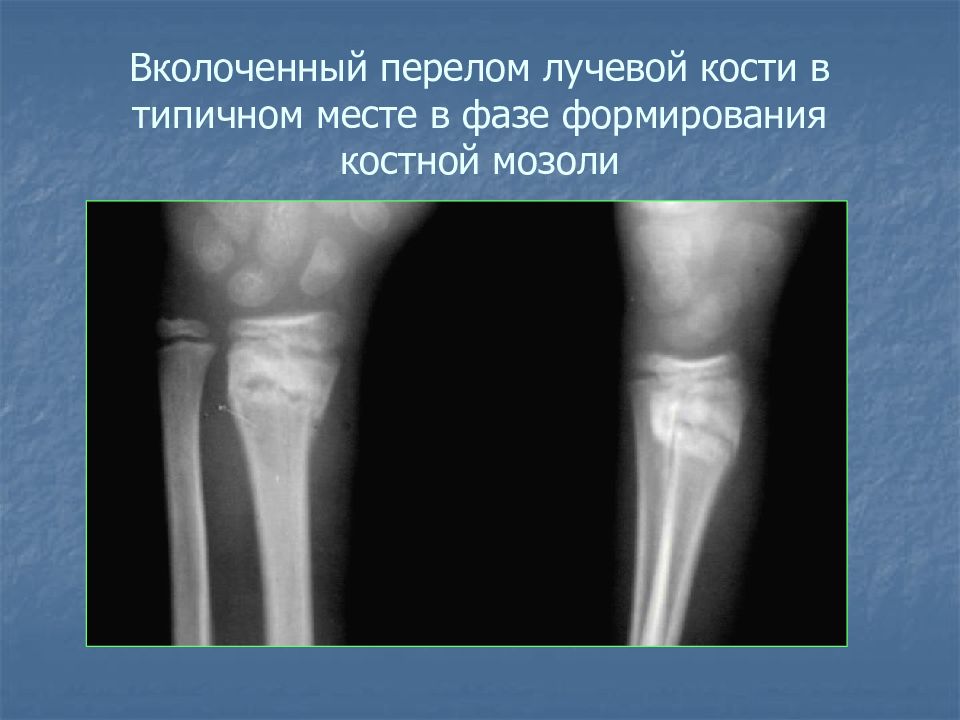 В течение последующего года кости не срастались. Пациентке было рекомендовано пройти курс радиальной ударно-волновой терапии. Было проведено 6 сеансов УВТ с интервалом в 1 неделю.
В течение последующего года кости не срастались. Пациентке было рекомендовано пройти курс радиальной ударно-волновой терапии. Было проведено 6 сеансов УВТ с интервалом в 1 неделю.
Замедленная консолидация перелома. Снимок до проведения радиальной ударно-волновой терапии, стрелками указаны места перелома. Кость несрасталась в течение 10 месяцев. |
Образование костной мозоли(сращение кости) после проведения 6 сеансов ударно-волновой терапии. На снимке видно уплотнение костной ткани и исчезновение перелома. |
Пример 2.
Замедленная консолидация перелома. Опреативная стабилизация отломков не была проведена. в течение 8 месяцев сращения кости не было. После 5 сеансов ударно-волновой терапии наблюдается сращение кости.
Незаживающий перелом, долечения УВТ. |
Образование костной мозоли после 5 сеансов УВТ, |
Пример 3 . Пациент с диагнозом: Открытый огнестрельный перелом нижней трети правой большеберцовой кости со смещением фрагментов. Гранулирующая рана передней поверхности нижней трети правой голени. На рентгенограмме замедленная консолидация фрагментов кости. Было проведено 7 процедур радиальной ударно-волновой терапии с интервалом 7 дней. После проведенного курса на рентгеновском снимке четко видно образование костной мозоли.
Перелом большеберцовой кости. Замедленная консолидация перелома. Состояние до проведения ударно-волновой терапии.
Состояние кости после проведения курса ударно-волновой терапии. Отмечается консолидация кости, исчезновение линий перелома.
Пример4.
Пациентка, 75 лет. Замедленная консолидация после перелома нижней трети плечевой кости.
Состояние после металлоостеосинтеза.
Замедленная консолидация перелома в нижней части плечевой кости. До лечения ударно-волновой терапией.
Срастание костных обломков плечевой кости после курса ударно-волновой терапии.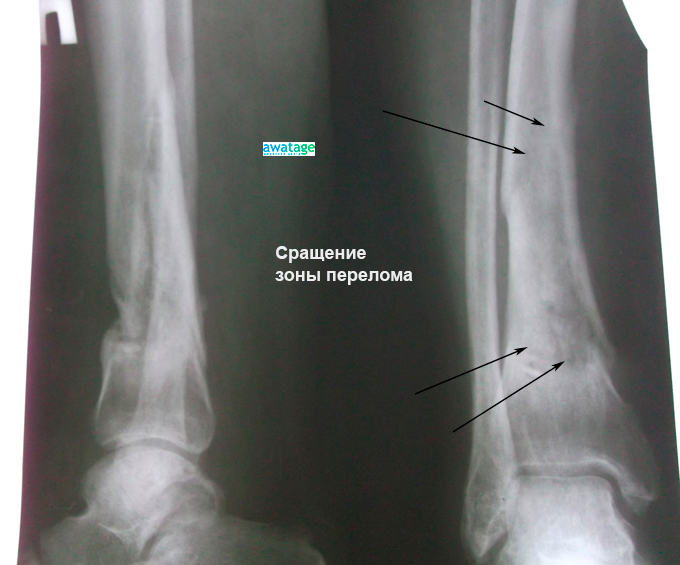 Стрелками указаны места где на месте линии перелома образовалась уплотнение кости и костная мозоль.
Стрелками указаны места где на месте линии перелома образовалась уплотнение кости и костная мозоль.
Пример 4.
Пациент с длительно (более 3х лет) несрастающимся переломов, который осложнился остеомиелитом. После 3х повторных операций и установки аппарата внешней фиксации сращение кости не наступило. Больной был направлен в МЦ “Аватаж” для прохождения курса ударно-волновой терапии и реабилитации. После прохождения курса УВТ из 10 процедур исчезли проявления остеомиелита и кость и образовалась костная мозоль. Через 2 месяца был снят аппарат внешней фиксации.
Повторная операция по стабилизации отломков, установлена внешняя конструкция. До лечения УВТ.
Замедленная консолидация перелома. Была проведена стабилизация обломков. До лечения УВТ.
После проведения курса радиальной ударно-волновой терапии произошла консолидация кости, были сняты металлические конструкции.
Запатентованные методики в реабилитации после переломов: методики лечения и профилактики замедленной консолидации переломов и псевдоартрозов.
Врачи медицинского центра “Аватаж” совместно со специалистами кафедры травматологии и ортопедии ЗГМедУ и врачами Запорожской областной клинической больницы запатентовали методику лечения замедленной консолидации переломов и псевдартрозов с помощью радиальной ударно-волновой терапии. А также была запатентована методика предотвращающая развитие замедленной консолидации переломов после оперативного лечения переломов.
Лечение замедленной консолидации переломов и псевдоартрозов (несращение кости) в Запорожье, дополнительная информация по телефонам: 050 435 87 00; 067 234 87 00.
|
Патент на способ лечения замедленной консолидации переломов и псевдоартрозов. |
Патент на способ профилактики замедленной консолидации переломов и псевдоартозов |
Лечение замедленной консолидации переломов (несращение кости) в Запорожье в медицинском центре “Аватаж”. Дополнительная информация по телефонам 067 234 8700 или 050 435 8700.
Массаж после переломов костей — статьи МИВМ
Перелом костей возникает в том случае, когда на кость воздействует сила, превышающая запас прочности кости. По характеру повреждения переломы бывают прямые, косые, винтообразные, оскольчатые, вколоченные, со смещением и без смещения. Тело кости сверху покрывает оболочка – надкостница, которая препятствует хаотичному разрастанию тела кости. При переломе надкостница вместе с телом кости разрушается и когда тело кости срастается, в месте перелома образуется так называемая костная мозоль. Это разрастание тела кости в месте повреждённой надкостницы. Массаж назначается при вялом образовании костной мозоли, на основе рентгенологических наблюдений.
При нормальном образовании костной мозоли массаж может способствовать так называемому пышному образованию костной мозоли, которая будет сдавливать сосуды, нервы, мышцы и, в некоторых случаях, может пальпаторно ощущаться под кожей. В некоторых местах, вследствие хорошего кровообращения, костная мозоль образуется довольно быстро (еапример, в области хирургической шейки плечевой кости) и из-за внутрисуставного характера перелома пышное образование костной мозоли может привести к ограничению подвижности в суставе.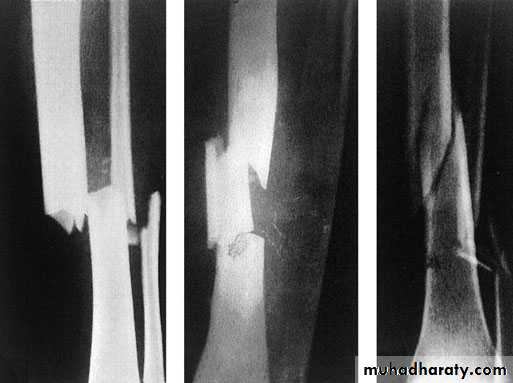
Не стоит недооценивать значение надкостницы, её повреждение случается и без перелома костей. Например, я наблюдал пациентку с точечным возвышением костной ткани в области правой надбровной дуги на лобной кости, после удара клювом курицы — травма произошла в детском возрасте и постепенно прогрессирует. Или, в практике массажа воротниковой зоны при остеохондрозе, наблюдал пациента, которому врач иссёк образовавшийся бугорок на кости нижней челюсти вместе с участком надкостницы, благодаря чему тело кости нижней челюсти получило возможность беспрепятственно развиваться, и у пациента образовалась гигантская костная мозоль, по размерам превосходящая голову человека. Поэтому роль надкостницы в опорно-двигательном аппарате немаловажна.
Возвращаясь к разговору о переломах костей, хочется отметить, что губчатые кости срастаются намного дольше, и чаще всего массаж назначается именно по поводу ускорения регенеративных процессов в таких костях. Например, после перелома костей в лучезапястном суставе массаж начинают уже на второй – третий день после травмы: массируют, главным образом, места, свободные от иммобилизации, а также здоровую конечность на противоположной стороне.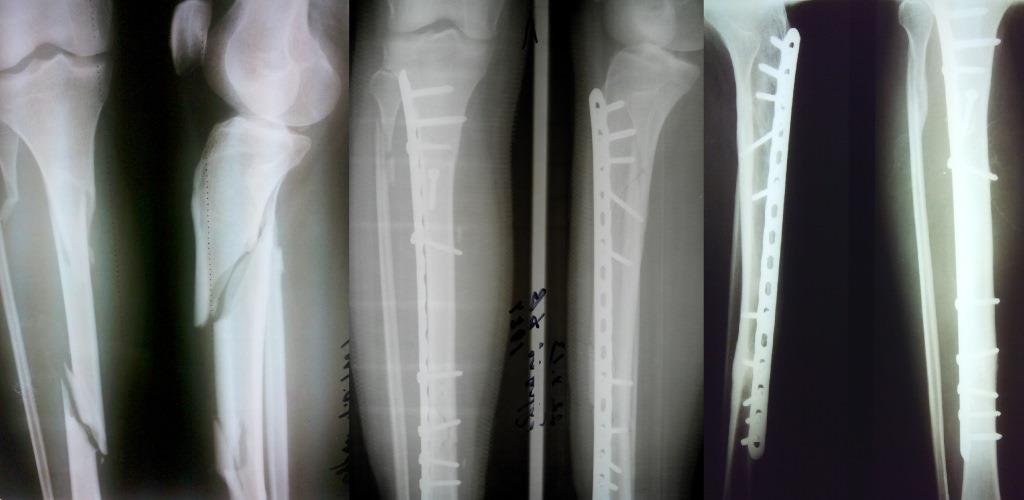
Отдельно стоит сказать о массаже здоровой конечности. Дело в том, что, например, обе верхние конечности, иннервируются из одного и того же отдела спинного мозга, поэтому при травме одной руки, массируют здоровую руку. Положительные нервные импульсы от здоровой руки через отдел спинного мозга поступают в травмированную руку и ускоряют процесс восстановления. Об этом свойстве массажа необходимо грамотно рассказать пациенту перед началом лечения, чтобы он адекватно реагировал на действия массажиста. Также массируют места выхода корешков спинно-мозговых нервов. Например, при массаже верхней конечности это будет шейно-воротниковая зона. При переломе костей таза и костей нижних конечностей массируют пояснично-крестцовую область, здоровую конечность и места, свободные от иммобилизации на повреждённой ноге. Место самого перелома массируют после снятия временной иммобилизации по назначению врача.
Особого внимания заслуживает период реабилитации. После снятия гипса часто наблюдается мышечная гипотрофия или атрофия мышц и контрактуры суставов на повреждённой конечности. В этом случае многое зависит от мастерства массажиста и от того, на сколько рано начата реабилитация. При этом состоянии массаж сочетается с физиотерапевтическими процедурами, прогреванием, ваннами, электрофорезом лекарственных средств. Разработка тугоподвижных суставов достаточно болезненна и требует деликатности и настойчивости от массажиста.
В этом случае многое зависит от мастерства массажиста и от того, на сколько рано начата реабилитация. При этом состоянии массаж сочетается с физиотерапевтическими процедурами, прогреванием, ваннами, электрофорезом лекарственных средств. Разработка тугоподвижных суставов достаточно болезненна и требует деликатности и настойчивости от массажиста.
Отдельное место в лечении травм костей занимает массаж после переломов позвоночника. Курс массажа после перелома позвоночника без разрыва спинного мозга составляет около тридцати процедур, которые проводятся по периодам. При переломе позвоночника со сдавлением или разрывом спинного мозга массаж проводится курсами, на протяжении длительного времени с интервалами между курсами полтора – два месяца.
В организме человека лишних костей нет. Травмированные кости изменяются навсегда и иногда могут не полностью восстанавливаться, причиняя человеку некоторые неудобства или страдания. Важно соблюдать меры предосторожности при активном отдыхе и передвижениях на транспорте, а также придерживаться диеты, в состав которой входят продукты, укрепляющие структуру костей, наращивать и укреплять мышечный корсет и вести здоровый образ жизни.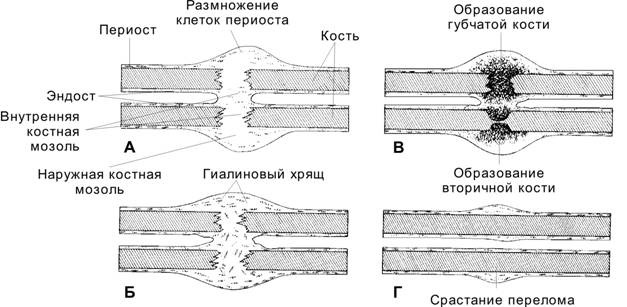
Переломы костей — ПроМедицина Уфа
Причины
В зависимости от причины возникновения различают травматические и патологические переломы. Причиной травматических переломов костей бывает резкое, внезапное действие механической ударной силы на кость.
Патологические переломы появляются при действии определенного патологического процесса на костную ткань. Это может быть результатом кисты или развития злокачественной опухоли. При этом структура костной ткани постепенно разрушается и даже небольшие нагрузки могут привести к перелому.
При втором виде опасность перелома возрастает в несколько раз. Доходит даже до того, что при ходьбе человек тоже может сломать ногу. Здесь причина заключается в том, что это патология самой кости, а не воздействие на нее со стороны.
Симптомы
Переломы костей имеют характерные симптомы, которые позволяют выявить патологию при ее возникновении, что очень важно для исключения осложнений. Можно выделить следующие основные относительные признаки перелома:
— Болевой синдром: резкая боль при разрыве кости и ноющая боль в дальнейшем, причем усиливающаяся при продольной нагрузке или ее имитации.
— Отечность: отек на пораженном участке развивается постепенно.
— Гематома: разного размера на пораженном участке; при этом гематома с пульсацией указывает на продолжение кровотечения.
Абсолютный признак перелома возникает в результате непосредственного разрушения кости и указывает на завершенность процесса. Таковыми признаками перелома являются:
— Характерный хруст (крепитация): возникает при разрыве костной ткани, в дальнейшем прослушивается с помощью фонендоскопа из-за трения обломков.
— Неестественное направление конечности или другой кости.
— Повышенная подвижность при разрыве сустава.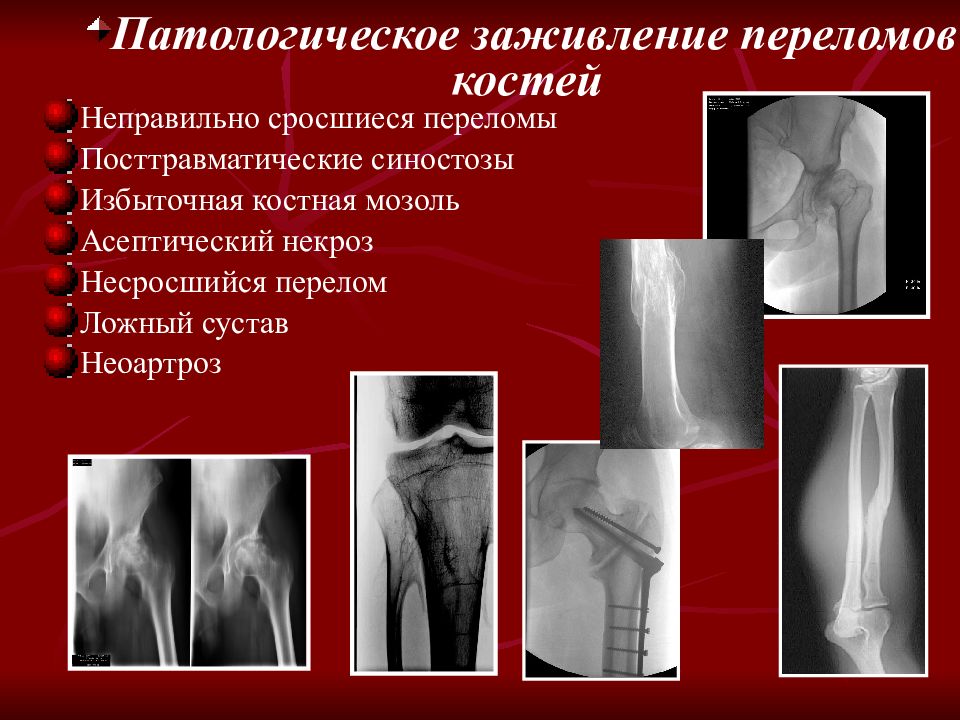
— Обломки кости заметны при открытом переломе визуально.
— Укорачивание конечности при смещении осколков, выпячивание сломанной кости.
Некоторые признаки при переломе без смещения или неполном переломе могут не проявиться, что осложнит диагностирование. Симптомы перелома однозначно определяются путем рентгенографии – фиксируются локализация, тип и степень разрушения.
Диагностика
При большинстве закрытых переломов рентгенодиагностика занимает ведущее значение. Это исследование необходимо не только для подтверждения диагноза перелома и его документирования. Очень важно травматологу на основании рентгенограмм составить представление о характере смещения отломков, направлении линий перелома и наличии дополнительных трещин, свидетельствующих о раскалывании отломка. Эти сведения нужны для определения лечебной тактики, выбора типа остеосинтеза.
Рентгенологическое исследование важно и в процессе лечения. Оно определяет полноту репозиции, правильность положения фиксирующей конструкции, отсутствие вторичного смещения (по спадению отека), появление и формирование костной мозоли.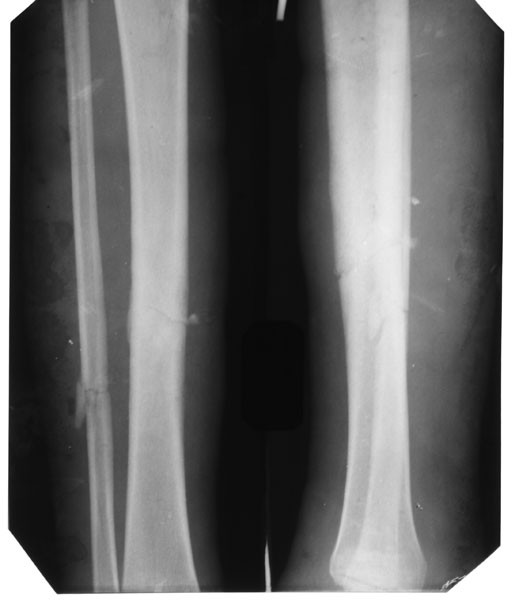 Хирург и травматолог должны соблюдать правила выполнения рентгенограмм при переломах.
Хирург и травматолог должны соблюдать правила выполнения рентгенограмм при переломах.
Лечение
Основными задачами лечения пострадавшего с переломом являются спасение его жизни и сохранение конечности, восстановление целости кости и анатомической формы сустава, функции поврежденной конечности и трудоспособности пострадавшего.
Первая помощь направлена на предотвращение смещения отломков костей, повреждения мягких тканей, инфицирования раны, развития травматического шока и массивной кровопотери. Необходимые действия: иммобилизовать поврежденный участок скелета, используя шину, захватывающую суставы выше и ниже места повреждения. Остановить кровотечение с помощью жгута и наложить на рану стерильную повязку. Дать обезболивающее средство: анальгин или промедол. Доставить пострадавшего в травмпункт.
При множественных переломах и травмах позвоночника передвигать больного до приезда скорой помощи не рекомендуется.
Консервативное лечение заключается в иммобилизации, использовании гипсовых повязок после закрытой репозиции перелома или без нее (если нет смещения). Конечность при наложении гипса должна находиться в физиологически правильном положении. Ее дистальные части (например, пальцы при переломе конечности) должны быть открытыми для возможности определения отека и предотвращения нарушения трофики тканей. Иногда при переломе необходима тракция — использование скелетного, манжеточного, клеевого или липкопластырного вытяжения. Этот метод помогает нейтрализовать действие мышечных пластов, которые крепятся к костным отломкам, предотвратить их смещение и создать условия для регенерации костной ткани. Наибольший эффект дает скелетное вытяжение. Груз, прикрепленный к спице, которая проведена через кость, обеспечивает поддержание костных отломков в положении, оптимальном для восстановления ткани. Недостаток – вынужденная иммобилизация пациента, приводящая к ухудшению его общего состояния.
Конечность при наложении гипса должна находиться в физиологически правильном положении. Ее дистальные части (например, пальцы при переломе конечности) должны быть открытыми для возможности определения отека и предотвращения нарушения трофики тканей. Иногда при переломе необходима тракция — использование скелетного, манжеточного, клеевого или липкопластырного вытяжения. Этот метод помогает нейтрализовать действие мышечных пластов, которые крепятся к костным отломкам, предотвратить их смещение и создать условия для регенерации костной ткани. Наибольший эффект дает скелетное вытяжение. Груз, прикрепленный к спице, которая проведена через кость, обеспечивает поддержание костных отломков в положении, оптимальном для восстановления ткани. Недостаток – вынужденная иммобилизация пациента, приводящая к ухудшению его общего состояния.
При трещинах в трубчатых костях и переломах небольших костей применяются функциональные методы. Они предполагают отсутствие иммобилизации или минимальное обездвиживание поврежденного участка и сводятся к обеспечению ему покоя.
Оперативное лечение необходимо при переломах челюсти (установка аппарата внешней фиксации), восстановлении губчатых костей (свод черепа), избыточном образовании костной мозоли и т.д.
В послеоперационном периоде место перелома иммобилизуют. Сроки восстановления – от нескольких недель до нескольких месяцев. В случае если восстановления кости не происходит, и формируется ложный сустав (стойкая ненормальная подвижность в месте перелома), применяют методы эндопротезирования (замена элементов опорно-двигательного аппарата имплантатами). После снятия гипса приступают к реабилитационной терапии.
Это, прежде всего, массаж. Назначается на 10-45 день после перелома. Он ускоряет процесс образования костной мозоли, улучшает кровообращение и питание тканей, препятствует атрофии мышц.
СРМ-терапия – это пассивная разработка суставов (без участия мышц) с помощью специально настроенного механического устройства.
Лечебная гимнастика. В первые 10 дней делаются упражнения для неповрежденных суставов и конечностей.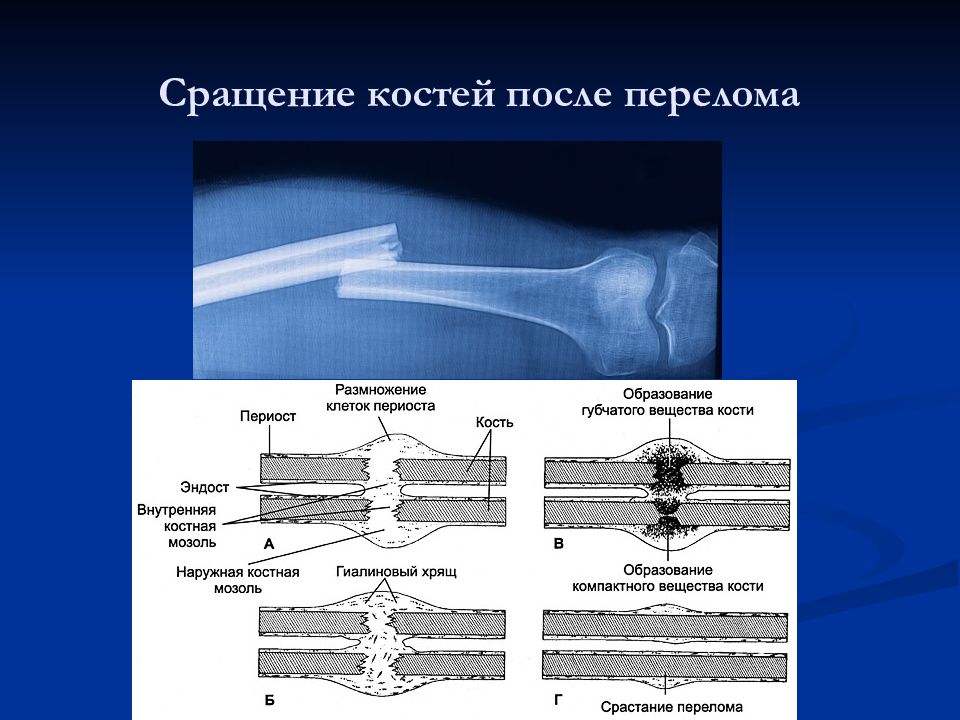 Они предотвращают мышечную слабость и возникновение тугоподвижности суставов.
Они предотвращают мышечную слабость и возникновение тугоподвижности суставов.
После снятия гипса ЛФК помогает восстановить подвижность поврежденных суставов и силу мышц. Нагрузку рекомендуется увеличивать постепенно, завершая реабилитацию активной гимнастикой, помогающей нейтрализовать последствия перелома.
Кальций для костей при переломах: профилактика переломов у детей
Содержание
Перелом возникает, когда давление на кость превышает допустимую нагрузку. Бывают состояния, которые ослабляют кость (например, остеопороз), и тогда достаточно минимального воздействия, чтобы произошел перелом.
Среди всех травм переломы костей составляют около 21,5%1. Заживление переломов — важнейший физиологический процесс, который требует значительных усилий от организма. Неправильное сращение приводит к тяжелым нарушениям функций опорно-двигательной системы и ухудшению качества жизни. Реабилитация после переломов занимает от 5-6 недель до года и больше. Для ускорения выздоровления в организм должно поступать достаточное количество кальция, который составляет основу костной ткани в виде гидроксиапатита.
Для ускорения выздоровления в организм должно поступать достаточное количество кальция, который составляет основу костной ткани в виде гидроксиапатита.
Нужно ли принимать кальций при переломе?
Кальций поступает в организм только извне и при недостатке вымывается из костей ради того, чтобы его уровень в крови оставался неизменным. Вот почему применение кальция оказывает значительную помощь при заживлении переломов.
В регуляции кальциевого обмена участвуют:
— гормоны паращитовидной железы;
— витамин D, от которого зависит всасывание минерала в кишечнике и его поступление в костную ткань (при недостатке витамина D кальций не усваивается, не поступает в достаточном количестве в кости: из-за этого плотность снижается).
Баланс кальция и витамина D — основа для формирования здоровой кости. Исследования показали, что препараты кальция эффективны в ускорении заживления переломов костей2, особенно при остеопорозе. Эти средства улучшают процесс отложения макроэлемента в костях и стимулируют формирование костной мозоли – важного этапа заживления перелома.
Препараты с кальцием при переломах костей
Создано три поколения средств для лечения травм и заболеваний костной системы:
Простые соли кальция (карбонат, цитрат, лактат, глюконат, фосфат) — препараты, которые содержат всего один компонент. Биодоступность кальция из них относительно невысокая, то есть в костную ткань поступает незначительное количество минерала. Для улучшения всасывания их нужно обязательно комбинировать с витамином D3.
Комбинация солей кальция (чаще – карбоната) и витамина D. Они не решают все задачи, так как для восстановления упругости и прочности костей нужны и другие микроэлементы4.
Препараты кальция с витамином D, в которые входят и другие минералы (магний, цинк, медь, марганец, бор). Примерами являются Кальцемин® и Кальцемин® Адванс, которые назначаются при переломах костей у детей и взрослых5. Такие средства обеспечивают не только поступление адекватной дозы кальция и витамина D, но и других важных микроэлементов. , утраченной ей за всю жизнь3.
, утраченной ей за всю жизнь3.
Если ребенок (подросток) не набрал пиковую костную массу, в дальнейшем у него может повыситься риск остеопороза. В группе риска также находятся люди, которые не употребляют достаточное количество продуктов, богатых кальцием, например молочных продуктов.
Какие препараты кальция лучше принимать при переломах костей?
В построении костной ткани участвует множество минералов и микроэлементов6. Чтобы ускорить процесс заживления, после перелома следует принимать средства, в составе которых есть:
— Магний. Регулирует обмен в костной ткани, ее минерализацию, поддерживает гибкость и прочность, усиливает возможности по восстановлению после переломов. Его применение способствует повышению минеральной плотности кости7. Недостаточное поступление магния может стать причиной остеопороза и низкой костной массы. Норма потребления — 400 мг/сутки.
— Цинк. Участвует во многих обменных процессах, принципиально важен для воспроизведения ДНК. В костной ткани содержится примерно 30% цинка всего организма6. Его концентрация в костях быстро падает, если снижается поступление или нарушается всасывание микроэлемента. Из-за дефицита цинка возможны дефекты развития костной ткани. Норма поступления для взрослых — 12 мг/сутки6.
В костной ткани содержится примерно 30% цинка всего организма6. Его концентрация в костях быстро падает, если снижается поступление или нарушается всасывание микроэлемента. Из-за дефицита цинка возможны дефекты развития костной ткани. Норма поступления для взрослых — 12 мг/сутки6.
— Медь. Компонент ферментов, которые участвуют в обмене железа, обеспечении тканей кислородом. В костной ткани отвечает за образование коллагена, его связь с эластином и общую минерализацию скелета. Недостаток меди приводит к нарушениям формирования костной и соединительной ткани, угнетению роста кости. Потребность для взрослых — 1 мг/сутки6.
— Марганец. Также участвует во всех видах обмена (углеводов, жиров, аминокислот). Дефицит марганца может стать причиной нарушений в репродуктивной системе, а также привести к повышенной хрупкости костей8. В сутки необходимо поступление 2 мг марганца.
— Бор. Влияет на обмен витамина D, содержание в костях кальция, фосфора, магния.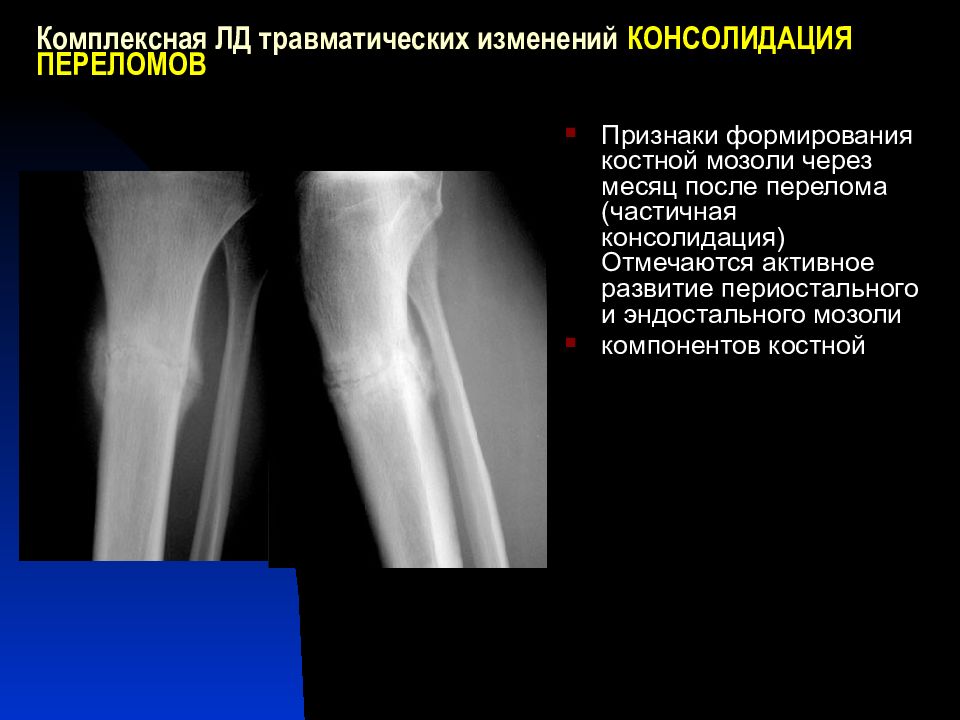 Улучшает всасывание кальция, предотвращает снижение плотности кости и развитие остеопороза. Ежедневно в организм должно поступать до 2 мг бора6.
Улучшает всасывание кальция, предотвращает снижение плотности кости и развитие остеопороза. Ежедневно в организм должно поступать до 2 мг бора6.
Для повышения эффективности лечения переломов целесообразно дополнительно принимать кальций в составе комбинированных препаратов (особенно пожилым людям). Препараты линейки Кальцемин® обеспечивают дополнительное поступление кальция, витамина D и других микроэлементов, необходимых для своевременного заживления переломов4. Они также способствуют формированию костной мозоли и повышению плотности кости для предупреждения повторных травм.
Профилактика переломов
Для предупреждения переломов важна профилактика остеопении (снижения минеральной плотности костей без структурных изменений костной ткани) и остеопороза. С этой целью назначают профилактические дозы кальция и витамина D, разрабатывают комплекс физических упражнений или подбирают оптимальный вид спорта (гимнастика, бег, плавание).
Если диагноз «остеопороз» уже поставлен, для его лечения (независимо от наличия переломов) требуются препараты, способные подавлять разрушение костной ткани и стимулировать ее образование. Только комплексный подход к профилактике переломов, в том числе остеопоротических, может ускорить заживление кости, сохранить ее гибкость и необходимую плотность, а в итоге – трудоспособность и качество жизни.
Только комплексный подход к профилактике переломов, в том числе остеопоротических, может ускорить заживление кости, сохранить ее гибкость и необходимую плотность, а в итоге – трудоспособность и качество жизни.
L.RU.MKT.CC.04.2019.2709
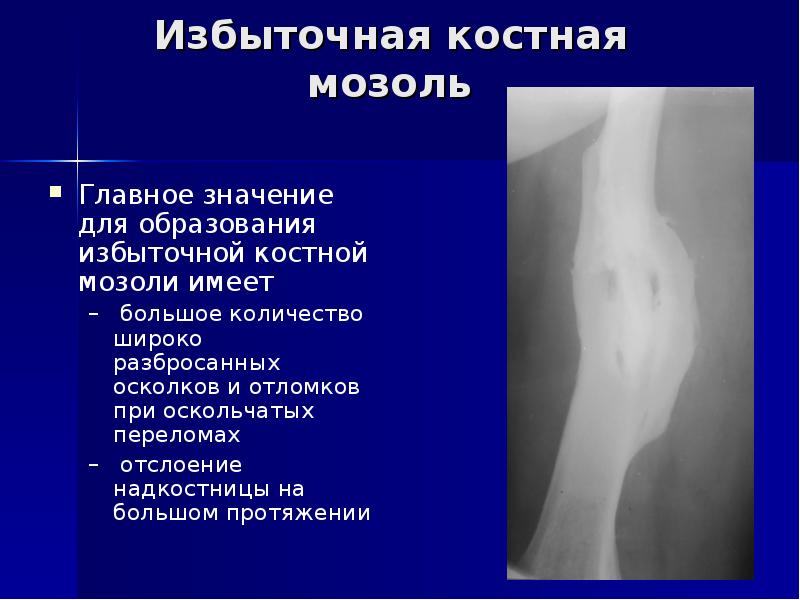
Почему образуется костная мозоль после перелома? | Здоровье — НАШЕ ВСЁ
Костная мозоль – это результат трансформации костной ткани (образованием в первичном регенерате волокон и хрящей) в процессе её восстановления после перелома. В подавляющем большинстве случаев, костная мозоль не мешает костям и далее выполнять свои функции.
В организме человека имеется два вида костей: длинные — лодыжка, голень, бедро, фаланги пальцев, плечо, предплечье и т.п.; плоские — лопатки, череп, ребра и т.п. Скорость и сам процесс восстановления в них отличается. Формирование костной мозоли после перелома возможно исключитеьно в длинных костях. Наиболее часто случаются переломы пальцев, которые зачастую сопровождаются разрывами сосудов и связок. Все это препятствует полноценному образованию костной мозоли. В данном случае показана иммобилизация металлическими конструкциями.
Все это препятствует полноценному образованию костной мозоли. В данном случае показана иммобилизация металлическими конструкциями.
Периостальная – такая мозоль появляется сразу после травмы в месте срастания. Часто сопровождает осколочные переломы мелких костей. Такая мозоль быстрее всего развивается из-за активного снабжения кровью.
Эндостальная — образуется во внутренней части кости одновременно с периостальной костной мозолью. Такое утолщение может нарастать прямо на месте перелома, на выпирающих косточках может быть заметна невооруженным взглядом.
Интермедиарная — возникает между двумя обломками кости, помогая нарастить костную ткань между ними.
Околокостная — мозоль формируется в местах срастания мышечной ткани. Для неё характерна отечность и припухлость. Пациент в течении длительного времени жалуется на чувство дискомфорта и боль в ареале перелома.
Параоссальная – эта разновидность мозоли самая опасная, она чаще появляется в трубчатых костях рук и ног, реже – в губчатых (пятка, запястье). Изменяет форму и структуру сломанной кости, окружая ее выступающим костным наростом, который часто ломается даже при минимальной нагрузке.
Изменяет форму и структуру сломанной кости, окружая ее выступающим костным наростом, который часто ломается даже при минимальной нагрузке.
- Некачественная репозиция отломков относительно своего природного положения;
- Недостаточная минерализация структуры мозоли на месте перелома;
- Замедленная трансформация грануляционной и хрящевой ткани в кость;
- Между костями обнаруживается прослойка фиброзной ткани – это несросшийся перелом;
- Изначально некачественная терапия, с последующими неоднократными попытками устранить смещение отломков;
- Слишком короткий период иммобилизации или перерывы в ношении фиксирующей гипсовой повязки;
- Несвоевременное удаление металлических фиксирующих конструкций;
- Неправильно подобранные физические упражнения или несвоевременное их назначение;
- Повреждение магистральных сосудов или нервов;
- Излишнее удаление мелких отломков при остеосинтезе;
- Хроническое воспаление и нагноение в местах перелома.
Костная мозоль не требует лечения, поскольку считается промежуточным звеном между переломом и восстановлением функциональных способностей кости. При замедленной консолидации необходимо обеспечить качественную иммобилизацию участка перелома, чтобы костная мозоль из хрящевой стадии могла трансформироваться в кость. Достаточно часто, по завершению сращевания, на кости остается утолщение в месте перелома. Если оно приносит эстетическое и психологическое неудобство или оказывает воздействие на нервные окончания, то необходима хирургическая коррекция.
В восстановительном периоде важное значение приобретает физиотерапия (электрофорез, магнитотерапия, УВЧ), массаж и лечебная физкультура. Это способствует предотвращению образования контрактур и спаек, а также благотворно влияет на восстановление функций костей и суставов.
Оригинал статьи размещен здесь: Почему образуется костная мозоль после перелома?
Понравилась статья, ставьте лайк, делитесь с друзьями и подписывайтесь на наш канал!
Препараты и материалы для репаративной регенерации костной ткани
Препараты и материалы для репаративной регенерации костной ткани
Человеческая кость — сложный орган со сложным иерархическим строением, выполняющий ряд механических и биологических функций. Костная ткань принимает участие в обменных процессах благодаря содержанию минеральных веществ. Она создает специфическое микроокружение для предшественников крови красного костного мозга.
Костная ткань принимает участие в обменных процессах благодаря содержанию минеральных веществ. Она создает специфическое микроокружение для предшественников крови красного костного мозга.
Репаративная регенерация костной ткани, или репаративный остеогенез — это процесс восстановления кости после повреждения, который в той или иной мере является усиленным физиологическим процессом. Репаративный остеогенез представляет собой важную теоретическую и практическую проблему стоматологии и хирургии.
В идеале консолидация перелома должна привести к образованию новой костной ткани, идентичной ее состоянию до момента перелома. Однако на практике сращение перелома — достаточно длительный многостадийный процесс, которой происходит под влиянием многочисленных внутренних и внешних факторов.
Согласно данным отечественных исследователей, костная ткань имеет значительный репаративный потенциал. Но восстановительные процессы сложно контролировать извне.
Нормально протекающие и патологически замедленные процессы репаративного остеогенеза можно ускорить за счет активации метаболизма лишь в небольшой степени. С другой стороны, процесс легко замедлить при недостаточном понимании физиологии кости и нарушении условий, способствующих регенерации.
Методы стимуляции репаративной регенерации костной ткани
Разработка методов регулирующего воздействия на репаративный остеогенез является актуальной задачей современной стоматологии, хирургии, травматологии и ортопедии.
Активное применение современных фиксатором далеко не всегда обеспечивает полноценное сращение костных отломков. Зачастую специалисты не уделяют должного внимания динамике процесса, влиянию новых важных факторов и рациональным тактическим решениям в ходе лечения.
Опыт применения малоинвазивных методик остеосинтеза при переломах длинных трубчатых костей, которые предпочитают менее чем в 20% случаев, указывает на то, что разработкой и совершенствованием фиксаторов решить проблему костной регенерации точно не удается.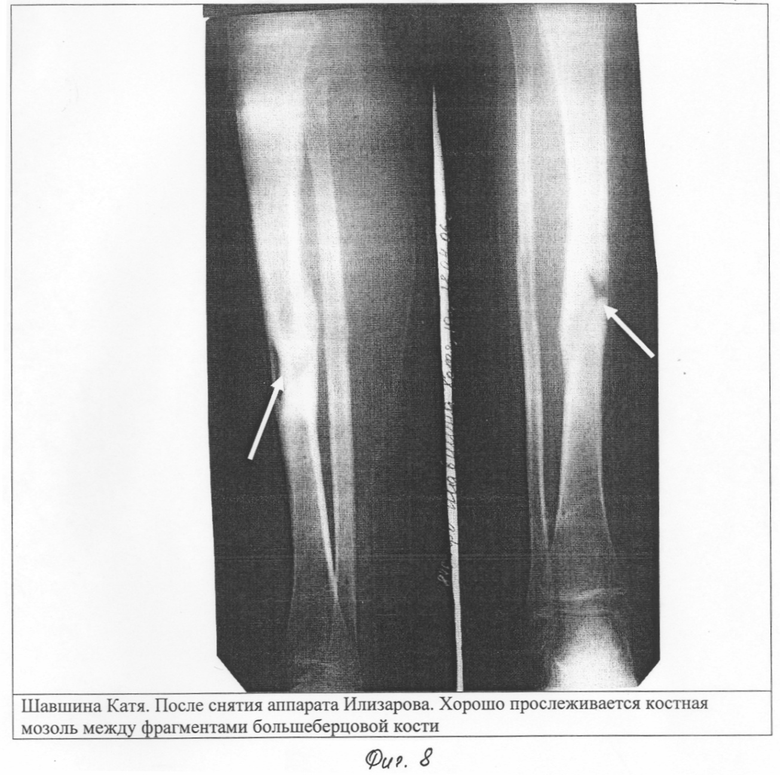
На основе системного подхода к решению этой проблемы можно эффективно разработать профилактические мероприятия и прогнозировать последствия заживления перелома. При этом вопросы поиска способов стимулирующего действия на область перелома с целью сокращения сроков сращения не являются новыми.
Поиск и обеспечение оптимальных условий протекания репаративно-регенераторных процессов при нарушении целостности костной ткани признано как перспективное и приоритетное направление научных исследований в XXI столетии.
На данный момент разработано большое количество методов оптимизации репаративного остеогенеза. В частности, был предложен метод направленного механического локального воздействия на зону костного дистракционного регенерата.
Известны отечественные и зарубежные экспериментальные исследования, в ходе которых оценивалась эффективность механических и гидродинамических влияний на формирование костной ткани в участке перелома при стимуляции заживления костной раны.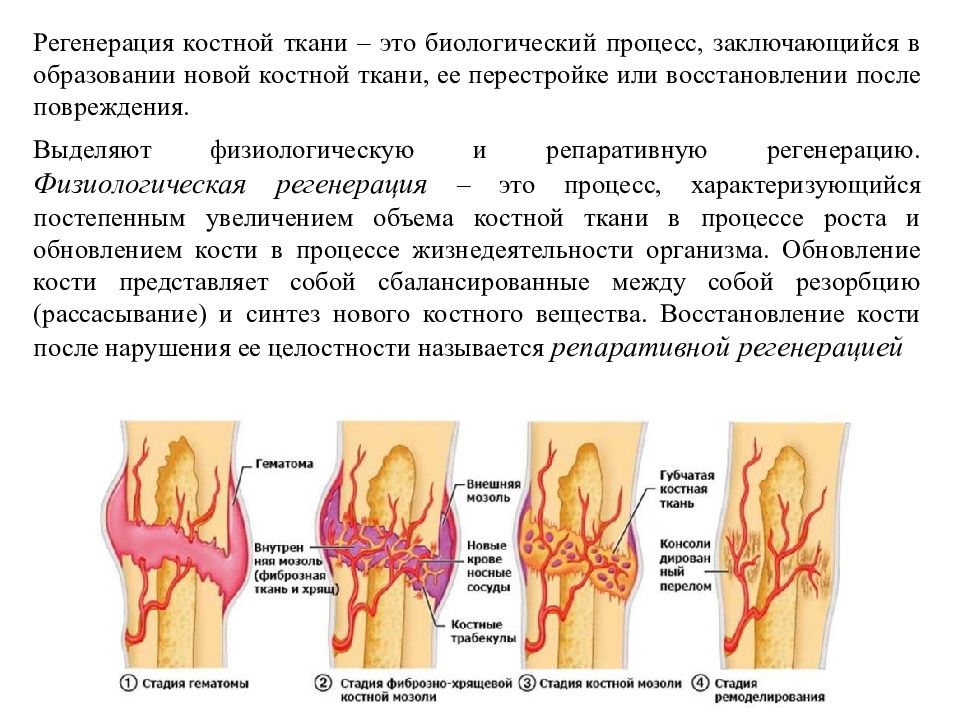
Рядом авторов было отмечено положительное рефлексотерапевтическое влияние на динамику репаративного процесса костной ткани при чрескостном дистракционном остеосинтезе.
В течение последних десятилетий интенсивно изучалась возможность использования физических методов воздействия с целью стимуляции остеогенеза. Эти методы не являются специфичными, но отличаются доступностью, и минимальной инвазивностью. Как правило, они не требуют специальных навыков персонала, дорогостоящего оборудования, характеризуются хорошими клиническими результатами и несравненно меньшим количеством осложнений по сравнению с традиционными методами.
Применение физических факторов обеспечивает стимулирующее влияние и оптимизацию репаративной регенерации костной ткани. Отечественными авторами часто отмечается положительное влияние переменного электромагнитного поля высокой частоты на процесс регенерации костной ткани и лечения инфекционных осложнений.
Для стимуляции регенерации костной ткани широко используется лазер. В ряде исследований отмечен положительный эффект применения механо-акустических волн. Ультразвуковые волны также отличаются выраженным стимулирующим действием на регенеративные процессы внутри костной ткани.
В ряде исследований отмечен положительный эффект применения механо-акустических волн. Ультразвуковые волны также отличаются выраженным стимулирующим действием на регенеративные процессы внутри костной ткани.
Неудовлетворительные с точки зрения хирургов результаты лечения, чрезмерная сложность и травматичность оперативных вмешательств побуждают исследователей к поиску новых, более совершенных способов и средств воздействия на репарацию костной ткани.
Современная остеотропная терапия
Многочисленные работы в России и за рубежом посвящены проблемам остеотропной терапии и целесообразности ее включения в лечение пациентов с переломами костей и нарушением консолидации костных отломков.
Эти научные сведения, при всей актуальности, достаточно разрозненные, а каждое из них содержит ограниченное количество наблюдений и рассматривает лишь отдельные аспекты проблемы заживления переломов.
Тем не менее доказано, что фармакологические препараты могут положительно влиять на различные стадии репаративного остеогенеза. Но связь между различными схемами использования препаратов и сращиванием костных отломков, их влияние на формирование регенерата на разных стадиях процесса продолжают вызывать дискуссии.
Далее упоминаются препараты для репаративной регенерации костной ткани:
-
Остеогенон
-
Цикло-3-форт
-
Бифосфонаты
-
Тивортин
-
Мексидол
-
Биофен
-
НПВП и др.
Международное сообщество по изучению регенерации после перелома (International Society for Fracture Repair) провело мультидисциплинарную рабочее совещание для разработки рекомендаций для клинической практики на основе оценки научных данных, по применению остеотропной терапии при переломах, в том числе на фоне лечения остеопороза.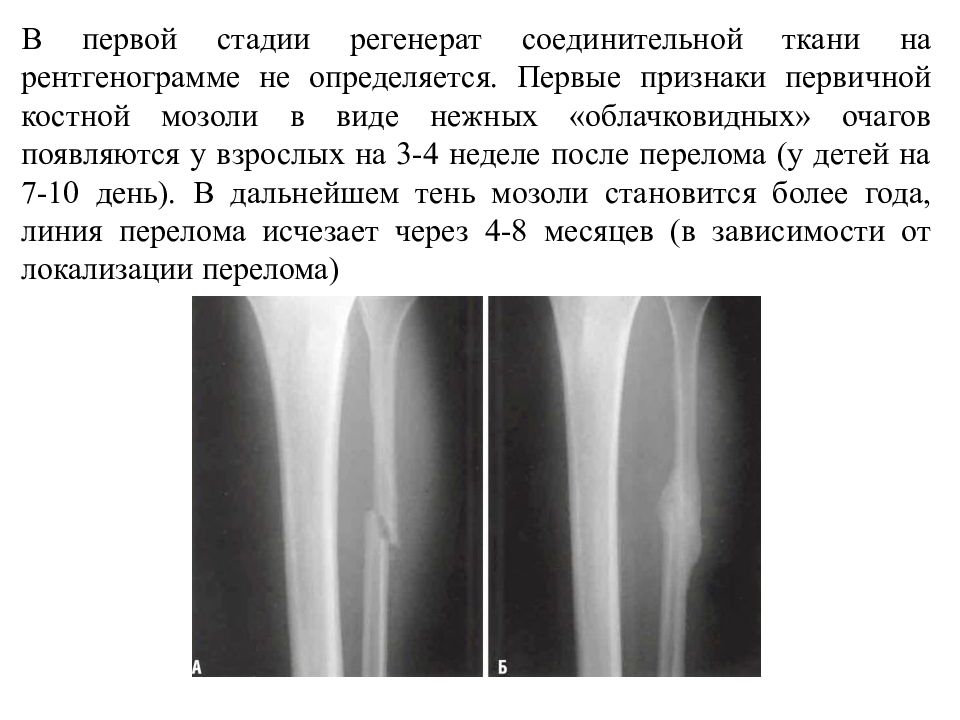
Единогласно было признано, что надежной доказательной базы не существует, поэтому эксперты призвали продолжать исследования в этом направлении и их систематизацию.
В источниках литературы встречаются единичные исследования, в которых проведен анализ частоты нарушений консолидации костных отломков у пациентов разных возрастов, которые получали остеотропную терапию или плацебо.
В результате авторами сделаны выводы о положительном влиянии остеотропной терапии на исследуемые процессы. Однако для подтверждения этого с позиции доказательной медицины необходимо проведение двойных слепых плацебо-контролируемых исследований.
Особое значение уделяется препаратам, которые влияют на массу и качество кортикальной кости, играющей ведущую роль не только в обеспечении способности кости противостоять механическим воздействиям, но и в достижении стабильного остеосинтеза.
Одним из таких перспективных препаратов является остеогенон, который, по данным гистоморфометрического анализа, существенно тормозит потерю кортикальной кости.
Данные экспериментальных исследований продемонстрировали морфологические особенности регенерата в области костного дефекта при введении остеогенона животным на разных стадиях процесса. Эксперименты показали, что прием остеогенон минимизирует деструктивно-дистрофические изменения в новообразованной костной мозоли и увеличивает образование кости вокруг имплантатов, вживленных в бедренную кость.
Также остеогенон стимулирует активность остеобластов, способствует своевременному формированию органического матрикса регенерата, предотвращает выведение кальция и способствует его сохранению в костной ткани.
Интересна работа, посвященная изучению влияния остеогенона на плотность регенерата костной ткани с помощью спиральной компьютерной томографии при лечении больных с переломами длинных костей и их последствиями.
Использование метода СКТ позволило количественно и качественно оценить ход образование регенерата в зоне повреждения и изучить динамику его развития.
Дальнейшие клинические исследования продемонстрировали многообещающие результаты применения остеогенона в лечении несращения костей при переломах. Приведенные данные свидетельствуют об эффективности применения и переносимости при лечении травматических переломов у лиц молодого возраста.
Доказано, что препарат может применяться для ускорения консолидации костных отломков при травматических переломах. Применение остеогенона с кальцием и витамином D3 после чрескостного остеосинтеза у пациентов с несращениями костных отломков свидетельствовало о положительном влиянии этой терапии.
Клинический эффект остеогенона обусловлен ускорением костного ремоделирования за счет активации костной резорбции и остеогенеза с преобладанием последнего; ростом потенциала биоэнергетических реакций, преобладанием локальной регуляции.
Клинически отмечено сокращение сроков лечения и положительная динамика минеральной плотности костной ткани, что обусловлено оптимизацией костного ремоделирования.
Украинские авторы изучали влияние комбинированной фармакотерапии, включающей остеогенон, поливитаминный препарат с гипогомоцистеинемическим эффектом декамевит и донатор оксида азота тивортин (аргинина гидрохлорид). Ю. Бессмертный и соавторы доказали его положительное влияние на остеорепаративный потенциал, существенное повышение эффективности лечения ложных суставов.
Положительное влияние остеотропной терапии остеогеноном на эффективность лечения расстройств репаративного остеогенеза отмечают и другие авторы.
В литературе встречаются отдельные свидетельства, что, хотя остеогенон ускоряет образование костной мозоли на 5-6 дней, процесс формирования мозоли протекает менее интенсивно по сравнению с другими стимуляторами (например, препарат цикло-3-форт).
Также препарат имеет ряд противопоказаний, которые существенно сужают рамки его применения в хирургии и травматологии.
На сегодня с целью активизации репаративного остеогенеза используют синтетические кальций-фосфатные биоматериалы в виде керамики или композитов.
Еще одним актуальным направлением является изучение регенерации кости в условиях терапии бисфосфонатами. Данные по различным бисфосфонатам неоднозначные.
Существует большая доказательная база, согласно которой бисфосфонаты снижают риск возникновения переломов. Однако в источниках литературы присутствуют противоречивые данные по поводу влияния различных препаратов класса бисфосфонатов на процесс регенерации и посттравматического ремоделирования кости.
Согласно данным доклинических исследований о влиянии бисфосфонатов на репаративный остеогенез, бисфосфонаты на ранних этапах регенерации способствуют формированию объемных регенератов, повышению механической прочности кости, однако в дальнейшем приводят к замедлению процесса ремоделирования регенерата.
Проведя эксперименты на животных моделях, некоторые исследователи заключили, что бисфосфонаты не нарушают консолидации костных отломков перелома, однако замедляют процессы эндохондрального окостенения.
Дальнейшие клинические исследования, оценивающие влияние бисфосфонатов на регенерацию кости, являются единичными, противоречивыми и неполными. Не все клинические исследования подтвердили данные, полученные при проведении экспериментальных разработок.
Специалисты отмечают, что негативное влияние на ремоделирование кости на поздних стадиях регенерации, указанное в большинстве доклинических исследований, не уменьшает ценности бифосфонатнои терапии, в результате которой повышаются прочностные характеристики кости и снижается риск повторных переломов.
Влияние кальцитонина на регенерацию костной ткани при переломах стал предметом дискуссии в отечественной и зарубежной литературе. Ряд исследователей не отметили значимого влияния кальцитонина на темпы образования костной мозоли. Другие, наоборот, отмечают положительный эффект препарата на регенерацию, а в некоторых исследованиях наблюдалось ухудшение качественно-прочностных характеристик регенерата.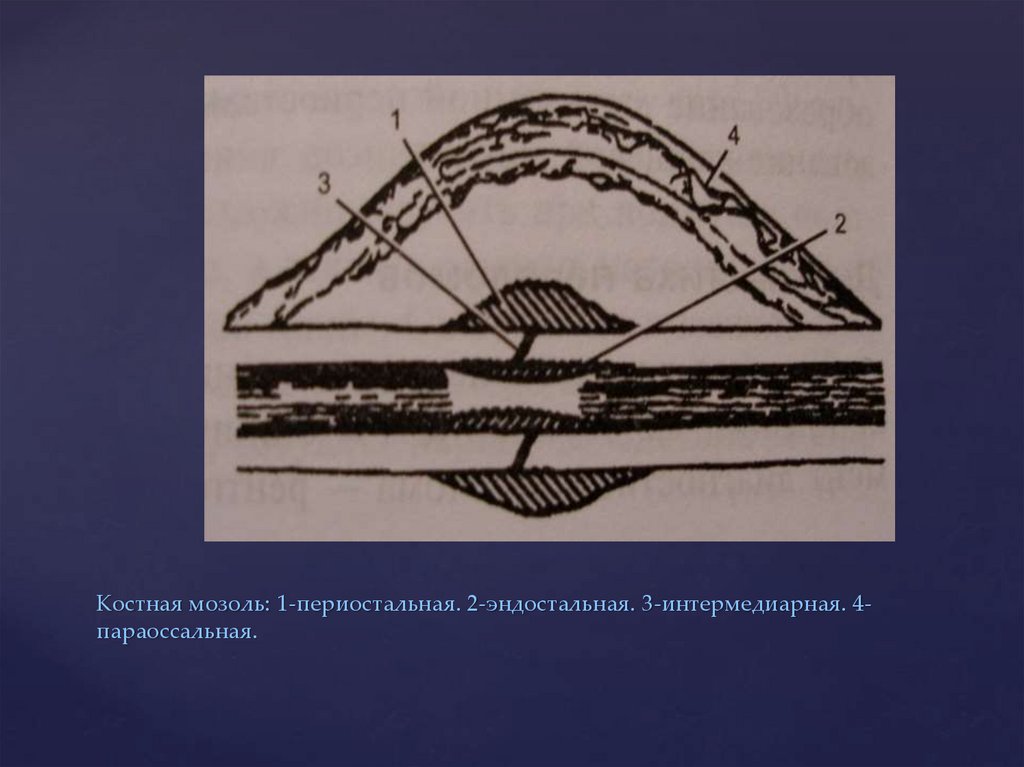
Изучение влияния кальцитонина лосося на репаративную регенерацию костной ткани в эксперименте указывает на нецелесообразность применения препарата на стадиях репаративного остеогенеза, которые охватывают воспалительный процесс.
При этом имело место замедление перестройки отломков материнской кости и снижение репаративного потенциала. По мнению ряда авторов, более оптимистичный прогноз возможен после введения препарата на стадии пролиферации, дифференцировки клеток и начала формирования тканевых структур.
В последние годы появились работы, посвященные влиянию фармакологических агентов с антиоксидантным действием на оптимизацию репаративной регенерации костной ткани.
Эти препараты снижают потребность клеток в кислороде и увеличивают их жизнеспособность в условиях гипоксии, ингибируют процессы перекисного окисления липидов и протеолиз, стимулируют регенерацию, усиливают детоксикацию, улучшают микроциркуляцию и реологические свойства крови.
Одно экспериментально-морфологическое исследование продемонстрировало оптимизацию репаративного остеогенеза при использовании препаратов мексидол и биофен, подтверждая регенераторные свойства этих лекарственных препаратов.
Следует отметить, что углубленное исследование препаратов остеотропного действия играет важную роль в лечении пациентов с переломами для уменьшения риска развития нарушений, связанных с замедленной консолидацией и различными вариантами несращений.
Роль НПВП в остеотропной терапии
В настоящее время обсуждается вопрос влияния нестероидных противовоспалительных препаратов (НПВП) на регенерацию костной ткани.
Анализ исследований по изучению влияния нестероидных противовоспалительных препаратов на остео- и хондрогенез продемонстрировал, что НПВП по-разному влияют на дифференцировку фибробластов, остеобластов и других клеток-предшественников в культуре мезенхимальных клеток человека.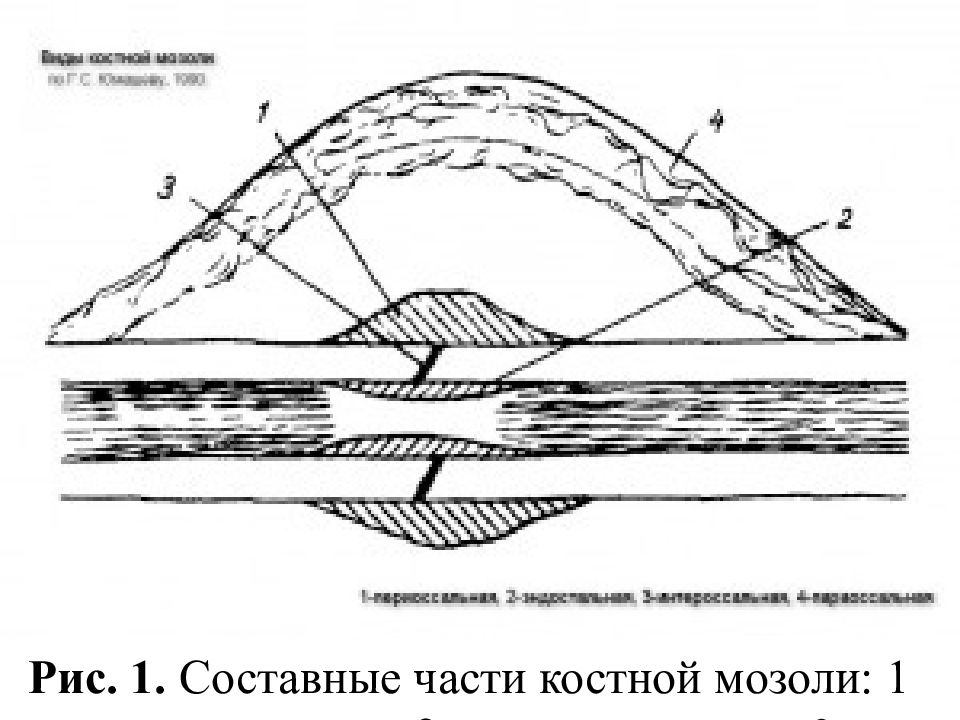
Неоднозначными остаются результаты экспериментальных исследований влияния НПВП на хондрогенез: одни авторы отрицают, а другие, наоборот, подтверждают наличие эффекта. По результатам исследований на лабораторных животных было выявлено стимулирующее действие ибупрофена (снижение сроков заживления костной раны).
В литературе имеется небольшое количество ретроспективных и еще меньше проспективных рандомизированных клинических исследований, которые посвящены консолидации переломов при приеме нестероидных противовоспалительных препаратов.
В двойном слепом рандомизированном исследовании продемонстрировано отсутствие воздействия пироксикама на заживление переломов. В другом подобном исследовании не выявлено отрицательного влияния ибупрофена на заживление перелома.
Однако Bhattacharyya и коллеги зафиксировали более высокий риск нарушений консолидации перелома у пациентов, принимающих НПВП.
Учитывая данные экспериментальных и клинических исследований, можно сделать вывод о необходимости проведения крупных рандомизированных исследований. Пока их результаты недоступны, целесообразно ограничить прием нестероидных противовоспалительных препаратов всех групп у пациентов с высоким риском несращения.
Пока их результаты недоступны, целесообразно ограничить прием нестероидных противовоспалительных препаратов всех групп у пациентов с высоким риском несращения.
Выбор материалов для репаративной регенерации костной ткани
При несращении переломов, атрофических гиповаскулярних ложных суставах и значительных дефектах длинных костей часто нужна биологическая стимуляция костеобразования в виде костной пластики (остеопластики).
В последнее время для оптимизации репаративного процесса врачи уделяют большое внимание использованию биологических остеопластических материалов, обладающих остеоиндуктивными или остеокондуктивными свойствами.
Наибольший объем исследований посвящен аутокости и аллокости, а также керамическому гидроксиапатиту и другим остеопластическим материалам. Однако проблема профилактики и лечения расстройств репаративного остеогенеза все еще актуальна.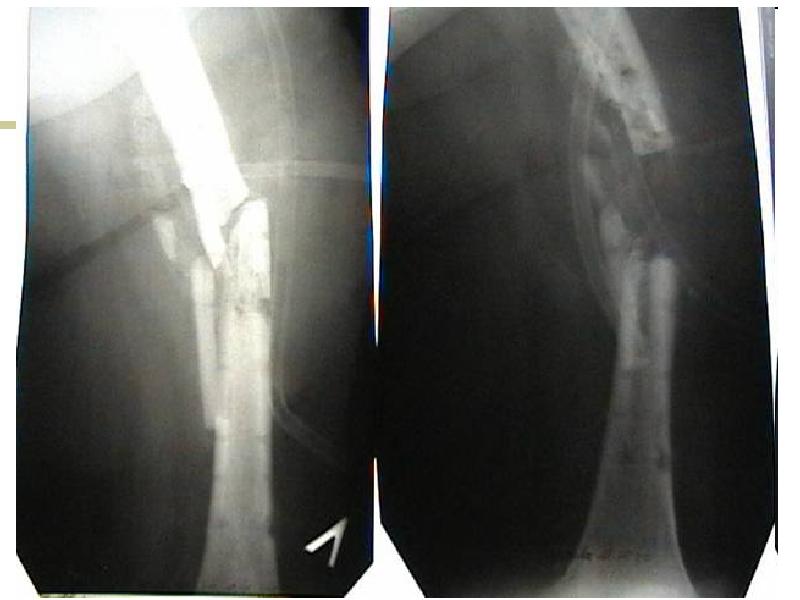
В связи с этим принципиально важна разработка технологий оптимизации репаративного остеогенеза с использованием остеопластических материалов, обеспечивающих:
-
Отсутствие токсичности
-
Бактериальную и вирусную безопасность
-
Полную биодеградацию
-
Биологическую совместимость
-
Сочетание остеоиндукции и остеокондукции.
К таким биологическим материалам относят аутологичный обогащенный тромбоцитами фибриновый гель, который представляет собой продукт из собственной крови больного.
Согласно современным данным, тромбоцитарно-фибриновий гель содержит большое количество факторов роста, оказывает стимулирующее и остеокондуктивное действие, способен влиять на остеогенез за счет наличия вышеуказанных факторов роста и разветвленной сети фибриновых волокон.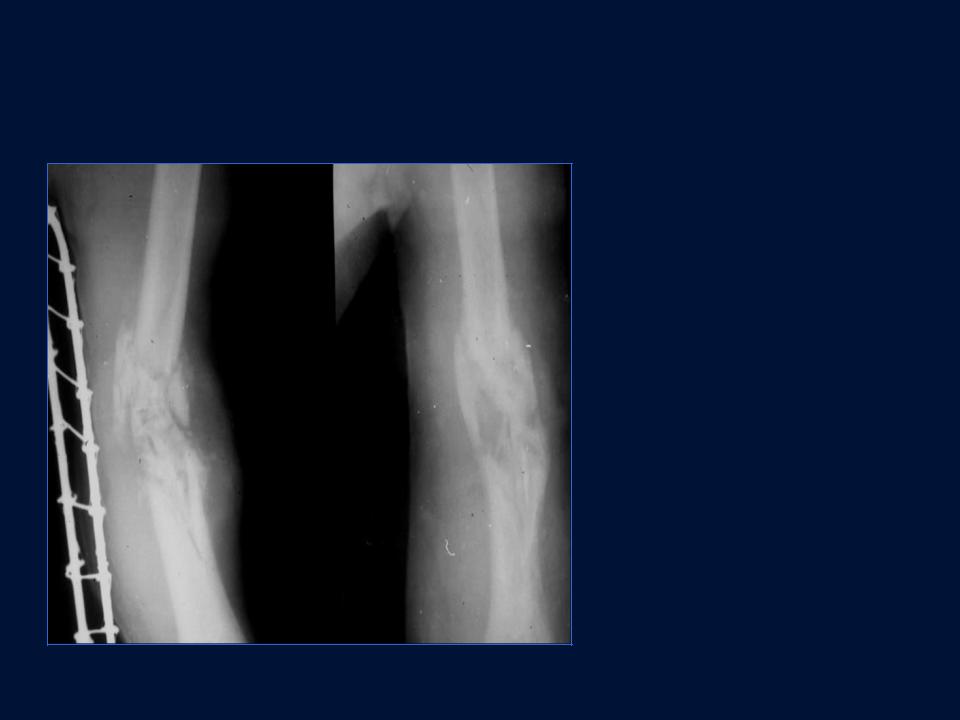
Экспериментально доказана эффективность одновременного применения аутокрови и различных биологических имплантатов в качестве оптимизирующих факторов репаративного остегенеза. Одновременное применение аутокрови и указанных компонентов стимулирует метаболические процессы остеобластических клеточных элементов регенерата.
Для замещения, восстановления структурной целостности и повышения остеогенного потенциала костной ткани в клинической практике используют костные трансплантаты.
Аутотрансплантат как золотой стандарт остеопластики
«Золотым стандартом» для замещения костных дефектов считается аутотрансплантат из губчатой кости. С биологической и клинической точки зрения материал идеально подходит для костной пластики.
Аутогенная губчатая кость из-за отсутствия иммуногенности имеет остеогенные и остеоиндуктивные свойства, а также идеальную структуру для остеокондукции. Он является идеальным остеопластическим материалом среди всех биологических позиций, хотя использование ограничено в объеме из-за сложности забора и механической прочности.
Он является идеальным остеопластическим материалом среди всех биологических позиций, хотя использование ограничено в объеме из-за сложности забора и механической прочности.
Возможности получения аутотрансплантата в достаточном количестве для замещения крупных костных дефектов действительно ограничены потребностью в дополнительном хирургическом вмешательстве и повышенным риском для пациента.
Забор аутотрансплантата связан с серьезными осложнениями, а недостатком способа является нанесение дополнительной операционной травмы, увеличение кровопотери и времени самого оперативного вмешательства, анестезии.
Другие материалы для репаративной регенерации костной ткани
В специализированной литературе хорошо описаны преимущества, недостатки и риски, связанные с использованным аллоимплантатов. По этой причине продолжается активный поиск заменителей, которые способны составить конкуренцию аутокости.
В источниках дана подробная характеристика идеального имплантата, приведены классификации материалов в зависимости от происхождения, состава, технологии получения и поведения в организме, а также механизмы воздействия этих материалов на процессы регенерации костной ткани.
За последние годы в мировой прессе накопилось значительное количество публикаций, посвященных изучению природы индукционного остеогенеза, возникающего в ответ на применение деминерализованных костных трансплантатов.
Установлено, что они сочетают остеоиндуктивные и остеокондуктивные свойства. Эти свойства обеспечиваются путем высвобождения из экстрацеллюлярного матрикса ряда субстанций, способствующих регенерации воспринимающего костного ложа.
Лишенные минеральной основы деминерализованной трансплантаты быстрее васкуляризируются в организме реципиента и замещаются новообразованной костной тканью. При комбинированной пересадке деминерализованная кость существенно увеличивает скорость перестройки других биологических трансплантатов.
Считается доказанным, что остеоиндуктивные свойства деминерализованных костных трансплантатов определяются не какой-либо химической субстанцией, а целым комплексом индуцирующих костных морфогенетических белков, остеогенная активность которых возрастает по мере удаления минеральных элементов.
Существуют единичные работы, в которых приведены данные морфологического анализа репаративного остеогенеза и хондрогенеза при имплантации в зону повреждения суставного хряща и дефекта кости гранулированного минерализированного костного матрикса.
Особое место среди искусственных имплантатов занимают кальций-фосфатные остеопластические материалы. Многочисленные исследования показали, что кальций-фосфатные материалы по сравнению с другими биоматериалами обладают уникальными свойствами, способствующими их применению в замещении костных дефектов.
Эти материалы по составу близки к костной ткани человека и индуцируют аналогичные биологические реакции при ремоделировании кости. Согласно данным литературы, кальцийсодержащие имплантаты из мраморной муки также могут быть биосовместимыми, подвергаются биорезорбции, имеют остеоиндуктивные свойства.
Согласно данным литературы, кальцийсодержащие имплантаты из мраморной муки также могут быть биосовместимыми, подвергаются биорезорбции, имеют остеоиндуктивные свойства.
Выбор методов лечения при нарушении остеорепарации
Современные рекомендации относительно выбора метода лечения при нарушениях процессов остеорепарации достаточно противоречивы.
Неудовлетворительные результаты лечения встречаются при использовании различных методов. По мнению В. Климовицкого и соавторов, выбор тактики лечения при костной дисрегенации должен начинаться с поиска и устранения факторов, которые вредят естественному протеканию репаративного остеогенеза.
Для достижения сращения в участке псевдоартроза длинных костей ряд авторов называют ведущим методом компрессионный остеосинтез аппаратом внешней фиксации. При этом, согласно Ю. Барабаш, оголение кости и остеопластика необязательны.
Если оперативный остеосинтез при ложном суставе выполняется погружным фиксатором, авторы рекомендуют обрабатывать костные концы в месте перелома, плотное соединять отломки в правильном положении, проводить биологическую стимуляцию регенерации с помощью остеопластики синтетическими материалами или остеоперфорацией.
В хирургии и травматологии разработан ряд эффективных методов чрескостного и внутрикостного остеосинтеза, способных оптимизировать репаративные свойства кости.
Однако реальные сроки сращений костной ткани остаются значительными.
Появление новых технологий, основанных на применении биоактивных интрамедуллярных имплантатов, призвана не только гарантировать положительный результат лечения переломов длинных костей, но и сократить сроки остеосинтеза, снизить количество осложнений.
В настоящее время отсутствует единое мнение относительно тактики оперативного лечения, времени, объема и способа фиксации костных отломков, показаний к изменению фиксаторов.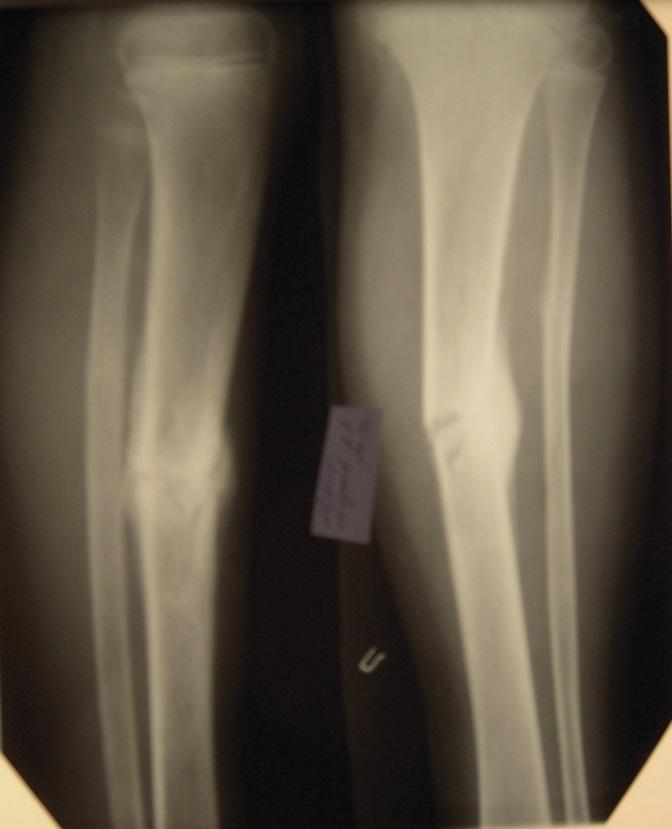
Отечественный исследователь К.М. Климов еще несколько десятилетий назад сформулировал основные принципы оперативного лечения несрастающихся переломов и ложных суставов длинных костей, в которых назвал показания к оперативному лечению:
-
Замедленное образования костной мозоли — оперативное лечение не показано.
-
Несрастающийся перелом без тенденции к сращиванию или ложного сустава — лечение методом остеопластики считается нерациональным. Щадящая операция.
-
Несрастающийся перелом с тенденцией к образованию ложного сустава — стабильный остеосинтез по типу внутреннего протеза.
При выполнении оперативного вмешательства рубцовую ткань, которая окружает костные отломки, Климов предлагал не удалять, а экономная резекция волокнистой и хрящевидной ткани рекомендовалась лишь для сопоставления костных фрагментов.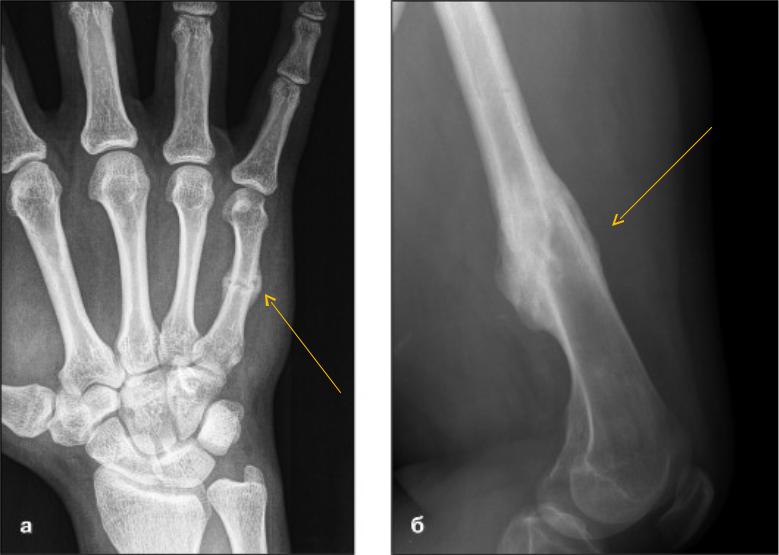
На основе предыдущих морфологических исследований исследователь утверждает, что склерозированные концы костных отломков способны к остеорепарации. Хотя среди врачей есть устойчивое мнение, что потенциальные репаративные возможности склерозированных тканей сведены на нет, а последняя подлежит обязательному удалению.
Дискуссионным является и первый постулат, поскольку есть сторонники оперативного лечения, даже ревизионного остеосинтеза при замедленной консолидации отломков.
А. Калашников и соавторы акцентируют внимание на объективизированной оценке процессов заживления переломов. Она позволяет отказаться от чрезмерного расширения показаний к оперативному лечению больных с замедленным сращением костных отломков и необходимости остеосинтеза в пограничных случаях, когда все возможности консервативного лечения не были исчерпаны.
Общим правилам проведения оперативных вмешательств при различных видах дисрегенераций являются:
-
Максимальное сохранение кровоснабжения отломков
-
Обеспечение максимально возможной плоскости контакта
-
Удаление нежизнеспособной костной ткани
-
Адекватная фиксация отломков.
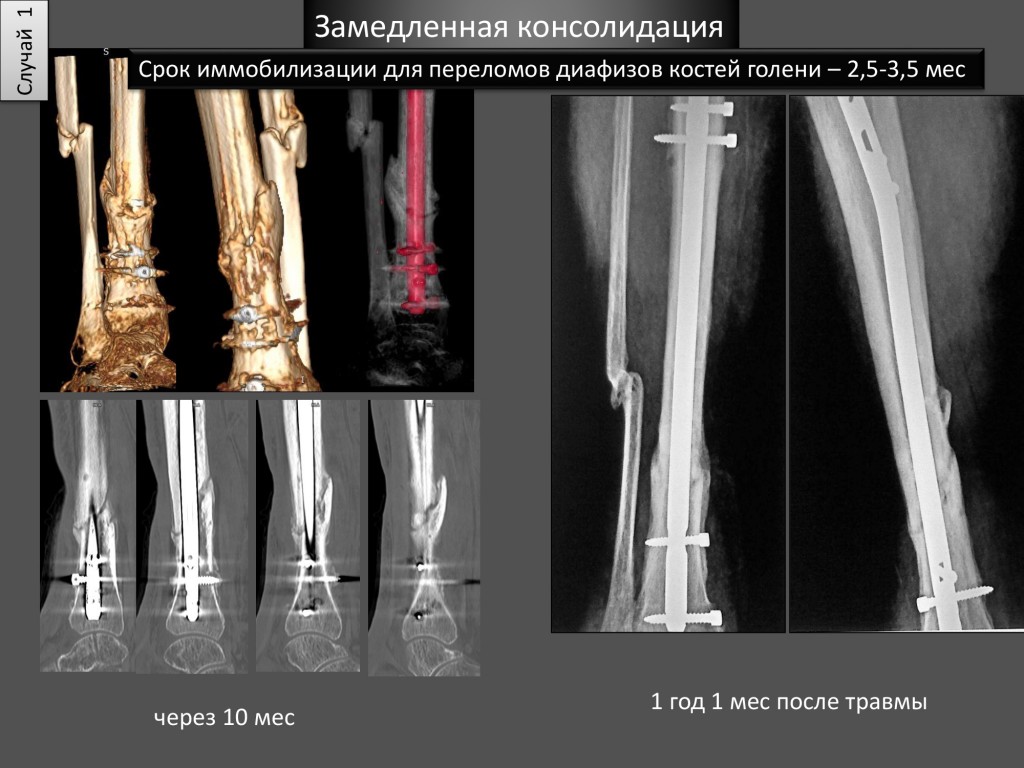
На постсоветском пространстве профессором В. Климовицким и соавторами были предложены следующие подходы к лечению дисрегенераций.
При лечении гипертрофических ложных суставов однокостных сегментов выполняют осевую компрессию между отломками. Во время процедуры происходит разрушение и резорбция костной и рубцовой ткани, восстанавливаются воспалительные процессы в межотломковой зоне и процессы остеорепарации.
На двукостном сегменте (голень) предварительно необходимо обязательно выполнить остеотомию малоберцовой кости, которая выполняет роль распорки. Авторы считают, что во время оперативного лечения гипертрофических ложных суставов в большинстве случаев нет необходимости вмешиваться в область повреждения.
Исключения составляют случаи удаления металлического фиксатора.
Лечение олиготрофического вида дисрегенерации требует вмешательства на очагах повреждения с целью активации пониженного остеогенного потенциала путем различных хирургических приемов (туннелизация по Беку или костно-надкостничная декортикация).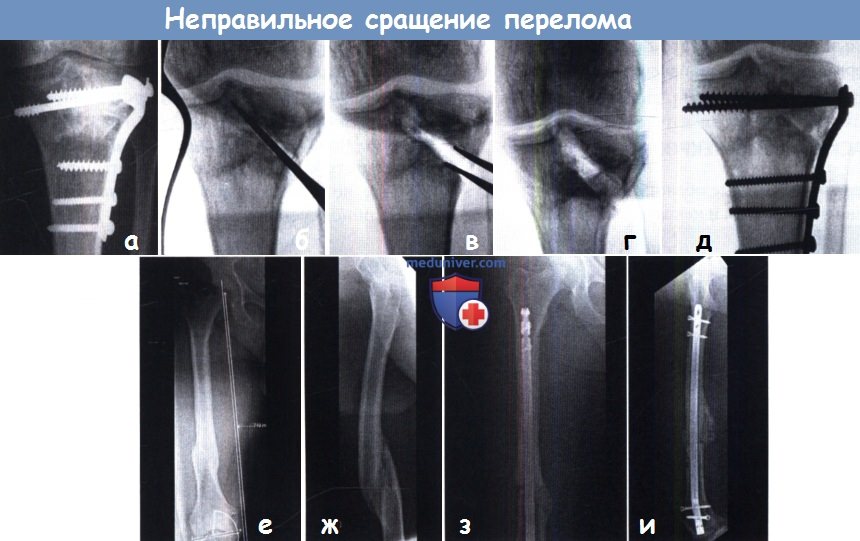
Лечение гипотрофических форм расстройств репаративного остеогенеза считается самым проблематичным, поскольку остеорепаративный потенциал в данном случае отсутствует.
Оперативное лечение обязательно должно включать вмешательства в области ложного сустава. В ходе процедуры выполняется резекция измененных концов с последующим перекрытием зоны несращения кортикально-губчатым трансплантатом.
Выбор того или иного способа замещения костного дефекта должен осуществляться индивидуально, в том числе с учетом возможностей хирурга.
Для оптимизации условий формирования регенерата, сокращения длительности лечения и профилактики осложнений применяют метод направленной стимуляции регенерации костной ткани путем введения интрамедулярных спиц с кальций-фосфатным покрытием.
В литературе описаны морфологические особенности остеогенеза при консолидации костных отломков длинных костей в условиях интрамедуллярного введения фиксаторов с биоактивным кальций-фосфатным покрытием из гидроксиапатита.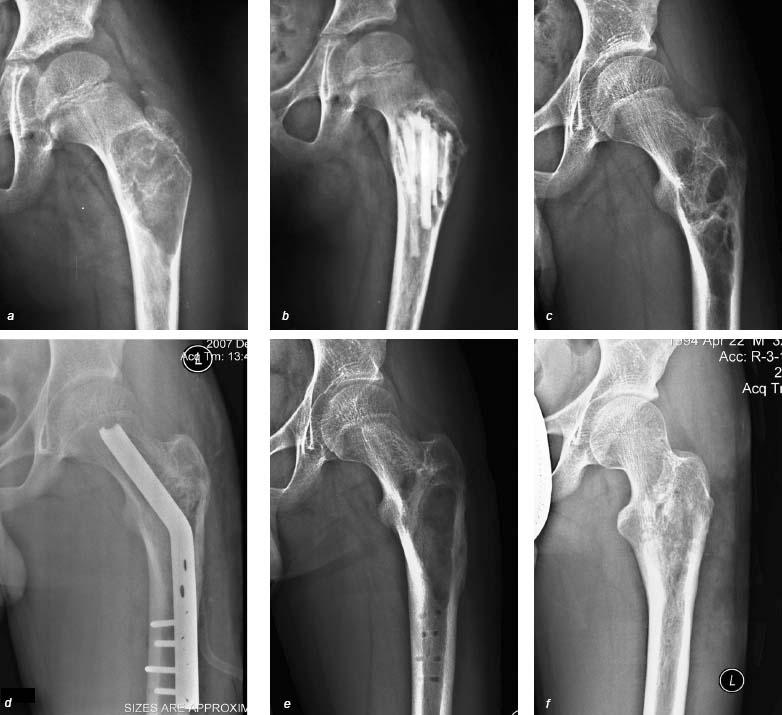
Результаты многочисленных работ свидетельствуют, что интрамедуллярные фиксаторы с покрытием из гидроксиапатита положительно влияют на интенсивность репаративного остеогенеза при заживлении переломов.
Один из способов стимуляции остеорепарации заключается в стимуляции локальных источников остеогенеза путем создания сквозных каналов в метафизах и диафизах длинных костей (туннелизация) или дырчатого дефекта (остеоперфорация), обеспечивающих стимуляцию внутрикостного кровообращения.
Работы по изучению морфологических особенностей репаративного остеогенеза при заживлении переломов большеберцовой кости в условиях чрескостного остеосинтеза и нарушения локального источника остеогенеза в контралатеральной конечности продемонстрировали многообещающие результаты.
Было доказано, что остеоперфорация активизирует репаративный остеогенез, ускоряет компактизацию и развитие костной ткани, повышает степень ее зрелости и обеспечивает формирование полноценного костного регенерата на ранних сроках.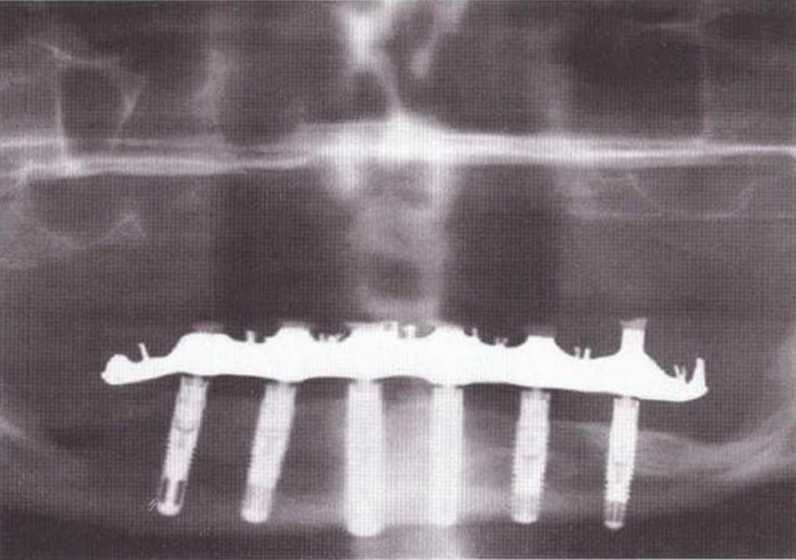
Приведенные данные указывают на нерешенность проблемы стимуляции репаративного остеогенеза, поскольку каждый из методов, наряду с положительными свойствами, имеет существенные недостатки и ограничения в клинической практике.
Предстоит поиск новых факторов, препаратов и материалов для репаративной регенерации костной ткани в стоматологии, хирургии, травматологии и других областях медицины.
Обзор заживления переломов — StatPearls
Определение / Введение
Перелом — это нарушение структурной целостности коры кости со степенью повреждения окружающих мягких тканей. После перелома начинается вторичное заживление, которое состоит из четырех этапов:
-
Образование гематомы
-
Образование фиброзно-хрящевой костной мозоли
-
Формирование костной мозоли
-
Ремоделирование кости
Может повлиять на неудачное заживление до 10% всех переломов и могут быть вызваны различными факторами, такими как измельчение, инфекция, опухоль и нарушение кровоснабжения. В этой статье мы подробно рассмотрим каждый из этих шагов, прежде чем коснемся первичного заживления, факторов, влияющих на заживление переломов, и методов стимуляции заживления переломов. [1] [2]
В этой статье мы подробно рассмотрим каждый из этих шагов, прежде чем коснемся первичного заживления, факторов, влияющих на заживление переломов, и методов стимуляции заживления переломов. [1] [2]
Проблемы, вызывающие озабоченность
Механизм заживления переломов — сложный и плавный процесс. Этот процесс можно разбить на четыре этапа. Однако эти этапы в значительной степени пересекаются.
Образование гематомы (дни с 1 по 5)
Эта стадия начинается сразу после перелома.Кровеносные сосуды, снабжающие кость и надкостницу, разрываются во время перелома, в результате чего вокруг места перелома образуется гематома. Гематома сворачивается и образует временный каркас для последующего заживления. Повреждение кости приводит к секреции провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNF-α), морфогенетические белки кости (BMP) и интерлейкины (IL-1, IL-6, IL-11, IL-23). ). Эти цитокины стимулируют важную клеточную биологию в этом месте, привлекая макрофаги, моноциты и лимфоциты.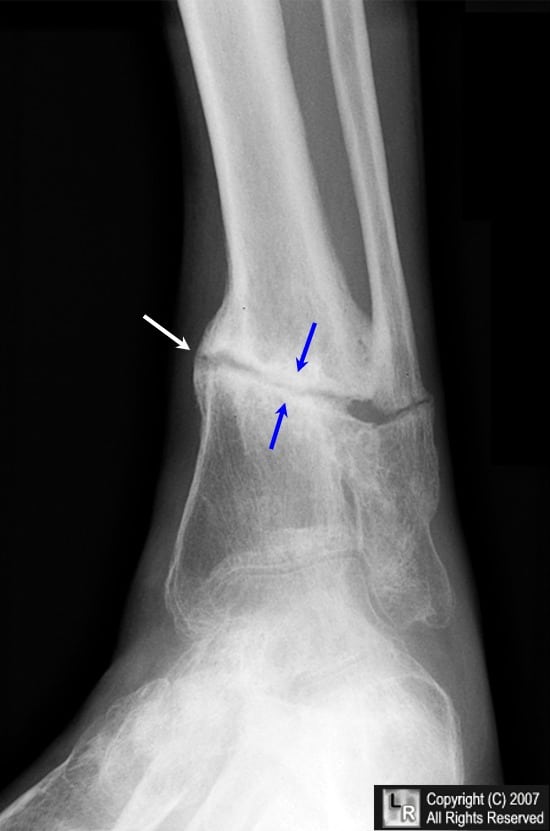 Эти клетки действуют вместе, удаляя поврежденные, некротические ткани и секретируя цитокины, такие как фактор роста эндотелия сосудов (VEGF), чтобы стимулировать заживление на этом участке.
Эти клетки действуют вместе, удаляя поврежденные, некротические ткани и секретируя цитокины, такие как фактор роста эндотелия сосудов (VEGF), чтобы стимулировать заживление на этом участке.
Образование фиброзно-хрящевой каллуса (дни с 5 по 11)
Высвобождение VEGF приводит к ангиогенезу в этом месте, а внутри гематомы начинает развиваться богатая фибрином грануляционная ткань. Далее мезенхимальные стволовые клетки привлекаются к этой области и начинают дифференцироваться (управляемая BMP) в фибробласты, хондробласты и остеобласты.В результате начинает происходить хондрогенез, закладывая богатую коллагеном фиброзно-хрящевую сеть, охватывающую концы перелома, с окружающей гиалиновой хрящевой оболочкой. В то же время, прилегающий к надкостничным слоям, слой тканой кости откладывается остеопрогениторными клетками.
Образование костной мозоли (дни с 11 по 28)
Хрящевая мозоль начинает подвергаться эндохондральной оссификации. RANK-L экспрессируется, стимулируя дальнейшую дифференцировку хондробластов, хондрокластов, остеобластов и остеокластов. В результате хрящевая мозоль рассасывается и начинает кальцифицироваться. Поднадкостнично тканая кость продолжает закладываться. Новообразованные кровеносные сосуды продолжают разрастаться, обеспечивая дальнейшую миграцию мезенхимальных стволовых клеток. В конце этой фазы образуется твердая кальцинированная мозоль из незрелой кости.
Ремоделирование кости (начиная с 18-го дня, продолжительностью от нескольких месяцев до нескольких лет)
При продолжающейся миграции остеобластов и остеокластов твердый костный мозг подвергается повторному ремоделированию — так называемому «парному ремоделированию».«Это« связанное ремоделирование »- это баланс резорбции остеокластами и образования новой кости остеобластами. В конечном итоге центр костной мозоли заменяется компактной костью, а края костной мозоли заменяются пластинчатой костью. Наряду с этими изменениями происходит существенное ремоделирование сосудистой сети. Процесс ремоделирования кости длится многие месяцы, что в конечном итоге приводит к восстановлению нормальной структуры кости. [3] [4] [5] [6]
[3] [4] [5] [6]
Важным моментом для дальнейшего развития является эндохондральная оссификация, так называется процесс преобразования хряща в кость.Как описано выше, это происходит во время образования костной мозоли, в которой новообразованная богатая коллагеном хрящевая мозоль заменяется незрелой костью. Этот процесс также является ключом к образованию длинных костей у плода, в которых костный скелет заменяет модель гиалинового хряща. Второй тип окостенения также встречается у плода; это внутримембранозное окостенение; это процесс, при котором мезенхимальная ткань (примитивная соединительная ткань) преобразуется непосредственно в кость, которая не является промежуточным звеном хряща.Этот процесс происходит в плоских костях черепа. [7]
Клиническая значимость
Первичное заживление кости — это восстановление коры головного мозга без образования костной мозоли. Это происходит, если перелом адекватно «зафиксирован» путем репозиции, иммобилизации и реабилитации. Вторичное заживление кости, как описано выше, происходит за счет образования костной мозоли и последующего ремоделирования.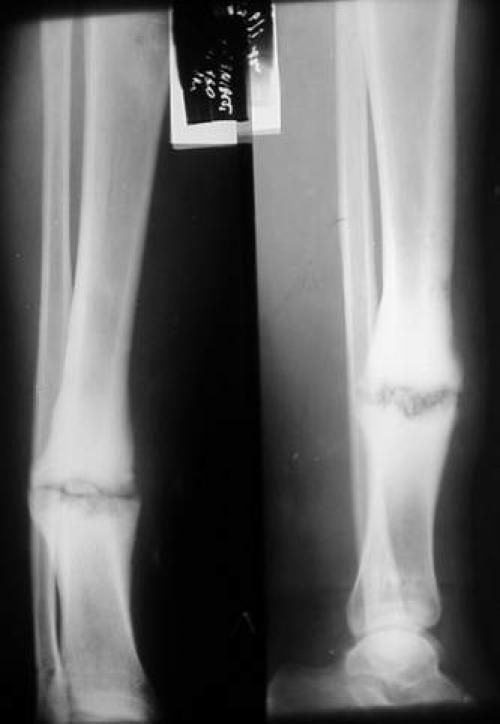
Путем репозиции и фиксации клиницист перемещает два конца перелома в плотное прилегание, что приводит к минимальному образованию грануляционной ткани и костной мозоли.«Режущие конусы» остеокластов пересекают место перелома до резорбированной поврежденной кости, а «формирующие зоны» остеобластов закладывают новую кость. [5] [8]
Репозиция и фиксация переломов могут быть как открытыми, так и закрытыми. Если лечить как закрытый, это происходит без надреза кожи. Открытый относится к необходимости или выбору вскрыть кожу хирургическим разрезом. Если картина излома кажется стабильной, то закрывается наиболее подходящий метод. Вариантами для этого было бы использование приведения (например,г., гипс Пэрис), ортез или шину. Открытая репозиция обычно используется при нестабильных переломах и обычно возникает вместе с внутренней фиксацией — отсюда и термин ORIF. Внутренняя фиксация предполагает использование хирургических имплантатов для удержания двух концов перелома вплотную друг к другу.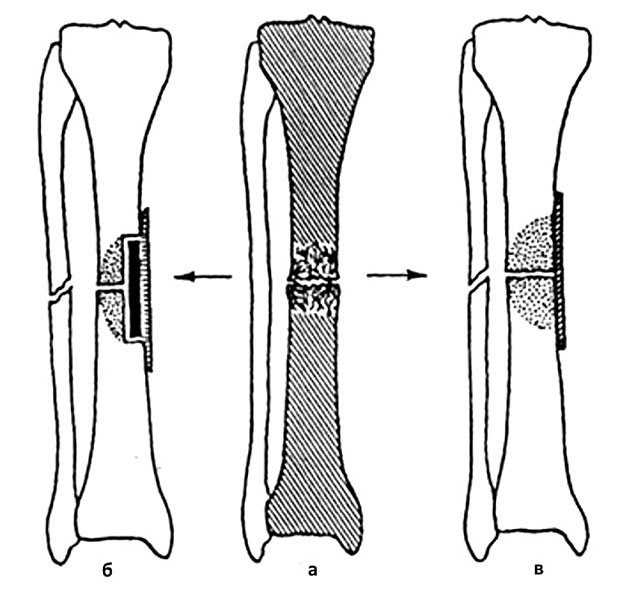 Обычно используемые методы внутренней фиксации включают покрытие, винты, проволоку и интрамедуллярные гвозди. Также возможен последний метод внешней фиксации, который включает в себя введение штифтов через кожу, которые затем удерживаются на месте внешней «каркасом».«Этот метод обычно используется при сложных переломах и может служить временным вариантом перед внутренней фиксацией. [9]
Обычно используемые методы внутренней фиксации включают покрытие, винты, проволоку и интрамедуллярные гвозди. Также возможен последний метод внешней фиксации, который включает в себя введение штифтов через кожу, которые затем удерживаются на месте внешней «каркасом».«Этот метод обычно используется при сложных переломах и может служить временным вариантом перед внутренней фиксацией. [9]
На заживление переломов влияет множество факторов, которые в широком смысле можно разделить на местные и системные категории.
Местные факторы
-
Характеристики перелома — чрезмерное движение, несоосность, обширное повреждение и попадание мягких тканей в концы перелома могут привести к замедленному или несращению
-
Инфекция — может привести к плохому заживлению и задержке или не союз.
-
Кровоснабжение — снижение кровоснабжения места перелома может привести к задержке или несращению.
Системные факторы (наличие любого из этих факторов предрасполагает к плохому заживлению)
Переломы приводят к значительной смертности и заболеваемости; поэтому для хороших результатов необходим межпрофессиональный подход. [10] [11] [12]
Существует несколько методов, которые межпрофессиональная группа может использовать для содействия / стимулирования заживления переломов, в том числе:
-
Пищевые добавки — кальций, белок, витамины C и D
-
Костные стимуляторы — которые могут быть электрическими, электромагнитными, и ультразвук.Текущая эффективность этих методов все еще сомнительна, и эта область требует дальнейших исследований.
- Костный трансплантат — это костный трансплантат, который используется в качестве основы для вновь формирующейся кости. Этот трансплантат может быть от тела пациента (аутотрансплантат) или от умершего донора (аллотрансплантат). [13] [14]
Обзор заживления переломов — StatPearls
Определение / Введение
Перелом — это нарушение структурной целостности коры кости со степенью повреждения окружающих мягких тканей.После перелома начинается вторичное заживление, которое состоит из четырех этапов:
-
Образование гематомы
-
Образование фиброзно-хрящевой костной мозоли
-
Формирование костной мозоли
-
Ремоделирование кости
Может повлиять на неудачное заживление до 10% всех переломов и могут быть вызваны различными факторами, такими как измельчение, инфекция, опухоль и нарушение кровоснабжения. В этой статье мы подробно рассмотрим каждый из этих шагов, прежде чем коснемся первичного заживления, факторов, влияющих на заживление переломов, и методов стимуляции заживления переломов.[1] [2]
В этой статье мы подробно рассмотрим каждый из этих шагов, прежде чем коснемся первичного заживления, факторов, влияющих на заживление переломов, и методов стимуляции заживления переломов.[1] [2]
Проблемы, вызывающие озабоченность
Механизм заживления перелома — сложный и плавный процесс. Этот процесс можно разбить на четыре этапа. Однако эти этапы в значительной степени пересекаются.
Образование гематомы (дни с 1 по 5)
Эта стадия начинается сразу после перелома. Кровеносные сосуды, снабжающие кость и надкостницу, разрываются во время перелома, в результате чего вокруг места перелома образуется гематома. Гематома сворачивается и образует временный каркас для последующего заживления.Повреждение кости приводит к секреции провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNF-α), морфогенетические белки кости (BMP) и интерлейкины (IL-1, IL-6, IL-11, IL-23). ). Эти цитокины стимулируют важную клеточную биологию в этом месте, привлекая макрофаги, моноциты и лимфоциты. Эти клетки действуют вместе, удаляя поврежденные, некротические ткани и секретируя цитокины, такие как фактор роста эндотелия сосудов (VEGF), чтобы стимулировать заживление на этом участке.
Образование фиброзно-хрящевой каллуса (дни с 5 по 11)
Высвобождение VEGF приводит к ангиогенезу в этом месте, а внутри гематомы начинает развиваться богатая фибрином грануляционная ткань.Далее мезенхимальные стволовые клетки привлекаются к этой области и начинают дифференцироваться (управляемая BMP) в фибробласты, хондробласты и остеобласты. В результате начинает происходить хондрогенез, закладывая богатую коллагеном фиброзно-хрящевую сеть, охватывающую концы перелома, с окружающей гиалиновой хрящевой оболочкой. В то же время, прилегающий к надкостничным слоям, слой тканой кости откладывается остеопрогениторными клетками.
Образование костной мозоли (дни с 11 по 28)
Хрящевая мозоль начинает подвергаться эндохондральной оссификации.RANK-L экспрессируется, стимулируя дальнейшую дифференцировку хондробластов, хондрокластов, остеобластов и остеокластов. В результате хрящевая мозоль рассасывается и начинает кальцифицироваться. Поднадкостнично тканая кость продолжает закладываться. Новообразованные кровеносные сосуды продолжают разрастаться, обеспечивая дальнейшую миграцию мезенхимальных стволовых клеток. В конце этой фазы образуется твердая кальцинированная мозоль из незрелой кости.
В результате хрящевая мозоль рассасывается и начинает кальцифицироваться. Поднадкостнично тканая кость продолжает закладываться. Новообразованные кровеносные сосуды продолжают разрастаться, обеспечивая дальнейшую миграцию мезенхимальных стволовых клеток. В конце этой фазы образуется твердая кальцинированная мозоль из незрелой кости.
Ремоделирование кости (начиная с 18-го дня, продолжительностью от нескольких месяцев до нескольких лет)
При продолжающейся миграции остеобластов и остеокластов твердый костный мозг подвергается повторному ремоделированию — так называемому «парному ремоделированию».«Это« связанное ремоделирование »- это баланс резорбции остеокластами и образования новой кости остеобластами. В конечном итоге центр костной мозоли заменяется компактной костью, а края костной мозоли заменяются пластинчатой костью. Наряду с этими изменениями происходит существенное ремоделирование сосудистой сети. Процесс ремоделирования кости длится многие месяцы, что в конечном итоге приводит к восстановлению нормальной структуры кости.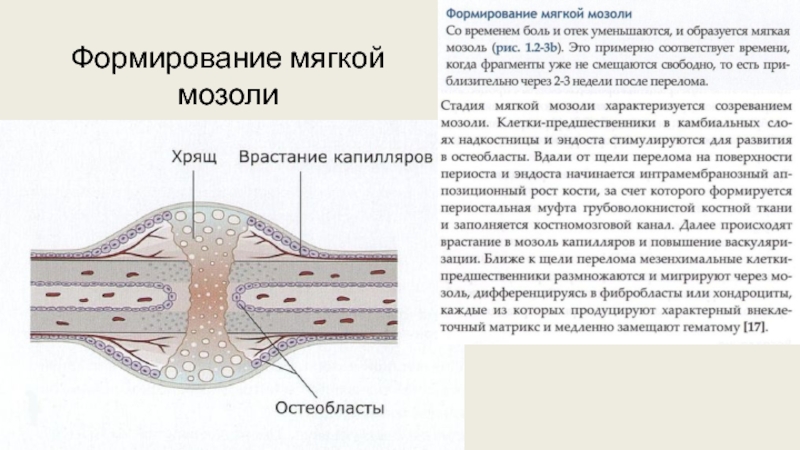 [3] [4] [5] [6]
[3] [4] [5] [6]
Важным моментом для дальнейшего развития является эндохондральная оссификация, так называется процесс преобразования хряща в кость.Как описано выше, это происходит во время образования костной мозоли, в которой новообразованная богатая коллагеном хрящевая мозоль заменяется незрелой костью. Этот процесс также является ключом к образованию длинных костей у плода, в которых костный скелет заменяет модель гиалинового хряща. Второй тип окостенения также встречается у плода; это внутримембранозное окостенение; это процесс, при котором мезенхимальная ткань (примитивная соединительная ткань) преобразуется непосредственно в кость, которая не является промежуточным звеном хряща.Этот процесс происходит в плоских костях черепа. [7]
Клиническая значимость
Первичное заживление кости — это восстановление коры головного мозга без образования костной мозоли. Это происходит, если перелом адекватно «зафиксирован» путем репозиции, иммобилизации и реабилитации. Вторичное заживление кости, как описано выше, происходит за счет образования костной мозоли и последующего ремоделирования.
Путем репозиции и фиксации клиницист перемещает два конца перелома в плотное прилегание, что приводит к минимальному образованию грануляционной ткани и костной мозоли.«Режущие конусы» остеокластов пересекают место перелома до резорбированной поврежденной кости, а «формирующие зоны» остеобластов закладывают новую кость. [5] [8]
Репозиция и фиксация переломов могут быть как открытыми, так и закрытыми. Если лечить как закрытый, это происходит без надреза кожи. Открытый относится к необходимости или выбору вскрыть кожу хирургическим разрезом. Если картина излома кажется стабильной, то закрывается наиболее подходящий метод. Вариантами для этого было бы использование приведения (например,г., гипс Пэрис), ортез или шину. Открытая репозиция обычно используется при нестабильных переломах и обычно возникает вместе с внутренней фиксацией — отсюда и термин ORIF. Внутренняя фиксация предполагает использование хирургических имплантатов для удержания двух концов перелома вплотную друг к другу. Обычно используемые методы внутренней фиксации включают покрытие, винты, проволоку и интрамедуллярные гвозди. Также возможен последний метод внешней фиксации, который включает в себя введение штифтов через кожу, которые затем удерживаются на месте внешней «каркасом».«Этот метод обычно используется при сложных переломах и может служить временным вариантом перед внутренней фиксацией. [9]
Обычно используемые методы внутренней фиксации включают покрытие, винты, проволоку и интрамедуллярные гвозди. Также возможен последний метод внешней фиксации, который включает в себя введение штифтов через кожу, которые затем удерживаются на месте внешней «каркасом».«Этот метод обычно используется при сложных переломах и может служить временным вариантом перед внутренней фиксацией. [9]
На заживление переломов влияет множество факторов, которые в широком смысле можно разделить на местные и системные категории.
Местные факторы
-
Характеристики перелома — чрезмерное движение, несоосность, обширное повреждение и попадание мягких тканей в концы перелома могут привести к замедленному или несращению
-
Инфекция — может привести к плохому заживлению и задержке или не союз.
-
Кровоснабжение — снижение кровоснабжения места перелома может привести к задержке или несращению.
Системные факторы (наличие любого из этих факторов предрасполагает к плохому заживлению)
Переломы приводят к значительной смертности и заболеваемости; поэтому для хороших результатов необходим межпрофессиональный подход.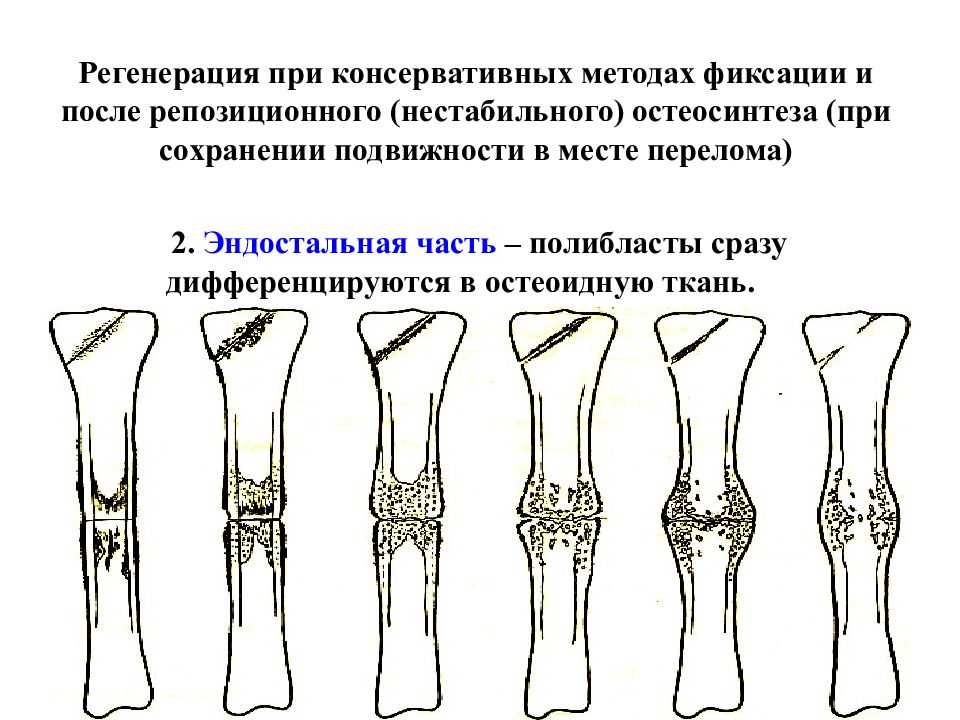 [10] [11] [12]
[10] [11] [12]
Существует несколько методов, которые межпрофессиональная группа может использовать для содействия / стимулирования заживления переломов, в том числе:
-
Пищевые добавки — кальций, белок, витамины C и D
-
Костные стимуляторы — которые могут быть электрическими, электромагнитными, и ультразвук.Текущая эффективность этих методов все еще сомнительна, и эта область требует дальнейших исследований.
- Костный трансплантат — это костный трансплантат, который используется в качестве основы для вновь формирующейся кости. Этот трансплантат может быть от тела пациента (аутотрансплантат) или от умершего донора (аллотрансплантат). [13] [14]
Обзор заживления переломов — StatPearls
Определение / Введение
Перелом — это нарушение структурной целостности коры кости со степенью повреждения окружающих мягких тканей.После перелома начинается вторичное заживление, которое состоит из четырех этапов:
-
Образование гематомы
-
Образование фиброзно-хрящевой костной мозоли
-
Формирование костной мозоли
-
Ремоделирование кости
Может повлиять на неудачное заживление до 10% всех переломов и могут быть вызваны различными факторами, такими как измельчение, инфекция, опухоль и нарушение кровоснабжения. В этой статье мы подробно рассмотрим каждый из этих шагов, прежде чем коснемся первичного заживления, факторов, влияющих на заживление переломов, и методов стимуляции заживления переломов.[1] [2]
В этой статье мы подробно рассмотрим каждый из этих шагов, прежде чем коснемся первичного заживления, факторов, влияющих на заживление переломов, и методов стимуляции заживления переломов.[1] [2]
Проблемы, вызывающие озабоченность
Механизм заживления перелома — сложный и плавный процесс. Этот процесс можно разбить на четыре этапа. Однако эти этапы в значительной степени пересекаются.
Образование гематомы (дни с 1 по 5)
Эта стадия начинается сразу после перелома. Кровеносные сосуды, снабжающие кость и надкостницу, разрываются во время перелома, в результате чего вокруг места перелома образуется гематома. Гематома сворачивается и образует временный каркас для последующего заживления.Повреждение кости приводит к секреции провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNF-α), морфогенетические белки кости (BMP) и интерлейкины (IL-1, IL-6, IL-11, IL-23). ). Эти цитокины стимулируют важную клеточную биологию в этом месте, привлекая макрофаги, моноциты и лимфоциты. Эти клетки действуют вместе, удаляя поврежденные, некротические ткани и секретируя цитокины, такие как фактор роста эндотелия сосудов (VEGF), чтобы стимулировать заживление на этом участке.
Эти клетки действуют вместе, удаляя поврежденные, некротические ткани и секретируя цитокины, такие как фактор роста эндотелия сосудов (VEGF), чтобы стимулировать заживление на этом участке.
Образование фиброзно-хрящевой каллуса (дни с 5 по 11)
Высвобождение VEGF приводит к ангиогенезу в этом месте, а внутри гематомы начинает развиваться богатая фибрином грануляционная ткань.Далее мезенхимальные стволовые клетки привлекаются к этой области и начинают дифференцироваться (управляемая BMP) в фибробласты, хондробласты и остеобласты. В результате начинает происходить хондрогенез, закладывая богатую коллагеном фиброзно-хрящевую сеть, охватывающую концы перелома, с окружающей гиалиновой хрящевой оболочкой. В то же время, прилегающий к надкостничным слоям, слой тканой кости откладывается остеопрогениторными клетками.
Образование костной мозоли (дни с 11 по 28)
Хрящевая мозоль начинает подвергаться эндохондральной оссификации.RANK-L экспрессируется, стимулируя дальнейшую дифференцировку хондробластов, хондрокластов, остеобластов и остеокластов. В результате хрящевая мозоль рассасывается и начинает кальцифицироваться. Поднадкостнично тканая кость продолжает закладываться. Новообразованные кровеносные сосуды продолжают разрастаться, обеспечивая дальнейшую миграцию мезенхимальных стволовых клеток. В конце этой фазы образуется твердая кальцинированная мозоль из незрелой кости.
В результате хрящевая мозоль рассасывается и начинает кальцифицироваться. Поднадкостнично тканая кость продолжает закладываться. Новообразованные кровеносные сосуды продолжают разрастаться, обеспечивая дальнейшую миграцию мезенхимальных стволовых клеток. В конце этой фазы образуется твердая кальцинированная мозоль из незрелой кости.
Ремоделирование кости (начиная с 18-го дня, продолжительностью от нескольких месяцев до нескольких лет)
При продолжающейся миграции остеобластов и остеокластов твердый костный мозг подвергается повторному ремоделированию — так называемому «парному ремоделированию».«Это« связанное ремоделирование »- это баланс резорбции остеокластами и образования новой кости остеобластами. В конечном итоге центр костной мозоли заменяется компактной костью, а края костной мозоли заменяются пластинчатой костью. Наряду с этими изменениями происходит существенное ремоделирование сосудистой сети. Процесс ремоделирования кости длится многие месяцы, что в конечном итоге приводит к восстановлению нормальной структуры кости. [3] [4] [5] [6]
[3] [4] [5] [6]
Важным моментом для дальнейшего развития является эндохондральная оссификация, так называется процесс преобразования хряща в кость.Как описано выше, это происходит во время образования костной мозоли, в которой новообразованная богатая коллагеном хрящевая мозоль заменяется незрелой костью. Этот процесс также является ключом к образованию длинных костей у плода, в которых костный скелет заменяет модель гиалинового хряща. Второй тип окостенения также встречается у плода; это внутримембранозное окостенение; это процесс, при котором мезенхимальная ткань (примитивная соединительная ткань) преобразуется непосредственно в кость, которая не является промежуточным звеном хряща.Этот процесс происходит в плоских костях черепа. [7]
Клиническая значимость
Первичное заживление кости — это восстановление коры головного мозга без образования костной мозоли. Это происходит, если перелом адекватно «зафиксирован» путем репозиции, иммобилизации и реабилитации. Вторичное заживление кости, как описано выше, происходит за счет образования костной мозоли и последующего ремоделирования.
Путем репозиции и фиксации клиницист перемещает два конца перелома в плотное прилегание, что приводит к минимальному образованию грануляционной ткани и костной мозоли.«Режущие конусы» остеокластов пересекают место перелома до резорбированной поврежденной кости, а «формирующие зоны» остеобластов закладывают новую кость. [5] [8]
Репозиция и фиксация переломов могут быть как открытыми, так и закрытыми. Если лечить как закрытый, это происходит без надреза кожи. Открытый относится к необходимости или выбору вскрыть кожу хирургическим разрезом. Если картина излома кажется стабильной, то закрывается наиболее подходящий метод. Вариантами для этого было бы использование приведения (например,г., гипс Пэрис), ортез или шину. Открытая репозиция обычно используется при нестабильных переломах и обычно возникает вместе с внутренней фиксацией — отсюда и термин ORIF. Внутренняя фиксация предполагает использование хирургических имплантатов для удержания двух концов перелома вплотную друг к другу. Обычно используемые методы внутренней фиксации включают покрытие, винты, проволоку и интрамедуллярные гвозди. Также возможен последний метод внешней фиксации, который включает в себя введение штифтов через кожу, которые затем удерживаются на месте внешней «каркасом».«Этот метод обычно используется при сложных переломах и может служить временным вариантом перед внутренней фиксацией. [9]
На заживление переломов влияет множество факторов, которые в широком смысле можно разделить на местные и системные категории.
Местные факторы
-
Характеристики перелома — чрезмерное движение, несоосность, обширное повреждение и попадание мягких тканей в концы перелома могут привести к замедленному или несращению
-
Инфекция — может привести к плохому заживлению и задержке или не союз.
-
Кровоснабжение — снижение кровоснабжения места перелома может привести к задержке или несращению.
Системные факторы (наличие любого из этих факторов предрасполагает к плохому заживлению)
Переломы приводят к значительной смертности и заболеваемости; поэтому для хороших результатов необходим межпрофессиональный подход. [10] [11] [12]
Существует несколько методов, которые межпрофессиональная группа может использовать для содействия / стимулирования заживления переломов, в том числе:
-
Пищевые добавки — кальций, белок, витамины C и D
-
Костные стимуляторы — которые могут быть электрическими, электромагнитными, и ультразвук.Текущая эффективность этих методов все еще сомнительна, и эта область требует дальнейших исследований.
- Костный трансплантат — это костный трансплантат, который используется в качестве основы для вновь формирующейся кости. Этот трансплантат может быть от тела пациента (аутотрансплантат) или от умершего донора (аллотрансплантат). [13] [14]
Обзор заживления переломов — StatPearls
Определение / Введение
Перелом — это нарушение структурной целостности коры кости со степенью повреждения окружающих мягких тканей.После перелома начинается вторичное заживление, которое состоит из четырех этапов:
-
Образование гематомы
-
Образование фиброзно-хрящевой костной мозоли
-
Формирование костной мозоли
-
Ремоделирование кости
Может повлиять на неудачное заживление до 10% всех переломов и могут быть вызваны различными факторами, такими как измельчение, инфекция, опухоль и нарушение кровоснабжения. В этой статье мы подробно рассмотрим каждый из этих шагов, прежде чем коснемся первичного заживления, факторов, влияющих на заживление переломов, и методов стимуляции заживления переломов.[1] [2]
Проблемы, вызывающие озабоченность
Механизм заживления перелома — сложный и плавный процесс. Этот процесс можно разбить на четыре этапа. Однако эти этапы в значительной степени пересекаются.
Образование гематомы (дни с 1 по 5)
Эта стадия начинается сразу после перелома. Кровеносные сосуды, снабжающие кость и надкостницу, разрываются во время перелома, в результате чего вокруг места перелома образуется гематома. Гематома сворачивается и образует временный каркас для последующего заживления.Повреждение кости приводит к секреции провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNF-α), морфогенетические белки кости (BMP) и интерлейкины (IL-1, IL-6, IL-11, IL-23). ). Эти цитокины стимулируют важную клеточную биологию в этом месте, привлекая макрофаги, моноциты и лимфоциты. Эти клетки действуют вместе, удаляя поврежденные, некротические ткани и секретируя цитокины, такие как фактор роста эндотелия сосудов (VEGF), чтобы стимулировать заживление на этом участке.
Образование фиброзно-хрящевой каллуса (дни с 5 по 11)
Высвобождение VEGF приводит к ангиогенезу в этом месте, а внутри гематомы начинает развиваться богатая фибрином грануляционная ткань.Далее мезенхимальные стволовые клетки привлекаются к этой области и начинают дифференцироваться (управляемая BMP) в фибробласты, хондробласты и остеобласты. В результате начинает происходить хондрогенез, закладывая богатую коллагеном фиброзно-хрящевую сеть, охватывающую концы перелома, с окружающей гиалиновой хрящевой оболочкой. В то же время, прилегающий к надкостничным слоям, слой тканой кости откладывается остеопрогениторными клетками.
Образование костной мозоли (дни с 11 по 28)
Хрящевая мозоль начинает подвергаться эндохондральной оссификации.RANK-L экспрессируется, стимулируя дальнейшую дифференцировку хондробластов, хондрокластов, остеобластов и остеокластов. В результате хрящевая мозоль рассасывается и начинает кальцифицироваться. Поднадкостнично тканая кость продолжает закладываться. Новообразованные кровеносные сосуды продолжают разрастаться, обеспечивая дальнейшую миграцию мезенхимальных стволовых клеток. В конце этой фазы образуется твердая кальцинированная мозоль из незрелой кости.
Ремоделирование кости (начиная с 18-го дня, продолжительностью от нескольких месяцев до нескольких лет)
При продолжающейся миграции остеобластов и остеокластов твердый костный мозг подвергается повторному ремоделированию — так называемому «парному ремоделированию».«Это« связанное ремоделирование »- это баланс резорбции остеокластами и образования новой кости остеобластами. В конечном итоге центр костной мозоли заменяется компактной костью, а края костной мозоли заменяются пластинчатой костью. Наряду с этими изменениями происходит существенное ремоделирование сосудистой сети. Процесс ремоделирования кости длится многие месяцы, что в конечном итоге приводит к восстановлению нормальной структуры кости. [3] [4] [5] [6]
Важным моментом для дальнейшего развития является эндохондральная оссификация, так называется процесс преобразования хряща в кость.Как описано выше, это происходит во время образования костной мозоли, в которой новообразованная богатая коллагеном хрящевая мозоль заменяется незрелой костью. Этот процесс также является ключом к образованию длинных костей у плода, в которых костный скелет заменяет модель гиалинового хряща. Второй тип окостенения также встречается у плода; это внутримембранозное окостенение; это процесс, при котором мезенхимальная ткань (примитивная соединительная ткань) преобразуется непосредственно в кость, которая не является промежуточным звеном хряща.Этот процесс происходит в плоских костях черепа. [7]
Клиническая значимость
Первичное заживление кости — это восстановление коры головного мозга без образования костной мозоли. Это происходит, если перелом адекватно «зафиксирован» путем репозиции, иммобилизации и реабилитации. Вторичное заживление кости, как описано выше, происходит за счет образования костной мозоли и последующего ремоделирования.
Путем репозиции и фиксации клиницист перемещает два конца перелома в плотное прилегание, что приводит к минимальному образованию грануляционной ткани и костной мозоли.«Режущие конусы» остеокластов пересекают место перелома до резорбированной поврежденной кости, а «формирующие зоны» остеобластов закладывают новую кость. [5] [8]
Репозиция и фиксация переломов могут быть как открытыми, так и закрытыми. Если лечить как закрытый, это происходит без надреза кожи. Открытый относится к необходимости или выбору вскрыть кожу хирургическим разрезом. Если картина излома кажется стабильной, то закрывается наиболее подходящий метод. Вариантами для этого было бы использование приведения (например,г., гипс Пэрис), ортез или шину. Открытая репозиция обычно используется при нестабильных переломах и обычно возникает вместе с внутренней фиксацией — отсюда и термин ORIF. Внутренняя фиксация предполагает использование хирургических имплантатов для удержания двух концов перелома вплотную друг к другу. Обычно используемые методы внутренней фиксации включают покрытие, винты, проволоку и интрамедуллярные гвозди. Также возможен последний метод внешней фиксации, который включает в себя введение штифтов через кожу, которые затем удерживаются на месте внешней «каркасом».«Этот метод обычно используется при сложных переломах и может служить временным вариантом перед внутренней фиксацией. [9]
На заживление переломов влияет множество факторов, которые в широком смысле можно разделить на местные и системные категории.
Местные факторы
-
Характеристики перелома — чрезмерное движение, несоосность, обширное повреждение и попадание мягких тканей в концы перелома могут привести к замедленному или несращению
-
Инфекция — может привести к плохому заживлению и задержке или не союз.
-
Кровоснабжение — снижение кровоснабжения места перелома может привести к задержке или несращению.
Системные факторы (наличие любого из этих факторов предрасполагает к плохому заживлению)
Переломы приводят к значительной смертности и заболеваемости; поэтому для хороших результатов необходим межпрофессиональный подход. [10] [11] [12]
Существует несколько методов, которые межпрофессиональная группа может использовать для содействия / стимулирования заживления переломов, в том числе:
-
Пищевые добавки — кальций, белок, витамины C и D
-
Костные стимуляторы — которые могут быть электрическими, электромагнитными, и ультразвук.Текущая эффективность этих методов все еще сомнительна, и эта область требует дальнейших исследований.
- Костный трансплантат — это костный трансплантат, который используется в качестве основы для вновь формирующейся кости. Этот трансплантат может быть от тела пациента (аутотрансплантат) или от умершего донора (аллотрансплантат). [13] [14]
Образование перелома: заживление перелома
Заживление перелома у детей происходит на тех же этапах, что и у взрослых, но происходит гораздо быстрее. Переломы заживают за счет образования костной мозоли, которая проходит через три перекрывающиеся фазы: воспалительную, репаративную и ремоделирующую.
|
|
Фазы заживления перелома
Воспалительная фаза (продолжительность: часы – дни): Сломанные кости приводят к разрыву кровеносных сосудов и образованию тромба или гематомы. Воспалительная реакция приводит к высвобождению цитокинов, факторов роста и простагландинов, которые важны для заживления. Гематома перелома становится организованной и затем инфильтрируется фиброваскулярной тканью, которая образует матрицу для образования кости и первичной мозоли.
Фаза репарации (продолжительность: дни-недели): Вокруг концов кости образуется плотная каллусная масса из-за гематомы перелома. Костеобразующие клетки привлекаются из нескольких источников для формирования новой кости, что можно увидеть на рентгенограммах в течение 7-10 дней после травмы (рис. 9). Мягкая мозоль организуется и превращается в твердую в течение нескольких недель. Мягкая мозоль пластична и может легко деформироваться или искривляться, если перелом не имеет адекватной поддержки. Твердая костная мозоль более слабая, чем нормальная кость, но лучше способна противостоять внешним воздействиям и приравнивается к стадии «клинического сращения», т.е.е. перелом не чувствителен к пальпации или движению.
Фаза ремоделирования (продолжительность: месяцы-годы): Это самая продолжительная фаза, которая может длиться несколько лет. Во время ремоделирования заживший перелом и окружающая костная мозоль реагируют на активность, внешние силы, функциональные требования и рост. Кость (внешняя мозоль), которая больше не нужна, удаляется, а место перелома сглаживается и скульптурируется до тех пор, пока на рентгеновском снимке он не станет более нормальным (рис. 9). Эпифизы постепенно перестраиваются, а остаточный угол может медленно исправляться в соответствии с правилами ремоделирования, описанными выше.
A
B
Рис. 9: Маленькие дети обладают прекрасным потенциалом ремоделирования. A. Это последовательные рентгеновские снимки ребенка с переломом середины диафиза правой плечевой кости при рождении. Обратите внимание на очень быстрое заживление обширной костной мозоли к 7 дню с последующим ремоделированием. B. Это последовательные рентгеновские снимки 14-месячного ребенка с переломом середины диафиза правой бедренной кости.Снова обратите внимание на быстрое заживление обширной мозоли к 18-му дню.
Исцеление костей — Факты о здоровье стопы
Как заживает кость?
Все сломанные кости заживают одинаково. Это верно независимо от того, была ли кость разрезана во время хирургической процедуры или сломана в результате травмы.
Процесс заживления кости состоит из трех перекрывающихся стадий: воспаления, образования кости и ремоделирования кости.
- Воспаление начинается сразу после перелома кости и длится несколько дней. Когда кость сломана, в эту область идет кровотечение, что приводит к воспалению и свертыванию крови в месте перелома. Это обеспечивает начальную структурную стабильность и основу для образования новой кости.
- Образование костей начинается, когда свернувшаяся кровь, образовавшаяся в результате воспаления, заменяется фиброзной тканью и хрящом (известным как мягкая мозоль).По мере заживления мягкая мозоль заменяется твердой костью (известной как твердый мозоль), которая видна на рентгеновских снимках через несколько недель после перелома.
- Ремоделирование кости, заключительная фаза заживления кости, длится несколько месяцев. При ремоделировании кость продолжает формироваться и становится компактной, возвращаясь к своей первоначальной форме. Кроме того, улучшается кровообращение в этой области. Как только произошло адекватное заживление кости, нагрузка (например, стояние или ходьба) способствует ремоделированию кости.
Как долго длится заживление костей?
Кости обычно в значительной степени заживают от шести до 12 недель. В целом детские кости заживают быстрее, чем взрослые. Хирург стопы и голеностопного сустава определит, когда пациент готов выдержать нагрузку на эту область. Это будет зависеть от местоположения и серьезности перелома, типа выполненной хирургической процедуры и других соображений.
Что способствует заживлению костей?
Если кость будет разрезана во время запланированной хирургической процедуры, некоторые шаги могут быть предприняты до и после операции, чтобы помочь оптимизировать заживление.Хирург может посоветовать диету и пищевые добавки, которые необходимы для роста костей. Отказ от курения и адекватный контроль уровня сахара в крови у людей, живущих с диабетом, очень важны. Курение и высокий уровень глюкозы мешают заживлению костей.
Для всех пациентов с переломами костей иммобилизация является важной частью лечения, потому что любое движение костных фрагментов замедляет начальный процесс заживления. В зависимости от типа перелома или хирургической процедуры хирург может использовать какую-либо форму фиксации (например, винты, пластины или проволоку) на сломанной кости и / или гипсовой повязке, чтобы кость не двигалась.В период иммобилизации ограничение веса тела в соответствии с указаниями хирурга.
После того, как кость полностью зажила, физиотерапия часто играет ключевую роль в реабилитации. Программа упражнений, разработанная для пациента, может помочь восстановить силы и равновесие и помочь вернуться к нормальной деятельности.
Что может препятствовать заживлению костей?
Замедлить процесс заживления может множество факторов. К ним относятся:
- Перемещение костных отломков; слишком ранний вес
- Курение, сужающее кровеносные сосуды и ухудшающее кровообращение
- Заболевания, такие как диабет, гормональные проблемы или сосудистые заболевания
- Некоторые лекарства, такие как кортикостероиды и другие иммунодепрессанты
- Переломы тяжелые, осложненные или инфицированные
- Пожилой возраст
- Плохое питание или нарушение обмена веществ
- Низкий уровень кальция и витамина D
Как лечить медленное заживление?
Если кость заживает не так хорошо, как ожидалось, или не заживает, хирург стопы и голеностопного сустава может выбрать один из множества вариантов лечения для ускорения роста кости, например, продолжительную иммобилизацию в течение более длительного периода, стимуляцию кости или операцию с пересадкой кости. или использование белков роста костей.
Сокращение разрыва | Природа
Перелом кости, который не заживает после начального лечения, может привести к длительной инвалидности. Регенеративная терапия может помочь возобновить процесс заживления костей, вернув пострадавших к действию.
Скачать PDF-файл с графикойХотя большинство переломов заживают полностью, небольшая, но заметная часть — нет.Эти тяжелые случаи, известные как переломы костей без сращения, могут вызывать длительную инвалидность и боль и часто требуют хирургического вмешательства для исправления. Чтобы определить, почему возникает несращивающийся перелом кости, важно понимать, как обычно происходит заживление кости.
Предоставлено: Люси Ридинг-Икканда
Сразу после перелома кровь из разорванных сосудов внутри кости начинает свертываться в опухшее образование, называемое гематомой. На этой ранней стадии крайне важно, чтобы фрагменты кости были возвращены на место, чтобы гарантировать, что они правильно выровнены, и чтобы помочь остановить потерю крови.
Предоставлено: Люси Ридинг-Икканда
. Мягко (2–6 недель)
Начинает формироваться мягкая мозоль, состоящая из новой соединительной ткани, микроскопических кровеносных сосудов, хряща и мягкой губчатой кости.
Люси Ридинг-Икканда
Закалка (6–12 недель)
Через 12 недель после перелома остеобласты превратили мягкую мозоль в твердую.Продолжительность периода заживления зависит от места перелома — кости нижних конечностей могут занять больше времени, потому что они больше.
Зажившая кость будет продолжать реконструироваться в ближайшие месяцы и годы в ответ на стрессы, вызванные физической нагрузкой.
Предоставлено: Люси Ридинг-Икканда
. Несчастный брак (6–9 месяцев)
Перелом костей без сращения диагностируется, если нет доказательств того, что сломанная кость полностью заживет без дальнейшего медицинского вмешательства.
Предоставлено: Люси Ридинг-Икканда
Около 5–10% переломов костей не заживают 1 . По мере старения населения развитых стран частота переломов, в том числе переломов несрастающихся костей, будет увеличиваться.
Предоставлено: Люси Ридинг-Икканда
Обычно лечение перелома несращающейся кости включает операцию по стабилизации места перелома и пересадку кости для стимуляции роста кости и новых кровеносных сосудов.В настоящее время исследователи обращаются к регенеративной медицине, чтобы помочь в лечении таких переломов.
Они нацелены на доставку мононуклеарных клеток, называемых эндотелиальными клетками-предшественниками (EPC), к месту перелома, чтобы вызвать регенерацию кровеносных сосудов и способствовать образованию кости. EPC экспрессируют на своей поверхности белок CD34, который действует как маркер, позволяющий идентифицировать их и извлекать из крови.
Предоставлено: Люси Ридинг-Икканда
Исследование 2014 года 4 , проведенное учеными из Японии, показало, что лечение CD34-экспрессирующими клетками кажется безопасным, а переломы костей заживают у всех людей, получавших терапию.Но исследование было слишком маленьким, чтобы определить какую-либо клиническую пользу. В 2015 году началось более крупное трехлетнее испытание в нескольких учреждениях по изучению эффектов терапии на основе CD34. Результаты должны показать, может ли регенеративная медицина помочь в заживлении сломанных костей.
Предоставлено: Люси Ридинг-Икканда
. Эта статья является частью библиотеки Перелом несращающейся кости Outline, редакционно независимое приложение, выпущенное при финансовой поддержке третьих лиц. Об этом содержании.
1. Миллс, Л. А. и Симпсон, А. Х. Р. У. BMJ Open 3 , e002276 (2013).
2. Дональдсон, Л. Дж., Рэклесс, И. П., Скоулз, С., Минделл, Дж. С. и Шелтон, Н. Дж. J. Epidemiol. Общественное здравоохранение 62 , 174–180 (2008).
3. Buza, J. A. III & Einhorn, T. Clin. Кейсы Майнер. Bone Metab. 13 , 101–105 (2016).
4. Курода Р. и др. . Стволовые клетки Пер. Med. 3 , 128–134 (2014).
Предоставлено: Люси Ридинг-Икканда
. Предоставлено: Люси Ридинг-Икканда
.Информация об авторе
Заметки автора
-
Дэвид Холмс — научный писатель из Соединенного Королевства.
Об этой статье
Цитируйте эту статью
Холмс, Д. Устранение разрыва. Nature 550, S194 – S195 (2017).https://doi.org/10.1038/550S194a
Ссылка для скачивания
Дополнительная литература
-
Использование костных ниш: прогрессирование диссеминированных опухолевых клеток до метастазов
- Аарон М. Мускарелла
- , Серхио Агирре
- , Сяосинь Хао
- , Сара М. Вальдфогель
- и Сян Х.-Ф.Чжан
Журнал клинических исследований (2021 год)
-
Асимметрично пористая мембрана с плазмидной ДНК для управляемой регенерации кости
- Се Хеанг О
- , Джун-Хо Бён
- , Со Ён Чан
- , Ён-Джу Чан
- и Джин Хо Ли
Журнал материаловедения и технологий (2021 год)
-
Внеклеточный матрикс ногтевого ложа человека способствует регенерации кости за счет поляризации макрофагов, опосредованной путем JAK2 / STAT3.
- Yaling Yu
- , Haomin Cui
- , Cheng Zhang
- , Demin Zhang
- , Jun Yin
- , Gen Wen
- и Yimin Chai
Журнал химии материалов B (2020)
-
Трехмерный (3D) напечатанный биомиметический иерархический каркас с ковалентной модульной системой высвобождения для остеогенеза
- Гуанхуа Чен
- , И Сун
- , Фанчжоу Лу
- , Анлонг Цзян
- , Дипендра Субеди
- , Пэнъю Конг
- , Сяоянь Ван
- , Тайлун Юй
- , Сон Чи
- , Кунью Лю
- , Пэнфэй Ци
- , Цзинлун Ян
- и Е Цзи
Материаловедение и инженерия: C (2019)
-
Клеточная терапия на основе костного мозга для лечения несращений длинных костей: систематический обзор и метаанализ — какое лечение является наилучшим из имеющихся?
- Сильвия Паломбелла
- , Сильвия Лопа
- , Сильвия Джанола
- , Луиджи Загра
- , Маттео Моретти
- и Арианна Б.

